化学平衡
图片预览





文档简介
课件19张PPT。
人教版高二化学选修4第二章第三节第1课时
授课教师:彭晓霞
化学平衡问题1:什么是可逆反应?定义:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应,叫做可逆反应.一、可逆反应例如: N2+3H2 2NH3用 表示正反应:从左向右进行的反应。
逆反应:从右向左进行的反应。《学案》P29 第1题 P28 变1一、可逆反应问题2:在一定条件下,2mol SO2与1mol O2反应能否得到2mol SO3?
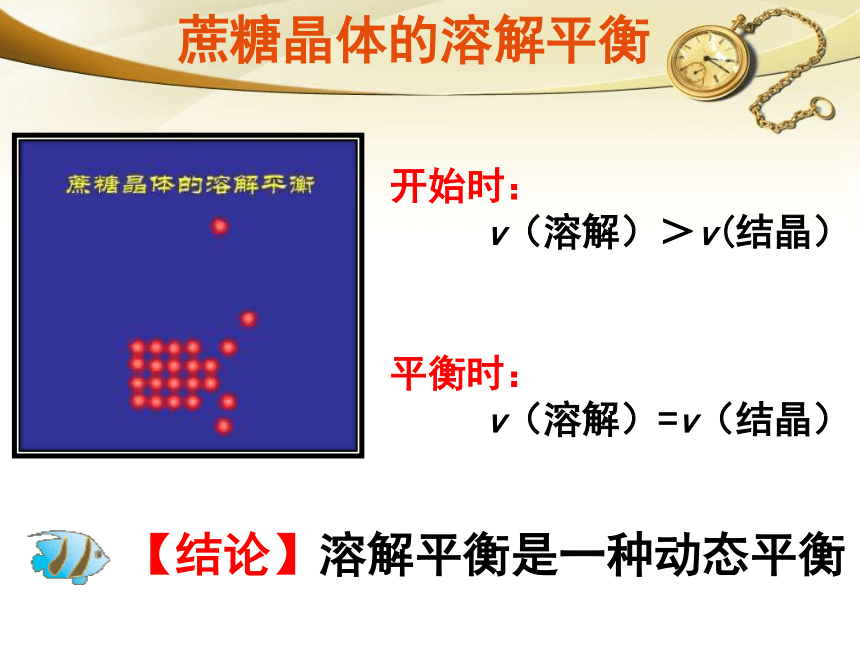
2SO2+ O2 2SO3不能!可逆反应不能进行到底,得到的总是反应物与生成物的混合物。(共存性)例题精析AD可逆反应不能进行到底,得到的总是反应物与生成物的混合物。《学案》P28 例1 P28 变2蔗糖晶体的溶解平衡开始时:
v(溶解)>v(结晶)
? 【结论】溶解平衡是一种动态平衡?平衡时:
v(溶解)=v(结晶)一定条件下,在容积为1L的密闭容器里,加0.01molCO(g)和0.01molH2O(g)
CO(g)+H2O(g) CO2(g)+H2(g)化学平衡状态的建立反应开始时,反应物浓度最_____,生成物浓度为_____.
所以,开始时正反应速率最_____,逆反应速率为______
随着反应的进行,反应物浓度逐渐______,生成物浓度逐渐_____
所以,正反应速率变_____,逆反应速率变______
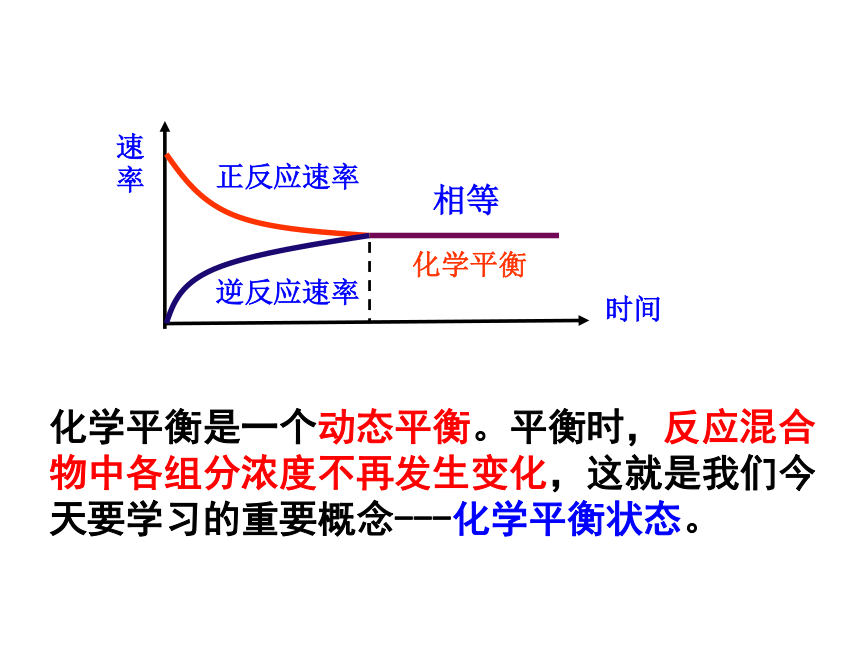
反应进行到一定程度,总有那么一刻,正反应速率和逆反应速率_______大0大0相等大小增大减小正反应速率逆反应速率相等化学平衡化学平衡是一个动态平衡。平衡时,反应混合物中各组分浓度不再发生变化,这就是我们今天要学习的重要概念---化学平衡状态。 化学平衡状态,就是指在一定条件下的可逆反应里,正反应速率和逆反应速率相等且不为0,反应混合物中各组分的浓度保持不变的状态。强调三点前提:可逆反应本质:v(正)= v(逆)表现:反应混合物中各组分的 浓度
保持不变二、化学平衡状态1、化学平衡的状态的定义:二、化学平衡状态2、化学平衡的状态的特征:(3)动:动态平衡(正逆反应仍在进行)(5)变:条件改变,原平衡被破坏,直到在新
的条件下建立新的平 衡。
(随条件而变)(4)定:反应混合物中各组分的浓度保持一定(1)逆:可逆反应;(2)等:正反应速率=逆反应速率二、化学平衡状态3、化学平衡的状态的标志:(1)直接标志:①速率关系: v(正)= v(逆)等如反应:A2(g)+2B2(g) 3C2(g)+4D2(g) v(正):A2、B2的消耗,C2、D2的生成v(逆):A2、B2的生成,C2、D2的消耗同种物质, v(正)= v(逆)
不同种物质, v(正):v(逆)=化学计量系数之比二、化学平衡状态3、化学平衡的状态的标志:(1)直接标志:①含量关系:各组分含量保持一定定含量一定:各组分物质的量(分数),质量(分数),气体的体积(分数)保持不变区分陷阱:
平衡时浓度变化之比等于化学计量系数之比?二、化学平衡状态3、化学平衡的状态的标志:(2)间接标志:即从变到不变(技巧)反应过程中如果哪个量在变,一旦它
不变了,就可以作为判断化学反应达
到平衡的状态。二、化学平衡状态3、化学平衡的状态的标志:(2)间接标志:即从变到不变(技巧)恒V时,对于反应 (1)2SO2(g)+O2 (g) 2SO3 (g)
(2)I2(g)+H2(g) 2HI(g)
气体的总压强、总物质的量、平衡相对分子质量、密度、颜色、温度保持不变能否作为可逆反应达到平衡的标志?①速率:v正=v逆
②各组分的浓度保持不变
③变的不再变(在化学反应进行过程中变化
的量,达到平衡时就不再变化了)二、化学平衡状态3、化学反应达到平衡状态的标志:(小结)直接间接《学案》P28 例2 P29 变3、变4 在一定温度下的恒容容器中,当下列物理量不再发生变化时,表明反应: A(固)+3B(气) 2C(气)+D(气)已达平衡状态的是 ( )
A.混合气体的压强 B.混合气体的密度
C.B的物质的量浓度 D.气体的总物质的量
BC《学案》P29 课时5 课时8 《学案》P29 课时2、 3、 4、 7 在一定温度下,下列叙述不是可逆反应
A(气)+3B(气) 2C(气)+2D(固)达到平衡的标志的是 ( )
①C的生成 速率与C的分解速率相等
②单位时间内生成amolA,同时生成3amolB
③A、B、C的浓度不再变化
④A、B、C的百分含量不在变化
⑤混合气体的总压强不再变化
⑥混合气体的物质的量不再变化
⑦单位时间内消耗amolA,同时生成 3amolB
⑧A、B、C、D的分子数之比为1:3:2:2
A.②⑧ B.②⑤⑧
C.①③④⑦ D.②⑤⑥⑧A小结一、可逆反应
二、化学平衡状态
1.定义
2.特征
3.判定例题精析【例2】可逆反应:2NO2 2NO+O2,在固定容积的密闭容器中达到平衡的标志是 ( )①单位时间内生成n molO2的同时生成2 n molNO2②单位时间内生成n molO2的同时生成2 n molNO⑦用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2:1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态⑥混合气体的平均相对分子质量不再改变的状态 ①③④⑥③NO2物质的量浓度不变例题精析【例3】可逆反应CO(g)+H2O(g) CO2(g)+H2(g),在固定容积的密闭容器中达到平衡的标志是 ( )①单位时间内生成n molCO2的同时生成n molCO④混合气体的密度不再改变的状态③混合气体的平均相对分子质量不再改变的状态①②②CO、H2O、CO2、H2浓度都不再发生变化
授课教师:彭晓霞
化学平衡问题1:什么是可逆反应?定义:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应,叫做可逆反应.一、可逆反应例如: N2+3H2 2NH3用 表示正反应:从左向右进行的反应。
逆反应:从右向左进行的反应。《学案》P29 第1题 P28 变1一、可逆反应问题2:在一定条件下,2mol SO2与1mol O2反应能否得到2mol SO3?
2SO2+ O2 2SO3不能!可逆反应不能进行到底,得到的总是反应物与生成物的混合物。(共存性)例题精析AD可逆反应不能进行到底,得到的总是反应物与生成物的混合物。《学案》P28 例1 P28 变2蔗糖晶体的溶解平衡开始时:
v(溶解)>v(结晶)
? 【结论】溶解平衡是一种动态平衡?平衡时:
v(溶解)=v(结晶)一定条件下,在容积为1L的密闭容器里,加0.01molCO(g)和0.01molH2O(g)
CO(g)+H2O(g) CO2(g)+H2(g)化学平衡状态的建立反应开始时,反应物浓度最_____,生成物浓度为_____.
所以,开始时正反应速率最_____,逆反应速率为______
随着反应的进行,反应物浓度逐渐______,生成物浓度逐渐_____
所以,正反应速率变_____,逆反应速率变______
反应进行到一定程度,总有那么一刻,正反应速率和逆反应速率_______大0大0相等大小增大减小正反应速率逆反应速率相等化学平衡化学平衡是一个动态平衡。平衡时,反应混合物中各组分浓度不再发生变化,这就是我们今天要学习的重要概念---化学平衡状态。 化学平衡状态,就是指在一定条件下的可逆反应里,正反应速率和逆反应速率相等且不为0,反应混合物中各组分的浓度保持不变的状态。强调三点前提:可逆反应本质:v(正)= v(逆)表现:反应混合物中各组分的 浓度
保持不变二、化学平衡状态1、化学平衡的状态的定义:二、化学平衡状态2、化学平衡的状态的特征:(3)动:动态平衡(正逆反应仍在进行)(5)变:条件改变,原平衡被破坏,直到在新
的条件下建立新的平 衡。
(随条件而变)(4)定:反应混合物中各组分的浓度保持一定(1)逆:可逆反应;(2)等:正反应速率=逆反应速率二、化学平衡状态3、化学平衡的状态的标志:(1)直接标志:①速率关系: v(正)= v(逆)等如反应:A2(g)+2B2(g) 3C2(g)+4D2(g) v(正):A2、B2的消耗,C2、D2的生成v(逆):A2、B2的生成,C2、D2的消耗同种物质, v(正)= v(逆)
不同种物质, v(正):v(逆)=化学计量系数之比二、化学平衡状态3、化学平衡的状态的标志:(1)直接标志:①含量关系:各组分含量保持一定定含量一定:各组分物质的量(分数),质量(分数),气体的体积(分数)保持不变区分陷阱:
平衡时浓度变化之比等于化学计量系数之比?二、化学平衡状态3、化学平衡的状态的标志:(2)间接标志:即从变到不变(技巧)反应过程中如果哪个量在变,一旦它
不变了,就可以作为判断化学反应达
到平衡的状态。二、化学平衡状态3、化学平衡的状态的标志:(2)间接标志:即从变到不变(技巧)恒V时,对于反应 (1)2SO2(g)+O2 (g) 2SO3 (g)
(2)I2(g)+H2(g) 2HI(g)
气体的总压强、总物质的量、平衡相对分子质量、密度、颜色、温度保持不变能否作为可逆反应达到平衡的标志?①速率:v正=v逆
②各组分的浓度保持不变
③变的不再变(在化学反应进行过程中变化
的量,达到平衡时就不再变化了)二、化学平衡状态3、化学反应达到平衡状态的标志:(小结)直接间接《学案》P28 例2 P29 变3、变4 在一定温度下的恒容容器中,当下列物理量不再发生变化时,表明反应: A(固)+3B(气) 2C(气)+D(气)已达平衡状态的是 ( )
A.混合气体的压强 B.混合气体的密度
C.B的物质的量浓度 D.气体的总物质的量
BC《学案》P29 课时5 课时8 《学案》P29 课时2、 3、 4、 7 在一定温度下,下列叙述不是可逆反应
A(气)+3B(气) 2C(气)+2D(固)达到平衡的标志的是 ( )
①C的生成 速率与C的分解速率相等
②单位时间内生成amolA,同时生成3amolB
③A、B、C的浓度不再变化
④A、B、C的百分含量不在变化
⑤混合气体的总压强不再变化
⑥混合气体的物质的量不再变化
⑦单位时间内消耗amolA,同时生成 3amolB
⑧A、B、C、D的分子数之比为1:3:2:2
A.②⑧ B.②⑤⑧
C.①③④⑦ D.②⑤⑥⑧A小结一、可逆反应
二、化学平衡状态
1.定义
2.特征
3.判定例题精析【例2】可逆反应:2NO2 2NO+O2,在固定容积的密闭容器中达到平衡的标志是 ( )①单位时间内生成n molO2的同时生成2 n molNO2②单位时间内生成n molO2的同时生成2 n molNO⑦用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2:1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态⑥混合气体的平均相对分子质量不再改变的状态 ①③④⑥③NO2物质的量浓度不变例题精析【例3】可逆反应CO(g)+H2O(g) CO2(g)+H2(g),在固定容积的密闭容器中达到平衡的标志是 ( )①单位时间内生成n molCO2的同时生成n molCO④混合气体的密度不再改变的状态③混合气体的平均相对分子质量不再改变的状态①②②CO、H2O、CO2、H2浓度都不再发生变化
