九年级人教化学下 9.2 溶解度 课件(共35张PPT)
文档属性
| 名称 | 九年级人教化学下 9.2 溶解度 课件(共35张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-02-20 00:00:00 | ||
图片预览









文档简介
课件35张PPT。3.溶液的组成--- 溶剂、溶质1.溶液的定义--- 一种或几种扩散到另外一种2.溶液的特征--- 均一、稳定、混合物4.洗涤剂除油污的原理---- 乳化现象5.汽油除油污的原理---- 相似相溶6.溶于水后使液体温度升高的物质有: ; 降温的有 。温故而知新:复习1、写出下列溶液中溶质的化学式:
1、食盐水 ;2、盐酸 ;
3、澄清石灰水 ;
4、稀硫酸 ; 碘酒 ;
5、酒精溶液 ;
6、硝酸铜和硝酸银的混合溶液 ;NaClHClCa(OH)2H2SO4C2H5OHI2Cu(NO3)2、AgNO3教 学 目 录阅读教材P33,实验9-5,思考: 一杯水是不是可以无限的溶解溶质呢? 在常温下,向装有20ml水的烧杯中加入5g氯化钠,搅拌,等氯化钠溶解后,再加入5g,搅拌,观察现象。然后再加入10ml水,搅拌,观察现象。全部溶解部分不溶部分不溶NaCl
又能溶解5gNaCl能溶解
在20mL水中10gNaCl不能
全部溶解加入溶剂,此溶液
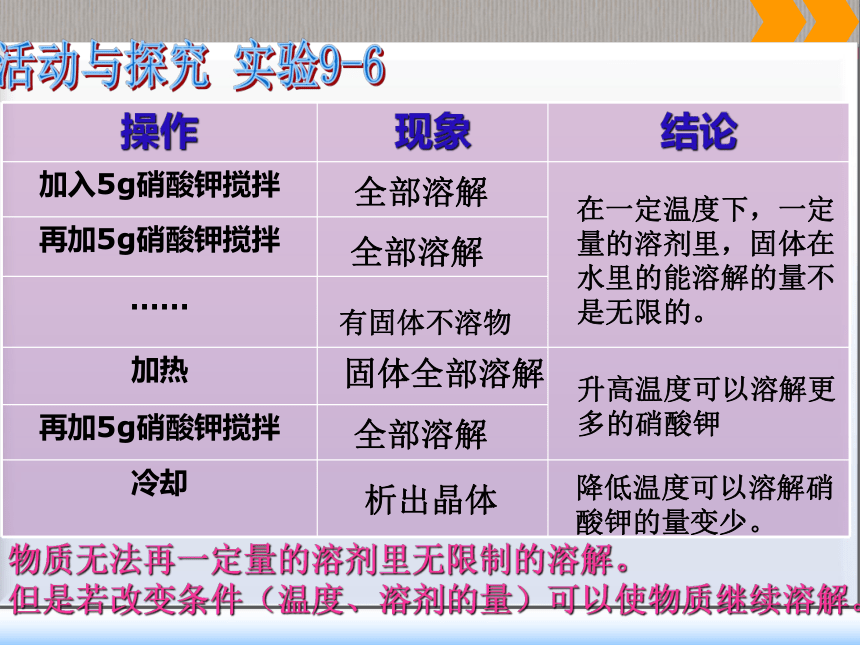
又能继续溶解溶质全部溶解在一定温度下,一定量的溶剂里,固体在水里的能溶解的量不是无限的。有固体不溶物全部溶解析出晶体固体全部溶解全部溶解升高温度可以溶解更多的硝酸钾降低温度可以溶解硝酸钾的量变少。活动与探究 实验9-6物质无法再一定量的溶剂里无限制的溶解。
但是若改变条件(温度、溶剂的量)可以使物质继续溶解。饱和溶液:在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,叫这种溶质的饱和溶液;
不饱和溶液:在一定温度下,在一定量的溶剂里,还能继续溶解某种溶质的溶液,叫这种溶质的不饱和溶液。饱和溶液二要素:“一定量的溶剂”和“一定温度下”
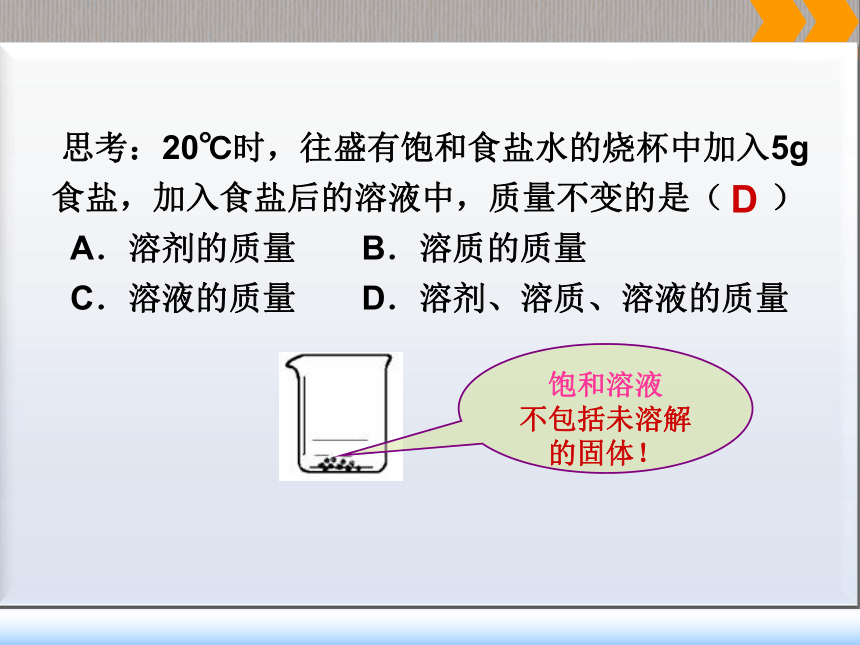
只有在指明“一定量的溶剂”和“在一定温度下”,饱和和不饱和才有确定的意义。如20℃时,100g水中溶解了31.6g硝酸钾达到饱和,若升高温度或增大溶剂的量,原来饱和的溶液就变不饱和了。 思考:20℃时,往盛有饱和食盐水的烧杯中加入5g食盐,加入食盐后的溶液中,质量不变的是( )
A.溶剂的质量 B.溶质的质量
C.溶液的质量 D.溶剂、溶质、溶液的质量饱和溶液
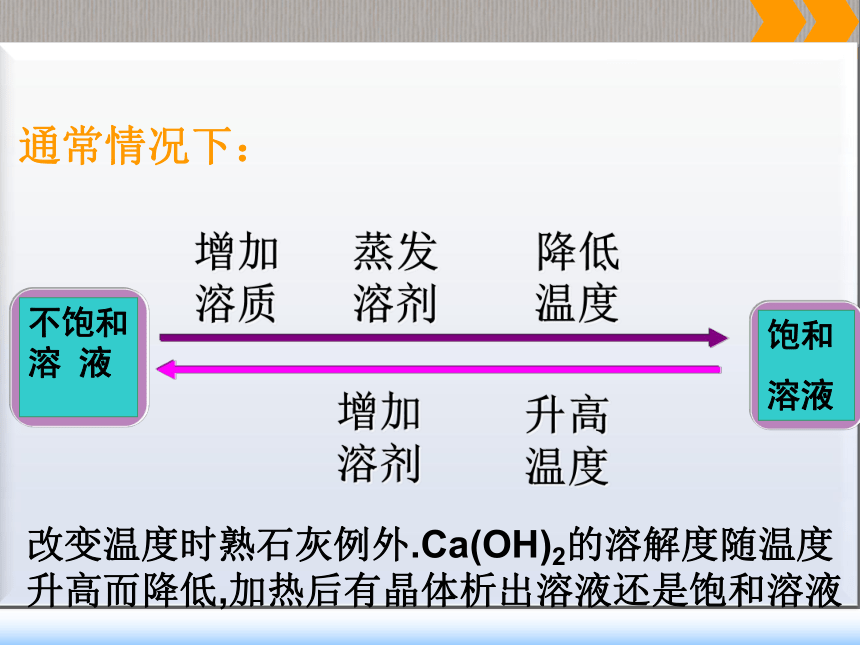
不包括未溶解的固体!D思考:有一瓶接近饱和的硝酸钾溶液,欲使其成为饱和溶液,可采用的方法有哪些?加入溶质、蒸发溶剂、降低温度加入硝酸钾、蒸发掉一些水、降低温度思考:将硝酸钾的饱和溶液配成不饱和溶液,可采用的方法有哪些? 增加溶剂、升高温度 5克硝酸钾20毫升水中加入饱和溶液不饱和溶液不饱和溶液通常情况下:增加溶质蒸发溶剂增加溶剂升高温度降低温度改变温度时熟石灰例外.Ca(OH)2的溶解度随温度升高而降低,加热后有晶体析出溶液还是饱和溶液饱和溶液降低温度会出现什么样的状况呢?还是饱和溶液吗?硝酸钾晶体结晶: 热的饱和溶液冷却后,溶质以晶体的形式析出。阅读教材P35,思考:
1.除了用冷却热的饱和溶液之外,还有什么方法获得晶体?
2.用海水晒盐有哪些过程?
3.生活中常说了苦卤指的是?为什么采用饱和氯化钠溶液反复冲洗粗盐,可以除去粗盐中的氯化钙、氯化镁等杂质,达到精制食盐的目的?1、饱和溶液是指 ( )A、浓度较大的溶液 B、还能继续溶解某种溶质的溶液C、不能再溶解某种溶质的溶液D、在一定的温度下,在一定量的溶剂中不能再继续溶解某种溶质的溶液D2、在一定的温度下,使固体物质的不饱和溶液变为饱和溶液一定能成功的方法是( )A.降低温度 B.升高温度
C.加入溶剂 D.蒸发溶剂D饱和溶液与不饱和溶液之间的转化方法:饱和
溶液不饱和溶液增加
溶剂升高
温度增加
溶质蒸发
溶剂降低
温度改变温度时熟石灰例外判断题 1.饱和溶液升高温度后变为不饱和溶液。
2、溶液降温析出晶体后,剩余的溶液还是饱和溶液。
3.同一种溶质的饱和溶液比不饱和溶液的溶质的质量分数大; ×√×现有下列方法:
1、升高温度 2、降低温度 3、增加硝酸钾 4、减少硝酸钾 5、增加水 6、蒸发水,能用来将硝酸钾不饱和溶液转化为饱和溶液的是( )A、1 3 6 B、2 3 6 C、1 3 5 D、2 4 6B溶解性:与溶质和溶剂的性质、及温度有关影响因素:一种物质溶解在另一种物质的能力表示方法:溶解性能力的大小常用溶解度来表示溶解度:在一定的温度下,某物质在100g溶剂里达到饱和状态下所溶解的质量。
注释:如果说不指名溶剂,通常所说的溶解度是指物质在水里的溶解度。1.定义: 在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度(符号S)。一定温度100克溶剂 (一般指水)饱和状态质量 (克)2.固体的溶解度的四要素:例:在20℃时,硝酸钾的溶解度是31.6g。在20℃时,100g水中最多可溶解溶质的质量为31.6g。在20℃时,100g水中溶解31.6g硝酸钾,溶液达到饱和。(主要受温度影响)从溶解度获得信息:1.在20℃时,36.0g的NaCl在100g中溶解达到饱和状态。
2.在20℃时,100g水中最多能溶解溶质36.0gNaCl。
3.溶剂的质量为100g,溶质的质量为36.0g,溶液的质量为136.0g。
4.此时的NaCl溶液是饱和的。溶解的程度为易溶。
5.溶质的质量分数为:36g/136g x 100%=26.5%在20℃时,食盐的溶解度(S)为36g.2、溶解度与溶解性的关系易溶 可溶 微溶 难(不)溶 >10g1g~10g
0.01~1g<0.01g 难(不)溶 微溶 可溶 易溶 1.不溶物就是绝对不溶于水的物质。此话是否正确? 2.20℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是___溶物质。 3.20℃时氯化钠的溶解度是36g,则氯化钠属于( )
A.易溶物质 B.可溶物质 C.微溶物质 D.难溶物质 DA例:判断正误:
1.l00g水中最多溶解38g氯化钠,所以氯化钠在水中的溶解度是38g。( )
2.在10℃时,烧杯内水中最多溶有140g硝酸铵,所以硝酸铵在水中的溶解度是140g。( )
3.在60℃,100g水中溶有75g硝酸钾,所以60℃时硝酸钾的溶解度为75g。( )
4.60℃,100g水中最多溶解124g硝酸钾,所以硝酸钾在这温度下的溶解度是124。( )××××缺少:溶剂缺少:达到饱和缺少:温度缺少:单位几种物质在不同温度时的溶解度.....硝酸钾.....A31.620.945.863.985.511013816820224613.303、溶解度的表示方法:(1)列表法:硝酸钾在不同温度时的溶解度(2)溶解度曲线.B溶解度(温度(℃)1601501401301201101009080706050403020102001901801701010090807060504030200硝酸铵硝酸钾硝酸钠氯化铵氯化钠硼酸几种物质的溶解度曲线.a从这些溶解度曲线图你能获取哪些信息?熟石灰的溶解度曲线溶解度(温度(℃)1601501401301201101009080706050403020102001901801701010090807060504030200硝酸铵硝酸钾硝酸钠氯化铵氯化钠硼酸几种物质的溶解度曲线.a1.同种物质在不同温度下的溶解度不同。2.曲线的交点表示这两种物质在该温度下的溶解度相同。3.曲线越陡,该物质的溶解度受温度影响越大。100硼酸硝酸 铵硝酸钠硝酸钾氯化铵氯化钾氯化钠6070501020304080901001101801701601501401301201902005010203040090607080温度/℃固体的溶解度曲线:1.横坐标60,纵坐标110 的交点表示什么意义? 练习:A..2.比较硝酸钠与硝酸钾的溶解度大小在680C时,NaNO3与KNO3的溶解度相等温度大于680C时, KNO3的溶解度大于NaNO3温度小于680C时,NaNO3的溶解度大于KNO3680C100硼酸硝酸铵硝酸钠硝酸钾氯化铵氯化钾氯化钠6070501020304080901001101801701601501401301201902005010203040090607080温度/℃固体的溶解度曲线:小于3.在40℃时,硝酸钾的溶解度__ __ (填大于、小于)硝酸钠的溶解。练习:4.在80℃时氯化钠、氯化钾、硼酸、氯化铵的溶解度由大到小的顺序是:
_____ __ __ _ 氯化铵、氯化钾、氯化钠、硼酸5.氯化钾、硝酸钾、硝酸铵中,哪一个受温度影响最大?哪一个最小最大:硝酸铵 最小:氯化钾0.050.100.150.2090704001020506080100300.050.100.150.209070400102050608010030温度/℃熟石灰的溶解度曲线:讨论:
固体物质溶解度受温度变化影响情况: 大多数固体物质溶解度随温度升高而增大,例如 硝酸钾等。 少数固体物质溶解度受温度影响不大,例如食盐。极少数固体物质溶解度随温度升高反而减小,例如熟石灰。1、如图是A、B、C三种物质在水中的溶解度曲线,请回答:
(1)M点的含义是_________________________
(2)当温度为t1oC,三种物质溶解度由小到大依次为_______,当温度为t3oC时,溶解度最大的是____.
(3)C可能表示哪种物质:
________________
A和C两种物质在t2oC时的溶解度相同C>A>BACa(OH)2或CO2等气体溶解度克温度(t)1601501401301201101009080706050403020102001901801701010090807060504030200硝酸钾氯化钠固体溶解度曲线的应用一、降温结晶
(又叫冷却热饱和溶液法)适用于溶解度随温度变化较大的物质(陡度较大)
分离NaCl和KNO3的混合物
1、先将混合物配成高温下的饱和溶液,再冷却,析出的晶体主要是 KNO3
2、过滤,主要得到KNO3晶体
3、蒸发滤液主要得到NaCl晶体。 二、蒸发溶剂法
(蒸发结晶)适用于溶解度随温度变化较小的物质(较为平缓)三、升温结晶
适用于溶解度随温度增大而减小的物质
给熟石灰的饱和溶液升高温度会有什么现象?
为什么?变浑浊,因为熟石灰的溶解度随温度升高而减小,升温后会有熟石灰固体析出固体溶解度曲线的应用注意:
思考类似题型的时候,一定要注意熟石灰【Ca(OH)2】这个特殊的例子!甲、乙两种固体的溶解度曲线如下图。现将两试管分别装入甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体),再放进盛有冰水的烧杯里, 则下列说
法正确的是................................( )
A.甲溶液中溶质的质量分数增大
B.乙溶液中剩余的固体减少
C.试管里甲、乙物质的溶解度都增大
D.试管里甲、乙两溶液中的溶质都减少
再放进盛有冰水的烧杯里, 则下列说
再放进盛有冰水的烧杯里, 则下列说
B右图是A.B两种物质的溶解度曲线,试回答下列问题
(1)t1oC时,A 的溶解度 B 的溶解度.(填< > 或=)
(2)A、B两物质饱和溶液溶质的质量分数相等的温度是 oC。
(3)当A、B两物质的溶液接近饱和时,采用增加溶质、蒸发溶剂、降低温度的方法可以达到饱和的是 物质的溶液。
1、食盐水 ;2、盐酸 ;
3、澄清石灰水 ;
4、稀硫酸 ; 碘酒 ;
5、酒精溶液 ;
6、硝酸铜和硝酸银的混合溶液 ;NaClHClCa(OH)2H2SO4C2H5OHI2Cu(NO3)2、AgNO3教 学 目 录阅读教材P33,实验9-5,思考: 一杯水是不是可以无限的溶解溶质呢? 在常温下,向装有20ml水的烧杯中加入5g氯化钠,搅拌,等氯化钠溶解后,再加入5g,搅拌,观察现象。然后再加入10ml水,搅拌,观察现象。全部溶解部分不溶部分不溶NaCl
又能溶解5gNaCl能溶解
在20mL水中10gNaCl不能
全部溶解加入溶剂,此溶液
又能继续溶解溶质全部溶解在一定温度下,一定量的溶剂里,固体在水里的能溶解的量不是无限的。有固体不溶物全部溶解析出晶体固体全部溶解全部溶解升高温度可以溶解更多的硝酸钾降低温度可以溶解硝酸钾的量变少。活动与探究 实验9-6物质无法再一定量的溶剂里无限制的溶解。
但是若改变条件(温度、溶剂的量)可以使物质继续溶解。饱和溶液:在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,叫这种溶质的饱和溶液;
不饱和溶液:在一定温度下,在一定量的溶剂里,还能继续溶解某种溶质的溶液,叫这种溶质的不饱和溶液。饱和溶液二要素:“一定量的溶剂”和“一定温度下”
只有在指明“一定量的溶剂”和“在一定温度下”,饱和和不饱和才有确定的意义。如20℃时,100g水中溶解了31.6g硝酸钾达到饱和,若升高温度或增大溶剂的量,原来饱和的溶液就变不饱和了。 思考:20℃时,往盛有饱和食盐水的烧杯中加入5g食盐,加入食盐后的溶液中,质量不变的是( )
A.溶剂的质量 B.溶质的质量
C.溶液的质量 D.溶剂、溶质、溶液的质量饱和溶液
不包括未溶解的固体!D思考:有一瓶接近饱和的硝酸钾溶液,欲使其成为饱和溶液,可采用的方法有哪些?加入溶质、蒸发溶剂、降低温度加入硝酸钾、蒸发掉一些水、降低温度思考:将硝酸钾的饱和溶液配成不饱和溶液,可采用的方法有哪些? 增加溶剂、升高温度 5克硝酸钾20毫升水中加入饱和溶液不饱和溶液不饱和溶液通常情况下:增加溶质蒸发溶剂增加溶剂升高温度降低温度改变温度时熟石灰例外.Ca(OH)2的溶解度随温度升高而降低,加热后有晶体析出溶液还是饱和溶液饱和溶液降低温度会出现什么样的状况呢?还是饱和溶液吗?硝酸钾晶体结晶: 热的饱和溶液冷却后,溶质以晶体的形式析出。阅读教材P35,思考:
1.除了用冷却热的饱和溶液之外,还有什么方法获得晶体?
2.用海水晒盐有哪些过程?
3.生活中常说了苦卤指的是?为什么采用饱和氯化钠溶液反复冲洗粗盐,可以除去粗盐中的氯化钙、氯化镁等杂质,达到精制食盐的目的?1、饱和溶液是指 ( )A、浓度较大的溶液 B、还能继续溶解某种溶质的溶液C、不能再溶解某种溶质的溶液D、在一定的温度下,在一定量的溶剂中不能再继续溶解某种溶质的溶液D2、在一定的温度下,使固体物质的不饱和溶液变为饱和溶液一定能成功的方法是( )A.降低温度 B.升高温度
C.加入溶剂 D.蒸发溶剂D饱和溶液与不饱和溶液之间的转化方法:饱和
溶液不饱和溶液增加
溶剂升高
温度增加
溶质蒸发
溶剂降低
温度改变温度时熟石灰例外判断题 1.饱和溶液升高温度后变为不饱和溶液。
2、溶液降温析出晶体后,剩余的溶液还是饱和溶液。
3.同一种溶质的饱和溶液比不饱和溶液的溶质的质量分数大; ×√×现有下列方法:
1、升高温度 2、降低温度 3、增加硝酸钾 4、减少硝酸钾 5、增加水 6、蒸发水,能用来将硝酸钾不饱和溶液转化为饱和溶液的是( )A、1 3 6 B、2 3 6 C、1 3 5 D、2 4 6B溶解性:与溶质和溶剂的性质、及温度有关影响因素:一种物质溶解在另一种物质的能力表示方法:溶解性能力的大小常用溶解度来表示溶解度:在一定的温度下,某物质在100g溶剂里达到饱和状态下所溶解的质量。
注释:如果说不指名溶剂,通常所说的溶解度是指物质在水里的溶解度。1.定义: 在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度(符号S)。一定温度100克溶剂 (一般指水)饱和状态质量 (克)2.固体的溶解度的四要素:例:在20℃时,硝酸钾的溶解度是31.6g。在20℃时,100g水中最多可溶解溶质的质量为31.6g。在20℃时,100g水中溶解31.6g硝酸钾,溶液达到饱和。(主要受温度影响)从溶解度获得信息:1.在20℃时,36.0g的NaCl在100g中溶解达到饱和状态。
2.在20℃时,100g水中最多能溶解溶质36.0gNaCl。
3.溶剂的质量为100g,溶质的质量为36.0g,溶液的质量为136.0g。
4.此时的NaCl溶液是饱和的。溶解的程度为易溶。
5.溶质的质量分数为:36g/136g x 100%=26.5%在20℃时,食盐的溶解度(S)为36g.2、溶解度与溶解性的关系易溶 可溶 微溶 难(不)溶 >10g1g~10g
0.01~1g<0.01g 难(不)溶 微溶 可溶 易溶 1.不溶物就是绝对不溶于水的物质。此话是否正确? 2.20℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是___溶物质。 3.20℃时氯化钠的溶解度是36g,则氯化钠属于( )
A.易溶物质 B.可溶物质 C.微溶物质 D.难溶物质 DA例:判断正误:
1.l00g水中最多溶解38g氯化钠,所以氯化钠在水中的溶解度是38g。( )
2.在10℃时,烧杯内水中最多溶有140g硝酸铵,所以硝酸铵在水中的溶解度是140g。( )
3.在60℃,100g水中溶有75g硝酸钾,所以60℃时硝酸钾的溶解度为75g。( )
4.60℃,100g水中最多溶解124g硝酸钾,所以硝酸钾在这温度下的溶解度是124。( )××××缺少:溶剂缺少:达到饱和缺少:温度缺少:单位几种物质在不同温度时的溶解度.....硝酸钾.....A31.620.945.863.985.511013816820224613.303、溶解度的表示方法:(1)列表法:硝酸钾在不同温度时的溶解度(2)溶解度曲线.B溶解度(温度(℃)1601501401301201101009080706050403020102001901801701010090807060504030200硝酸铵硝酸钾硝酸钠氯化铵氯化钠硼酸几种物质的溶解度曲线.a从这些溶解度曲线图你能获取哪些信息?熟石灰的溶解度曲线溶解度(温度(℃)1601501401301201101009080706050403020102001901801701010090807060504030200硝酸铵硝酸钾硝酸钠氯化铵氯化钠硼酸几种物质的溶解度曲线.a1.同种物质在不同温度下的溶解度不同。2.曲线的交点表示这两种物质在该温度下的溶解度相同。3.曲线越陡,该物质的溶解度受温度影响越大。100硼酸硝酸 铵硝酸钠硝酸钾氯化铵氯化钾氯化钠6070501020304080901001101801701601501401301201902005010203040090607080温度/℃固体的溶解度曲线:1.横坐标60,纵坐标110 的交点表示什么意义? 练习:A..2.比较硝酸钠与硝酸钾的溶解度大小在680C时,NaNO3与KNO3的溶解度相等温度大于680C时, KNO3的溶解度大于NaNO3温度小于680C时,NaNO3的溶解度大于KNO3680C100硼酸硝酸铵硝酸钠硝酸钾氯化铵氯化钾氯化钠6070501020304080901001101801701601501401301201902005010203040090607080温度/℃固体的溶解度曲线:小于3.在40℃时,硝酸钾的溶解度__ __ (填大于、小于)硝酸钠的溶解。练习:4.在80℃时氯化钠、氯化钾、硼酸、氯化铵的溶解度由大到小的顺序是:
_____ __ __ _ 氯化铵、氯化钾、氯化钠、硼酸5.氯化钾、硝酸钾、硝酸铵中,哪一个受温度影响最大?哪一个最小最大:硝酸铵 最小:氯化钾0.050.100.150.2090704001020506080100300.050.100.150.209070400102050608010030温度/℃熟石灰的溶解度曲线:讨论:
固体物质溶解度受温度变化影响情况: 大多数固体物质溶解度随温度升高而增大,例如 硝酸钾等。 少数固体物质溶解度受温度影响不大,例如食盐。极少数固体物质溶解度随温度升高反而减小,例如熟石灰。1、如图是A、B、C三种物质在水中的溶解度曲线,请回答:
(1)M点的含义是_________________________
(2)当温度为t1oC,三种物质溶解度由小到大依次为_______,当温度为t3oC时,溶解度最大的是____.
(3)C可能表示哪种物质:
________________
A和C两种物质在t2oC时的溶解度相同C>A>BACa(OH)2或CO2等气体溶解度克温度(t)1601501401301201101009080706050403020102001901801701010090807060504030200硝酸钾氯化钠固体溶解度曲线的应用一、降温结晶
(又叫冷却热饱和溶液法)适用于溶解度随温度变化较大的物质(陡度较大)
分离NaCl和KNO3的混合物
1、先将混合物配成高温下的饱和溶液,再冷却,析出的晶体主要是 KNO3
2、过滤,主要得到KNO3晶体
3、蒸发滤液主要得到NaCl晶体。 二、蒸发溶剂法
(蒸发结晶)适用于溶解度随温度变化较小的物质(较为平缓)三、升温结晶
适用于溶解度随温度增大而减小的物质
给熟石灰的饱和溶液升高温度会有什么现象?
为什么?变浑浊,因为熟石灰的溶解度随温度升高而减小,升温后会有熟石灰固体析出固体溶解度曲线的应用注意:
思考类似题型的时候,一定要注意熟石灰【Ca(OH)2】这个特殊的例子!甲、乙两种固体的溶解度曲线如下图。现将两试管分别装入甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体),再放进盛有冰水的烧杯里, 则下列说
法正确的是................................( )
A.甲溶液中溶质的质量分数增大
B.乙溶液中剩余的固体减少
C.试管里甲、乙物质的溶解度都增大
D.试管里甲、乙两溶液中的溶质都减少
再放进盛有冰水的烧杯里, 则下列说
再放进盛有冰水的烧杯里, 则下列说
B右图是A.B两种物质的溶解度曲线,试回答下列问题
(1)t1oC时,A 的溶解度 B 的溶解度.(填< > 或=)
(2)A、B两物质饱和溶液溶质的质量分数相等的温度是 oC。
(3)当A、B两物质的溶液接近饱和时,采用增加溶质、蒸发溶剂、降低温度的方法可以达到饱和的是 物质的溶液。
同课章节目录
