九年级人教化学下8.2 金属的化学性质 课件(共26张PPT)
文档属性
| 名称 | 九年级人教化学下8.2 金属的化学性质 课件(共26张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 572.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-02-20 16:59:08 | ||
图片预览






文档简介
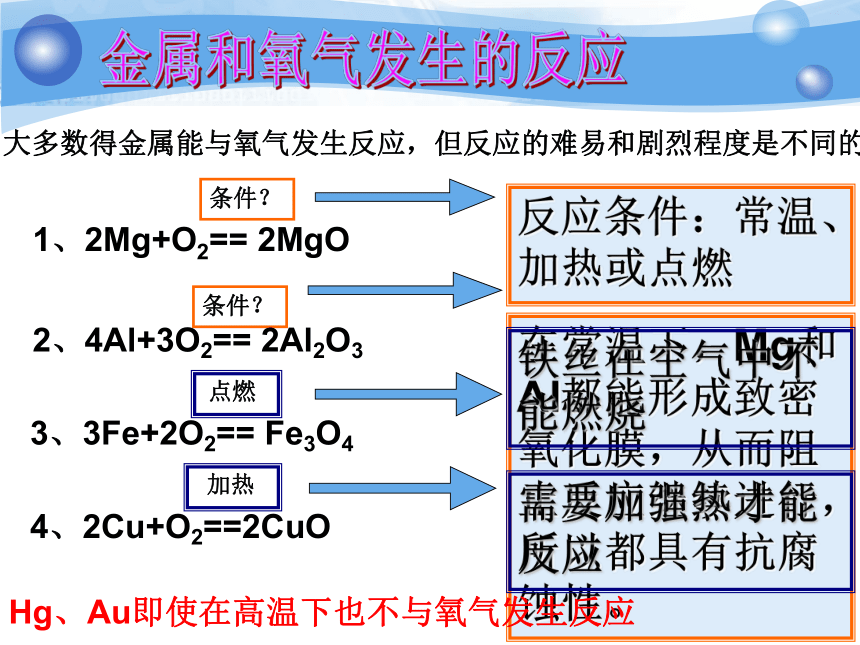
课件26张PPT。课题2 金属的化学性质主讲人:教学目录 Contents 点燃加热点燃点燃金属和氧气发生的反应大多数得金属能与氧气发生反应,但反应的难易和剧烈程度是不同的。金属和氧气发生的反应Hg、Au即使在高温下也不与氧气发生反应根据以上事实,我们可以判断出这些金属的活泼程度:
几种金属的活动性顺序:Mg>Al>Fe,Cu>Au
不同金属活泼性不同
▲ 在相同的条件下,金属与氧气反应
反应越容易,金属的活泼性越强,
反应越剧烈,金属的活泼性越强。
例如,铁(Fe)比铜(Cu)活泼,所以铁与氧气反应比铜氧气反应剧烈。
【思考】既然铝的化学性质很活泼,在常温下就能与氧气发生,为什么还可以用铝制作电线?在清洗铝制品时应注意些什么?
【回答】 铝制品是由于铝和空气中的氧气发生,在其表面生成一层致密的氧化膜,从而阻止铝的进一步氧化。在清洗铝制品的时候尽量不用钢刷,砂纸等擦洗,避免氧化铝膜被除掉。习题讲习下列叙述不正确的是( )
A.铝、镁在空气中与氧气反应,表面生成致密氧化膜。
B.金(Au)的性质不活泼,在高温也不与氧气反应。
C.镁在氧气中剧烈燃烧,发出耀眼白光,生成白色固体。
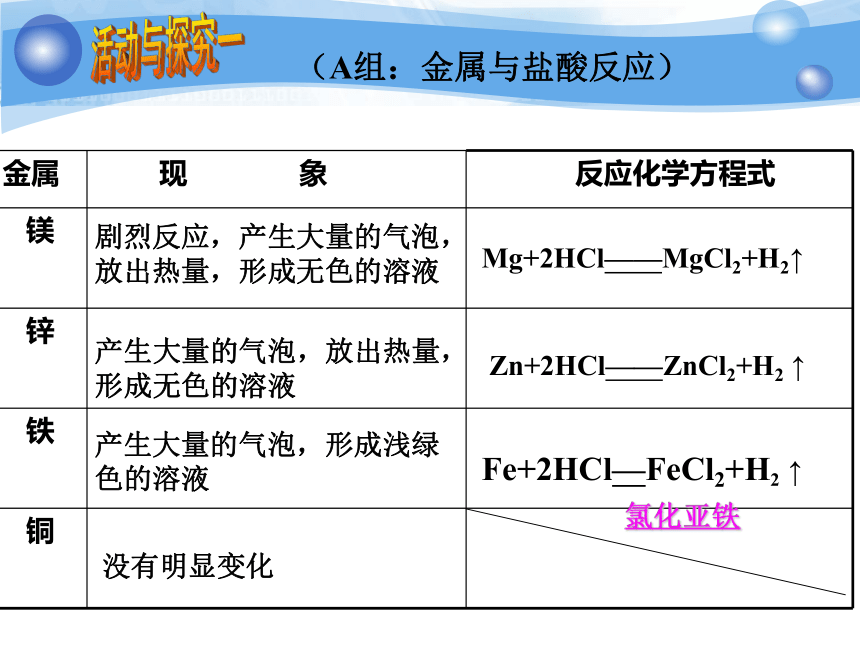
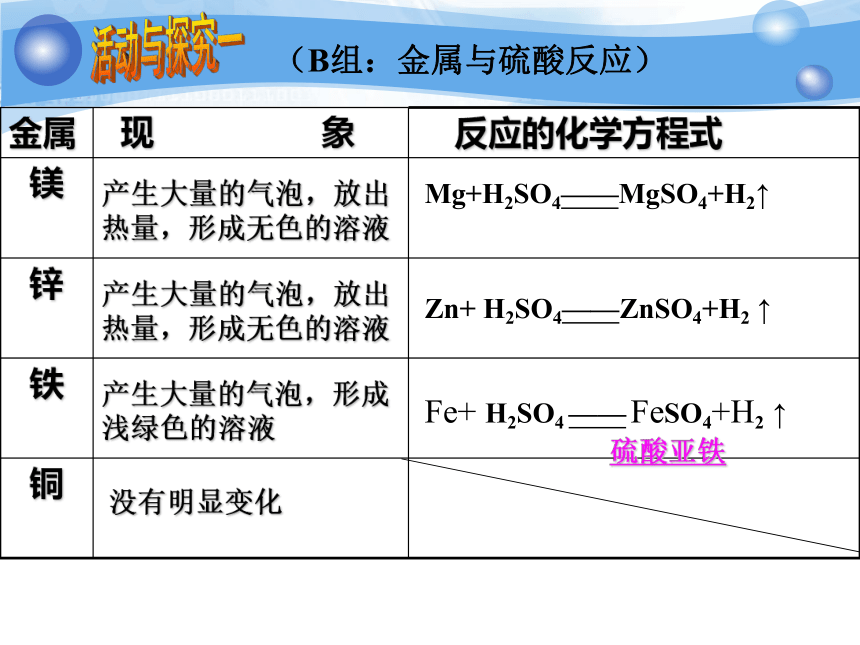
D.铁丝加热后放在氧气中,剧烈燃烧,生成Fe2O3固体。活动与探究一 在4支试管里分别放入两小块镁(Mg)、锌(Zn)、铁(Fe)、铜(Cu),再依次加入约占试管容积1/4的稀盐酸(或稀硫酸),仔细观察金属表面与溶液的变化,比较反应的剧烈程度。选择反应比较快的用燃着的小木条放在试管口,检验产生的气体。请记录实验现象。2.金属与盐酸(HCl)、稀硫酸(H2SO4)的反应(A组:金属与盐酸反应)剧烈反应,产生大量的气泡,放出热量,形成无色的溶液Mg+2HCl——MgCl2+H2↑Zn+2HCl——ZnCl2+H2 ↑Fe+2HCl—FeCl2+H2 ↑没有明显变化产生大量的气泡,放出热量,形成无色的溶液产生大量的气泡,形成浅绿色的溶液活动与探究一氯化亚铁(B组:金属与硫酸反应)Mg+H2SO4——MgSO4+H2↑Zn+ H2SO4——ZnSO4+H2 ↑Fe+ H2SO4 —— FeSO4+H2 ↑产生大量的气泡,放出热量,形成无色的溶液产生大量的气泡,放出热量,形成无色的溶液产生大量的气泡,形成浅绿色的溶液没有明显变化活动与探究一硫酸亚铁镁、锌、铁、铜与盐酸的反应MgZnFeCu小黑点表表产生的气泡小意思,我撑得住!God
Save me!为什么受伤的总是我!我得意的笑,
得意的笑…置换反应从反应物和生成物的角度分析,这些反应有何特点?将这一类反应与化合反应、分解反应进行比较。
置换反应单质 + 化合物 == 另化合物 + 另单质
A + BC == AC + B置换反应(2)金属置换金属 Fe+CuSO4=Cu+FeSO4
下列反应属于置换反应的是()
A.CO+CuO=Cu+CO2 B.SO2+2NaOH=Na2SO3+H2O
C.CaO+H2O=Ca(OH)2 D.Zn+CuSO4=ZnSO4+Cu
判断某化学反应是不是置换反应,要着眼于反应物和生成物的种类是否都是“一种单质和一种化合物”点燃MnO2习题精析1.(2013.上海)镁条在在二氧化碳中可以剧烈燃烧,生成白色固体,其化学方程式为:
2Mg+CO2=C+2MgO,该反应属于( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2.下列反应不属于置换反应的是( )
A.CH4+2O2=CO2+2H2O B.C+2CuO=2Cu+CO2
C.Zn+Cu(NO3)2=Zn(NO3)2+Cu D.C+H2O=H2+CO点燃点燃高温高温CA一.金属与氧气的反应(化合反应)二.金属与某些化合物溶液的反应(置换反应)Fe >H Fe>Cu 可以判断反应能否发生和金属活动性的强弱知识复习活动探究二提出问题:
铝、铜、银三种金属的活动性顺序的强弱铝表面覆盖一层红色的铜铜表面覆盖一层银白色的银2Al+3CuSO4=Al2(SO4)3+3CuCu+2AgNO3=Cu(NO3)2+2Ag没现象1.以上反应类型都属于 反应。
2.铝能够置换出硫酸铜溶液中的铜,铜能够置换出硝酸银溶液中的银,铜不能置换出硫酸铝中的铝。
3.铝、铜、汞三种金属的活动性顺序是:
置换Al > Cu >Ag铁与硫酸铜溶液的反应:
Fe+CuSO4==FeSO4+Cu结论:金属单质的活动性比金属化合物溶液中的金属元素的活动性强,才能把它从溶液中置换出来金属活动顺序钾 钙 钠 镁 铝 锌 铁 锡 铅 氢 铜 汞 银 铂 金
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
金属活动性由强逐渐减弱1.在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。
2.在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢。
【氢前金属能置(置换)氢,氢后金属不反应】
3.在金属活动顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液中置换出来。 一般来说,发生置换反应时,金属活动性差异越大,越易进行;如把Fe投入到AgNO3、Cu(NO3)2混合溶液中,置换出金属的先后顺序是Ag、Cu。K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au优先置换原理:
若某一溶液中同时含有多种金属离子,则加入一种金属时,优先置换出金属活动性弱的金属的离子。例题讲习1.下列各组金属中,按金属活动性有强到弱顺序排列的是( )
A.Na、Fe、Mg B.K、Cu 、Fe
C.Ca、Ag、Zn D.Al、Zn、Hg
2.能用铁制容器盛放的试剂是( )
A.盐酸 B.硫酸 C.硫酸铜溶液 D.酒精
3.下列反应能否进行?写出能发生的反应方程式并判断他们是否是置换反应。
(1)银与稀盐酸 (2)锌与稀硫酸反应
(3)铜与硫酸锌溶液 (4)铝与硝酸银溶液DD(5)铜和稀硫酸√√XXX现有X、Y、Z三种金属,如果把X放在由金属Y组成的溶液中,能置换金属Y,则金属活动性X Y;如果把金属Y放在由金属Z组成的溶液中,能置换出金属Z,则金属活动性Y Z;由此可以推断金属活动性,X Y Z。若把金属XYZ都投入到稀硫酸中,只有Z不发生反应,则X、Y、Z与氢元素(H)的活动性为:
现有X、Y、Z三种金属,如果把X、Y分别投入到稀盐酸中,只有Y溶解并产生气泡,则金属活动性X Y;如果把X和Z投入到硝酸银溶液中,过一会,在X表面有金属Ag析出,而Z没有变化,则金属活动性X Z;由此可以推断出X、Y、Z的金属活动性顺序为:
你还能推断出X、Y、Z与 H、Ag的顺序吗?
>>>>X >Y>(H)>Z <> Y>X>Z Y>(H)>X>Ag>Z能力提升W g铁与足量的稀硫酸充分反应生成a g氢气,W g锌与足量的稀盐酸反应充分反应生成b g氢气,则a与b的关系是( )
A. a>b B. a往AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。根据上诉实验现象,你得出的结论是
A.滤渣中一定有铁粉
B.滤渣中一定有铜粉
C.滤液中一定有Fe2+
D.滤液中一定有Ag+、Cu2+Thank You !
几种金属的活动性顺序:Mg>Al>Fe,Cu>Au
不同金属活泼性不同
▲ 在相同的条件下,金属与氧气反应
反应越容易,金属的活泼性越强,
反应越剧烈,金属的活泼性越强。
例如,铁(Fe)比铜(Cu)活泼,所以铁与氧气反应比铜氧气反应剧烈。
【思考】既然铝的化学性质很活泼,在常温下就能与氧气发生,为什么还可以用铝制作电线?在清洗铝制品时应注意些什么?
【回答】 铝制品是由于铝和空气中的氧气发生,在其表面生成一层致密的氧化膜,从而阻止铝的进一步氧化。在清洗铝制品的时候尽量不用钢刷,砂纸等擦洗,避免氧化铝膜被除掉。习题讲习下列叙述不正确的是( )
A.铝、镁在空气中与氧气反应,表面生成致密氧化膜。
B.金(Au)的性质不活泼,在高温也不与氧气反应。
C.镁在氧气中剧烈燃烧,发出耀眼白光,生成白色固体。
D.铁丝加热后放在氧气中,剧烈燃烧,生成Fe2O3固体。活动与探究一 在4支试管里分别放入两小块镁(Mg)、锌(Zn)、铁(Fe)、铜(Cu),再依次加入约占试管容积1/4的稀盐酸(或稀硫酸),仔细观察金属表面与溶液的变化,比较反应的剧烈程度。选择反应比较快的用燃着的小木条放在试管口,检验产生的气体。请记录实验现象。2.金属与盐酸(HCl)、稀硫酸(H2SO4)的反应(A组:金属与盐酸反应)剧烈反应,产生大量的气泡,放出热量,形成无色的溶液Mg+2HCl——MgCl2+H2↑Zn+2HCl——ZnCl2+H2 ↑Fe+2HCl—FeCl2+H2 ↑没有明显变化产生大量的气泡,放出热量,形成无色的溶液产生大量的气泡,形成浅绿色的溶液活动与探究一氯化亚铁(B组:金属与硫酸反应)Mg+H2SO4——MgSO4+H2↑Zn+ H2SO4——ZnSO4+H2 ↑Fe+ H2SO4 —— FeSO4+H2 ↑产生大量的气泡,放出热量,形成无色的溶液产生大量的气泡,放出热量,形成无色的溶液产生大量的气泡,形成浅绿色的溶液没有明显变化活动与探究一硫酸亚铁镁、锌、铁、铜与盐酸的反应MgZnFeCu小黑点表表产生的气泡小意思,我撑得住!God
Save me!为什么受伤的总是我!我得意的笑,
得意的笑…置换反应从反应物和生成物的角度分析,这些反应有何特点?将这一类反应与化合反应、分解反应进行比较。
置换反应单质 + 化合物 == 另化合物 + 另单质
A + BC == AC + B置换反应(2)金属置换金属 Fe+CuSO4=Cu+FeSO4
下列反应属于置换反应的是()
A.CO+CuO=Cu+CO2 B.SO2+2NaOH=Na2SO3+H2O
C.CaO+H2O=Ca(OH)2 D.Zn+CuSO4=ZnSO4+Cu
判断某化学反应是不是置换反应,要着眼于反应物和生成物的种类是否都是“一种单质和一种化合物”点燃MnO2习题精析1.(2013.上海)镁条在在二氧化碳中可以剧烈燃烧,生成白色固体,其化学方程式为:
2Mg+CO2=C+2MgO,该反应属于( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2.下列反应不属于置换反应的是( )
A.CH4+2O2=CO2+2H2O B.C+2CuO=2Cu+CO2
C.Zn+Cu(NO3)2=Zn(NO3)2+Cu D.C+H2O=H2+CO点燃点燃高温高温CA一.金属与氧气的反应(化合反应)二.金属与某些化合物溶液的反应(置换反应)Fe >H Fe>Cu 可以判断反应能否发生和金属活动性的强弱知识复习活动探究二提出问题:
铝、铜、银三种金属的活动性顺序的强弱铝表面覆盖一层红色的铜铜表面覆盖一层银白色的银2Al+3CuSO4=Al2(SO4)3+3CuCu+2AgNO3=Cu(NO3)2+2Ag没现象1.以上反应类型都属于 反应。
2.铝能够置换出硫酸铜溶液中的铜,铜能够置换出硝酸银溶液中的银,铜不能置换出硫酸铝中的铝。
3.铝、铜、汞三种金属的活动性顺序是:
置换Al > Cu >Ag铁与硫酸铜溶液的反应:
Fe+CuSO4==FeSO4+Cu结论:金属单质的活动性比金属化合物溶液中的金属元素的活动性强,才能把它从溶液中置换出来金属活动顺序钾 钙 钠 镁 铝 锌 铁 锡 铅 氢 铜 汞 银 铂 金
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
金属活动性由强逐渐减弱1.在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。
2.在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢。
【氢前金属能置(置换)氢,氢后金属不反应】
3.在金属活动顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液中置换出来。 一般来说,发生置换反应时,金属活动性差异越大,越易进行;如把Fe投入到AgNO3、Cu(NO3)2混合溶液中,置换出金属的先后顺序是Ag、Cu。K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au优先置换原理:
若某一溶液中同时含有多种金属离子,则加入一种金属时,优先置换出金属活动性弱的金属的离子。例题讲习1.下列各组金属中,按金属活动性有强到弱顺序排列的是( )
A.Na、Fe、Mg B.K、Cu 、Fe
C.Ca、Ag、Zn D.Al、Zn、Hg
2.能用铁制容器盛放的试剂是( )
A.盐酸 B.硫酸 C.硫酸铜溶液 D.酒精
3.下列反应能否进行?写出能发生的反应方程式并判断他们是否是置换反应。
(1)银与稀盐酸 (2)锌与稀硫酸反应
(3)铜与硫酸锌溶液 (4)铝与硝酸银溶液DD(5)铜和稀硫酸√√XXX现有X、Y、Z三种金属,如果把X放在由金属Y组成的溶液中,能置换金属Y,则金属活动性X Y;如果把金属Y放在由金属Z组成的溶液中,能置换出金属Z,则金属活动性Y Z;由此可以推断金属活动性,X Y Z。若把金属XYZ都投入到稀硫酸中,只有Z不发生反应,则X、Y、Z与氢元素(H)的活动性为:
现有X、Y、Z三种金属,如果把X、Y分别投入到稀盐酸中,只有Y溶解并产生气泡,则金属活动性X Y;如果把X和Z投入到硝酸银溶液中,过一会,在X表面有金属Ag析出,而Z没有变化,则金属活动性X Z;由此可以推断出X、Y、Z的金属活动性顺序为:
你还能推断出X、Y、Z与 H、Ag的顺序吗?
>>>>X >Y>(H)>Z <> Y>X>Z Y>(H)>X>Ag>Z能力提升W g铁与足量的稀硫酸充分反应生成a g氢气,W g锌与足量的稀盐酸反应充分反应生成b g氢气,则a与b的关系是( )
A. a>b B. a往AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。根据上诉实验现象,你得出的结论是
A.滤渣中一定有铁粉
B.滤渣中一定有铜粉
C.滤液中一定有Fe2+
D.滤液中一定有Ag+、Cu2+Thank You !
同课章节目录
