黑龙江省龙东联盟2024-2025学年高三上学期10月月考试题 化学 (PDF版含解析)
文档属性
| 名称 | 黑龙江省龙东联盟2024-2025学年高三上学期10月月考试题 化学 (PDF版含解析) |  | |
| 格式 | |||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-12 11:49:09 | ||
图片预览

文档简介
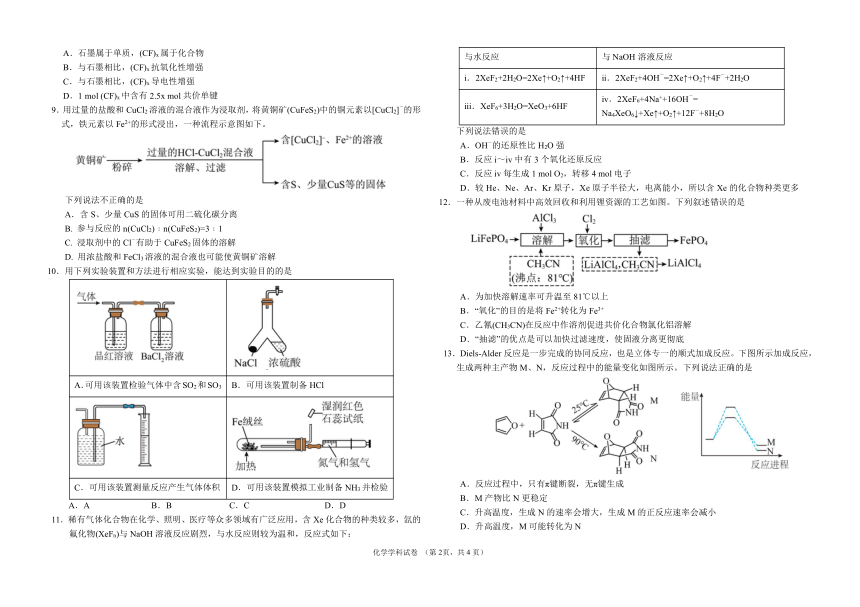
4.下列方程式与所给事实不相符的是
“龙东联盟”2022 级高三学年上学期 10 月月考试题
A - -.海水提溴过程中,用氯气氧化苦卤得到溴单质:2Br +Cl2=2Cl +Br2
B.铅酸蓄电池充电时的阳极反应:Pb2++2H2O-2e-=PbO +4H+(化学学科) 2
C.TiCl4加入水中:TiCl4+(x+2)H2O=TiO2·xH -2O↓+4H++4Cl
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,考试结束后,将答题卡交回。 D.用 Na2CO3 溶液将水垢中的 CaSO4转化为 CaCO3:CaSO4+CO32-=CaCO3+SO -42
注意事项: 5.以 Na2SO4为原料制备 Na2S,理论上可用下列两个反应进行。
1.答题前,考生先将自己的姓名、准考证号码填写清楚,将条形码准确粘贴在考生信息条形
反应ⅰ:Na2SO4(s)=Na2S(s)+2O2(g) ΔH=+1011 kJ·mol-1 ΔS=+357 J·K-1·mol-1
码粘贴区。
反应ⅱ:Na2SO4(s)+4C(s)=Na2S(s)+4CO(g)
2.选择题必须使用 2B 铅笔填涂;非选择题必须使用 0.5 毫米黑色字迹的签字笔书写,字体工 NA为阿伏加德罗常数的值,下列说法不正确的是
整、笔迹清楚。 A.反应ⅰ需在高温下才能自发进行
3.请按照题号顺序在各题目的答题区域作答,超出答题区域书写的答案无效;在草稿纸、试 B.反应ⅰ中,每分解 142 g Na2SO4产生 44.8 L O2(标准状况)
题卷上答题无效。 C.由反应ⅰ、ⅱ分别制备 0.5 mol Na2S,转移电子数均为 4NA
4.保持卡面清洁,不得折叠,不要弄破、弄皱,不准使用涂改液、修正带、刮纸刀。 D.0.10 mol/L Na2S -溶液中含 S2 数目为 0.1NA
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 K-39 Br-80 6.在给定条件下,下列制备过程涉及的物质转化均可实现的是
第 I 卷(选择题,共 45 分) A.制备高纯硅:石英 盐酸 SiCl 氢气4 高纯硅
一、选择题(每小题只有一个正确选项,每小题 3 分,共 45 分) B.金属 Mg 制备:Mg OH 电解 盐 酸 MgCl2 2 溶液 Mg
1.文物见证历史,化学创造文明。下列文物据其主要成分不能与其他三项归为一类的是
A C.纯碱工业:饱和 NaCl(aq)
N H3和 CO 2 NaHCO3(s)
加 热 Na CO
.西汉皇后之玺 2 3
O H O
B.兽首玛瑙杯 D.硫酸工业: FeS 2 22 SO2 H2SO高温 4
C.唐瑞兽葡萄纹铜镜 7.破损的镀锌铁皮在氨水中发生电化学腐蚀,生成[Zn(NH3)4]2+和 H2,下列说法不正确的是
D.元釉下褐彩凤鸟纹荷叶盖陶罐 A.氨水浓度越大,腐蚀趋势越大
2.物质性质决定用途,下列两者对应关系错误的是 B.随着腐蚀的进行,溶液 pH 变大
A.石灰乳除去废气中二氧化硫,体现了 Ca(OH)2的碱性 C.铁电极上的电极反应式为:2NH +2e- -3 =2NH2 +H2↑
B.铝合金可用于制作门窗框架,体现了铝的硬度大、密度小 D.每生成标准状况下 224 mL H2,消耗 0.010 mol Zn
C.制作豆腐时添加石膏,体现了 CaSO4的难溶性 8.石墨与 F2 在 450℃反应,石墨层间插入 F 得到层状结构化合物(CF)x,该物质仍具润滑性,其单
D.用氨水配制银氨溶液,体现了 NH3的配位性 层局部结构如图所示。下列关于该化合物的说法不正确的是
3.固态的氧有多种形态,如淡蓝色、红色、粉红色、暗蓝色还有橙色等。下图为 O2 在超高压
下转化为平行六面体的红氧(O8)分子。下列说法错误的是
A.O2 和 O8 互为同素异形体
B.O8 中存在不同的氧氧键
C.O2 转化为 O8 是熵减反应
D.常压低温下 O8 能稳定存在
化学学科试卷 (第 1页,共 4 页)
{#{QQABbQKAogAAAIIAAAgCAwH4CEIQkACAAYgOBAAIoAAAiQFABCA=}#}
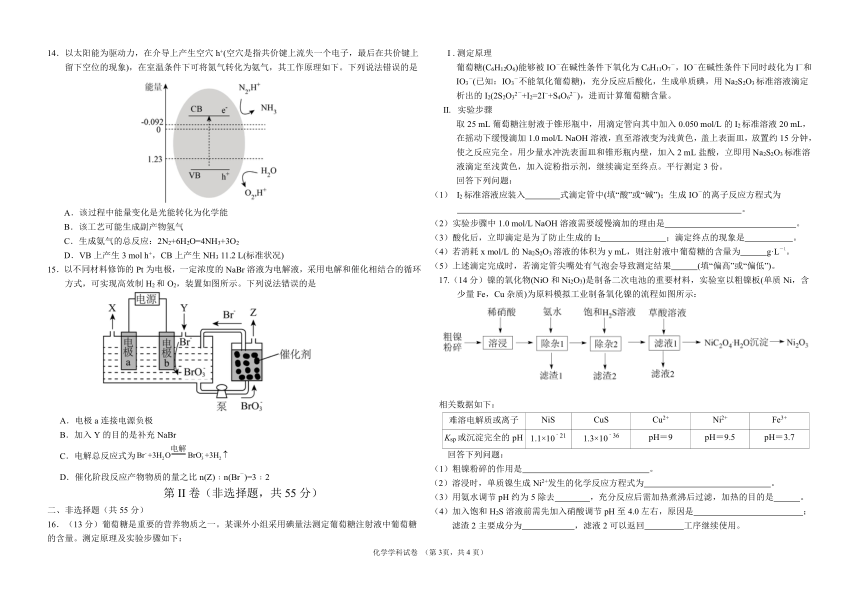
A.石墨属于单质,(CF)x 属于化合物 与水反应 与 NaOH 溶液反应
B.与石墨相比,(CF)x抗氧化性增强
- -
C.与石墨相比,(CF) 导电性增强 i.2XeF2+2H2O=2Xe↑+O2↑+4HF ii.2XeF2+4OH =2Xe↑+Ox 2↑+4F +2H2O
D.1 mol (CF)x中含有 2.5x mol 共价单键 iv.2XeF -6+4Na++16OH =
9.用过量的盐酸和 CuCl -溶液的混合液作为浸取剂,将黄铜矿(CuFeS )中的铜元素以[CuCl ] 的形 iii.XeF6+3H2O=XeO3+6HF2 2 2 Na4XeO6↓+Xe↑+O2↑+12F-+8H2O
式,铁元素以 Fe2+的形式浸出,一种流程示意图如下。
下列说法错误的是
A OH-. 的还原性比 H2O 强
B.反应 i~iv 中有 3 个氧化还原反应
C.反应 iv 每生成 1 mol O2,转移 4 mol 电子
D.较 He、Ne、Ar、Kr 原子,Xe 原子半径大,电离能小,所以含 Xe 的化合物种类更多
下列说法不正确的是 12.一种从废电池材料中高效回收和利用锂资源的工艺如图。下列叙述错误的是
A.含 S、少量 CuS 的固体可用二硫化碳分离
B. 参与反应的 n(CuCl2)﹕n(CuFeS2)=3﹕1
C. 浸取剂中的 Cl-有助于 CuFeS2固体的溶解
D. 用浓盐酸和 FeCl3溶液的混合液也可能使黄铜矿溶解
10.用下列实验装置和方法进行相应实验,能达到实验目的的是
A.为加快溶解速率可升温至 81℃以上
B.“氧化”的目的是将 Fe2+转化为 Fe3+
C.乙氰(CH3CN)在反应中作溶剂促进共价化合物氯化铝溶解
D.“抽滤”的优点是可以加快过滤速度,使固液分离更彻底
13.Diels-Alder 反应是一步完成的协同反应,也是立体专一的顺式加成反应。下图所示加成反应,
生成两种主产物 M、N,反应过程中的能量变化如图所示。下列说法正确的是
A.可用该装置检验气体中含SO2和SO3 B.可用该装置制备 HCl
C.可用该装置测量反应产生气体体积 D.可用该装置模拟工业制备 NH3并检验 A.反应过程中,只有π键断裂,无π键生成
B.M 产物比 N 更稳定
A.A B.B C.C D.D
C.升高温度,生成 N 的速率会增大,生成 M 的正反应速率会减小
11.稀有气体化合物在化学、照明、医疗等众多领域有广泛应用,含 Xe 化合物的种类较多,氙的
D.升高温度,M 可能转化为 N
氟化物(XeFn)与 NaOH 溶液反应剧烈,与水反应则较为温和,反应式如下:
化学学科试卷 (第 2页,共 4 页)
{#{QQABbQKAogAAAIIAAAgCAwH4CEIQkACAAYgOBAAIoAAAiQFABCA=}#}
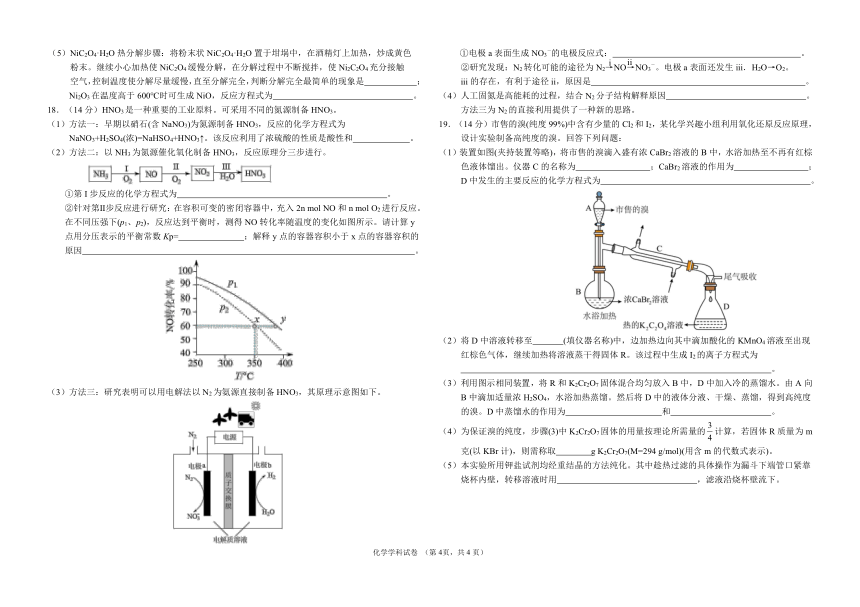
14.以太阳能为驱动力,在介导上产生空穴 h+(空穴是指共价键上流失一个电子,最后在共价键上 Ⅰ .测定原理
- - - -
留下空位的现象),在室温条件下可将氮气转化为氨气,其工作原理如下。下列说法错误的是 葡萄糖(C6H12O6)能够被 IO 在碱性条件下氧化为 C6H11O7 ,IO 在碱性条件下同时歧化为 I 和
IO - -3 (已知:IO3 不能氧化葡萄糖),充分反应后酸化,生成单质碘,用 Na2S2O3标准溶液滴定
析出的 I2(2S -2O32 +I2=2I +S4O62-),进而计算葡萄糖含量。
Ⅱ. 实验步骤
取 25 mL 葡萄糖注射液于锥形瓶中,用滴定管向其中加入 0.050 mol/L 的 I2标准溶液 20 mL,
在摇动下缓慢滴加 1.0 mol/L NaOH 溶液,直至溶液变为浅黄色,盖上表面皿,放置约 15 分钟,
使之反应完全。用少量水冲洗表面皿和锥形瓶内壁,加入 2 mL 盐酸,立即用 Na2S2O3标准溶
液滴定至浅黄色,加入淀粉指示剂,继续滴定至终点。平行测定 3 份。
回答下列问题:
(1) I2标准溶液应装入 式滴定管中(填“酸”或“碱”);生成 IO-的离子反应方程式为
A.该过程中能量变化是光能转化为化学能 。
B.该工艺可能生成副产物氢气 (2)实验步骤中 1.0 mol/L NaOH 溶液需要缓慢滴加的理由是 。
C.生成氨气的总反应:2N +6H O=4NH +3O (3)酸化后,立即滴定是为了防止生成的 I2 ;滴定终点的现象是 。2 2 3 2
-1
D.VB 上产生 3 mol h+,CB 上产生 NH 11.2 L(标准状况) (4)若消耗 x mol/L 的 Na2S2O3 溶液的体积为 y mL,则注射液中葡萄糖的含量为 g·L 。3
15.以不同材料修饰的 Pt 为电极,一定浓度的 NaBr 溶液为电解液,采用电解和催化相结合的循环 (5)上述滴定完成时,若滴定管尖嘴处有气泡会导致测定结果 (填“偏高”或“偏低”)。
方式,可实现高效制 H 和 O ,装置如图所示。下列说法错误的是 17.(14 分)镍的氧化物(NiO 和 Ni2O3)是制备二次电池的重要材料,实验室以粗镍板(单质 Ni,含2 2
少量 Fe,Cu 杂质)为原料模拟工业制备氧化镍的流程如图所示:
相关数据如下:
A.电极 a 连接电源负极 难溶电解质或离子 NiS CuS Cu2+ Ni2+ Fe3+
B.加入 Y 的目的是补充 NaBr Ksp 或沉淀完全的 pH 1.1×10﹣21 1.3×10﹣36 pH=9 pH=9.5 pH=3.7
C Br-
电解
+3H O BrO-.电解总反应式为 2 3 +3H2 回答下列问题:
(1)粗镍粉碎的作用是 。
D -.催化阶段反应产物物质的量之比 n(Z)﹕n(Br )=3﹕2
(2)溶浸时,单质镍生成 Ni2+发生的化学反应方程式为 。
第 II 卷(非选择题,共 55 分) (3)用氨水调节 pH 约为 5 除去 ,充分反应后需加热煮沸后过滤,加热的目的是 。
二、非选择题(共 55 分) (4)加入饱和 H2S 溶液前需先加入硝酸调节 pH 至 4.0 左右,原因是 ;
16.(13 分)葡萄糖是重要的营养物质之一。某课外小组采用碘量法测定葡萄糖注射液中葡萄糖 滤渣 2 主要成分为 ,滤液 2 可以返回 工序继续使用。
的含量。测定原理及实验步骤如下:
化学学科试卷 (第 3页,共 4 页)
{#{QQABbQKAogAAAIIAAAgCAwH4CEIQkACAAYgOBAAIoAAAiQFABCA=}#}
-
(5)NiC2O4·H2O 热分解步骤:将粉末状 NiC2O4·H2O 置于坩埚中,在酒精灯上加热,炒成黄色 ①电极 a 表面生成 NO3 的电极反应式: 。
i ii -
粉末。继续小心加热使 NiC2O4 缓慢分解,在分解过程中不断搅拌,使 Ni2C2O4充分接触 ②研究发现:N2 转化可能的途径为 N2→NO→NO3 。电极 a 表面还发生 iii.H2O→O2。
空气,控制温度使分解尽量缓慢,直至分解完全,判断分解完全最简单的现象是 ; iii 的存在,有利于途径 ii,原因是 。
Ni2O3在温度高于 600℃时可生成 NiO,反应方程式为 。 (4)人工固氮是高能耗的过程,结合 N2 分子结构解释原因 。
18.(14 分)HNO3是一种重要的工业原料。可采用不同的氮源制备 HNO3。 方法三为 N2 的直接利用提供了一种新的思路。
(1)方法一:早期以硝石(含 NaNO3)为氮源制备 HNO3,反应的化学方程式为 19.(14 分)市售的溴(纯度 99%)中含有少量的 Cl2和 I2,某化学兴趣小组利用氧化还原反应原理,
NaNO3+H2SO4(浓)=NaHSO4+HNO3↑。该反应利用了浓硫酸的性质是酸性和 。 设计实验制备高纯度的溴。回答下列问题:
(2)方法二:以 NH3为氮源催化氧化制备 HNO3,反应原理分三步进行。 (1)装置如图(夹持装置等略),将市售的溴滴入盛有浓 CaBr2溶液的 B 中,水浴加热至不再有红棕
色液体馏出。仪器 C 的名称为 ;CaBr2溶液的作用为 ;
D 中发生的主要反应的化学方程式为 。
①第 I 步反应的化学方程式为 。
②针对第Ⅱ步反应进行研究:在容积可变的密闭容器中,充入 2n mol NO 和 n mol O2 进行反应。
在不同压强下(p1、p2),反应达到平衡时,测得 NO 转化率随温度的变化如图所示。请计算 y
点用分压表示的平衡常数 Kp= ;解释 y 点的容器容积小于 x 点的容器容积的
原因 。
(2)将 D 中溶液转移至 (填仪器名称)中,边加热边向其中滴加酸化的 KMnO4 溶液至出现
红棕色气体,继续加热将溶液蒸干得固体 R。该过程中生成 I2的离子方程式为
。
(3)利用图示相同装置,将 R 和 K2Cr2O7 固体混合均匀放入 B 中,D 中加入冷的蒸馏水。由 A 向
(3)方法三:研究表明可以用电解法以 N2为氨源直接制备 HNO3,其原理示意图如下。 B 中滴加适量浓 H2SO4,水浴加热蒸馏。然后将 D 中的液体分液、干燥、蒸馏,得到高纯度
的溴。D 中蒸馏水的作用为 和 。
3
(4)为保证溴的纯度,步骤(3)中 K2Cr2O7固体的用量按理论所需量的 计算,若固体 R 质量为 m4
克(以 KBr 计),则需称取 g K2Cr2O7(M=294 g/mol)(用含 m 的代数式表示)。
(5)本实验所用钾盐试剂均经重结晶的方法纯化。其中趁热过滤的具体操作为漏斗下端管口紧靠
烧杯内壁,转移溶液时用 ,滤液沿烧杯壁流下。
化学学科试卷 (第 4页,共 4 页)
{#{QQABbQKAogAAAIIAAAgCAwH4CEIQkACAAYgOBAAIoAAAiQFABCA=}#}
“龙东联盟”2022 级高三学年上学期 10 月月考试题化学评分标准
一、选择题(每小题只有一个正确选项,每小题 3 分,共 45 分)
题号 1 2 3 4 5 6 7 8
答案 C C D B D C C C
题号 9 10 11 12 13 14 15
答案 B D C A D D B
【16】(13 分)
(1)酸(1 分);I2 + 2OH- = IO- + I- +H2O(2 分)
(2)防止加碱速率过快,生成的 IO-来不及氧化葡萄糖,影响实验结果(2 分);
(3)挥发(2 分);溶液蓝色褪去,半分钟不恢复原色(2 分);
1(8 2-xy)
(4) (2 分)
5
(5)偏高(2 分)
【17】(14 分)
(1)增大接触面积,加快反应速率,增大浸出率(1 分);
(2)3Ni + 8HNO3 3Ni(NO3)2 + 2NO + 4H2O(2 分);
(3)铁元素(1 分);防止胶体生成,易于沉淀分离(2 分)
(4)防止 H 2-2S 与氨水反应,增大溶液中的 S 浓度,使 Ni 元素沉淀(2 分);CuS(1 分);
溶浸(1 分)
>600℃
(5)无火星产生(2 分);2Ni2O3 4NiO+3O2(2 分)
【18】(14 分,每空 2 分)
(1)难挥发性
催化剂
(2)① 4NH3 +5O2 4NO+6H 2
O ②27/(2p1);
反应正向气体分子总数减小,同温时,p1条件下 NO 转化率高于 p2,故 p1>p2 ,x、y
点转化率相同,此时压强对容积的影响大于温度对容积的影响
(3)N2-10e-+6H2O=2NO -3 +12H+;
反应 iii 生成 O2,O2将 NO 氧化 NO2,NO2更易转化成 NO -3 ;
(4)N2中存在氮氮三键,键能高,断键时需要较大的能量,故人工固氮是高能耗的过程
【19】(14 分)
(1)直形冷凝管(1 分);除去市售的溴中少量的 Cl2(2 分) ;
Δ
Br2 +K2C2O4 2KBr+2CO2 (2 分)
2 - - +
Δ 2+
( )蒸发皿(1 分); 2MnO4 +10I +16H 2Mn +5I2 +8H2O(2 分)
(3)液封(1 分)降低温度(1 分)
(4)0.31m(147m/476 合理即可)(2 分)
(5)玻璃棒引流,玻璃棒下端靠在三层滤纸处(2 分)
“龙东联盟”2022 级高三学年上学期 10 月月考试题化学解析 A.石英(SiO2)与盐酸不反应,A 项不符合题意;
1 C B.氢氧化镁和盐酸反应可以得到氯化镁溶液,但是电解氯化镁溶液不能得到 Mg,电解熔融 . 物质的成分、分类
MgCl2才能得到金属镁单质,故 B 的转化不能实现; 西汉皇后之玺是西汉玉器,唐兽首玛瑙杯是唐代玉器,元釉下褐彩凤鸟纹荷叶盖罐是陶瓷,三
C.纯碱工业是在饱和食盐水中通入 NH 和 CO 先得到 NaHCO ,然后 NaHCO 受热分解为
者的主要成分都是硅酸盐属于传统无机非金属材料;唐瑞兽葡萄纹铜镜铜镜是青铜器,主要成 3 2 3 3
Na2CO3,故 C 的转化能实现; 分是铜的合金,属于金属材料。
2 C D.工业制备硫酸,首先黄铁矿和氧气反应生成 SO2,但是 SO2和水反应生成 H. 物质的性质与用途 2SO3,不能得到
A H SO ,故 D 的转化不能实现; .SO 是酸性氧化物,石灰乳为 Ca(OH) ,呈碱性,吸收 SO 2 42 2 2体现了 Ca(OH)2的碱性;
B 7.C 电化学腐蚀 .铝用于制作门窗框架,利用了铝的硬度大、密度小、抗腐蚀等性质;
C A.氨水浓度越大,越容易生成[Zn(NH ) ]
2+,腐蚀趋势越大,A 正确;
.制作豆腐时添加石膏,利用的是在胶体中加入电解质发生聚沉这一性质,与 CaSO4难溶性 3 4
B.腐蚀的总反应为 Zn+4NH ·H O=[Zn(NH ) ]2++H ↑+2H O+2OH-,有 OH- 3 2 3 4 2 2 离子生成,溶液 pH 无关;
D B .银氨溶液的配制是在硝酸银中逐滴加入氨水,先生成白色沉淀 AgOH,最后生成易溶于水的 变大, 正确;
Ag(NH ) OH,Ag(NH ) OH 中 Ag+ C Zn和 NH 之间以配位键结合,体现了 NH 的配位性。 .该电化学腐蚀中 作负极,Fe 作正极,正极上氢离子得电子生成氢气,铁电极上的电极反 3 2 3 2 3 3
3 D O 应式为:2H2O+2e
-=H +2OH- C
. 分子结构、同素异形体 2 , 错误;
3
A D.O 和 O 是 O 元素形成的不同单质,两者互为同素异形体; .根据得失电子守恒,每生成标准状况下 224 mL H2,转移电子数为 0.02 mol,消耗 0.01 mol Zn 2 8
B D .O8分子为平行六面体,由其结构知,O8中存在两种氧氧键:上下底面中的氧氧键、上下底 正确。
8 C
面间的氧氧键; . 物质性质
A.石墨属于单质,(CF)
超高压 x
属于化合物
C.O2转化为 O8可表示为 4O2 O8,气体分子数减少,故 O2转化为 O8是熵减反应; B.(CF)x中 C 原子的所有价键均参与成键,未有未参与成键的孤电子或者不饱和键,故与石墨
D.O O 相比,(CF) 抗氧化性增强,正确; 2在超高压下转化成 8,则在常压低温下 O8会转化成 O2,不能稳定存在,D 项错误。 x
4 B C.石墨晶体中每个碳原子上未参与杂化的 1 个 2p 轨道上电子在层内离域运动,故石墨晶体能 . 离子方程式的书写和判断正误
A 导电,而(CF)x中没有未参与杂化的 2p 轨道上的电子,故与石墨相比,(CF)x导电性减弱,错误; .氯气氧化苦卤得到溴单质,发生置换反应,离子方程式正确;
2 D.由题干结构示意图可知,在(CF)x 中 C 与周围的 3 个碳原子形成共价键,每个 C-C 键被 2 B.铅酸电池在充电时阳极失电子,其电极式为:PbSO -2e-4 +2H2O=PbO2+4H++SO 4 ,B 错误;
个碳原子共用,和 1 个 F 原子形成共价键,即 1 mol (CF)x中含有 2.5x mol 共价单键,正确。
C.TiCl4容易与水反应发生水解,反应的离子方程式为 TiCl4+(x+2)H2O=TiO2·xH2O↓+4H++4Cl 9.B 元素化合物
-; A.S 易溶于二硫化碳,A 正确;
D.用 Na2CO3溶液将水垢中的 CaSO4转化为 CaCO3:CaSO4+CO 2-=CaCO 2-3 3+SO4 。 B.溶解过程中发生的反应为 CuFeS2+3CuCl2+4HCl=4H[CuCl2]+2S+FeCl2,但由于含有少量 CuS
5.D 阿伏加德罗常数、与物质的量有关的计算
生成,所以参与反应的 n CuCl : n CuFeS 3:1,B 错误;
A.反应 i 的 ΔH>0、ΔS>0,ΔG=ΔH-TΔS<0 反应自发,故 T 较大时反应 i 的 ΔG<0,反应ⅰ 2 2需在
C.由于生成的亚铜离子能与氯离子结合形成络合物,因此浸取剂中的 Cl
-有助于 CuFeS 固体
高 2
温下才能自发进行,A 正确; 的溶解,C 正确;
B.142 g Na SO D.铁离子具有氧化性,因此也能用浓盐酸和 FeCl 溶液的混合液也可能使黄铜矿溶解,D 正确。2 4物质的量为 1 mol,根据反应 i 的化学方程式,产生 O2物质的量为 2 mol,标 3
10.D 实验操作
准状况下体积约为 44.8 L,B 正确;
C.由反应ⅰ、ⅱ制备 Na2S 都是以 Na2SO4为反应物,硫的化合价都是从+6 -2
A.二氧化硫可以使品红溶液褪色,故可以使用品红溶液检验二氧化硫,但三氧化硫也
变为 ,每生成 1 mol
Na2S 失 8 mol 电子,故由反应ⅰ、ⅱ分别制备 0.5 mol Na S
被品红溶液吸收,不能检验三氧化硫,A 错误;
2 ,转移电子数均为 4NA,C 正确;
D Na S B.浓硫酸和氯化钠反应需要加热生成挥发性氯化氢气体,B 错误; . 2 溶液中,S2-发生水解,且未给体积,D 错误;选 D。
6 C C.用排液体法测量气体体积,伸入量筒的导管尽可能伸入到底部,题中所给装置,伸 . 物质转化
入量筒的导管太短,C 错误;
D.N2和 H2在 Fe 绒丝作催化剂且加热的条件下生成 NH3,NH3可使湿润的红色石蕊试 Y
纸变蓝,D 正确。 的目的是补充 H2O,维持 NaBr 溶液为一定浓度,B 项错误;
11.C 氧化还原反应 电解
C -.根据分析电解总反应式为 Br-+3H2O BrO3 +3H2↑,C 项正确;
A.由 iii、iv 两组实验对比可知,在氢氧化钠溶液中,XeF6可以发生还原反应,而在水中则发
生非氧化还原反应,故可知:OH-的还原性比 H2O 强,A 正确; D.催化阶段,Br 元素的化合价由+5 价降至-1 价,生成 1molBr-得到 6mol 电子,O 元素的化
B.i、ii、iv 三组化学反应均为氧化还原反应,B 正确; 合价由-2 价升至 0 价,生成 1molO2失去 4mol 电子,根据得失电子守恒,反应产物物质的量之
C.分析 iv 可知,每生成一个 O2,整个反应转移 6 个电子,故每生成 1 mol O2,转移 6 mol 电 比 n(O -2) ∶n(Br )=6∶4=3∶2,D 项正确。
子,C 错误; 16.(13 分)
D.与同族的 0 族元素相比,氙原子的最外层虽然为 8e-稳定结构,但原子半径大,电离能小, (1)酸(1 分);I2 + 2OH- = IO- + I- +H2O(2 分)
所以氙原子的性质相对活泼,形成的化合物种类更多,故 D 正确。 (2)防止加碱速率过快,生成的 IO-来不及氧化葡萄糖,影响实验结果(2 分);
12.A 元素化合物转化、分离提纯 (3)挥发(2 分);溶液蓝色褪去,半分钟不恢复原色(2 分);
废电池材料中加入氯化铝和 CH3CN 进行溶解,再通入氯气,将 Fe2+转化为 Fe3+,充分反应后, 1(8 2-xy)
(4) (2 分)
抽滤,得到磷酸铁沉淀,滤液处理后得到 LiAlCl4。 5
A.为加快溶解速率可升温至 81℃以上,CH3CN 会挥发,A 错误; (5)偏高(2 分)
B.Cl 2+2将 Fe 氧化为 Fe3+,B 正确; 解析:
C.观察流程可知,乙氰没有参与反应,它是有机溶剂,促进共价化合物氯化铝溶解,C 正确; (1)I 标准溶液应装入酸式滴定管;生成 IO-的离子反应为 I - - - 2 2 + 2OH = IO + I +H2O。
D.抽滤可以加快过滤速度,使固液分离更完全,D 正确。 (2)已知,IO-在碱性条件下易发生歧化反应;故 NaOH 溶液需要缓慢滴加目的为:防止加碱
13.D 化学反应中的能量变化 速率过快,生成的 IO-来不及氧化葡萄糖,影响实验结果。
(3)酸化后,立即滴定是为了防止生成的 I 挥发;滴定终点的现象是最后半滴 Na S O 溶液加
A 2 2 2 3.反应过程中该结构中 有 π 键的断裂及 π 键的生成,A 错误;
入后,溶液蓝色变为无色,且半分钟不变色。
B.能量越低越稳定,由图可知 N 的能量低,故 N 更稳定,B 错误; (4)注射液中葡萄糖的含量为[(0.05×0.02-x·y·1/2)×180]/0.025 g·L-1。
C.不管是吸热反应还是放热反应,升高温度反应速率均增大,只是增大的程度不同,所以升 (5)若滴定管尖嘴处有气泡,硫代硫酸钠体积小则会导致测定结果偏高。
高温度生成 N、M 的反应速率均增大,C 错误; 17.(14 分)
D.由图可知升高温度时,更有利于生成 N,导致反应物浓度降低使得生成 M 的平衡逆向移动, (1)增大接触面积,加快反应速率,增大浸出率(1 分);
则 M 可能转化为 N,D 正确; (2)3Ni + 8HNO3 3Ni(NO3)2 + 2NO + 4H2O(2 分);
故选 D。 (3)铁元素(1 分);防止胶体生成,易于沉淀分离(2 分)
14.D 化学反应中的能量变化 (4)防止 H 2-2S 与氨水反应,增大溶液中的 S 浓度,使 Ni 元素沉淀(2 分);CuS(1 分);
A.以太阳能为驱动力,在室温条件下可将氮气转化为氨气,能量变化是光能转化为化学能,A 溶浸(1 分)
正确;
>600℃
B.图中氢离子可能得到电子发生还原反应生成副产物氢气,B 正确; (5)无火星产生(2 分);2Ni2O3 4NiO+3O2(2 分)
C .由图,总反应为氮气和水在光催化作用下生成氨气和氧气,C 正确; 解析:
D.氮化合价由 0 变为-3 得到氨气,则 VB 上产生 3 mol h+,CB 上产生 1mol 氨气,为 22.4L(标 (1)粗镍粉碎的作用是增大接触面积,加快反应速率,增大浸出率;
) D (2准状况 , 错误。 )溶浸时,单质镍生成 Ni
2+发生的化学反应方程式为 3Ni + 8HNO3 3Ni(NO3)2 + 2NO +
15 B 4H O . 电化学基础 2 ;
A.根据分析,电极 a 为阴极,连接电源负极,A 项正确; (3)用氨水调节 pH 约为 5 除去铁元素,充分反应后需加热煮沸后过滤,加热的目的是防止
B.根据分析电解过程中消耗 H O 和 Br-2 ,而催化阶段 BrO -3 被还原成 Br-循环使用,故加入 胶体生成,易于沉淀分离;
市售的溴(纯度 99%)中含有少量的 Cl2和 I2,实验利用氧化还原反应原理制备高纯度的溴,市售的
(4)加入饱和 H2S 溶液前需先加入硝酸调节 pH 至 4.0 左右,原因是防止 H2S 与氨水反应,增大 溴滴入盛有浓 CaBr2溶液中,Cl2可与 CaBr2发生氧化还原反应而除去,I2与 Br2一起蒸馏入草酸钾
溶液中的 S2-浓度,使 Ni 元素沉淀;滤渣 2 为 CuS,滤液 2 中含有硝酸。 溶液中,并被草酸钾还原为 I-、Br-,并向溶液中滴加高锰酸钾溶液氧化 I-,加热蒸干得 KBr 固
(5)判断分解完全最简单的现象是:无火星产生。因为草酸盐分解有 CO 产生,故有火星; 体,将 KBr 固体和 K2Cr2O7固体混合均匀加入冷的蒸馏水,同时滴加适量浓 H2SO4,水浴加热蒸馏,
>600℃
2Ni2O3 4NiO+3O2。 得到的液体分液、干燥、蒸馏,可得高纯度的溴。
18.(14 分,每空 2 分) (1)仪器 C 为直形冷凝管,用于冷凝蒸气;市售的溴中含有少量的 Cl2,Cl2可与 CaBr2发生氧化
(1)难挥发性 还原反应而除去;水浴加热时,Br2、I2蒸发进入装置 D 中,分别与 K2C2O4发生氧化还原反应,由
Δ
催化剂 于 Br2为进入 D 的主要物质,故主要反应的化学方程式为Br2 +K2C2O4 2KBr+2CO2 ;
(2)① 4NH3 +5O2 4NO+6H2O ②27/(2p1);反应正向气体分子总数减小,同温时,p1条件
(2)将 D 中溶液转移至蒸发皿中,边加热边向其中滴加酸化的 KMnO4溶液至出现红棕色气体
下 NO 转化率高于 p2,故 p1>p2,x、y 点转化率相同,此时压强对容积的影响大于温度对容 (Br2),即说明 KMnO4已将 KI 全部氧化,发生反应的离子方程式为
积的影响。
Δ
(3)N2-10e-+6H2O=2NO -+12H+
- - + 2+
3 ;反应 iii 生成 O2,O2将 NO 氧化 NO2,NO2更易转化成 NO - 3 2MnO4 +10I +16H 2Mn +5I2 +8H2O;KBr 几乎未被氧化,继续加热将溶液蒸干所得固体 R 的主
(4)N2中存在氮氮三键,键能高,断键时需要较大的能量,故人工固氮是高能耗的过程
要成分为 KBr;
解析:
(3)密度液溴大于水,D 中冷的蒸馏水起到液封的作用,同时冷的蒸馏水温度较低,均可减少溴
(1)浓硫酸难挥发,产物 HNO3为气体,有利于复分解反应进行体现了浓硫酸的难挥发性和酸性。
的挥发;
催化剂
(2)①第 I 步反应为氨气的催化氧化,化学方程式为 4NH3 +5O m2 4NO+6H2O;
(4)m 克 KBr 固体的物质的量为 mol
-
,根据转移电子相等可得关系式6KBr~6e ~K Cr O ,则
119 2 2 7
②27/(2p1); 2NO+O2 2NO2 ,该反应正向气体分子总数减小,同温时, p1 条件下 NO 转化 1 m
理论上需要K2Cr2O7 的物质的量为 mol,实际所需称取 K Cr6 119 2 2
O7的质量为
T
率高于 p2 ,故 p1>p2 ,根据V nR p ,x、y 点转化率相同,则 n 相同,此时压强对容积的影 1 m mol 3 294g mol-1 0.31mg ;
响大于温度对容积的影响,故 y 点的容器容积小于 x 点的容器容积。 6 119 4
3 ① a a (5)趁热过滤的具体操作:漏斗下端管口紧靠烧杯内壁,转移溶液时用玻璃棒引流,玻璃棒下端( ) 由电极 上的物质转化可知,氮元素化合价升高,发生氧化反应,电极 为阳极,电极反
应式为 N -10e-+6H O=2NO -+12H+ 靠在三层滤纸处,滤液沿烧杯壁流下。 2 2 3 ;
②反应 iii 生成 O2,O2将 NO 氧化 NO2,NO2更易转化成 NO -3 。
(4)N2中存在氮氮三键,键能高,断键时需要较大的能量,故人工固氮是高能耗的过程。
19.(14 分)
(1)直形冷凝管(1 分);除去市售的溴中少量的 Cl2(2 分) ;
Δ
Br2 +K2C2O4 2KBr+2CO2 (2 分)
Δ
(2)蒸发皿(1 分); 2MnO-4 +10I
- +16H+ 2Mn2+ +5I2 +8H2O(2 分)
(3)液封(1 分)降低温度(1 分)
(4)0.31m(2 分)
(5)玻璃棒引流,玻璃棒下端靠在三层滤纸处(2 分)
解析:
“龙东联盟”2022 级高三学年上学期 10 月月考试题
A - -.海水提溴过程中,用氯气氧化苦卤得到溴单质:2Br +Cl2=2Cl +Br2
B.铅酸蓄电池充电时的阳极反应:Pb2++2H2O-2e-=PbO +4H+(化学学科) 2
C.TiCl4加入水中:TiCl4+(x+2)H2O=TiO2·xH -2O↓+4H++4Cl
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,考试结束后,将答题卡交回。 D.用 Na2CO3 溶液将水垢中的 CaSO4转化为 CaCO3:CaSO4+CO32-=CaCO3+SO -42
注意事项: 5.以 Na2SO4为原料制备 Na2S,理论上可用下列两个反应进行。
1.答题前,考生先将自己的姓名、准考证号码填写清楚,将条形码准确粘贴在考生信息条形
反应ⅰ:Na2SO4(s)=Na2S(s)+2O2(g) ΔH=+1011 kJ·mol-1 ΔS=+357 J·K-1·mol-1
码粘贴区。
反应ⅱ:Na2SO4(s)+4C(s)=Na2S(s)+4CO(g)
2.选择题必须使用 2B 铅笔填涂;非选择题必须使用 0.5 毫米黑色字迹的签字笔书写,字体工 NA为阿伏加德罗常数的值,下列说法不正确的是
整、笔迹清楚。 A.反应ⅰ需在高温下才能自发进行
3.请按照题号顺序在各题目的答题区域作答,超出答题区域书写的答案无效;在草稿纸、试 B.反应ⅰ中,每分解 142 g Na2SO4产生 44.8 L O2(标准状况)
题卷上答题无效。 C.由反应ⅰ、ⅱ分别制备 0.5 mol Na2S,转移电子数均为 4NA
4.保持卡面清洁,不得折叠,不要弄破、弄皱,不准使用涂改液、修正带、刮纸刀。 D.0.10 mol/L Na2S -溶液中含 S2 数目为 0.1NA
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 K-39 Br-80 6.在给定条件下,下列制备过程涉及的物质转化均可实现的是
第 I 卷(选择题,共 45 分) A.制备高纯硅:石英 盐酸 SiCl 氢气4 高纯硅
一、选择题(每小题只有一个正确选项,每小题 3 分,共 45 分) B.金属 Mg 制备:Mg OH 电解 盐 酸 MgCl2 2 溶液 Mg
1.文物见证历史,化学创造文明。下列文物据其主要成分不能与其他三项归为一类的是
A C.纯碱工业:饱和 NaCl(aq)
N H3和 CO 2 NaHCO3(s)
加 热 Na CO
.西汉皇后之玺 2 3
O H O
B.兽首玛瑙杯 D.硫酸工业: FeS 2 22 SO2 H2SO高温 4
C.唐瑞兽葡萄纹铜镜 7.破损的镀锌铁皮在氨水中发生电化学腐蚀,生成[Zn(NH3)4]2+和 H2,下列说法不正确的是
D.元釉下褐彩凤鸟纹荷叶盖陶罐 A.氨水浓度越大,腐蚀趋势越大
2.物质性质决定用途,下列两者对应关系错误的是 B.随着腐蚀的进行,溶液 pH 变大
A.石灰乳除去废气中二氧化硫,体现了 Ca(OH)2的碱性 C.铁电极上的电极反应式为:2NH +2e- -3 =2NH2 +H2↑
B.铝合金可用于制作门窗框架,体现了铝的硬度大、密度小 D.每生成标准状况下 224 mL H2,消耗 0.010 mol Zn
C.制作豆腐时添加石膏,体现了 CaSO4的难溶性 8.石墨与 F2 在 450℃反应,石墨层间插入 F 得到层状结构化合物(CF)x,该物质仍具润滑性,其单
D.用氨水配制银氨溶液,体现了 NH3的配位性 层局部结构如图所示。下列关于该化合物的说法不正确的是
3.固态的氧有多种形态,如淡蓝色、红色、粉红色、暗蓝色还有橙色等。下图为 O2 在超高压
下转化为平行六面体的红氧(O8)分子。下列说法错误的是
A.O2 和 O8 互为同素异形体
B.O8 中存在不同的氧氧键
C.O2 转化为 O8 是熵减反应
D.常压低温下 O8 能稳定存在
化学学科试卷 (第 1页,共 4 页)
{#{QQABbQKAogAAAIIAAAgCAwH4CEIQkACAAYgOBAAIoAAAiQFABCA=}#}
A.石墨属于单质,(CF)x 属于化合物 与水反应 与 NaOH 溶液反应
B.与石墨相比,(CF)x抗氧化性增强
- -
C.与石墨相比,(CF) 导电性增强 i.2XeF2+2H2O=2Xe↑+O2↑+4HF ii.2XeF2+4OH =2Xe↑+Ox 2↑+4F +2H2O
D.1 mol (CF)x中含有 2.5x mol 共价单键 iv.2XeF -6+4Na++16OH =
9.用过量的盐酸和 CuCl -溶液的混合液作为浸取剂,将黄铜矿(CuFeS )中的铜元素以[CuCl ] 的形 iii.XeF6+3H2O=XeO3+6HF2 2 2 Na4XeO6↓+Xe↑+O2↑+12F-+8H2O
式,铁元素以 Fe2+的形式浸出,一种流程示意图如下。
下列说法错误的是
A OH-. 的还原性比 H2O 强
B.反应 i~iv 中有 3 个氧化还原反应
C.反应 iv 每生成 1 mol O2,转移 4 mol 电子
D.较 He、Ne、Ar、Kr 原子,Xe 原子半径大,电离能小,所以含 Xe 的化合物种类更多
下列说法不正确的是 12.一种从废电池材料中高效回收和利用锂资源的工艺如图。下列叙述错误的是
A.含 S、少量 CuS 的固体可用二硫化碳分离
B. 参与反应的 n(CuCl2)﹕n(CuFeS2)=3﹕1
C. 浸取剂中的 Cl-有助于 CuFeS2固体的溶解
D. 用浓盐酸和 FeCl3溶液的混合液也可能使黄铜矿溶解
10.用下列实验装置和方法进行相应实验,能达到实验目的的是
A.为加快溶解速率可升温至 81℃以上
B.“氧化”的目的是将 Fe2+转化为 Fe3+
C.乙氰(CH3CN)在反应中作溶剂促进共价化合物氯化铝溶解
D.“抽滤”的优点是可以加快过滤速度,使固液分离更彻底
13.Diels-Alder 反应是一步完成的协同反应,也是立体专一的顺式加成反应。下图所示加成反应,
生成两种主产物 M、N,反应过程中的能量变化如图所示。下列说法正确的是
A.可用该装置检验气体中含SO2和SO3 B.可用该装置制备 HCl
C.可用该装置测量反应产生气体体积 D.可用该装置模拟工业制备 NH3并检验 A.反应过程中,只有π键断裂,无π键生成
B.M 产物比 N 更稳定
A.A B.B C.C D.D
C.升高温度,生成 N 的速率会增大,生成 M 的正反应速率会减小
11.稀有气体化合物在化学、照明、医疗等众多领域有广泛应用,含 Xe 化合物的种类较多,氙的
D.升高温度,M 可能转化为 N
氟化物(XeFn)与 NaOH 溶液反应剧烈,与水反应则较为温和,反应式如下:
化学学科试卷 (第 2页,共 4 页)
{#{QQABbQKAogAAAIIAAAgCAwH4CEIQkACAAYgOBAAIoAAAiQFABCA=}#}
14.以太阳能为驱动力,在介导上产生空穴 h+(空穴是指共价键上流失一个电子,最后在共价键上 Ⅰ .测定原理
- - - -
留下空位的现象),在室温条件下可将氮气转化为氨气,其工作原理如下。下列说法错误的是 葡萄糖(C6H12O6)能够被 IO 在碱性条件下氧化为 C6H11O7 ,IO 在碱性条件下同时歧化为 I 和
IO - -3 (已知:IO3 不能氧化葡萄糖),充分反应后酸化,生成单质碘,用 Na2S2O3标准溶液滴定
析出的 I2(2S -2O32 +I2=2I +S4O62-),进而计算葡萄糖含量。
Ⅱ. 实验步骤
取 25 mL 葡萄糖注射液于锥形瓶中,用滴定管向其中加入 0.050 mol/L 的 I2标准溶液 20 mL,
在摇动下缓慢滴加 1.0 mol/L NaOH 溶液,直至溶液变为浅黄色,盖上表面皿,放置约 15 分钟,
使之反应完全。用少量水冲洗表面皿和锥形瓶内壁,加入 2 mL 盐酸,立即用 Na2S2O3标准溶
液滴定至浅黄色,加入淀粉指示剂,继续滴定至终点。平行测定 3 份。
回答下列问题:
(1) I2标准溶液应装入 式滴定管中(填“酸”或“碱”);生成 IO-的离子反应方程式为
A.该过程中能量变化是光能转化为化学能 。
B.该工艺可能生成副产物氢气 (2)实验步骤中 1.0 mol/L NaOH 溶液需要缓慢滴加的理由是 。
C.生成氨气的总反应:2N +6H O=4NH +3O (3)酸化后,立即滴定是为了防止生成的 I2 ;滴定终点的现象是 。2 2 3 2
-1
D.VB 上产生 3 mol h+,CB 上产生 NH 11.2 L(标准状况) (4)若消耗 x mol/L 的 Na2S2O3 溶液的体积为 y mL,则注射液中葡萄糖的含量为 g·L 。3
15.以不同材料修饰的 Pt 为电极,一定浓度的 NaBr 溶液为电解液,采用电解和催化相结合的循环 (5)上述滴定完成时,若滴定管尖嘴处有气泡会导致测定结果 (填“偏高”或“偏低”)。
方式,可实现高效制 H 和 O ,装置如图所示。下列说法错误的是 17.(14 分)镍的氧化物(NiO 和 Ni2O3)是制备二次电池的重要材料,实验室以粗镍板(单质 Ni,含2 2
少量 Fe,Cu 杂质)为原料模拟工业制备氧化镍的流程如图所示:
相关数据如下:
A.电极 a 连接电源负极 难溶电解质或离子 NiS CuS Cu2+ Ni2+ Fe3+
B.加入 Y 的目的是补充 NaBr Ksp 或沉淀完全的 pH 1.1×10﹣21 1.3×10﹣36 pH=9 pH=9.5 pH=3.7
C Br-
电解
+3H O BrO-.电解总反应式为 2 3 +3H2 回答下列问题:
(1)粗镍粉碎的作用是 。
D -.催化阶段反应产物物质的量之比 n(Z)﹕n(Br )=3﹕2
(2)溶浸时,单质镍生成 Ni2+发生的化学反应方程式为 。
第 II 卷(非选择题,共 55 分) (3)用氨水调节 pH 约为 5 除去 ,充分反应后需加热煮沸后过滤,加热的目的是 。
二、非选择题(共 55 分) (4)加入饱和 H2S 溶液前需先加入硝酸调节 pH 至 4.0 左右,原因是 ;
16.(13 分)葡萄糖是重要的营养物质之一。某课外小组采用碘量法测定葡萄糖注射液中葡萄糖 滤渣 2 主要成分为 ,滤液 2 可以返回 工序继续使用。
的含量。测定原理及实验步骤如下:
化学学科试卷 (第 3页,共 4 页)
{#{QQABbQKAogAAAIIAAAgCAwH4CEIQkACAAYgOBAAIoAAAiQFABCA=}#}
-
(5)NiC2O4·H2O 热分解步骤:将粉末状 NiC2O4·H2O 置于坩埚中,在酒精灯上加热,炒成黄色 ①电极 a 表面生成 NO3 的电极反应式: 。
i ii -
粉末。继续小心加热使 NiC2O4 缓慢分解,在分解过程中不断搅拌,使 Ni2C2O4充分接触 ②研究发现:N2 转化可能的途径为 N2→NO→NO3 。电极 a 表面还发生 iii.H2O→O2。
空气,控制温度使分解尽量缓慢,直至分解完全,判断分解完全最简单的现象是 ; iii 的存在,有利于途径 ii,原因是 。
Ni2O3在温度高于 600℃时可生成 NiO,反应方程式为 。 (4)人工固氮是高能耗的过程,结合 N2 分子结构解释原因 。
18.(14 分)HNO3是一种重要的工业原料。可采用不同的氮源制备 HNO3。 方法三为 N2 的直接利用提供了一种新的思路。
(1)方法一:早期以硝石(含 NaNO3)为氮源制备 HNO3,反应的化学方程式为 19.(14 分)市售的溴(纯度 99%)中含有少量的 Cl2和 I2,某化学兴趣小组利用氧化还原反应原理,
NaNO3+H2SO4(浓)=NaHSO4+HNO3↑。该反应利用了浓硫酸的性质是酸性和 。 设计实验制备高纯度的溴。回答下列问题:
(2)方法二:以 NH3为氮源催化氧化制备 HNO3,反应原理分三步进行。 (1)装置如图(夹持装置等略),将市售的溴滴入盛有浓 CaBr2溶液的 B 中,水浴加热至不再有红棕
色液体馏出。仪器 C 的名称为 ;CaBr2溶液的作用为 ;
D 中发生的主要反应的化学方程式为 。
①第 I 步反应的化学方程式为 。
②针对第Ⅱ步反应进行研究:在容积可变的密闭容器中,充入 2n mol NO 和 n mol O2 进行反应。
在不同压强下(p1、p2),反应达到平衡时,测得 NO 转化率随温度的变化如图所示。请计算 y
点用分压表示的平衡常数 Kp= ;解释 y 点的容器容积小于 x 点的容器容积的
原因 。
(2)将 D 中溶液转移至 (填仪器名称)中,边加热边向其中滴加酸化的 KMnO4 溶液至出现
红棕色气体,继续加热将溶液蒸干得固体 R。该过程中生成 I2的离子方程式为
。
(3)利用图示相同装置,将 R 和 K2Cr2O7 固体混合均匀放入 B 中,D 中加入冷的蒸馏水。由 A 向
(3)方法三:研究表明可以用电解法以 N2为氨源直接制备 HNO3,其原理示意图如下。 B 中滴加适量浓 H2SO4,水浴加热蒸馏。然后将 D 中的液体分液、干燥、蒸馏,得到高纯度
的溴。D 中蒸馏水的作用为 和 。
3
(4)为保证溴的纯度,步骤(3)中 K2Cr2O7固体的用量按理论所需量的 计算,若固体 R 质量为 m4
克(以 KBr 计),则需称取 g K2Cr2O7(M=294 g/mol)(用含 m 的代数式表示)。
(5)本实验所用钾盐试剂均经重结晶的方法纯化。其中趁热过滤的具体操作为漏斗下端管口紧靠
烧杯内壁,转移溶液时用 ,滤液沿烧杯壁流下。
化学学科试卷 (第 4页,共 4 页)
{#{QQABbQKAogAAAIIAAAgCAwH4CEIQkACAAYgOBAAIoAAAiQFABCA=}#}
“龙东联盟”2022 级高三学年上学期 10 月月考试题化学评分标准
一、选择题(每小题只有一个正确选项,每小题 3 分,共 45 分)
题号 1 2 3 4 5 6 7 8
答案 C C D B D C C C
题号 9 10 11 12 13 14 15
答案 B D C A D D B
【16】(13 分)
(1)酸(1 分);I2 + 2OH- = IO- + I- +H2O(2 分)
(2)防止加碱速率过快,生成的 IO-来不及氧化葡萄糖,影响实验结果(2 分);
(3)挥发(2 分);溶液蓝色褪去,半分钟不恢复原色(2 分);
1(8 2-xy)
(4) (2 分)
5
(5)偏高(2 分)
【17】(14 分)
(1)增大接触面积,加快反应速率,增大浸出率(1 分);
(2)3Ni + 8HNO3 3Ni(NO3)2 + 2NO + 4H2O(2 分);
(3)铁元素(1 分);防止胶体生成,易于沉淀分离(2 分)
(4)防止 H 2-2S 与氨水反应,增大溶液中的 S 浓度,使 Ni 元素沉淀(2 分);CuS(1 分);
溶浸(1 分)
>600℃
(5)无火星产生(2 分);2Ni2O3 4NiO+3O2(2 分)
【18】(14 分,每空 2 分)
(1)难挥发性
催化剂
(2)① 4NH3 +5O2 4NO+6H 2
O ②27/(2p1);
反应正向气体分子总数减小,同温时,p1条件下 NO 转化率高于 p2,故 p1>p2 ,x、y
点转化率相同,此时压强对容积的影响大于温度对容积的影响
(3)N2-10e-+6H2O=2NO -3 +12H+;
反应 iii 生成 O2,O2将 NO 氧化 NO2,NO2更易转化成 NO -3 ;
(4)N2中存在氮氮三键,键能高,断键时需要较大的能量,故人工固氮是高能耗的过程
【19】(14 分)
(1)直形冷凝管(1 分);除去市售的溴中少量的 Cl2(2 分) ;
Δ
Br2 +K2C2O4 2KBr+2CO2 (2 分)
2 - - +
Δ 2+
( )蒸发皿(1 分); 2MnO4 +10I +16H 2Mn +5I2 +8H2O(2 分)
(3)液封(1 分)降低温度(1 分)
(4)0.31m(147m/476 合理即可)(2 分)
(5)玻璃棒引流,玻璃棒下端靠在三层滤纸处(2 分)
“龙东联盟”2022 级高三学年上学期 10 月月考试题化学解析 A.石英(SiO2)与盐酸不反应,A 项不符合题意;
1 C B.氢氧化镁和盐酸反应可以得到氯化镁溶液,但是电解氯化镁溶液不能得到 Mg,电解熔融 . 物质的成分、分类
MgCl2才能得到金属镁单质,故 B 的转化不能实现; 西汉皇后之玺是西汉玉器,唐兽首玛瑙杯是唐代玉器,元釉下褐彩凤鸟纹荷叶盖罐是陶瓷,三
C.纯碱工业是在饱和食盐水中通入 NH 和 CO 先得到 NaHCO ,然后 NaHCO 受热分解为
者的主要成分都是硅酸盐属于传统无机非金属材料;唐瑞兽葡萄纹铜镜铜镜是青铜器,主要成 3 2 3 3
Na2CO3,故 C 的转化能实现; 分是铜的合金,属于金属材料。
2 C D.工业制备硫酸,首先黄铁矿和氧气反应生成 SO2,但是 SO2和水反应生成 H. 物质的性质与用途 2SO3,不能得到
A H SO ,故 D 的转化不能实现; .SO 是酸性氧化物,石灰乳为 Ca(OH) ,呈碱性,吸收 SO 2 42 2 2体现了 Ca(OH)2的碱性;
B 7.C 电化学腐蚀 .铝用于制作门窗框架,利用了铝的硬度大、密度小、抗腐蚀等性质;
C A.氨水浓度越大,越容易生成[Zn(NH ) ]
2+,腐蚀趋势越大,A 正确;
.制作豆腐时添加石膏,利用的是在胶体中加入电解质发生聚沉这一性质,与 CaSO4难溶性 3 4
B.腐蚀的总反应为 Zn+4NH ·H O=[Zn(NH ) ]2++H ↑+2H O+2OH-,有 OH- 3 2 3 4 2 2 离子生成,溶液 pH 无关;
D B .银氨溶液的配制是在硝酸银中逐滴加入氨水,先生成白色沉淀 AgOH,最后生成易溶于水的 变大, 正确;
Ag(NH ) OH,Ag(NH ) OH 中 Ag+ C Zn和 NH 之间以配位键结合,体现了 NH 的配位性。 .该电化学腐蚀中 作负极,Fe 作正极,正极上氢离子得电子生成氢气,铁电极上的电极反 3 2 3 2 3 3
3 D O 应式为:2H2O+2e
-=H +2OH- C
. 分子结构、同素异形体 2 , 错误;
3
A D.O 和 O 是 O 元素形成的不同单质,两者互为同素异形体; .根据得失电子守恒,每生成标准状况下 224 mL H2,转移电子数为 0.02 mol,消耗 0.01 mol Zn 2 8
B D .O8分子为平行六面体,由其结构知,O8中存在两种氧氧键:上下底面中的氧氧键、上下底 正确。
8 C
面间的氧氧键; . 物质性质
A.石墨属于单质,(CF)
超高压 x
属于化合物
C.O2转化为 O8可表示为 4O2 O8,气体分子数减少,故 O2转化为 O8是熵减反应; B.(CF)x中 C 原子的所有价键均参与成键,未有未参与成键的孤电子或者不饱和键,故与石墨
D.O O 相比,(CF) 抗氧化性增强,正确; 2在超高压下转化成 8,则在常压低温下 O8会转化成 O2,不能稳定存在,D 项错误。 x
4 B C.石墨晶体中每个碳原子上未参与杂化的 1 个 2p 轨道上电子在层内离域运动,故石墨晶体能 . 离子方程式的书写和判断正误
A 导电,而(CF)x中没有未参与杂化的 2p 轨道上的电子,故与石墨相比,(CF)x导电性减弱,错误; .氯气氧化苦卤得到溴单质,发生置换反应,离子方程式正确;
2 D.由题干结构示意图可知,在(CF)x 中 C 与周围的 3 个碳原子形成共价键,每个 C-C 键被 2 B.铅酸电池在充电时阳极失电子,其电极式为:PbSO -2e-4 +2H2O=PbO2+4H++SO 4 ,B 错误;
个碳原子共用,和 1 个 F 原子形成共价键,即 1 mol (CF)x中含有 2.5x mol 共价单键,正确。
C.TiCl4容易与水反应发生水解,反应的离子方程式为 TiCl4+(x+2)H2O=TiO2·xH2O↓+4H++4Cl 9.B 元素化合物
-; A.S 易溶于二硫化碳,A 正确;
D.用 Na2CO3溶液将水垢中的 CaSO4转化为 CaCO3:CaSO4+CO 2-=CaCO 2-3 3+SO4 。 B.溶解过程中发生的反应为 CuFeS2+3CuCl2+4HCl=4H[CuCl2]+2S+FeCl2,但由于含有少量 CuS
5.D 阿伏加德罗常数、与物质的量有关的计算
生成,所以参与反应的 n CuCl : n CuFeS 3:1,B 错误;
A.反应 i 的 ΔH>0、ΔS>0,ΔG=ΔH-TΔS<0 反应自发,故 T 较大时反应 i 的 ΔG<0,反应ⅰ 2 2需在
C.由于生成的亚铜离子能与氯离子结合形成络合物,因此浸取剂中的 Cl
-有助于 CuFeS 固体
高 2
温下才能自发进行,A 正确; 的溶解,C 正确;
B.142 g Na SO D.铁离子具有氧化性,因此也能用浓盐酸和 FeCl 溶液的混合液也可能使黄铜矿溶解,D 正确。2 4物质的量为 1 mol,根据反应 i 的化学方程式,产生 O2物质的量为 2 mol,标 3
10.D 实验操作
准状况下体积约为 44.8 L,B 正确;
C.由反应ⅰ、ⅱ制备 Na2S 都是以 Na2SO4为反应物,硫的化合价都是从+6 -2
A.二氧化硫可以使品红溶液褪色,故可以使用品红溶液检验二氧化硫,但三氧化硫也
变为 ,每生成 1 mol
Na2S 失 8 mol 电子,故由反应ⅰ、ⅱ分别制备 0.5 mol Na S
被品红溶液吸收,不能检验三氧化硫,A 错误;
2 ,转移电子数均为 4NA,C 正确;
D Na S B.浓硫酸和氯化钠反应需要加热生成挥发性氯化氢气体,B 错误; . 2 溶液中,S2-发生水解,且未给体积,D 错误;选 D。
6 C C.用排液体法测量气体体积,伸入量筒的导管尽可能伸入到底部,题中所给装置,伸 . 物质转化
入量筒的导管太短,C 错误;
D.N2和 H2在 Fe 绒丝作催化剂且加热的条件下生成 NH3,NH3可使湿润的红色石蕊试 Y
纸变蓝,D 正确。 的目的是补充 H2O,维持 NaBr 溶液为一定浓度,B 项错误;
11.C 氧化还原反应 电解
C -.根据分析电解总反应式为 Br-+3H2O BrO3 +3H2↑,C 项正确;
A.由 iii、iv 两组实验对比可知,在氢氧化钠溶液中,XeF6可以发生还原反应,而在水中则发
生非氧化还原反应,故可知:OH-的还原性比 H2O 强,A 正确; D.催化阶段,Br 元素的化合价由+5 价降至-1 价,生成 1molBr-得到 6mol 电子,O 元素的化
B.i、ii、iv 三组化学反应均为氧化还原反应,B 正确; 合价由-2 价升至 0 价,生成 1molO2失去 4mol 电子,根据得失电子守恒,反应产物物质的量之
C.分析 iv 可知,每生成一个 O2,整个反应转移 6 个电子,故每生成 1 mol O2,转移 6 mol 电 比 n(O -2) ∶n(Br )=6∶4=3∶2,D 项正确。
子,C 错误; 16.(13 分)
D.与同族的 0 族元素相比,氙原子的最外层虽然为 8e-稳定结构,但原子半径大,电离能小, (1)酸(1 分);I2 + 2OH- = IO- + I- +H2O(2 分)
所以氙原子的性质相对活泼,形成的化合物种类更多,故 D 正确。 (2)防止加碱速率过快,生成的 IO-来不及氧化葡萄糖,影响实验结果(2 分);
12.A 元素化合物转化、分离提纯 (3)挥发(2 分);溶液蓝色褪去,半分钟不恢复原色(2 分);
废电池材料中加入氯化铝和 CH3CN 进行溶解,再通入氯气,将 Fe2+转化为 Fe3+,充分反应后, 1(8 2-xy)
(4) (2 分)
抽滤,得到磷酸铁沉淀,滤液处理后得到 LiAlCl4。 5
A.为加快溶解速率可升温至 81℃以上,CH3CN 会挥发,A 错误; (5)偏高(2 分)
B.Cl 2+2将 Fe 氧化为 Fe3+,B 正确; 解析:
C.观察流程可知,乙氰没有参与反应,它是有机溶剂,促进共价化合物氯化铝溶解,C 正确; (1)I 标准溶液应装入酸式滴定管;生成 IO-的离子反应为 I - - - 2 2 + 2OH = IO + I +H2O。
D.抽滤可以加快过滤速度,使固液分离更完全,D 正确。 (2)已知,IO-在碱性条件下易发生歧化反应;故 NaOH 溶液需要缓慢滴加目的为:防止加碱
13.D 化学反应中的能量变化 速率过快,生成的 IO-来不及氧化葡萄糖,影响实验结果。
(3)酸化后,立即滴定是为了防止生成的 I 挥发;滴定终点的现象是最后半滴 Na S O 溶液加
A 2 2 2 3.反应过程中该结构中 有 π 键的断裂及 π 键的生成,A 错误;
入后,溶液蓝色变为无色,且半分钟不变色。
B.能量越低越稳定,由图可知 N 的能量低,故 N 更稳定,B 错误; (4)注射液中葡萄糖的含量为[(0.05×0.02-x·y·1/2)×180]/0.025 g·L-1。
C.不管是吸热反应还是放热反应,升高温度反应速率均增大,只是增大的程度不同,所以升 (5)若滴定管尖嘴处有气泡,硫代硫酸钠体积小则会导致测定结果偏高。
高温度生成 N、M 的反应速率均增大,C 错误; 17.(14 分)
D.由图可知升高温度时,更有利于生成 N,导致反应物浓度降低使得生成 M 的平衡逆向移动, (1)增大接触面积,加快反应速率,增大浸出率(1 分);
则 M 可能转化为 N,D 正确; (2)3Ni + 8HNO3 3Ni(NO3)2 + 2NO + 4H2O(2 分);
故选 D。 (3)铁元素(1 分);防止胶体生成,易于沉淀分离(2 分)
14.D 化学反应中的能量变化 (4)防止 H 2-2S 与氨水反应,增大溶液中的 S 浓度,使 Ni 元素沉淀(2 分);CuS(1 分);
A.以太阳能为驱动力,在室温条件下可将氮气转化为氨气,能量变化是光能转化为化学能,A 溶浸(1 分)
正确;
>600℃
B.图中氢离子可能得到电子发生还原反应生成副产物氢气,B 正确; (5)无火星产生(2 分);2Ni2O3 4NiO+3O2(2 分)
C .由图,总反应为氮气和水在光催化作用下生成氨气和氧气,C 正确; 解析:
D.氮化合价由 0 变为-3 得到氨气,则 VB 上产生 3 mol h+,CB 上产生 1mol 氨气,为 22.4L(标 (1)粗镍粉碎的作用是增大接触面积,加快反应速率,增大浸出率;
) D (2准状况 , 错误。 )溶浸时,单质镍生成 Ni
2+发生的化学反应方程式为 3Ni + 8HNO3 3Ni(NO3)2 + 2NO +
15 B 4H O . 电化学基础 2 ;
A.根据分析,电极 a 为阴极,连接电源负极,A 项正确; (3)用氨水调节 pH 约为 5 除去铁元素,充分反应后需加热煮沸后过滤,加热的目的是防止
B.根据分析电解过程中消耗 H O 和 Br-2 ,而催化阶段 BrO -3 被还原成 Br-循环使用,故加入 胶体生成,易于沉淀分离;
市售的溴(纯度 99%)中含有少量的 Cl2和 I2,实验利用氧化还原反应原理制备高纯度的溴,市售的
(4)加入饱和 H2S 溶液前需先加入硝酸调节 pH 至 4.0 左右,原因是防止 H2S 与氨水反应,增大 溴滴入盛有浓 CaBr2溶液中,Cl2可与 CaBr2发生氧化还原反应而除去,I2与 Br2一起蒸馏入草酸钾
溶液中的 S2-浓度,使 Ni 元素沉淀;滤渣 2 为 CuS,滤液 2 中含有硝酸。 溶液中,并被草酸钾还原为 I-、Br-,并向溶液中滴加高锰酸钾溶液氧化 I-,加热蒸干得 KBr 固
(5)判断分解完全最简单的现象是:无火星产生。因为草酸盐分解有 CO 产生,故有火星; 体,将 KBr 固体和 K2Cr2O7固体混合均匀加入冷的蒸馏水,同时滴加适量浓 H2SO4,水浴加热蒸馏,
>600℃
2Ni2O3 4NiO+3O2。 得到的液体分液、干燥、蒸馏,可得高纯度的溴。
18.(14 分,每空 2 分) (1)仪器 C 为直形冷凝管,用于冷凝蒸气;市售的溴中含有少量的 Cl2,Cl2可与 CaBr2发生氧化
(1)难挥发性 还原反应而除去;水浴加热时,Br2、I2蒸发进入装置 D 中,分别与 K2C2O4发生氧化还原反应,由
Δ
催化剂 于 Br2为进入 D 的主要物质,故主要反应的化学方程式为Br2 +K2C2O4 2KBr+2CO2 ;
(2)① 4NH3 +5O2 4NO+6H2O ②27/(2p1);反应正向气体分子总数减小,同温时,p1条件
(2)将 D 中溶液转移至蒸发皿中,边加热边向其中滴加酸化的 KMnO4溶液至出现红棕色气体
下 NO 转化率高于 p2,故 p1>p2,x、y 点转化率相同,此时压强对容积的影响大于温度对容 (Br2),即说明 KMnO4已将 KI 全部氧化,发生反应的离子方程式为
积的影响。
Δ
(3)N2-10e-+6H2O=2NO -+12H+
- - + 2+
3 ;反应 iii 生成 O2,O2将 NO 氧化 NO2,NO2更易转化成 NO - 3 2MnO4 +10I +16H 2Mn +5I2 +8H2O;KBr 几乎未被氧化,继续加热将溶液蒸干所得固体 R 的主
(4)N2中存在氮氮三键,键能高,断键时需要较大的能量,故人工固氮是高能耗的过程
要成分为 KBr;
解析:
(3)密度液溴大于水,D 中冷的蒸馏水起到液封的作用,同时冷的蒸馏水温度较低,均可减少溴
(1)浓硫酸难挥发,产物 HNO3为气体,有利于复分解反应进行体现了浓硫酸的难挥发性和酸性。
的挥发;
催化剂
(2)①第 I 步反应为氨气的催化氧化,化学方程式为 4NH3 +5O m2 4NO+6H2O;
(4)m 克 KBr 固体的物质的量为 mol
-
,根据转移电子相等可得关系式6KBr~6e ~K Cr O ,则
119 2 2 7
②27/(2p1); 2NO+O2 2NO2 ,该反应正向气体分子总数减小,同温时, p1 条件下 NO 转化 1 m
理论上需要K2Cr2O7 的物质的量为 mol,实际所需称取 K Cr6 119 2 2
O7的质量为
T
率高于 p2 ,故 p1>p2 ,根据V nR p ,x、y 点转化率相同,则 n 相同,此时压强对容积的影 1 m mol 3 294g mol-1 0.31mg ;
响大于温度对容积的影响,故 y 点的容器容积小于 x 点的容器容积。 6 119 4
3 ① a a (5)趁热过滤的具体操作:漏斗下端管口紧靠烧杯内壁,转移溶液时用玻璃棒引流,玻璃棒下端( ) 由电极 上的物质转化可知,氮元素化合价升高,发生氧化反应,电极 为阳极,电极反
应式为 N -10e-+6H O=2NO -+12H+ 靠在三层滤纸处,滤液沿烧杯壁流下。 2 2 3 ;
②反应 iii 生成 O2,O2将 NO 氧化 NO2,NO2更易转化成 NO -3 。
(4)N2中存在氮氮三键,键能高,断键时需要较大的能量,故人工固氮是高能耗的过程。
19.(14 分)
(1)直形冷凝管(1 分);除去市售的溴中少量的 Cl2(2 分) ;
Δ
Br2 +K2C2O4 2KBr+2CO2 (2 分)
Δ
(2)蒸发皿(1 分); 2MnO-4 +10I
- +16H+ 2Mn2+ +5I2 +8H2O(2 分)
(3)液封(1 分)降低温度(1 分)
(4)0.31m(2 分)
(5)玻璃棒引流,玻璃棒下端靠在三层滤纸处(2 分)
解析:
同课章节目录
