4.1.3 怎样根据化学式进行计算 课件(共23张PPT) 2024-2025学年化学科粤版九年级上册
文档属性
| 名称 | 4.1.3 怎样根据化学式进行计算 课件(共23张PPT) 2024-2025学年化学科粤版九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-14 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
1.计算相对分子质量和组成物质各元素的质量比。
2.计算物质中某元素的质量分数。
3.能看懂某些商品标签或说明书上标示的物质成分及含量。
【知识回顾】相对原子质量的算法你还记得吗?
相对原子质量=
原子的实际质量
碳12原子质量的1/12
氢原子的相对原子质量≈1
碳原子的相对原子质量≈12
氧原子的相对原子质量≈16
我们在使用时,相对原子质量可以在元素周期表中查询得到。
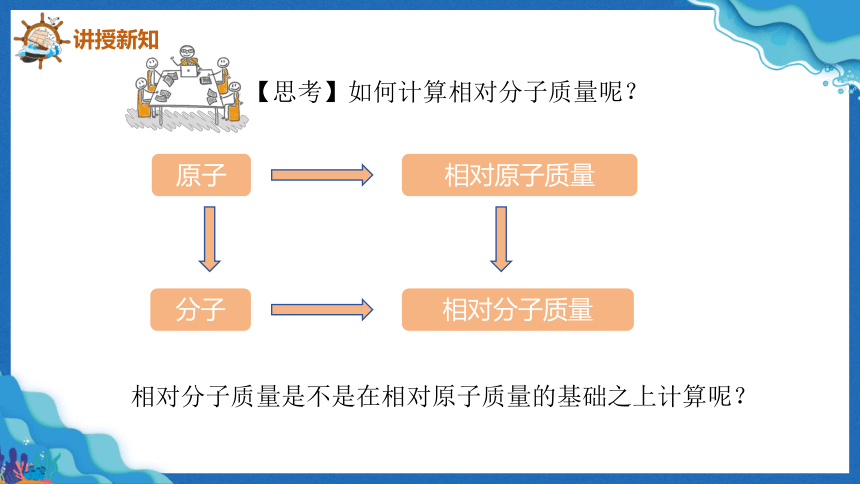
【思考】如何计算相对分子质量呢?
原子
相对原子质量
分子
相对分子质量
相对分子质量是不是在相对原子质量的基础之上计算呢?
相对分子质量:化学式中各原子的相对原子质量总和。
相对原子质量:H-1 O-16
例1:计算水(H2O)的相对分子质量。
解:水(H2O)的相对分子质量=1×2+16×1=18
一、计算相对分子质量
练习1:计算碳酸钙(CaCO3)的相对分子质量。
解:碳酸钙(CaCO3)的相对分子质量
=40×1+12×1+16×3=100
练习2:计算硝酸铵(NH4NO3)的相对分子质量。
解:硝酸铵(NH4NO3)的相对分子质量
=14×2+1×4+16×3=80
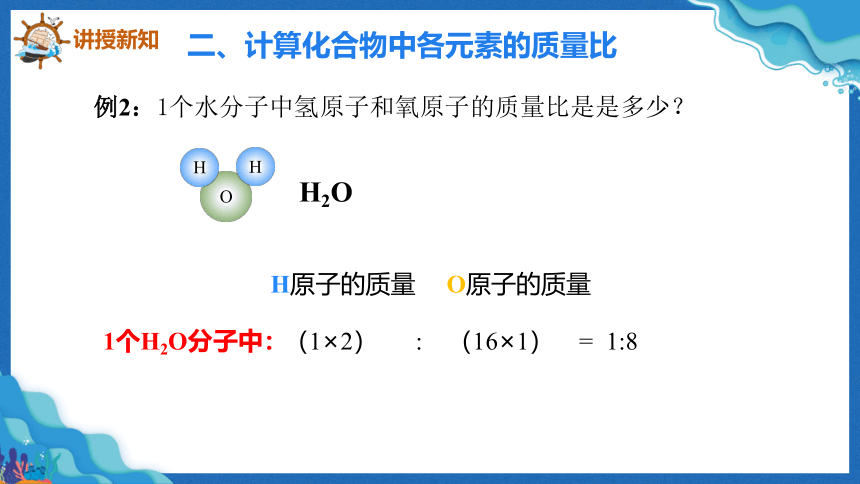
例2:1个水分子中氢原子和氧原子的质量比是是多少?
O
H
H
H2O
H原子的质量
O原子的质量
(1×2) : (16×1) = 1:8
1个H2O分子中:
二、计算化合物中各元素的质量比
2个、10个、n个水分子中氢原子和氧原子的质量比是是多少?
H原子的质量
O原子的质量
(1×2)×2 : (16×1)×2 = 1:8
2个H2O分子中:
(1×2)×10 :(16×1)×10 = 1:8
10个H2O分子中:
(1×2)×n : (16×1)×n = 1:8
n个H2O分子中:
水中各元素的质量比该怎么计算?
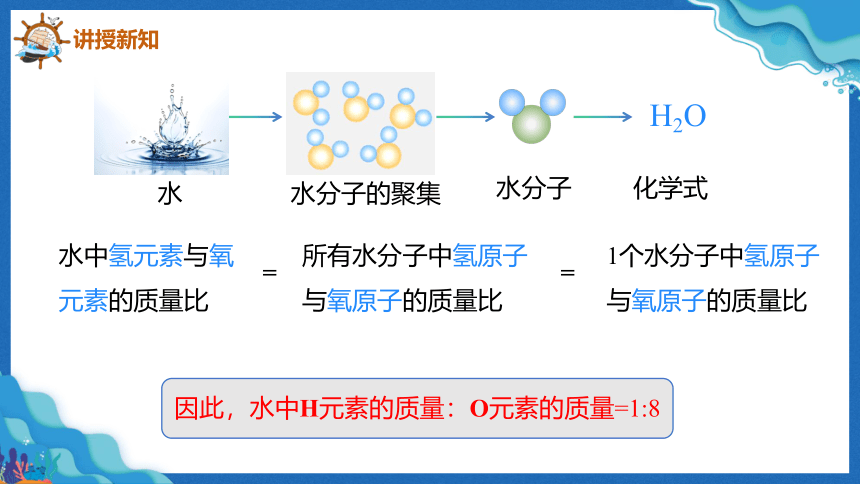
水
水分子的聚集
水分子
H2O
化学式
水中氢元素与氧元素的质量比
所有水分子中氢原子与氧原子的质量比
1个水分子中氢原子与氧原子的质量比
=
=
因此,水中H元素的质量:O元素的质量=1:8
各元素之间的质量比=各原子的相对原子质量总和之比
例3:求Fe2O3中铁元素和氧元素的质量比。
解:Fe2O3中铁元素和氧元素的质量比
m(Fe):m(O)=(56×2) :(16×3)=112:48=7:3
相对原子质量:N-14 O-16 Si-28 Fe-56
练习3:氮化硅(Si3N4)是一种新型陶瓷材料,其相对分子质量为_____,其中硅元素与氮元素的质量比为_______。
140
3:2
相对原子质量:N-14 O-16 Si-28 Fe-56
各元素之间的质量比=各原子的相对原子质量总和之比
【归纳总结】
1.如果题目中没有规定元素的比例顺序,解题时一般按照化学式中出现的元素顺序列比例式。
2.物质由几种元素组成就列几个比例项,化学式中同种元素的原子要合在一起计算。
3.计算结果一般要约成最简整数比。
这里的百分含量是什么?我们能否通过计算的方式来验证一下这里的部分营养成分是否准确呢?
某元素的质量分数=
该元素相对原子质量×原子个数
化合物的相对分子质量
× 100%
注意事项:
①质量分数——用百分数来表示
每100克该物质中含有某元素的质量
②意义:
三、计算化合物中某一元素的质量分数
例4:(1)计算二氧化硫(SO2)中硫元素的质量分数。
(2)计算64t二氧化硫中硫元素的质量。
解:(1)SO2的相对分子质量=32+16×2=64
SO2中硫元素的质量分数=
S的相对原子质量×1
SO2的相对分子质量
×100%
=
32
64
=50%
×100%
某元素的质量分数=
该元素相对原子质量×原子个数
化合物的相对分子质量
× 100%
某元素的质量=物质的质量×某元素的质量分数
某元素的质量分数 =
某元素的质量
化合物的质量
×100%
化合物的质量=某元素的质量÷某元素的质量分数
四、元素质量与化合物质量的相互换算
例5:(2)计算64t二氧化硫中硫元素的质量。
某元素的质量=物质的质量×某元素的质量分数
解:(2)64t二氧化硫中硫元素的质量=64t×50%=32t
例6:多少克二氧化碳(CO2)中含碳元素12g?
解:设质量为x的二氧化碳中含碳元素12g。
x×
12
44
×100% = 12g
x = 44g
原子个数比即化学式中各原子右下角的个数比
例7:硝酸铵(NH4NO3)中各原子的个数比。
解:N、H、O的个数比 = 2 : 4 : 3
五、计算物质中各元素的原子个数比
练习4:我国女科学家屠呦呦因提炼出用以治疗疟疾的青蒿素(C15H22O5)而获得诺贝尔奖,请回答:
(1)青蒿素分子中C、H、O原子个数比为 _____________。
(2)青蒿素中C、H、O元素的质量比为____________ 。
(3)列式计算141g青蒿素中氧元素的质量为 ________。
15 ∶22 ∶5
(2)(12×15) ∶(1×22) ∶(16×5)= 90 ∶ 11 ∶ 40
90 ∶11 ∶40
(3)
40
90+11+40
141g× ×100% =40g
40g
相对分子质量
有关相对分子质量的计算
物质组成元素
的质量比
物质中某元素的质量分数
化学式中各原子的相对原子质量的总和
各原子的相对原子质量总和之比
该元素相对原子质量×原子个数
化合物的相对分子质量
×100%
1.常用药材金银花的有效成分之一绿原酸(化学式为C16H18O9)具有抗菌、抗病毒等作用。下列关于绿原酸的说法正确的是( )
A.碳、氧元素的质量比为16:9
B.相对分子质量为258g
C.由3种元素组成
D.由 43 个原子构成
C
2.吸烟危害健康。吸烟时会吸人多种有害气体,其中有一种是氧化物,它所含的氧元素与另一种元素的质量比为4:3,这种气体是( )
A. CO B. NO C. CO2 D. SO2
A
1.计算相对分子质量和组成物质各元素的质量比。
2.计算物质中某元素的质量分数。
3.能看懂某些商品标签或说明书上标示的物质成分及含量。
【知识回顾】相对原子质量的算法你还记得吗?
相对原子质量=
原子的实际质量
碳12原子质量的1/12
氢原子的相对原子质量≈1
碳原子的相对原子质量≈12
氧原子的相对原子质量≈16
我们在使用时,相对原子质量可以在元素周期表中查询得到。
【思考】如何计算相对分子质量呢?
原子
相对原子质量
分子
相对分子质量
相对分子质量是不是在相对原子质量的基础之上计算呢?
相对分子质量:化学式中各原子的相对原子质量总和。
相对原子质量:H-1 O-16
例1:计算水(H2O)的相对分子质量。
解:水(H2O)的相对分子质量=1×2+16×1=18
一、计算相对分子质量
练习1:计算碳酸钙(CaCO3)的相对分子质量。
解:碳酸钙(CaCO3)的相对分子质量
=40×1+12×1+16×3=100
练习2:计算硝酸铵(NH4NO3)的相对分子质量。
解:硝酸铵(NH4NO3)的相对分子质量
=14×2+1×4+16×3=80
例2:1个水分子中氢原子和氧原子的质量比是是多少?
O
H
H
H2O
H原子的质量
O原子的质量
(1×2) : (16×1) = 1:8
1个H2O分子中:
二、计算化合物中各元素的质量比
2个、10个、n个水分子中氢原子和氧原子的质量比是是多少?
H原子的质量
O原子的质量
(1×2)×2 : (16×1)×2 = 1:8
2个H2O分子中:
(1×2)×10 :(16×1)×10 = 1:8
10个H2O分子中:
(1×2)×n : (16×1)×n = 1:8
n个H2O分子中:
水中各元素的质量比该怎么计算?
水
水分子的聚集
水分子
H2O
化学式
水中氢元素与氧元素的质量比
所有水分子中氢原子与氧原子的质量比
1个水分子中氢原子与氧原子的质量比
=
=
因此,水中H元素的质量:O元素的质量=1:8
各元素之间的质量比=各原子的相对原子质量总和之比
例3:求Fe2O3中铁元素和氧元素的质量比。
解:Fe2O3中铁元素和氧元素的质量比
m(Fe):m(O)=(56×2) :(16×3)=112:48=7:3
相对原子质量:N-14 O-16 Si-28 Fe-56
练习3:氮化硅(Si3N4)是一种新型陶瓷材料,其相对分子质量为_____,其中硅元素与氮元素的质量比为_______。
140
3:2
相对原子质量:N-14 O-16 Si-28 Fe-56
各元素之间的质量比=各原子的相对原子质量总和之比
【归纳总结】
1.如果题目中没有规定元素的比例顺序,解题时一般按照化学式中出现的元素顺序列比例式。
2.物质由几种元素组成就列几个比例项,化学式中同种元素的原子要合在一起计算。
3.计算结果一般要约成最简整数比。
这里的百分含量是什么?我们能否通过计算的方式来验证一下这里的部分营养成分是否准确呢?
某元素的质量分数=
该元素相对原子质量×原子个数
化合物的相对分子质量
× 100%
注意事项:
①质量分数——用百分数来表示
每100克该物质中含有某元素的质量
②意义:
三、计算化合物中某一元素的质量分数
例4:(1)计算二氧化硫(SO2)中硫元素的质量分数。
(2)计算64t二氧化硫中硫元素的质量。
解:(1)SO2的相对分子质量=32+16×2=64
SO2中硫元素的质量分数=
S的相对原子质量×1
SO2的相对分子质量
×100%
=
32
64
=50%
×100%
某元素的质量分数=
该元素相对原子质量×原子个数
化合物的相对分子质量
× 100%
某元素的质量=物质的质量×某元素的质量分数
某元素的质量分数 =
某元素的质量
化合物的质量
×100%
化合物的质量=某元素的质量÷某元素的质量分数
四、元素质量与化合物质量的相互换算
例5:(2)计算64t二氧化硫中硫元素的质量。
某元素的质量=物质的质量×某元素的质量分数
解:(2)64t二氧化硫中硫元素的质量=64t×50%=32t
例6:多少克二氧化碳(CO2)中含碳元素12g?
解:设质量为x的二氧化碳中含碳元素12g。
x×
12
44
×100% = 12g
x = 44g
原子个数比即化学式中各原子右下角的个数比
例7:硝酸铵(NH4NO3)中各原子的个数比。
解:N、H、O的个数比 = 2 : 4 : 3
五、计算物质中各元素的原子个数比
练习4:我国女科学家屠呦呦因提炼出用以治疗疟疾的青蒿素(C15H22O5)而获得诺贝尔奖,请回答:
(1)青蒿素分子中C、H、O原子个数比为 _____________。
(2)青蒿素中C、H、O元素的质量比为____________ 。
(3)列式计算141g青蒿素中氧元素的质量为 ________。
15 ∶22 ∶5
(2)(12×15) ∶(1×22) ∶(16×5)= 90 ∶ 11 ∶ 40
90 ∶11 ∶40
(3)
40
90+11+40
141g× ×100% =40g
40g
相对分子质量
有关相对分子质量的计算
物质组成元素
的质量比
物质中某元素的质量分数
化学式中各原子的相对原子质量的总和
各原子的相对原子质量总和之比
该元素相对原子质量×原子个数
化合物的相对分子质量
×100%
1.常用药材金银花的有效成分之一绿原酸(化学式为C16H18O9)具有抗菌、抗病毒等作用。下列关于绿原酸的说法正确的是( )
A.碳、氧元素的质量比为16:9
B.相对分子质量为258g
C.由3种元素组成
D.由 43 个原子构成
C
2.吸烟危害健康。吸烟时会吸人多种有害气体,其中有一种是氧化物,它所含的氧元素与另一种元素的质量比为4:3,这种气体是( )
A. CO B. NO C. CO2 D. SO2
A
同课章节目录
