3.2 氧气的制取课件(共74张PPT)
文档属性
| 名称 | 3.2 氧气的制取课件(共74张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-16 00:00:00 | ||
图片预览









文档简介
(共74张PPT)
第三单元 维持生命的物质--氧气、水
3.2 氧气的制取
目的 学习实验室制取氧气的方法,并验证氧气的化学性质。
【实验3-4】
提出问题
实验室用高锰酸钾制取氧气的装置是怎么样的
实验过程中应注意哪些操作
设计实验
实验室制取气体的装置由发生装置和收集装置两部分组成。
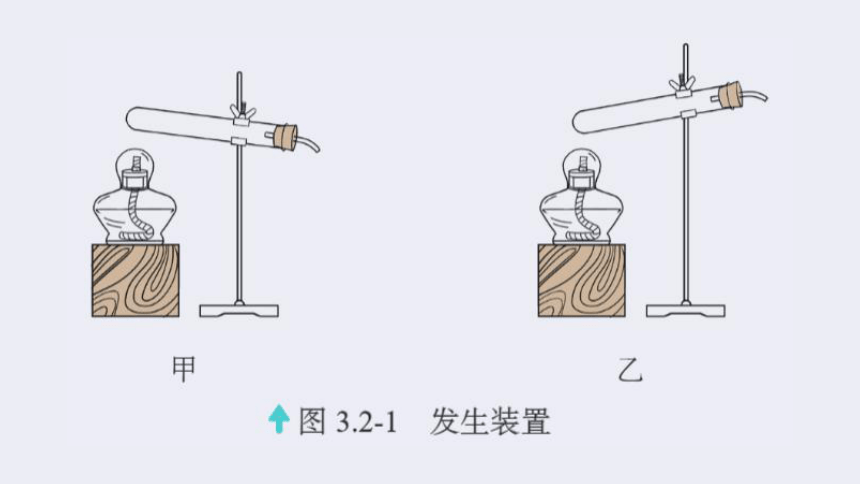
发生装置
加热高锰酸钾固体制取氧气应该选用图3.2-1装置中的哪种安装方式 说说你的理由。
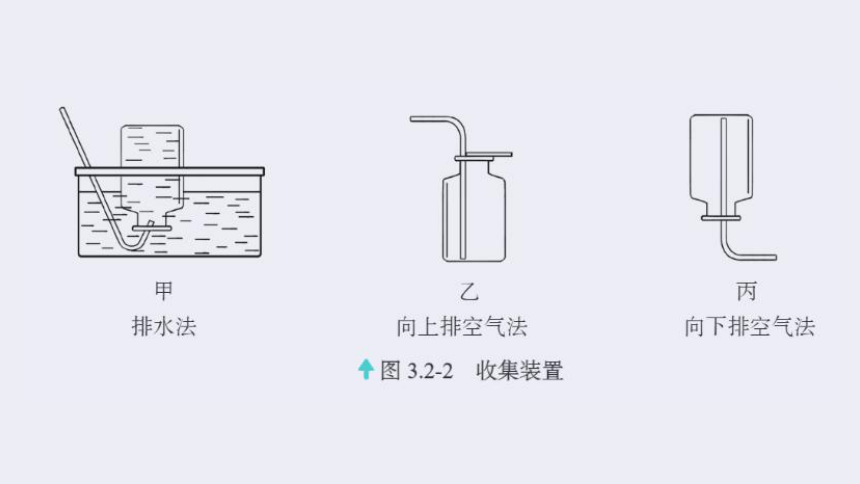
收集装置
图3.2-2的收集装置中能用于收集氧气的是为什么
请设计氧气的制取装置,在下面方框中画出装置图。
操作指引 >>>
实验开始前,先来学习仪器的简单连接操作。
进行实验
请按照制取氧气的实验装置图(如图3.2-4),准备好实验用品和仪器并组装装置。
完成组装后,按照图3.2-5的步骤实施实验。边实验边思考,边观察边记录。
反思评价
1.采用排水法或向上排空气法收集氧气,如何判断气体是否集满
当使用排水法收集氧气时,可以通过观察集气瓶口来判断氧气是否收集满
2.如果采用向上排空气法收集,实验步骤有何不同
反思评价
3.实验结束后,反思实验前的准备、实验过程中的安全注意事项实验后的清洁卫生情况。
撰写实验报告
氧气的实验室制取和性质检验
姓名:______班级:______日期:______
实验目的:学习实验室制取氧气的方法,并验证氧气的化学性质。
实验原理:
实验用品:
酒精灯、大试管、带铁夹的铁架台、玻璃导管、单孔橡胶塞、胶皮管、集气瓶、水槽、玻璃片、坩埚钳、细铁丝、木条、棉花、火柴。高锰酸钾、木炭、澄清石灰水。
实验内容与步骤 现象与结论
1.检查气密性:将导管伸入水中,手握试管,观察水中导管口的现象(如图 3.2-5a)。 观察到________________,则说叨装置的气密性良好
2.装试剂:在试管小加入在试管口放入一团棉花塞上胶塞(如图3.2-5b)
导管口有气泡冒出
实验内容与步骤 现象与结论
3.固定装置:试管口略向下倾斜,固定在铁架台上。将盛满水的集气瓶倒立在盛有水的水槽内,要求瓶内没有气泡。垫高酒精灯到适当位置,将导管伸入水槽中
实验内容与步骤 现象与结论
4.加热试管,收集气体:点燃酒精灯,先使酒精灯火焰在试管下方来回移动,再用外焰集中加热盛试剂的部位。导管口开始有气泡放出时, ▲开始加热时,观察到水槽中___________
加热片刻后,观察到的现象是__________________
实验内容与步骤 现象与结论
不宜立即收集,当气泡连续并比较均匀地放出时,再把导管口伸入集气瓶中集气(如图3.2-5d)。集满后,在水中盖好玻璃片,取出集气瓶,正放在桌上。 当观察到______________
说明集气瓶中氧气已经集满。
实验内容与步骤 现象与结论
5.撤离导管,停止加热:先将导管从水槽中移出,再熄灭酒精灯(如图 3.2-5e)。 当观察到______________
说明集气瓶中氧气已经集满。
实验内容与步骤 现象与结论
6.验证氧气的化学性质:用坩埚钳夹一小块木炭,先在空气中加热至红热,再伸人所收集的氧气瓶中,观察(如图3.2-5g)。 ▲木炭在空气中加热,观察到__________________伸入氧气瓶中观察到_________________
实验内容与步骤 现象与结论
7.整理归位:试剂归位,清洗仪器,整理实验台(如图 3.2-5g)
分析与讨论
1.装试剂后,为什么要在试管口放一团棉花
防止加热时高锰酸钾粉末进入导管,使导管堵塞。
2.若收集到的氧气不纯,你认为可能的原因有哪些
用排空气法收集氧气,时间不够长或导气管未伸到集气瓶的底部。
3.若在实验过程中出现试管炸裂,你认为可能的原因有哪些
试管受热不均匀会导致试管炸裂
实验反思
1.实验室制取氧气的装置包括发生装置和收集装置,它们的组装顺序是从下到上、从左往右。请问拆卸装置的顺序是怎样的
从左向右,自下而上
2.从反应物、生成物、反应条件、排水集气操作等方面,归纳实验室用高锰酸钾制取氧气的注意事项。
实验室常用分解过氧化氢的方法制得氧气。
观察活动 >>>
目的 观察过氧化氢在二氧化锰存在下的分解如图 3.2-6)。
包括加快和减慢
物理性质可能改变
黑色粉末
无色液体
检查站
现在你已经学习了三种实验室制取氧气的方法,请完善下表。回顾用高锰酸钾制取氧气的实验装置,设计一套用氯酸钾制取氧气的装置。
氯酸钾制取氧气的实验装置图
由一种物质生成两种或两种以上其他物质的反应,叫作分解反应。
从空气中分离氧气
液化空气制氧气是工业上常用的方法。已知液氮的沸点是-196℃,液氧的沸点是-183℃,所以当空气液化后,适当升温到-196 ℃至-183℃之间,液氮即汽化为氮气,而剩下的主要就是液氧了。
为了常温贮存、运输和使用,工厂将液态氧汽化成为氧气,用150倍大气压强的气压加以压缩后,贮存于钢瓶里。你如果在医院或气焊的工厂里,看到外壳漆蓝色的钢瓶,那就是氧气瓶利用膜分离技术富集空气中的氧气,是近年来出现的新方法。
在一定压力下,让空气通过具有氧气富集功能的薄膜,反复进行多级分离,便可得到含氧气 90% 以上的富氧空气,它在医疗、化工、炼钢、发酵等方面都有广泛的应用。
1.过氧化氢溶液俗称双氧水。向一定浓度的过氧化氢溶液中加一些二氧化锰立即产生氧气,下列说法正确的是(
A.过氧化氢中含有水和氧气
B.过氧化氢使二氧化锰分解产生氧气
C.反应物有过氧化氢和二氧化锰,不属于分解反应
D.二氧化锰促进过氧化氢分解生成氧气和水
2.实验室用高锰酸钾制取氧气的主要步骤有:①固定装置、②装人试剂、③加热、④检查装置的气密性、⑤用排水法收集。其正确操作顺序是( )
A.①②③④⑤ B.②③①④⑤
C. ④②①③⑤ D.④①②⑤③
3.在下列各个变化中,属于物理变化的是____________;属于分解反应的是_________,属于化合反应的是_________ (填序号)
①磷在空气中燃烧②分离液态空气制氧气③向过氧化氢溶液中加入二氧化锰,得到水和氧气④加热高锰酸钾制氧气⑤我国航天员在空间站通过电解水获取氧气
4.除二氧化锰外,碎瓷片和红砖小颗粒也可作为氯酸钾制氧气的催化剂。悦悦想探究哪一种催化剂可使氯酸钾分解速度更快,完成了下列的实验。
(1)悦悦选取_________ (填“A”或“B”)方式安装发生装置,并设计一组对照实验制取、收集氧气,测量反应速率。(2)实验过程中,悦悦记录如下数据。
①该实验研究了催化剂的__________对氯酸钾分解生成氧气速率的影响
②对比上述实验,________催化氯酸钾分解的速率最快。
5.调查家用制氧机、鱼缸增氧剂等生活中常见的获得氧气的途径,分析它们的制氧原理。
问题的提出:
调查的方法:
结果的分析:
第三单元 维持生命的物质--氧气、水
3.2 氧气的制取
目的 学习实验室制取氧气的方法,并验证氧气的化学性质。
【实验3-4】
提出问题
实验室用高锰酸钾制取氧气的装置是怎么样的
实验过程中应注意哪些操作
设计实验
实验室制取气体的装置由发生装置和收集装置两部分组成。
发生装置
加热高锰酸钾固体制取氧气应该选用图3.2-1装置中的哪种安装方式 说说你的理由。
收集装置
图3.2-2的收集装置中能用于收集氧气的是为什么
请设计氧气的制取装置,在下面方框中画出装置图。
操作指引 >>>
实验开始前,先来学习仪器的简单连接操作。
进行实验
请按照制取氧气的实验装置图(如图3.2-4),准备好实验用品和仪器并组装装置。
完成组装后,按照图3.2-5的步骤实施实验。边实验边思考,边观察边记录。
反思评价
1.采用排水法或向上排空气法收集氧气,如何判断气体是否集满
当使用排水法收集氧气时,可以通过观察集气瓶口来判断氧气是否收集满
2.如果采用向上排空气法收集,实验步骤有何不同
反思评价
3.实验结束后,反思实验前的准备、实验过程中的安全注意事项实验后的清洁卫生情况。
撰写实验报告
氧气的实验室制取和性质检验
姓名:______班级:______日期:______
实验目的:学习实验室制取氧气的方法,并验证氧气的化学性质。
实验原理:
实验用品:
酒精灯、大试管、带铁夹的铁架台、玻璃导管、单孔橡胶塞、胶皮管、集气瓶、水槽、玻璃片、坩埚钳、细铁丝、木条、棉花、火柴。高锰酸钾、木炭、澄清石灰水。
实验内容与步骤 现象与结论
1.检查气密性:将导管伸入水中,手握试管,观察水中导管口的现象(如图 3.2-5a)。 观察到________________,则说叨装置的气密性良好
2.装试剂:在试管小加入在试管口放入一团棉花塞上胶塞(如图3.2-5b)
导管口有气泡冒出
实验内容与步骤 现象与结论
3.固定装置:试管口略向下倾斜,固定在铁架台上。将盛满水的集气瓶倒立在盛有水的水槽内,要求瓶内没有气泡。垫高酒精灯到适当位置,将导管伸入水槽中
实验内容与步骤 现象与结论
4.加热试管,收集气体:点燃酒精灯,先使酒精灯火焰在试管下方来回移动,再用外焰集中加热盛试剂的部位。导管口开始有气泡放出时, ▲开始加热时,观察到水槽中___________
加热片刻后,观察到的现象是__________________
实验内容与步骤 现象与结论
不宜立即收集,当气泡连续并比较均匀地放出时,再把导管口伸入集气瓶中集气(如图3.2-5d)。集满后,在水中盖好玻璃片,取出集气瓶,正放在桌上。 当观察到______________
说明集气瓶中氧气已经集满。
实验内容与步骤 现象与结论
5.撤离导管,停止加热:先将导管从水槽中移出,再熄灭酒精灯(如图 3.2-5e)。 当观察到______________
说明集气瓶中氧气已经集满。
实验内容与步骤 现象与结论
6.验证氧气的化学性质:用坩埚钳夹一小块木炭,先在空气中加热至红热,再伸人所收集的氧气瓶中,观察(如图3.2-5g)。 ▲木炭在空气中加热,观察到__________________伸入氧气瓶中观察到_________________
实验内容与步骤 现象与结论
7.整理归位:试剂归位,清洗仪器,整理实验台(如图 3.2-5g)
分析与讨论
1.装试剂后,为什么要在试管口放一团棉花
防止加热时高锰酸钾粉末进入导管,使导管堵塞。
2.若收集到的氧气不纯,你认为可能的原因有哪些
用排空气法收集氧气,时间不够长或导气管未伸到集气瓶的底部。
3.若在实验过程中出现试管炸裂,你认为可能的原因有哪些
试管受热不均匀会导致试管炸裂
实验反思
1.实验室制取氧气的装置包括发生装置和收集装置,它们的组装顺序是从下到上、从左往右。请问拆卸装置的顺序是怎样的
从左向右,自下而上
2.从反应物、生成物、反应条件、排水集气操作等方面,归纳实验室用高锰酸钾制取氧气的注意事项。
实验室常用分解过氧化氢的方法制得氧气。
观察活动 >>>
目的 观察过氧化氢在二氧化锰存在下的分解如图 3.2-6)。
包括加快和减慢
物理性质可能改变
黑色粉末
无色液体
检查站
现在你已经学习了三种实验室制取氧气的方法,请完善下表。回顾用高锰酸钾制取氧气的实验装置,设计一套用氯酸钾制取氧气的装置。
氯酸钾制取氧气的实验装置图
由一种物质生成两种或两种以上其他物质的反应,叫作分解反应。
从空气中分离氧气
液化空气制氧气是工业上常用的方法。已知液氮的沸点是-196℃,液氧的沸点是-183℃,所以当空气液化后,适当升温到-196 ℃至-183℃之间,液氮即汽化为氮气,而剩下的主要就是液氧了。
为了常温贮存、运输和使用,工厂将液态氧汽化成为氧气,用150倍大气压强的气压加以压缩后,贮存于钢瓶里。你如果在医院或气焊的工厂里,看到外壳漆蓝色的钢瓶,那就是氧气瓶利用膜分离技术富集空气中的氧气,是近年来出现的新方法。
在一定压力下,让空气通过具有氧气富集功能的薄膜,反复进行多级分离,便可得到含氧气 90% 以上的富氧空气,它在医疗、化工、炼钢、发酵等方面都有广泛的应用。
1.过氧化氢溶液俗称双氧水。向一定浓度的过氧化氢溶液中加一些二氧化锰立即产生氧气,下列说法正确的是(
A.过氧化氢中含有水和氧气
B.过氧化氢使二氧化锰分解产生氧气
C.反应物有过氧化氢和二氧化锰,不属于分解反应
D.二氧化锰促进过氧化氢分解生成氧气和水
2.实验室用高锰酸钾制取氧气的主要步骤有:①固定装置、②装人试剂、③加热、④检查装置的气密性、⑤用排水法收集。其正确操作顺序是( )
A.①②③④⑤ B.②③①④⑤
C. ④②①③⑤ D.④①②⑤③
3.在下列各个变化中,属于物理变化的是____________;属于分解反应的是_________,属于化合反应的是_________ (填序号)
①磷在空气中燃烧②分离液态空气制氧气③向过氧化氢溶液中加入二氧化锰,得到水和氧气④加热高锰酸钾制氧气⑤我国航天员在空间站通过电解水获取氧气
4.除二氧化锰外,碎瓷片和红砖小颗粒也可作为氯酸钾制氧气的催化剂。悦悦想探究哪一种催化剂可使氯酸钾分解速度更快,完成了下列的实验。
(1)悦悦选取_________ (填“A”或“B”)方式安装发生装置,并设计一组对照实验制取、收集氧气,测量反应速率。(2)实验过程中,悦悦记录如下数据。
①该实验研究了催化剂的__________对氯酸钾分解生成氧气速率的影响
②对比上述实验,________催化氯酸钾分解的速率最快。
5.调查家用制氧机、鱼缸增氧剂等生活中常见的获得氧气的途径,分析它们的制氧原理。
问题的提出:
调查的方法:
结果的分析:
同课章节目录
