华师大版科学八年级上册6.3物质的分类 (课件 22PPT)
文档属性
| 名称 | 华师大版科学八年级上册6.3物质的分类 (课件 22PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 667.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2024-10-18 00:00:00 | ||
图片预览







文档简介
(共22张PPT)
考点聚焦
1、化学式
认识常见物质的化学式
解释化学式所表示的含义
b
b
2、相对原子质量和相对分子质量
知道相对原子质量和相对分子质量的概念
会查阅相对原子质量
根据化学式计算物质的相对分子质量
a
b
b
小明同学想在实验室里用大理石和稀盐酸制取一瓶二氧化碳,请写出该反应的反应物(主要成分)和生成物的化学式。
CaCO3 HCl CO2 CaCl2 H2O
认识常见物质的化学式 b
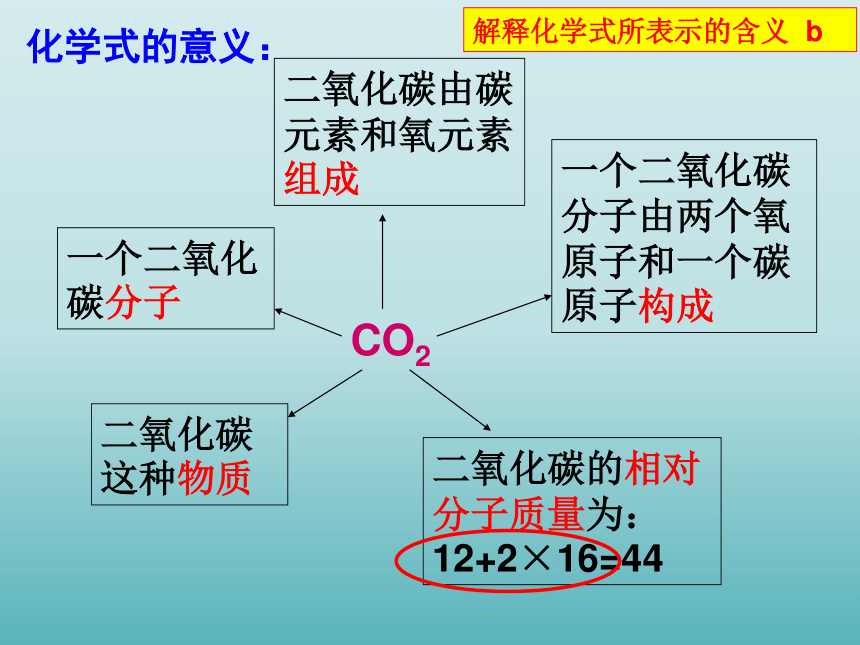
这些化学式表示什么意思?
CO2
二氧化碳这种物质
一个二氧化碳分子
二氧化碳由碳元素和氧元素组成
一个二氧化碳分子由两个氧原子和一个碳原子构成
二氧化碳的相对分子质量为:12+2×16=44
化学式的意义:
解释化学式所表示的含义 b
知道相对原子质量和相对分子质量的概念 a
C-12 O-16
把其他原子的质量与一个C-12原子质量的1/12进行比较,所得比值就是相对原子质量。
一个分子中各原子的相对原子质量总和为相对分子质量。
相对分子质量等于各原子的相对原子质量之和
会查阅相对原子质量 b
根据化学式计算物质的相对分子质量 b
12+2×16=44
下列物质的俗称(或主要成分)与其化学式不相符的是( )
A、熟石灰Ca(OH)2
B、石灰石CaCO3
C、胆矾CuSO4.5H2O
D、纯碱NaOH
经典例题
D
课堂训练
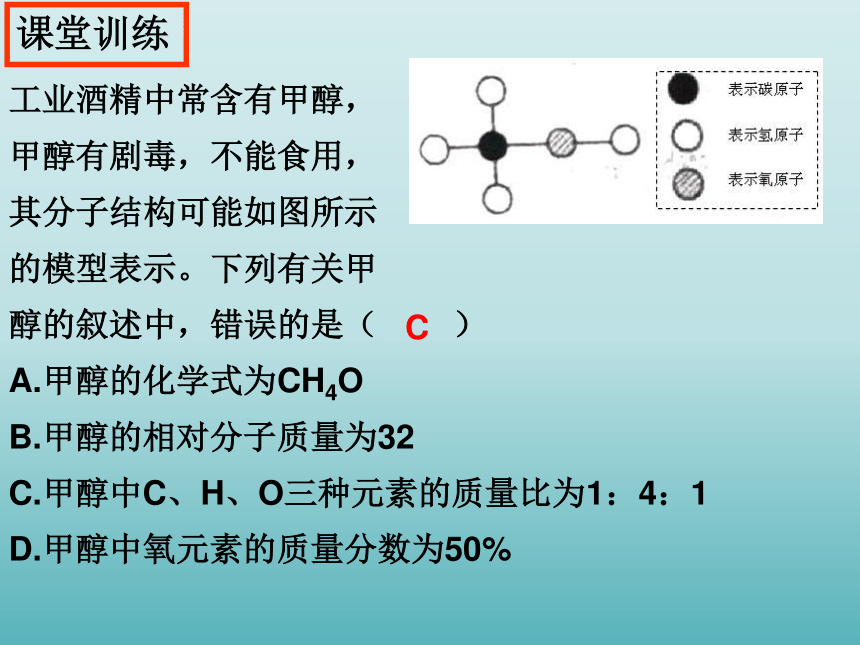
工业酒精中常含有甲醇,
甲醇有剧毒,不能食用,
其分子结构可能如图所示
的模型表示。下列有关甲
醇的叙述中,错误的是( )
A.甲醇的化学式为CH4O
B.甲醇的相对分子质量为32
C.甲醇中C、H、O三种元素的质量比为1:4:1
D.甲醇中氧元素的质量分数为50%
C
课堂训练
震后灾区要特别注意环境消毒,防止疫情发生。次氯酸钠(NaClO)是灾区使用的消毒剂之一,它与水反应的化学方程式为:NaClO+H2O=NaOH+X,反应生成的X具有强杀菌作用,X的相对分子质量为 __________。
52.5
自第十一届奥运会以来,历届奥运会都要举行颇为隆重的“火炬接力”,火炬的可燃物为丁烷(化学式C4H10),它燃烧时,火苗高且亮,在白天,二百米以外也能清晰可见,下列关于丁烷的叙述正确的是( )
①丁烷是由碳、氢两种元素组成的
②丁烷是由丁烷分子构成的
③丁烷分子是由碳、氢两种元素组成的
④丁烷由4个碳原子和10个氢原子组成
⑤丁烷分子是由碳原子和氧原子构成的
A、①②③④⑤ B、①②⑤
C、②③④⑤ D、①②④⑤
B
课堂训练
考点聚焦
3、物质的分类
运用物质组成的分类方法对常见物质进行分类
指认具体物质的类别
c
a
4、纯净物和混合物
区别纯净物和混合物
说明混合物分离的主要方法(过滤、蒸发)及操作要点
说明粗盐提纯的过程
b
b
b
小明同学所用的药品:大理石、稀盐酸
充分反应后所得:二氧化碳气体、氯化钙溶液
哪些是纯净物?哪些是混合物?
纯净物:
混合物:
大理石、稀盐酸、氯化钙溶液
二氧化碳气体
区别纯净物和混合物 b
碳酸钙+其他杂质
氯化氢+水
氯化钙+水
只有一种物质
由多种物质组成
纯净物 混合物
宏观组成 由一种物质组成 由多种物质组成
微观构成
(对由分子构成的物质而言) 由同种分子构成 由不同种分子构成
特征 一定条件下,有固定的熔点、沸点和密度 无固定的熔点、沸点和密度
联系
纯净物 混合物
多种纯净物混合
提纯
课堂训练
1.2007年底,我市市民汽车拥有量已突破30万辆。汽车给市民生活带来便捷的同时,也造成了环境污染。
(1)汽车尾气中含有二氧化碳、一氧化碳、二氧化硫、氮氧化物等物质,由此推断汽车尾气属于 ________(选填“纯净物”或“混合物”)。
混合物
课堂训练
2、下列模型中,表示纯净物的是( )
A C
化合物
单质
纯净物
单质
化合物
无机化合物
有机化合物
金属
非金属
氧化物
酸
碱
盐
金属氧化物
非金属氧化物
混合物
物质
物质的分类
运用物质组成的分类方法对常见物质进行分类 b
1、食品受潮后更易变质,因此许多食品包装中常放置干燥剂。其中生石灰(CaO)和硅胶(主要成分二氧化硅)是常用的干燥剂,生石灰和二氧化硅都属于( )
A、酸 B、碱
C、盐 D、氧化物
经典例题
D
美国和日本的三位科学家以导电有机高分子材料的研究成果,荣获了2000年度诺贝尔化学奖。在其相关技术中,用碘来掺杂聚合物,使其导电能力增加107倍,具有金属般的导电能力。碘(I2)属于( )
A.非金属单质 B.混合物 C.化合物 D.金属单质
A
课堂训练
指认具体物质的类别 b
二氧化碳制取之后,容器里留下了氯化钙溶液和剩余的大理石块,小明同学想取得氯化钙晶体,他该怎么做?
先过滤,再蒸发结晶
说明混合物分离的主要方法(过滤、蒸发)及操作要点 b
能除去液体中混有的较小的固体杂质
装置:铁架台、漏斗、滤纸、玻璃棒、烧杯等
过滤法
操作要点:
一贴:滤纸紧贴漏斗的内壁
二低:过滤时滤纸的边缘应低于漏斗的边缘,漏斗内液体的液面低于滤纸的边缘
三靠: 倾倒液体的烧杯嘴紧靠引流的玻璃棒,引流的玻璃棒轻轻靠在三层滤纸的一边,漏斗的下端紧靠接收的烧杯壁
蒸发法
能除去溶解在水中的杂质
装置:铁架台、蒸发皿、酒精灯、玻璃棒等
操作要点:
蒸发过程中玻璃棒要不断搅拌,防止液体往外飞溅,蒸发快结束时,撤走酒精灯,继续搅拌,利用蒸发皿的余热将水分蒸发干。
说明粗盐提纯的过程 b
步骤 玻璃棒的作用
溶解
过滤
蒸发
转移
搅拌,加速溶解
引流
搅拌,使液体受热均匀
转移晶体
1.用足量的含不溶性固体杂质(其含量不详)的粗盐,经提纯后配制一定溶质质量分数的NaCl溶液,实验操作有
①称量 ②过滤 ③蒸发结晶 ④计算 ⑤溶解 ⑥干燥。其先后顺序正确的是 ( )
A.④⑤②③⑤①⑥ B.④⑤②③①⑥⑤
C.⑤②③⑥④①⑤ D.④①⑤②③⑥⑤
C
2.粗盐提纯实验中,必须用到的一组仪器是 ( )
A.量筒、酒精灯、漏斗、玻璃棒
B.烧杯,漏斗、坩埚、玻璃棒
C.烧杯、酒精灯、玻璃棒、漏斗、蒸发皿
D.铁架台、烧杯、胶头滴管、酒精灯
C
课堂训练
考点聚焦
1、化学式
认识常见物质的化学式
解释化学式所表示的含义
b
b
2、相对原子质量和相对分子质量
知道相对原子质量和相对分子质量的概念
会查阅相对原子质量
根据化学式计算物质的相对分子质量
a
b
b
小明同学想在实验室里用大理石和稀盐酸制取一瓶二氧化碳,请写出该反应的反应物(主要成分)和生成物的化学式。
CaCO3 HCl CO2 CaCl2 H2O
认识常见物质的化学式 b
这些化学式表示什么意思?
CO2
二氧化碳这种物质
一个二氧化碳分子
二氧化碳由碳元素和氧元素组成
一个二氧化碳分子由两个氧原子和一个碳原子构成
二氧化碳的相对分子质量为:12+2×16=44
化学式的意义:
解释化学式所表示的含义 b
知道相对原子质量和相对分子质量的概念 a
C-12 O-16
把其他原子的质量与一个C-12原子质量的1/12进行比较,所得比值就是相对原子质量。
一个分子中各原子的相对原子质量总和为相对分子质量。
相对分子质量等于各原子的相对原子质量之和
会查阅相对原子质量 b
根据化学式计算物质的相对分子质量 b
12+2×16=44
下列物质的俗称(或主要成分)与其化学式不相符的是( )
A、熟石灰Ca(OH)2
B、石灰石CaCO3
C、胆矾CuSO4.5H2O
D、纯碱NaOH
经典例题
D
课堂训练
工业酒精中常含有甲醇,
甲醇有剧毒,不能食用,
其分子结构可能如图所示
的模型表示。下列有关甲
醇的叙述中,错误的是( )
A.甲醇的化学式为CH4O
B.甲醇的相对分子质量为32
C.甲醇中C、H、O三种元素的质量比为1:4:1
D.甲醇中氧元素的质量分数为50%
C
课堂训练
震后灾区要特别注意环境消毒,防止疫情发生。次氯酸钠(NaClO)是灾区使用的消毒剂之一,它与水反应的化学方程式为:NaClO+H2O=NaOH+X,反应生成的X具有强杀菌作用,X的相对分子质量为 __________。
52.5
自第十一届奥运会以来,历届奥运会都要举行颇为隆重的“火炬接力”,火炬的可燃物为丁烷(化学式C4H10),它燃烧时,火苗高且亮,在白天,二百米以外也能清晰可见,下列关于丁烷的叙述正确的是( )
①丁烷是由碳、氢两种元素组成的
②丁烷是由丁烷分子构成的
③丁烷分子是由碳、氢两种元素组成的
④丁烷由4个碳原子和10个氢原子组成
⑤丁烷分子是由碳原子和氧原子构成的
A、①②③④⑤ B、①②⑤
C、②③④⑤ D、①②④⑤
B
课堂训练
考点聚焦
3、物质的分类
运用物质组成的分类方法对常见物质进行分类
指认具体物质的类别
c
a
4、纯净物和混合物
区别纯净物和混合物
说明混合物分离的主要方法(过滤、蒸发)及操作要点
说明粗盐提纯的过程
b
b
b
小明同学所用的药品:大理石、稀盐酸
充分反应后所得:二氧化碳气体、氯化钙溶液
哪些是纯净物?哪些是混合物?
纯净物:
混合物:
大理石、稀盐酸、氯化钙溶液
二氧化碳气体
区别纯净物和混合物 b
碳酸钙+其他杂质
氯化氢+水
氯化钙+水
只有一种物质
由多种物质组成
纯净物 混合物
宏观组成 由一种物质组成 由多种物质组成
微观构成
(对由分子构成的物质而言) 由同种分子构成 由不同种分子构成
特征 一定条件下,有固定的熔点、沸点和密度 无固定的熔点、沸点和密度
联系
纯净物 混合物
多种纯净物混合
提纯
课堂训练
1.2007年底,我市市民汽车拥有量已突破30万辆。汽车给市民生活带来便捷的同时,也造成了环境污染。
(1)汽车尾气中含有二氧化碳、一氧化碳、二氧化硫、氮氧化物等物质,由此推断汽车尾气属于 ________(选填“纯净物”或“混合物”)。
混合物
课堂训练
2、下列模型中,表示纯净物的是( )
A C
化合物
单质
纯净物
单质
化合物
无机化合物
有机化合物
金属
非金属
氧化物
酸
碱
盐
金属氧化物
非金属氧化物
混合物
物质
物质的分类
运用物质组成的分类方法对常见物质进行分类 b
1、食品受潮后更易变质,因此许多食品包装中常放置干燥剂。其中生石灰(CaO)和硅胶(主要成分二氧化硅)是常用的干燥剂,生石灰和二氧化硅都属于( )
A、酸 B、碱
C、盐 D、氧化物
经典例题
D
美国和日本的三位科学家以导电有机高分子材料的研究成果,荣获了2000年度诺贝尔化学奖。在其相关技术中,用碘来掺杂聚合物,使其导电能力增加107倍,具有金属般的导电能力。碘(I2)属于( )
A.非金属单质 B.混合物 C.化合物 D.金属单质
A
课堂训练
指认具体物质的类别 b
二氧化碳制取之后,容器里留下了氯化钙溶液和剩余的大理石块,小明同学想取得氯化钙晶体,他该怎么做?
先过滤,再蒸发结晶
说明混合物分离的主要方法(过滤、蒸发)及操作要点 b
能除去液体中混有的较小的固体杂质
装置:铁架台、漏斗、滤纸、玻璃棒、烧杯等
过滤法
操作要点:
一贴:滤纸紧贴漏斗的内壁
二低:过滤时滤纸的边缘应低于漏斗的边缘,漏斗内液体的液面低于滤纸的边缘
三靠: 倾倒液体的烧杯嘴紧靠引流的玻璃棒,引流的玻璃棒轻轻靠在三层滤纸的一边,漏斗的下端紧靠接收的烧杯壁
蒸发法
能除去溶解在水中的杂质
装置:铁架台、蒸发皿、酒精灯、玻璃棒等
操作要点:
蒸发过程中玻璃棒要不断搅拌,防止液体往外飞溅,蒸发快结束时,撤走酒精灯,继续搅拌,利用蒸发皿的余热将水分蒸发干。
说明粗盐提纯的过程 b
步骤 玻璃棒的作用
溶解
过滤
蒸发
转移
搅拌,加速溶解
引流
搅拌,使液体受热均匀
转移晶体
1.用足量的含不溶性固体杂质(其含量不详)的粗盐,经提纯后配制一定溶质质量分数的NaCl溶液,实验操作有
①称量 ②过滤 ③蒸发结晶 ④计算 ⑤溶解 ⑥干燥。其先后顺序正确的是 ( )
A.④⑤②③⑤①⑥ B.④⑤②③①⑥⑤
C.⑤②③⑥④①⑤ D.④①⑤②③⑥⑤
C
2.粗盐提纯实验中,必须用到的一组仪器是 ( )
A.量筒、酒精灯、漏斗、玻璃棒
B.烧杯,漏斗、坩埚、玻璃棒
C.烧杯、酒精灯、玻璃棒、漏斗、蒸发皿
D.铁架台、烧杯、胶头滴管、酒精灯
C
课堂训练
同课章节目录
- 第1章 运动和力
- 1 机械运动
- 2 力
- 3 几种常见的力
- 4 运动和力
- 5 二力平衡的条件
- 第2章 压力 压强
- 1 压强
- 2 液体内部的压强
- 3 大气压强
- 4 流体的压强与流速的关系
- 第3章 浮力
- 1 密度
- 2 浮力
- 3 阿基米德原理
- 4 物体浮沉条件及其应用
- 第4章 植物的物质和能量的转化
- 1 绿色开花植物的营养器官
- 2 水在植物体中的代谢
- 3 无机盐在植物体内的代谢
- 4 植物的光合作用和呼吸作用
- 第5章 人体的物质和能量的转化
- 1 食物的消化和吸收
- 2 人体的呼吸
- 3 人体内的物质运输
- 4 人体的排泄
- 5 人体生命活动过程中物质和能量的转化
- 第6章 物质的构成
- 1 构成物质的微粒
- 2 元素
- 3 物质的分类
- 4 化学式
- 5 固态物质
