3.2.1 氧气的制取 课件(共28张PPT内嵌视频)—初中化学科粤版(2024)九年级上册
文档属性
| 名称 | 3.2.1 氧气的制取 课件(共28张PPT内嵌视频)—初中化学科粤版(2024)九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 11.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-18 00:00:00 | ||
图片预览








文档简介
(共28张PPT)
课题2 氧气的制取
旧知回顾
1.氧气的物理性质
2.氧气的化学性质
3.氧气的用途
4.什么是氧化反应?什么是化合反应?
新知导入
在上节课我们学习了氧气的性质及用途,那么这么重要的氧气在实验室中该如何制取呢?
绿色植物的光合作用?
氧化汞分解?
从空气中分离?
实验室制取气体要从反应速率、药品价格、来源、安全、所得产物是否纯净等方面综合考虑
氧气的实验室制法
加热分解高锰酸钾制取氧气
分解过氧化氢制取氧气
加热氯酸钾制取氧气
加热分解
高锰酸钾制取氧气
PART 01
1.反应原理
2.发生装置的选择
固固加热型
固液常温型
√
收集方法
适用条件
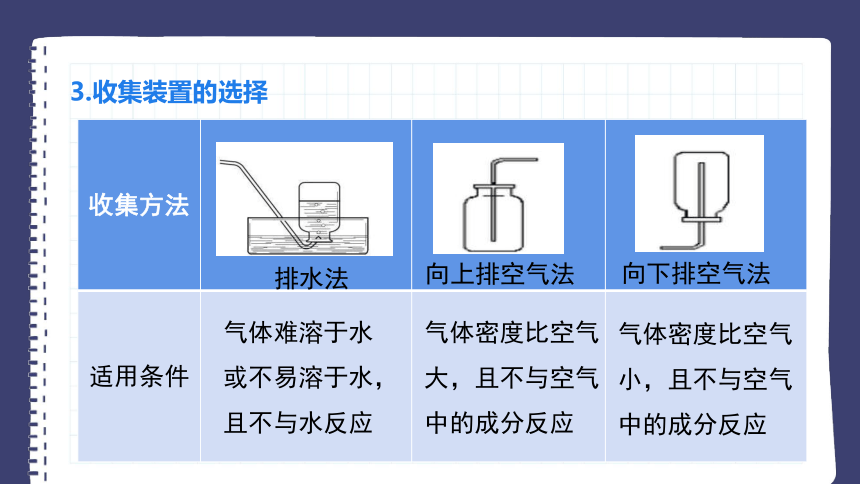
3.收集装置的选择
排水法
向上排空气法
向下排空气法
气体难溶于水或不易溶于水,且不与水反应
气体密度比空气大,且不与空气中的成分反应
气体密度比空气小,且不与空气中的成分反应
3.收集装置的选择
排水法
向上排空气法
氧气的密度比空气大,且不和空气中的成分反应,可选择向上排空气法。(收集的气体较干燥)
氧气不易溶于水,且不和水反应,可选择排水法。(收集的气体较纯净)
4.氧气的验满方法
排水法:集气瓶口有大气泡冒出时,说明氧气已集满。
向上排空气法:将带火星的木条放在集气瓶口,木条复燃,
说明氧气已集满
5.实验装置
发生装置
收集装置
酒精灯
试管
棉花
铁架台
导管
集气瓶
水槽
仪器连接
① 将玻璃管口用水润湿,稍用力将玻璃管插入胶皮管。
② 将玻璃管口用水润湿,对准胶塞的孔稍用力转动插入。
③ 手拿容器 ( 切勿抵桌面 ),将胶塞慢慢转动旋进容器口。
装置气密性的检查
方法:把导气管的一段浸入水中,用手紧握试管或热毛巾捂住试管,一段时间后把手或热毛巾移开。
现象:开始时看到导管口有气泡冒出,手或热毛巾移开一段时间后,导管中会形成一段水柱。
装置气密性的检查
方法:夹紧止水夹,向长颈漏斗中加水至长颈漏斗下端浸入液面。
现象:注入水一段时间后,长颈漏斗中液面不下降。
装置气密性的检查
方法:先加水将长颈漏斗下端浸没,缓慢推或拉注射器的活塞。
现象:长颈漏斗下端有气泡产生,长颈漏斗内液面上升。
进行实验
1.检查气密性:
将导管伸入水中,手握试管,观察水中导管口的现象。
进行实验
2.装试剂:
在试管中加入高锰酸钾,在试管口放入一团棉花,塞上胶塞。
进行实验
3.固定装置:
试管口略向下倾斜,固定在铁架台上。将盛满水的集气瓶倒立在盛有水的水槽内,要求瓶内没有气泡。垫高酒精灯至适当位置,将导管伸入水槽中
进行实验
4.加热试管,收集气体:
点燃酒精灯,先使酒精灯火焰在试管下方来回移动,再用外焰集中加热盛试剂的部位。导管口开始有气泡放出时,不宜立即收集,当气泡连续并比较均匀地放出时,再把导管口伸入集气瓶中集气。集满后,在水中盖好玻璃片,取出集气瓶,正放在桌上。
进行实验
5.撤离导管,停止加热:
先将导管从水槽中移出,再熄灭酒精灯
进行实验
6.验证氧气的化学性质:
用坩埚钳夹一小块木炭,先在空气中加热至红热,再伸入所收集的氧气瓶中,观察现象。
现象:木炭在空气中加热,观察到木炭红热;伸入氧气瓶中,观察到木炭剧烈燃烧,发出白光
进行实验
7.整理归位:
试剂归位,清洗仪器,整理实验台
实验注意事项
1.试剂要平铺在试管底部——便于均匀受热
2.试管口要略向下倾斜——防止冷凝水倒流使试管炸裂
3.试管内的导管稍稍伸出橡胶塞即可——便于气体导出
4.排水法收集气体时,待气泡连续且均匀冒出再开始收集——
防止收集到的气体中混有空气而不纯
5.实验结束时,先撤导管,再熄灭酒精灯——防止水槽中的水倒吸,炸裂试管
分析与讨论
1.装试剂后,为什么要在试管口放一团棉花?
2.若收集到的氧气不纯,你认为可能的原因有哪些?
3.若在实验过程中出现试管炸裂,你认为可能的原因有哪些?
防止加热时试管内的粉末状物质进入导管,堵塞导管
①集气瓶中未装满水;②导管口一有气泡就开始收集等
试管外壁有水、没有预热就直接加热、加热过程中试管底部触到焰心、实验结束时先熄灭酒精灯后撤导管、未待试管冷却至室温就洗涤等。
随堂练习
D
1.下列实验室制取氧气的装置和操作不正确的是( )
A.检查装置气密性 B.装入试剂
C.制氧气 D.收集氧气
2.实验室用高锰酸钾制取氧气时有如下操作步骤:
①加热 ②检查装置气密性 ③装药品 ④用排水集气法收集
⑤从水槽中取出导气管 ⑥熄灭酒精灯 ⑦连接仪器
其中操作顺序正确的是( )
A.①⑦③②⑤④⑥ B.⑦②③①④⑤⑥
C.⑤⑦③②①④⑥ D.⑦②③①④⑥⑤
随堂练习
B
3.实验室制取氧气的装置中,有关几个“口”的位置错误的是( )
A.给试管中药品加热时,试管口不应朝向人
B.用排空气法收集时,集气瓶口应向下
C.试管内的导管口稍露出胶塞即可,不能伸入太长
D.需要加热时,装固体药品的试管口应略向下倾斜
随堂练习
B
谢谢观看
课题2 氧气的制取
旧知回顾
1.氧气的物理性质
2.氧气的化学性质
3.氧气的用途
4.什么是氧化反应?什么是化合反应?
新知导入
在上节课我们学习了氧气的性质及用途,那么这么重要的氧气在实验室中该如何制取呢?
绿色植物的光合作用?
氧化汞分解?
从空气中分离?
实验室制取气体要从反应速率、药品价格、来源、安全、所得产物是否纯净等方面综合考虑
氧气的实验室制法
加热分解高锰酸钾制取氧气
分解过氧化氢制取氧气
加热氯酸钾制取氧气
加热分解
高锰酸钾制取氧气
PART 01
1.反应原理
2.发生装置的选择
固固加热型
固液常温型
√
收集方法
适用条件
3.收集装置的选择
排水法
向上排空气法
向下排空气法
气体难溶于水或不易溶于水,且不与水反应
气体密度比空气大,且不与空气中的成分反应
气体密度比空气小,且不与空气中的成分反应
3.收集装置的选择
排水法
向上排空气法
氧气的密度比空气大,且不和空气中的成分反应,可选择向上排空气法。(收集的气体较干燥)
氧气不易溶于水,且不和水反应,可选择排水法。(收集的气体较纯净)
4.氧气的验满方法
排水法:集气瓶口有大气泡冒出时,说明氧气已集满。
向上排空气法:将带火星的木条放在集气瓶口,木条复燃,
说明氧气已集满
5.实验装置
发生装置
收集装置
酒精灯
试管
棉花
铁架台
导管
集气瓶
水槽
仪器连接
① 将玻璃管口用水润湿,稍用力将玻璃管插入胶皮管。
② 将玻璃管口用水润湿,对准胶塞的孔稍用力转动插入。
③ 手拿容器 ( 切勿抵桌面 ),将胶塞慢慢转动旋进容器口。
装置气密性的检查
方法:把导气管的一段浸入水中,用手紧握试管或热毛巾捂住试管,一段时间后把手或热毛巾移开。
现象:开始时看到导管口有气泡冒出,手或热毛巾移开一段时间后,导管中会形成一段水柱。
装置气密性的检查
方法:夹紧止水夹,向长颈漏斗中加水至长颈漏斗下端浸入液面。
现象:注入水一段时间后,长颈漏斗中液面不下降。
装置气密性的检查
方法:先加水将长颈漏斗下端浸没,缓慢推或拉注射器的活塞。
现象:长颈漏斗下端有气泡产生,长颈漏斗内液面上升。
进行实验
1.检查气密性:
将导管伸入水中,手握试管,观察水中导管口的现象。
进行实验
2.装试剂:
在试管中加入高锰酸钾,在试管口放入一团棉花,塞上胶塞。
进行实验
3.固定装置:
试管口略向下倾斜,固定在铁架台上。将盛满水的集气瓶倒立在盛有水的水槽内,要求瓶内没有气泡。垫高酒精灯至适当位置,将导管伸入水槽中
进行实验
4.加热试管,收集气体:
点燃酒精灯,先使酒精灯火焰在试管下方来回移动,再用外焰集中加热盛试剂的部位。导管口开始有气泡放出时,不宜立即收集,当气泡连续并比较均匀地放出时,再把导管口伸入集气瓶中集气。集满后,在水中盖好玻璃片,取出集气瓶,正放在桌上。
进行实验
5.撤离导管,停止加热:
先将导管从水槽中移出,再熄灭酒精灯
进行实验
6.验证氧气的化学性质:
用坩埚钳夹一小块木炭,先在空气中加热至红热,再伸入所收集的氧气瓶中,观察现象。
现象:木炭在空气中加热,观察到木炭红热;伸入氧气瓶中,观察到木炭剧烈燃烧,发出白光
进行实验
7.整理归位:
试剂归位,清洗仪器,整理实验台
实验注意事项
1.试剂要平铺在试管底部——便于均匀受热
2.试管口要略向下倾斜——防止冷凝水倒流使试管炸裂
3.试管内的导管稍稍伸出橡胶塞即可——便于气体导出
4.排水法收集气体时,待气泡连续且均匀冒出再开始收集——
防止收集到的气体中混有空气而不纯
5.实验结束时,先撤导管,再熄灭酒精灯——防止水槽中的水倒吸,炸裂试管
分析与讨论
1.装试剂后,为什么要在试管口放一团棉花?
2.若收集到的氧气不纯,你认为可能的原因有哪些?
3.若在实验过程中出现试管炸裂,你认为可能的原因有哪些?
防止加热时试管内的粉末状物质进入导管,堵塞导管
①集气瓶中未装满水;②导管口一有气泡就开始收集等
试管外壁有水、没有预热就直接加热、加热过程中试管底部触到焰心、实验结束时先熄灭酒精灯后撤导管、未待试管冷却至室温就洗涤等。
随堂练习
D
1.下列实验室制取氧气的装置和操作不正确的是( )
A.检查装置气密性 B.装入试剂
C.制氧气 D.收集氧气
2.实验室用高锰酸钾制取氧气时有如下操作步骤:
①加热 ②检查装置气密性 ③装药品 ④用排水集气法收集
⑤从水槽中取出导气管 ⑥熄灭酒精灯 ⑦连接仪器
其中操作顺序正确的是( )
A.①⑦③②⑤④⑥ B.⑦②③①④⑤⑥
C.⑤⑦③②①④⑥ D.⑦②③①④⑥⑤
随堂练习
B
3.实验室制取氧气的装置中,有关几个“口”的位置错误的是( )
A.给试管中药品加热时,试管口不应朝向人
B.用排空气法收集时,集气瓶口应向下
C.试管内的导管口稍露出胶塞即可,不能伸入太长
D.需要加热时,装固体药品的试管口应略向下倾斜
随堂练习
B
谢谢观看
同课章节目录
