高考化学原电池化学电源专题复习真题分类汇编2020-2024(含答案)
文档属性
| 名称 | 高考化学原电池化学电源专题复习真题分类汇编2020-2024(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 3.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-20 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
专题13 原电池 化学电源
考向 五年考情(2020-2024) 命题趋势
考点一 原电池的工作原理及应用 2024·贵州卷;2023·广东卷;2021·广东卷;2021·山东卷 纵观近5年高考选择题,可知对原电池和化学电源的考查主要方向是以新型电池为背景的综合性电化学装置分析,涉及电极的判断、电极反应式书写、电极产物的判断、电子的转移或电流的方向和溶液中离子的移动方向的判断、溶液pH的变化、离子交换膜作用以及有关计算等。
考点二 化学电源 2024·全国甲卷;2024·新课标卷;2024·安徽卷;2024·江苏卷;2024·河北卷;2023·全国乙卷;2023·新课标卷;2023·河北卷;2023·福建卷;2023·山东卷;2023·辽宁卷;2022·湖南卷;2022·福建卷;2022·全国乙卷;2022·广东卷等
考点三 多池和多室电化学装置 2022·全国甲卷;2022·山东卷;2021·湖南卷;2020·山东卷
考点一 原电池的工作原理及应用
1.(2024·贵州卷)根据下列实验操作及现象所推出的结论正确的是
选项 实验操作及现象 结论
A 将Zn和溶液与Cu和溶液组成双液原电池,连通后铜片上有固体沉积 原电池中Zn作正极,Cu作负极
B 向洁净试管中加入新制银氨溶液,滴入几滴乙醛,振荡,水浴加热,试管壁上出现银镜 乙醛有氧化性
C 向苯酚浊液中加入足量溶液,溶液由浑浊变澄清 苯酚的酸性比强
D 向溶液中先通入适量,无明显现象,再加入稀,有白色沉淀生成 稀有氧化性
2.(2023·广东卷)负载有和的活性炭,可选择性去除实现废酸的纯化,其工作原理如图。下列说法正确的是
A.作原电池正极
B.电子由经活性炭流向
C.表面发生的电极反应:
D.每消耗标准状况下的,最多去除
3.(2021·广东卷)火星大气中含有大量,一种有参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
A.负极上发生还原反应
B.在正极上得电子
C.阳离子由正极移向负极
D.将电能转化为化学能
4.(2021·山东卷)以KOH溶液为离子导体,分别组成CH3OH—O2、N2H4—O2、(CH3)2NNH2—O2清洁燃料电池,下列说法正确的是
A.放电过程中,K+均向负极移动
B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH3)2NNH2—O2燃料电池的理论放电量最大
D.消耗1molO2时,理论上N2H4—O2燃料电池气体产物的体积在标准状况下为11.2L
考点二 化学电源
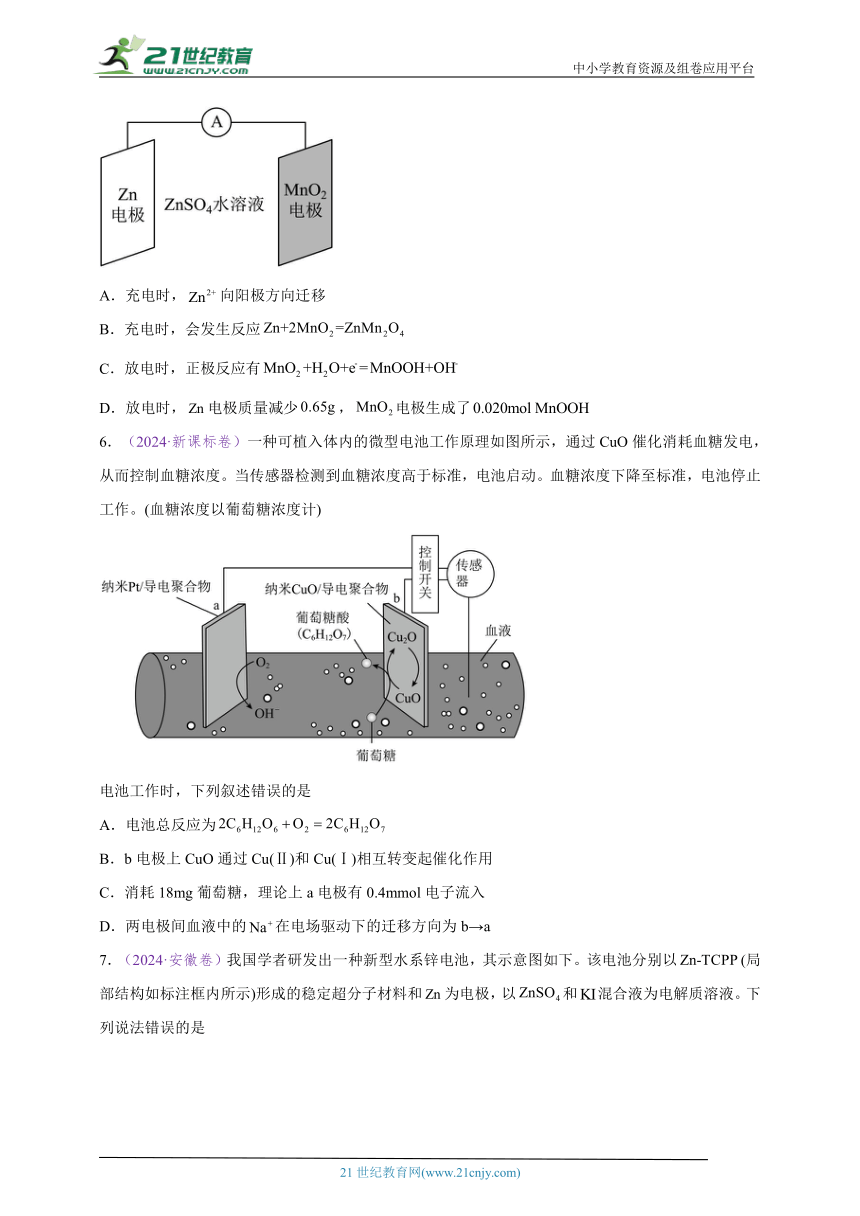
5.(2024·全国甲卷)科学家使用研制了一种可充电电池(如图所示)。电池工作一段时间后,电极上检测到和少量。下列叙述正确的是
A.充电时,向阳极方向迁移
B.充电时,会发生反应
C.放电时,正极反应有
D.放电时,电极质量减少,电极生成了
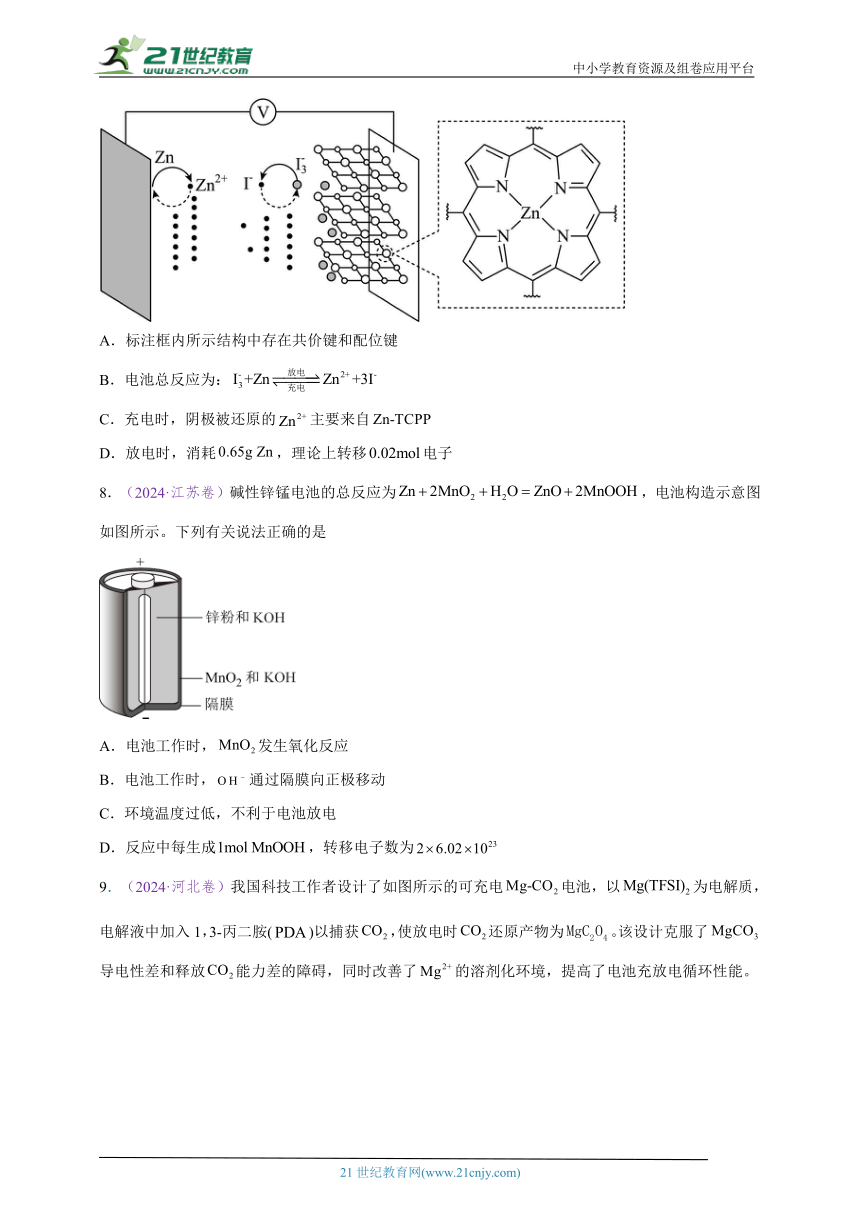
6.(2024·新课标卷)一种可植入体内的微型电池工作原理如图所示,通过CuO催化消耗血糖发电,从而控制血糖浓度。当传感器检测到血糖浓度高于标准,电池启动。血糖浓度下降至标准,电池停止工作。(血糖浓度以葡萄糖浓度计)
电池工作时,下列叙述错误的是
A.电池总反应为
B.b电极上CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用
C.消耗18mg葡萄糖,理论上a电极有0.4mmol电子流入
D.两电极间血液中的在电场驱动下的迁移方向为b→a
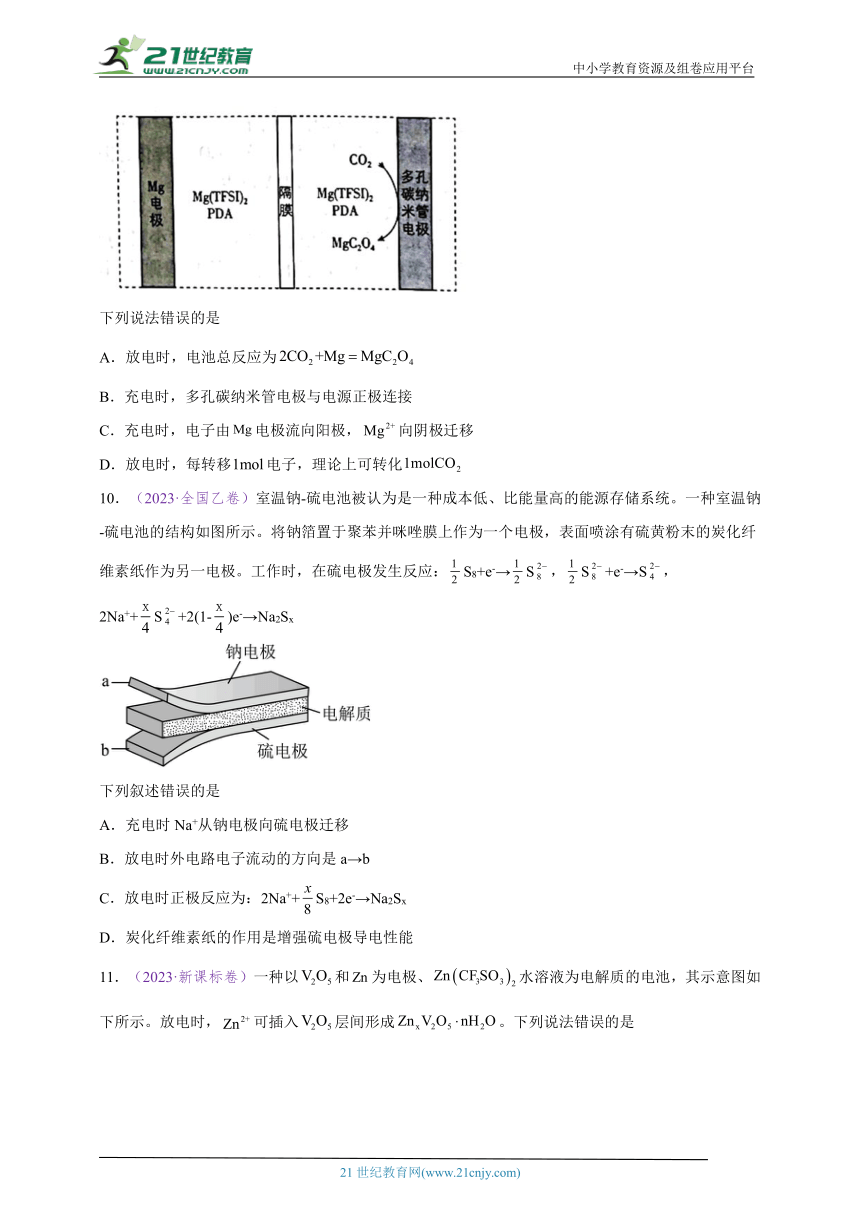
7.(2024·安徽卷)我国学者研发出一种新型水系锌电池,其示意图如下。该电池分别以(局部结构如标注框内所示)形成的稳定超分子材料和为电极,以和混合液为电解质溶液。下列说法错误的是
A.标注框内所示结构中存在共价键和配位键
B.电池总反应为:
C.充电时,阴极被还原的主要来自
D.放电时,消耗,理论上转移电子
8.(2024·江苏卷)碱性锌锰电池的总反应为,电池构造示意图如图所示。下列有关说法正确的是
A.电池工作时,发生氧化反应
B.电池工作时,通过隔膜向正极移动
C.环境温度过低,不利于电池放电
D.反应中每生成,转移电子数为
9.(2024·河北卷)我国科技工作者设计了如图所示的可充电电池,以为电解质,电解液中加入1,3-丙二胺()以捕获,使放电时还原产物为。该设计克服了导电性差和释放能力差的障碍,同时改善了的溶剂化环境,提高了电池充放电循环性能。
下列说法错误的是
A.放电时,电池总反应为
B.充电时,多孔碳纳米管电极与电源正极连接
C.充电时,电子由电极流向阳极,向阴极迁移
D.放电时,每转移电子,理论上可转化
10.(2023·全国乙卷)室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。工作时,在硫电极发生反应:S8+e-→S,S+e-→S,2Na++S+2(1-)e-→Na2Sx
下列叙述错误的是
A.充电时Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为:2Na++S8+2e-→Na2Sx
D.炭化纤维素纸的作用是增强硫电极导电性能
11.(2023·新课标卷)一种以和为电极、水溶液为电解质的电池,其示意图如下所示。放电时,可插入层间形成。下列说法错误的是
A.放电时为正极
B.放电时由负极向正极迁移
C.充电总反应:
D.充电阳极反应:
12.(2023·海南卷)利用金属Al、海水及其中的溶解氧可组成电池,如图所示。下列说法正确的是
A.b电极为电池正极
B.电池工作时,海水中的向a电极移动
C.电池工作时,紧邻a电极区域的海水呈强碱性
D.每消耗1kgAl,电池最多向外提供37mol电子的电量
13.(2023·河北卷)我国科学家发明了一种以和为电极材料的新型电池,其内部结构如下图所示,其中①区、②区、③区电解质溶液的酸碱性不同。放电时,电极材料转化为。下列说法错误的是
A.充电时,b电极上发生还原反应
B.充电时,外电源的正极连接b电极
C.放电时,①区溶液中的向②区迁移
D.放电时,a电极的电极反应式为
14.(2023·福建卷)一种可在较高温下安全快充的铝-硫电池的工作原理如图,电解质为熔融氯铝酸盐(由和形成熔点为的共熔物),其中氯铝酸根起到结合或释放的作用。电池总反应:。下列说法错误的是
A.含个键
B.中同时连接2个原子的原子有个
C.充电时,再生单质至少转移电子
D.放电时间越长,负极附近熔融盐中n值小的浓度越高
15.(2023·山东卷)利用热再生氨电池可实现电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是
A.甲室电极为正极
B.隔膜为阳离子膜
C.电池总反应为:
D.扩散到乙室将对电池电动势产生影响
16.(2023·辽宁卷)某低成本储能电池原理如下图所示。下列说法正确的是
A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧通过质子交换膜移向左侧
D.充电总反应:
17.(2022·湖南卷)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误的是
A.海水起电解质溶液作用
B.N极仅发生的电极反应:
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
18.(2022·福建卷)一种化学“自充电”的锌-有机物电池,电解质为和水溶液。将电池暴露于空气中,某电极无需外接电源即能实现化学自充电,该电极充放电原理如下图所示。下列说法正确的是
A.化学自充电时,增大
B.化学自充电时,电能转化为化学能
C.化学自充电时,锌电极反应式:
D.放电时,外电路通过电子,正极材料损耗
19.(2022·全国乙卷)电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家研究了一种光照充电电池(如图所示)。光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应(Li2O2+2h+=2Li++O2)对电池进行充电。下列叙述错误的是
A.充电时,电池的总反应
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应
20.(2022·广东卷)科学家基于易溶于的性质,发展了一种无需离子交换膜的新型氯流电池,可作储能设备(如图)。充电时电极a的反应为: 。下列说法正确的是
A.充电时电极b是阴极
B.放电时溶液的减小
C.放电时溶液的浓度增大
D.每生成,电极a质量理论上增加
21.(2022·浙江卷)通过电解废旧锂电池中的可获得难溶性的和,电解示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。下列说法不正确的是
A.电极A为阴极,发生还原反应
B.电极B的电极发应:
C.电解一段时间后溶液中浓度保持不变
D.电解结束,可通过调节除去,再加入溶液以获得
22.(2022·辽宁卷)某储能电池原理如图。下列说法正确的是
A.放电时负极反应:
B.放电时透过多孔活性炭电极向中迁移
C.放电时每转移电子,理论上吸收
D.充电过程中,溶液浓度增大
23.(2021·河北卷)K—O2电池结构如图,a和b为两个电极,其中之一为单质钾片。关于该电池,下列说法错误的是
A.隔膜允许K+通过,不允许O2通过
B.放电时,电流由b电极沿导线流向a电极;充电时,b电极为阳极
C.产生1Ah电量时,生成KO2的质量与消耗O2的质量比值约为2.22
D.用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗0.9g水
24.(2021·浙江卷)某全固态薄膜锂离子电池截面结构如图所示,电极A为非晶硅薄膜,充电时得电子成为Li嵌入该薄膜材料中;电极B为薄膜;集流体起导电作用。下列说法不正确的是
A.充电时,集流体A与外接电源的负极相连
B.放电时,外电路通过电子时,薄膜电解质损失
C.放电时,电极B为正极,反应可表示为
D.电池总反应可表示为
25.(2020·新课标Ⅰ卷)科学家近年发明了一种新型Zn CO2水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
下列说法错误的是
A. 放电时,负极反应为
B. 放电时,1 mol CO2转化为HCOOH,转移的电子数为2 mol
C. 充电时,电池总反应为
D. 充电时,正极溶液中OH 浓度升高
26.(2020·新课标Ⅲ卷)一种高性能的碱性硼化钒(VB2)—空气电池如下图所示,其中在VB2电极发生反应:该电池工作时,下列说法错误的是
A. 负载通过0.04 mol电子时,有0.224 L(标准状况)O2参与反应
B. 正极区溶液的pH降低、负极区溶液的pH升高
C. 电池总反应为
D. 电流由复合碳电极经负载、VB2电极、KOH溶液回到复合碳电极
27.(2020·天津卷)熔融钠-硫电池性能优良,是具有应用前景的储能电池。下图中的电池反应为(x=5~3,难溶于熔融硫),下列说法错误的是
A. Na2S4的电子式为
B. 放电时正极反应为
C. Na和Na2Sx分别为电池的负极和正极
D. 该电池是以为隔膜的二次电池
考点三 多池和多室电化学装置
28.(2022·全国甲卷)一种水性电解液Zn-MnO2离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以Zn(OH)存在)。电池放电时,下列叙述错误的是
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO通过隔膜向Ⅱ区迁移
C. MnO2电极反应:MnO2+2e-+4H+=Mn2++2H2O
D.电池总反应:Zn+4OH-+MnO2+4H+=Zn(OH)+Mn2++2H2O
29.(2022·山东卷)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成,将废旧锂离子电池的正极材料转化为,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为
D.若甲室减少,乙室增加,则此时已进行过溶液转移
30.(2021·湖南卷)锌溴液流电池是一种先进的水溶液电解质电池,广泛应用于再生能源储能和智能电网的备用电源等。三单体串联锌溴液流电池工作原理如图所:
下列说法错误的是
A.放电时,N极为正极
B.放电时,左侧贮液器中的浓度不断减小
C.充电时,M极的电极反应式为
D.隔膜允许阳离子通过,也允许阴离子通过
31.(2020·山东卷)微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含 CH3COO-的溶液为例)。下列说法错误的是
A. 负极反应为
B. 隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C. 当电路中转移1mol电子时,模拟海水理论上除盐58.5g
D. 电池工作一段时间后,正、负极产生气体的物质的量之比为2:1
专题13 原电池 化学电源
考向 五年考情(2020-2024) 命题趋势
考点一 原电池的工作原理及应用 2024·贵州卷;2023·广东卷;2021·广东卷;2021·山东卷 纵观近5年高考选择题,可知对原电池和化学电源的考查主要方向是以新型电池为背景的综合性电化学装置分析,涉及电极的判断、电极反应式书写、电极产物的判断、电子的转移或电流的方向和溶液中离子的移动方向的判断、溶液pH的变化、离子交换膜作用以及有关计算等。
考点二 化学电源 2024·全国甲卷;2024·新课标卷;2024·安徽卷;2024·江苏卷;2024·河北卷;2023·全国乙卷;2023·新课标卷;2023·河北卷;2023·福建卷;2023·山东卷;2023·辽宁卷;2022·湖南卷;2022·福建卷;2022·全国乙卷;2022·广东卷等
考点三 多池和多室电化学装置 2022·全国甲卷;2022·山东卷;2021·湖南卷;2020·山东卷
考点一 原电池的工作原理及应用
1.(2024·贵州卷)根据下列实验操作及现象所推出的结论正确的是
选项 实验操作及现象 结论
A 将Zn和溶液与Cu和溶液组成双液原电池,连通后铜片上有固体沉积 原电池中Zn作正极,Cu作负极
B 向洁净试管中加入新制银氨溶液,滴入几滴乙醛,振荡,水浴加热,试管壁上出现银镜 乙醛有氧化性
C 向苯酚浊液中加入足量溶液,溶液由浑浊变澄清 苯酚的酸性比强
D 向溶液中先通入适量,无明显现象,再加入稀,有白色沉淀生成 稀有氧化性
【答案】D
【解析】A.将Zn和溶液与Cu和溶液组成双液原电池,Zn活泼做负极,电极反应为: ,Cu做正极,电极反应为:,连通后铜片上有固体沉积,A错误;
B.新制银氨溶液与乙醛反应,乙醛具有还原性被新制银氨溶液氧化,,试管壁上出现银镜,B错误;
C.向苯酚浊液中加入足量溶液,溶液由浑浊变澄清,说明苯酚与反应生成苯酚钠与,酸性: 苯酚,无法判断苯酚与的酸性大小,C错误;
D.向溶液中先通入适量,无明显现象,不能用弱酸制强酸,加入稀可以氧化,,则可以和Ba2+有白色沉淀生成,D正确;
故选D。
2.(2023·广东卷)负载有和的活性炭,可选择性去除实现废酸的纯化,其工作原理如图。下列说法正确的是
A.作原电池正极
B.电子由经活性炭流向
C.表面发生的电极反应:
D.每消耗标准状况下的,最多去除
【答案】B
【分析】在Pt得电子发生还原反应,Pt为正极,Ag失去电子与溶液中的Cl-反应,Ag为负极。
【解析】A.由分析可知,Ag失去电子与溶液中的Cl-反应生成AgCl,Ag为负极,A错误;
B.电子由负极经活性炭流向正极,B正确;
C.溶液为酸性,故表面发生的电极反应为,C错误;
D.每消耗标准状况下的,转移电子2mol,而失去2mol电子,故最多去除,D错误。
故选B。
3.(2021·广东卷)火星大气中含有大量,一种有参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
A.负极上发生还原反应
B.在正极上得电子
C.阳离子由正极移向负极
D.将电能转化为化学能
【答案】B
【解析】根据题干信息可知,放电时总反应为4Na+3CO2=2Na2CO3+C。
A.放电时负极上Na发生氧化反应失去电子生成Na+,故A错误;
B.放电时正极为CO2得到电子生成C,故B正确;
C.放电时阳离子移向还原电极,即阳离子由负极移向正极,故C错误;
D.放电时装置为原电池,能量转化关系为化学能转化为电能和化学能等,故D正确;
综上所述,符合题意的为B项,故答案为B。
4.(2021·山东卷)以KOH溶液为离子导体,分别组成CH3OH—O2、N2H4—O2、(CH3)2NNH2—O2清洁燃料电池,下列说法正确的是
A.放电过程中,K+均向负极移动
B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH3)2NNH2—O2燃料电池的理论放电量最大
D.消耗1molO2时,理论上N2H4—O2燃料电池气体产物的体积在标准状况下为11.2L
【答案】C
【分析】碱性环境下,甲醇燃料电池总反应为:2CH3OH+3O2+4KOH=2K2CO3+6H2O;N2H4-O2清洁燃料电池总反应为:N2H4+O2=N2+2H2O;偏二甲肼[(CH3)2NNH2]中C和N的化合价均为-2价,H元素化合价为+1价,所以根据氧化还原反应原理可推知其燃料电池的总反应为:(CH3)2NNH2+4O2+4KOH=2K2CO3+N2+6H2O,据此结合原电池的工作原理分析解答。
【解析】A.放电过程为原电池工作原理,所以钾离子均向正极移动,A错误;
B.根据上述分析可知,N2H4-O2清洁燃料电池的产物为氮气和水,其总反应中未消耗KOH,所以KOH的物质的量不变,其他两种燃料电池根据总反应可知,KOH的物质的量减小,B错误;
C.理论放电量与燃料的物质的量和转移电子数有关,设消耗燃料的质量均为mg,则甲醇、N2H4和(CH3)2NNH2放电量(物质的量表达式)分别是:、、,通过比较可知(CH3)2NNH2理论放电量最大,C正确;
D.根据转移电子数守恒和总反应式可知,消耗1molO2生成的氮气的物质的量为1mol,在标准状况下为22.4L,D错误;
故选C。
考点二 化学电源
5.(2024·全国甲卷)科学家使用研制了一种可充电电池(如图所示)。电池工作一段时间后,电极上检测到和少量。下列叙述正确的是
A.充电时,向阳极方向迁移
B.充电时,会发生反应
C.放电时,正极反应有
D.放电时,电极质量减少,电极生成了
【答案】C
【分析】Zn具有比较强的还原性,具有比较强的氧化性,自发的氧化还原反应发生在Zn与MnO2之间,所以电极为正极,Zn电极为负极,则充电时电极为阳极、Zn电极为阴极。
【解析】A.充电时该装置为电解池,电解池中阳离子向阴极迁移,即向阴极方向迁移,A不正确;
B.放电时,负极的电极反应为,则充电时阴极反应为Zn2++2e-=Zn,即充电时Zn元素化合价应降低,而选项中Zn元素化合价升高,B不正确;
C.放电时电极为正极,正极上检测到和少量,则正极上主要发生的电极反应是,C正确;
D.放电时,Zn电极质量减少0.65g(物质的量为0.010mol),电路中转移0.020mol电子,由正极的主要反应可知,若正极上只有生成,则生成的物质的量为0.020mol,但是正极上还有生成,因此,的物质的量小于0.020mol,D不正确;
综上所述,本题选C。
6.(2024·新课标卷)一种可植入体内的微型电池工作原理如图所示,通过CuO催化消耗血糖发电,从而控制血糖浓度。当传感器检测到血糖浓度高于标准,电池启动。血糖浓度下降至标准,电池停止工作。(血糖浓度以葡萄糖浓度计)
电池工作时,下列叙述错误的是
A.电池总反应为
B.b电极上CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用
C.消耗18mg葡萄糖,理论上a电极有0.4mmol电子流入
D.两电极间血液中的在电场驱动下的迁移方向为b→a
【答案】C
【分析】由题中信息可知,b电极为负极,发生反应,然后再发生;a电极为正极,发生反应,在这个过程中发生的总反应为。
【解析】A.由题中信息可知,当电池开始工作时,a电极为电池正极,血液中的在a电极上得电子生成,电极反应式为;b电极为电池负极, 在b电极上失电子转化成CuO,电极反应式为,然后葡萄糖被CuO氧化为葡萄糖酸,CuO被还原为,则电池总反应为,A正确;
B.b电极上CuO将葡萄糖被CuO氧化为葡萄糖酸后被还原为,在b电极上失电子转化成CuO,在这个过程中CuO的质量和化学性质保持不变,因此,CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用,B正确;
C.根据反应可知,参加反应时转移2 mol电子,的物质的量为0.1 mmol,则消耗18 mg葡萄糖时,理论上a电极有0.2 mmol电子流入,C错误;
D.原电池中阳离子从负极移向正极迁移,故迁移方向为b→a,D正确。
综上所述,本题选C。
7.(2024·安徽卷)我国学者研发出一种新型水系锌电池,其示意图如下。该电池分别以(局部结构如标注框内所示)形成的稳定超分子材料和为电极,以和混合液为电解质溶液。下列说法错误的是
A.标注框内所示结构中存在共价键和配位键
B.电池总反应为:
C.充电时,阴极被还原的主要来自
D.放电时,消耗,理论上转移电子
【答案】C
【解析】由图中信息可知,该新型水系锌电池的负极是锌、正极是超分子材料;负极的电极反应式为,则充电时,该电极为阴极,电极反应式为;正极上发生,则充电时,该电极为阳极,电极反应式为。标注框内所示结构属于配合物,配位体中存在碳碳单键、碳碳双键、碳氮单键、碳氮双键和碳氢键等多种共价键,还有由提供孤电子对、提供空轨道形成的配位键,A正确;由以上分析可知,该电池总反应为,B正确;充电时,阴极电极反应式为,被还原的Zn2+主要来自电解质溶液,C错误;放电时,负极的电极反应式为,因此消耗0.65 g Zn(物质的量为0.01mol),理论上转移0.02 mol电子,D正确。
8.(2024·江苏卷)碱性锌锰电池的总反应为,电池构造示意图如图所示。下列有关说法正确的是
A.电池工作时,发生氧化反应
B.电池工作时,通过隔膜向正极移动
C.环境温度过低,不利于电池放电
D.反应中每生成,转移电子数为
【答案】C
【分析】Zn为负极,电极反应式为:,MnO2为正极,电极反应式为:。
【解析】A.电池工作时,为正极,得到电子,发生还原反应,故A错误;
B.电池工作时,通过隔膜向负极移动,故B错误;
C.环境温度过低,化学反应速率下降,不利于电池放电,故C正确;
D.由电极反应式可知,反应中每生成,转移电子数为,故D错误;
故选C。
9.(2024·河北卷)我国科技工作者设计了如图所示的可充电电池,以为电解质,电解液中加入1,3-丙二胺()以捕获,使放电时还原产物为。该设计克服了导电性差和释放能力差的障碍,同时改善了的溶剂化环境,提高了电池充放电循环性能。
下列说法错误的是
A.放电时,电池总反应为
B.充电时,多孔碳纳米管电极与电源正极连接
C.充电时,电子由电极流向阳极,向阴极迁移
D.放电时,每转移电子,理论上可转化
【答案】C
【分析】放电时CO2转化为MgC2O4,碳元素化合价由+4价降低为+3价,发生还原反应,所以放电时,多孔碳纳米管电极为正极、电极为负极,则充电时多孔碳纳米管电极为阳极、电极为阴极:
定位:二次电池,放电时阳离子向正极移动,充电时阳离子向阴极移动。 电极过程电极反应式电极放电充电多孔碳纳米管电极放电充电
【解析】A.根据以上分析,放电时正极反应式为、负极反应式为,将放电时正、负电极反应式相加,可得放电时电池总反应:,故A正确;
B.充电时,多孔碳纳米管电极上发生失电子的氧化反应,则多孔碳纳米管在充电时是阳极,与电源正极连接,故B正确;
C.充电时,电极为阴极,电子从电源负极经外电路流向电极,同时向阴极迁移,故C错误;
D.根据放电时的电极反应式可知,每转移电子,有参与反应,因此每转移电子,理论上可转化,故D正确;
故答案为:C。
10.(2023·全国乙卷)室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。工作时,在硫电极发生反应:S8+e-→S,S+e-→S,2Na++S+2(1-)e-→Na2Sx
下列叙述错误的是
A.充电时Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为:2Na++S8+2e-→Na2Sx
D.炭化纤维素纸的作用是增强硫电极导电性能
【答案】A
【分析】由题意可知放电时硫电极得电子,硫电极为原电池正极,钠电极为原电池负极。
【解析】A.充电时为电解池装置,阳离子移向阴极,即钠电极,故充电时,Na+由硫电极迁移至钠电极,A错误;
B.放电时Na在a电极失去电子,失去的电子经外电路流向b电极,硫黄粉在b电极上得电子与a电极释放出的Na+结合得到Na2Sx,电子在外电路的流向为a→b,B正确;
C.由题给的的一系列方程式相加可以得到放电时正极的反应式为2Na++S8+2e-→Na2Sx,C正确;
D.炭化纤维素纸中含有大量的炭,炭具有良好的导电性,可以增强硫电极的导电性能,D正确;
故答案选A。
11.(2023·新课标卷)一种以和为电极、水溶液为电解质的电池,其示意图如下所示。放电时,可插入层间形成。下列说法错误的是
A.放电时为正极
B.放电时由负极向正极迁移
C.充电总反应:
D.充电阳极反应:
【答案】C
【分析】由题中信息可知,该电池中Zn为负极、为正极,电池的总反应为。
【解析】A.由题信息可知,放电时,可插入层间形成,发生了还原反应,则放电时为正极,A说法正确;
B.Zn为负极,放电时Zn失去电子变为,阳离子向正极迁移,则放电时由负极向正极迁移,B说法正确;
C.电池在放电时的总反应为,则其在充电时的总反应为,C说法不正确;
D.充电阳极上被氧化为,则阳极的电极反应为,D说法正确;
综上所述,本题选C。
12.(2023·海南卷)利用金属Al、海水及其中的溶解氧可组成电池,如图所示。下列说法正确的是
A.b电极为电池正极
B.电池工作时,海水中的向a电极移动
C.电池工作时,紧邻a电极区域的海水呈强碱性
D.每消耗1kgAl,电池最多向外提供37mol电子的电量
【答案】A
【分析】铝为活泼金属,发生氧化反应为负极,则石墨为正极;
【解析】A.由分析可知,b电极为电池正极,A正确;
B.电池工作时,阳离子向正极移动,故海水中的向b电极移动,B错误;
C.电池工作时,a电极反应为铝失去电子生成铝离子,铝离子水解显酸性,C错误;
D.由C分析可知,每消耗1kgAl(为),电池最多向外提供mol电子的电量,D错误;
故选A。
13.(2023·河北卷)我国科学家发明了一种以和为电极材料的新型电池,其内部结构如下图所示,其中①区、②区、③区电解质溶液的酸碱性不同。放电时,电极材料转化为。下列说法错误的是
A.充电时,b电极上发生还原反应
B.充电时,外电源的正极连接b电极
C.放电时,①区溶液中的向②区迁移
D.放电时,a电极的电极反应式为
【答案】B
【分析】放电时,电极材料转化为,电极反应 -2ne-= +2nK+,是原电池的负极,阳离子增多需要通过阳离子交换膜进入②区;二氧化锰得到电子变成锰离子,是原电池的正极,电极反应:,阳离子减少,多余的阴离子需要通过阴离子交换膜进入②区,故③为碱性溶液是电极,①为酸性溶液是二氧化锰电极。
【解析】A.充电时,b电极上得到电子,发生还原反应,A正确;
B.充电时,外电源的正极连接a电极相连,电极失去电子,电极反应为,B错误;
C.放电时,①区溶液中多余的向②区迁移,C正确;
D.放电时,a电极的电极反应式为,D正确;
故选:B。
14.(2023·福建卷)一种可在较高温下安全快充的铝-硫电池的工作原理如图,电解质为熔融氯铝酸盐(由和形成熔点为的共熔物),其中氯铝酸根起到结合或释放的作用。电池总反应:。下列说法错误的是
A.含个键
B.中同时连接2个原子的原子有个
C.充电时,再生单质至少转移电子
D.放电时间越长,负极附近熔融盐中n值小的浓度越高
【答案】D
【分析】放电时铝失去电子生成铝离子做负极,硫单质得到电子做正极,充电时铝离子得到电子生成铝发生在阴极,硫离子失去电子生成硫单质发生在阳极,依此解题。
【解析】A.的结构为,所以含个键,A正确;
B.由的结构可知同时连接2个原子的原子有个,B正确;
C.由总反应可知充电时,再生单质需由铝离子得到电子生成,所以至少转移电子,C正确;
D.由总反应可知放电时间越长,负极铝失去电子生成的铝离子越多所以n值大的浓度越高,D错误;
故选D。
15.(2023·山东卷)利用热再生氨电池可实现电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是
A.甲室电极为正极
B.隔膜为阳离子膜
C.电池总反应为:
D.扩散到乙室将对电池电动势产生影响
【答案】CD
【解析】A. 向甲室加入足量氨水后电池开始工作,则甲室电极溶解,变为铜离子与氨气形成,因此甲室电极为负极,故A错误;
B. 再原电池内电路中阳离子向正极移动,若隔膜为阳离子膜,电极溶解生成的铜离子要向右侧移动,通入氨气要消耗铜离子,显然左侧阳离子不断减小,明显不利于电池反应正常进行,故B错误;
C. 左侧负极是,正极是,则电池总反应为:,故C正确;
D. 扩散到乙室会与铜离子反应生成,铜离子浓度降低,铜离子得电子能力减弱,因此将对电池电动势产生影响,故D正确。
综上所述,答案为CD。
16.(2023·辽宁卷)某低成本储能电池原理如下图所示。下列说法正确的是
A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧通过质子交换膜移向左侧
D.充电总反应:
【答案】B
【分析】该储能电池放电时,Pb为负极,失电子结合硫酸根离子生成PbSO4,则多孔碳电极为正极,正极上Fe3+得电子转化为Fe2+,充电时,多孔碳电极为阳极,Fe2+失电子生成Fe3+,PbSO4电极为阴极,PbSO4得电子生成Pb和硫酸。
【解析】A.放电时负极上Pb失电子结合硫酸根离子生成PbSO4附着在负极上,负极质量增大,A错误;
B.储能过程中,该装置为电解池,将电能转化为化学能,B正确;
C.放电时,右侧为正极,电解质溶液中的阳离子向正极移动,左侧的H+通过质子交换膜移向右侧,C错误;
D.充电时,总反应为PbSO4+2Fe2+=Pb++2Fe3+,D错误;
故答案选B。
17.(2022·湖南卷)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误的是
A.海水起电解质溶液作用
B.N极仅发生的电极反应:
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
【答案】B
【解析】锂海水电池的总反应为2Li+2H2O═2LiOH+H2↑, M极上Li失去电子发生氧化反应,则M电极为负极,电极反应为Li-e-=Li+,N极为正极,电极反应为2H2O+2e-=2OH-+H2↑,同时氧气也可以在N极得电子,电极反应为O2+4e-+2H2O=4OH-。
A.海水中含有丰富的电解质,如氯化钠、氯化镁等,可作为电解质溶液,故A正确;
B.由上述分析可知,N为正极,电极反应为2H2O+2e-=2OH-+H2↑,和反应O2+4e-+2H2O=4OH-,故B错误;
C.Li为活泼金属,易与水反应,玻璃陶瓷的作用是防止水和Li反应,并能传导离子,故C正确;
D.该电池不可充电,属于一次电池,故D正确;
答案选B。
18.(2022·福建卷)一种化学“自充电”的锌-有机物电池,电解质为和水溶液。将电池暴露于空气中,某电极无需外接电源即能实现化学自充电,该电极充放电原理如下图所示。下列说法正确的是
A.化学自充电时,增大
B.化学自充电时,电能转化为化学能
C.化学自充电时,锌电极反应式:
D.放电时,外电路通过电子,正极材料损耗
【答案】A
【解析】A.由图可知,化学自充电时,消耗O2,该反应为O2+2H2O+4e-=4OH-,增大,故A正确;
B.化学自充电时,无需外接电源即能实现化学自充电,该过程不是电能转化为化学能,故B错误;
C.由图可知,化学自充电时,锌电极作阴极,该电极的电极反应式为O2+2H2O+4e-=4OH-,故C错误;
D.放电时,1mol转化为 ,消耗2mol K+,外电路通过电子时,正极物质增加0.02mol K+,增加的质量为0.02mol×39g/mol =0.78g,故D错误;
故选A。
19.(2022·全国乙卷)电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家研究了一种光照充电电池(如图所示)。光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应(Li2O2+2h+=2Li++O2)对电池进行充电。下列叙述错误的是
A.充电时,电池的总反应
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应
【答案】C
【解析】充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应(Li2O2+2h+=2Li++O2),则充电时总反应为Li2O2=2Li+O2,结合图示,充电时金属Li电极为阴极,光催化电极为阳极;则放电时金属Li电极为负极,光催化电极为正极;据此作答。
A.光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应对电池进行充电,结合阴极反应和阳极反应,充电时电池的总反应为Li2O2=2Li+O2,A正确;
B.充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空穴有关,故充电效率与光照产生的电子和空穴量有关,B正确;
C.放电时,金属Li电极为负极,光催化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;
D.放电时总反应为2Li+O2=Li2O2,正极反应为O2+2Li++2e-=Li2O2,D正确;
答案选C。
20.(2022·广东卷)科学家基于易溶于的性质,发展了一种无需离子交换膜的新型氯流电池,可作储能设备(如图)。充电时电极a的反应为: 。下列说法正确的是
A.充电时电极b是阴极
B.放电时溶液的减小
C.放电时溶液的浓度增大
D.每生成,电极a质量理论上增加
【答案】C
【解析】A.由充电时电极a的反应可知,充电时电极a发生还原反应,所以电极a是阴极,则电极b是阳极,故A错误;
B.放电时电极反应和充电时相反,则由放电时电极a的反应为可知,NaCl溶液的pH不变,故B错误;
C.放电时负极反应为,正极反应为,反应后Na+和Cl-浓度都增大,则放电时NaCl溶液的浓度增大,故C正确;
D.充电时阳极反应为,阴极反应为,由得失电子守恒可知,每生成1molCl2,电极a质量理论上增加23g/mol2mol=46g,故D错误;
答案选C。
21.(2022·浙江卷)通过电解废旧锂电池中的可获得难溶性的和,电解示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。下列说法不正确的是
A.电极A为阴极,发生还原反应
B.电极B的电极发应:
C.电解一段时间后溶液中浓度保持不变
D.电解结束,可通过调节除去,再加入溶液以获得
【答案】C
【解析】A.由电解示意图可知,电极B上Mn2+转化为了MnO2,锰元素化合价升高,失电子,则电极B为阳极,电极A为阴极,得电子,发生还原反应,A正确;
B.由电解示意图可知,电极B上Mn2+失电子转化为了MnO2,电极反应式为:2H2O+Mn2+-2e-=MnO2+4H+,B正确;
C.电极A为阴极, LiMn2O4得电子,电极反应式为:2LiMn2O4+6e-+16H+=2Li++4Mn2++8H2O,依据得失电子守恒,电解池总反应为:2LiMn2O4+4H+=2Li++Mn2++3MnO2+2H2O,反应生成了Mn2+,Mn2+浓度增大,C错误;
D.电解池总反应为:2LiMn2O4+4H+=2Li++Mn2++3MnO2+2H2O,电解结束后,可通过调节溶液pH将锰离子转化为沉淀除去,然后再加入碳酸钠溶液,从而获得碳酸锂,D正确;
答案选C。
22.(2022·辽宁卷)某储能电池原理如图。下列说法正确的是
A.放电时负极反应:
B.放电时透过多孔活性炭电极向中迁移
C.放电时每转移电子,理论上吸收
D.充电过程中,溶液浓度增大
【答案】A
【分析】放电时负极反应:,正极反应:Cl2+2e-=2Cl-,消耗氯气,放电时,阴离子移向负极,充电时阳极:2Cl--2e-=Cl2,由此解析。
【解析】A. 放电时负极失电子,发生氧化反应,电极反应:,故A正确;
B. 放电时,阴离子移向负极,放电时透过多孔活性炭电极向NaCl中迁移,故B错误;
C. 放电时每转移电子,正极:Cl2+2e-=2Cl-,理论上释放,故C错误;
D. 充电过程中,阳极:2Cl--2e-=Cl2,消耗氯离子,溶液浓度减小,故D错误;
故选A。
23.(2021·河北卷)K—O2电池结构如图,a和b为两个电极,其中之一为单质钾片。关于该电池,下列说法错误的是
A.隔膜允许K+通过,不允许O2通过
B.放电时,电流由b电极沿导线流向a电极;充电时,b电极为阳极
C.产生1Ah电量时,生成KO2的质量与消耗O2的质量比值约为2.22
D.用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗0.9g水
【答案】D
【分析】由图可知,a电极为原电池的负极,单质钾片失去电子发生氧化反应生成钾离子,电极反应式为K—e-=K+,b电极为正极,在钾离子作用下,氧气在正极得到电子发生还原反应生成超氧化钾;据以上分析解答。
【解析】A.金属性强的金属钾易与氧气反应,为防止钾与氧气反应,电池所选择隔膜应允许通过,不允许通过,故A正确;
B.由分析可知,放电时,a为负极,b为正极,电流由b电极沿导线流向a电极,充电时,b电极应与直流电源的正极相连,做电解池的为阳极,故B正确;
C.由分析可知,生成1mol超氧化钾时,消耗1mol氧气,两者的质量比值为1mol×71g/mol:1mol×32g/mol≈2.22:1,故C正确;
D.铅酸蓄电池充电时的总反应方程式为2PbSO4+2H2O=PbO2+Pb+2H2SO4,反应消耗2mol水,转移2mol电子,由得失电子数目守恒可知,耗钾时,铅酸蓄电池消耗水的质量为×18g/mol=1.8g,故D错误;
故选D。
24.(2021·浙江卷)某全固态薄膜锂离子电池截面结构如图所示,电极A为非晶硅薄膜,充电时得电子成为Li嵌入该薄膜材料中;电极B为薄膜;集流体起导电作用。下列说法不正确的是
A.充电时,集流体A与外接电源的负极相连
B.放电时,外电路通过电子时,薄膜电解质损失
C.放电时,电极B为正极,反应可表示为
D.电池总反应可表示为
【答案】B
【分析】由题中信息可知,该电池充电时得电子成为Li嵌入电极A中,可知电极A在充电时作阴极,故其在放电时作电池的负极,而电极B是电池的正极。
【解析】A.由图可知,集流体A与电极A相连,充电时电极A作阴极,故充电时集流体A与外接电源的负极相连,A说法正确;
B.放电时,外电路通过a mol电子时,内电路中有a mol 通过LiPON薄膜电解质从负极迁移到正极,但是LiPON薄膜电解质没有损失,B说法不正确;
C.放电时,电极B为正极,发生还原反应,反应可表示为,C说法正确;
D.电池放电时,嵌入在非晶硅薄膜中的锂失去电子变成,正极上得到电子和变为,故电池总反应可表示为,D说法正确。
综上所述,相关说法不正确的是B,本题选B。
25.(2020·新课标Ⅰ卷)科学家近年发明了一种新型Zn CO2水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
下列说法错误的是
A. 放电时,负极反应为
B. 放电时,1 mol CO2转化为HCOOH,转移的电子数为2 mol
C. 充电时,电池总反应为
D. 充电时,正极溶液中OH 浓度升高
【答案】D
【解析】由题可知,放电时,CO2转化为HCOOH,即CO2发生还原反应,故放电时右侧电极为正极,左侧电极为负极,Zn发生氧化反应生成;充电时,右侧为阳极,H2O发生氧化反应生成O2,左侧为阴极,发生还原反应生成Zn,以此分析解答。放电时,负极上Zn发生氧化反应,电极反应式为:,故A正确;放电时,CO2转化为HCOOH,C元素化合价降低2,则1molCO2转化为HCOOH时,转移电子数为2mol,故B正确;充电时,阳极上H2O转化为O2,负极上转化为Zn,电池总反应为:,故C正确;充电时,正极即为阳极,电极反应式为:,溶液中H+浓度增大,溶液中c(H+) c(OH-)=KW,温度不变时,KW不变,因此溶液中OH-浓度降低,故D错误。
26.(2020·新课标Ⅲ卷)一种高性能的碱性硼化钒(VB2)—空气电池如下图所示,其中在VB2电极发生反应:该电池工作时,下列说法错误的是
A. 负载通过0.04 mol电子时,有0.224 L(标准状况)O2参与反应
B. 正极区溶液的pH降低、负极区溶液的pH升高
C. 电池总反应为
D. 电流由复合碳电极经负载、VB2电极、KOH溶液回到复合碳电极
【答案】B
【解析】根据图示的电池结构,左侧VB2发生失电子的反应生成和,反应的电极方程式如题干所示,右侧空气中的氧气发生得电子的反应生成OH-,反应的电极方程式为O2+4e-+2H2O=4OH-,电池的总反应方程式为4VB2+11O2+20OH-+6H2O=8+4,据此分析。当负极通过0.04mol电子时,正极也通过0.04mol电子,根据正极的电极方程式,通过0.04mol电子消耗0.01mol氧气,在标况下为0.224L,A正确;反应过程中正极生成大量的OH-使正极区pH升高,负极消耗OH-使负极区OH-浓度减小pH降低,B错误;根据分析,电池的总反应为4VB2+11O2+20OH-+6H2O=8+4,C正确;电池中,电子由VB2电极经负载流向复合碳电极,电流流向与电子流向相反,则电流流向为复合碳电极→负载→VB2电极→KOH溶液→复合碳电极,D正确。
27.(2020·天津卷)熔融钠-硫电池性能优良,是具有应用前景的储能电池。下图中的电池反应为(x=5~3,难溶于熔融硫),下列说法错误的是
A. Na2S4的电子式为
B. 放电时正极反应为
C. Na和Na2Sx分别为电池的负极和正极
D. 该电池是以为隔膜的二次电池
【答案】C
【解析】根据电池反应:可知,放电时,钠作负极,发生氧化反应,电极反应为:Na-e-= Na+,硫作正极,发生还原反应,电极反应为,据此分析。Na2S4属于离子化合物,4个硫原子间形成三对共用电子对,电子式为,故A正确;放电时发生的是原电池反应,正极发生还原反应,电极反应为:,故B正确;放电时,Na为电池的负极,正极为硫单质,故C错误;放电时,该电池是以钠作负极,硫作正极的原电池,充电时,是电解池,为隔膜,起到电解质溶液的作用,该电池为二次电池,故D正确;答案选C
考点三 多池和多室电化学装置
28.(2022·全国甲卷)一种水性电解液Zn-MnO2离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以Zn(OH)存在)。电池放电时,下列叙述错误的是
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO通过隔膜向Ⅱ区迁移
C. MnO2电极反应:MnO2+2e-+4H+=Mn2++2H2O
D.电池总反应:Zn+4OH-+MnO2+4H+=Zn(OH)+Mn2++2H2O
【答案】A
【解析】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为Zn-2e-+4OH-=Zn(OH),Ⅰ区MnO2为电池的正极,电极反应为MnO2+2e-+4H+=Mn2++2H2O;电池在工作过程中,由于两个离子选择隔膜没有指明的阳离子隔膜还是阴离子隔膜,故两个离子隔膜均可以通过阴、阳离子,因此可以得到Ⅰ区消耗H+,生成Mn2+,Ⅱ区的K+向Ⅰ区移动或Ⅰ区的SO向Ⅱ区移动,Ⅲ区消耗OH-,生成Zn(OH),Ⅱ区的SO向Ⅲ区移动或Ⅲ区的K+向Ⅱ区移动。据此分析答题。
A.根据分析,Ⅱ区的K+只能向Ⅰ区移动,A错误;
B.根据分析,Ⅰ区的SO向Ⅱ区移动,B正确;
C.MnO2电极的电极反应式为MnO2+2e-+4H+=Mn2++2H2O,C正确;
D.电池的总反应为Zn+4OH-+MnO2+4H+=Zn(OH)+Mn2++2H2O,D正确;
故答案选A。
29.(2022·山东卷)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成,将废旧锂离子电池的正极材料转化为,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为
D.若甲室减少,乙室增加,则此时已进行过溶液转移
【答案】BD
【解析】由于乙室中两个电极的电势差比甲室大,所以乙室是原电池,甲室是电解池,然后根据原电池、电解池反应原理分析解答。
A.电池工作时,甲室中细菌上乙酸盐的阴离子失去电子被氧化为CO2气体,Co2+在另一个电极上得到电子,被还原产生Co单质,CH3COO-失去电子后,Na+通过阳膜进入阴极室,溶液变为NaCl溶液,溶液由碱性变为中性,溶液pH减小,A错误;
B.对于乙室,正极上LiCoO2得到电子,被还原为Co2+,同时得到Li+,其中的O与溶液中的H+结合H2O,因此电池工作一段时间后应该补充盐酸,B正确;
C.电解质溶液为酸性,不可能大量存在OH-,乙室电极反应式为:LiCoO2+e-+4H+=Li++Co2++2H2O,C错误;
D.若甲室Co2+减少200 mg,电子转移物质的量为n(e-)= ,乙室Co2+增加300 mg,转移电子的物质的量为n(e-)=,说明此时已进行过溶液转移,D正确;
故合理选项是BD。
30.(2021·湖南卷)锌溴液流电池是一种先进的水溶液电解质电池,广泛应用于再生能源储能和智能电网的备用电源等。三单体串联锌溴液流电池工作原理如图所:
下列说法错误的是
A.放电时,N极为正极
B.放电时,左侧贮液器中的浓度不断减小
C.充电时,M极的电极反应式为
D.隔膜允许阳离子通过,也允许阴离子通过
【答案】B
【分析】由图可知,放电时,N电极为电池的正极,溴在正极上得到电子发生还原反应生成溴离子,电极反应式为Br2+2e—=2Br—,M电极为负极,锌失去电子发生氧化反应生成锌离子,电极反应式为Zn—2e—=Zn2+,正极放电生成的溴离子通过离子交换膜进入左侧,同时锌离子通过交换膜进入右侧,维持两侧溴化锌溶液的浓度保持不变;充电时,M电极与直流电源的负极相连,做电解池的阴极,N电极与直流电源的正极相连,做阳极。
【解析】A.由分析可知,放电时,N电极为电池的正极,故A正确;
B.由分析可知,放电或充电时,左侧储液器和右侧储液器中溴化锌的浓度维持不变,故B错误;
C.由分析可知,充电时,M电极与直流电源的负极相连,做电解池的阴极,锌离子在阴极上得到电子发生还原反应生成锌,电极反应式为Zn2++2e—=Zn,故C正确;
D.由分析可知,放电或充电时,交换膜允许锌离子和溴离子通过,维持两侧溴化锌溶液的浓度保持不变,故D正确;
故选B。
31.(2020·山东卷)微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含 CH3COO-的溶液为例)。下列说法错误的是
A. 负极反应为
B. 隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C. 当电路中转移1mol电子时,模拟海水理论上除盐58.5g
D. 电池工作一段时间后,正、负极产生气体的物质的量之比为2:1
【答案】B
【解析】据图可知a极上CH3COOˉ转化为CO2和H+,C元素被氧化,所以a极为该原电池的负极,则b极为正极。a极为负极,CH3COOˉ失电子被氧化成CO2和H+,结合电荷守恒可得电极反应式为CH3COOˉ+2H2O-8eˉ=2CO2↑+7H+,故A正确;为了实现海水的淡化,模拟海水中的氯离子需要移向负极,即a极,则隔膜1为阴离子交换膜,钠离子需要移向正极,即b极,则隔膜2为阳离子交换膜,故B错误;
当电路中转移1mol电子时,根据电荷守恒可知,海水中会有1molClˉ移向负极,同时有1molNa+移向正极,即除去1molNaCl,质量为58.5g,故C正确;b极为正极,水溶液为酸性,所以氢离子得电子产生氢气,电极反应式为2H++2eˉ=H2↑,所以当转移8mol电子时,正极产生4mol气体,根据负极反应式可知负极产生2mol气体,物质的量之比为4:2=2:1,故D正确;故答案为B。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
专题13 原电池 化学电源
考向 五年考情(2020-2024) 命题趋势
考点一 原电池的工作原理及应用 2024·贵州卷;2023·广东卷;2021·广东卷;2021·山东卷 纵观近5年高考选择题,可知对原电池和化学电源的考查主要方向是以新型电池为背景的综合性电化学装置分析,涉及电极的判断、电极反应式书写、电极产物的判断、电子的转移或电流的方向和溶液中离子的移动方向的判断、溶液pH的变化、离子交换膜作用以及有关计算等。
考点二 化学电源 2024·全国甲卷;2024·新课标卷;2024·安徽卷;2024·江苏卷;2024·河北卷;2023·全国乙卷;2023·新课标卷;2023·河北卷;2023·福建卷;2023·山东卷;2023·辽宁卷;2022·湖南卷;2022·福建卷;2022·全国乙卷;2022·广东卷等
考点三 多池和多室电化学装置 2022·全国甲卷;2022·山东卷;2021·湖南卷;2020·山东卷
考点一 原电池的工作原理及应用
1.(2024·贵州卷)根据下列实验操作及现象所推出的结论正确的是
选项 实验操作及现象 结论
A 将Zn和溶液与Cu和溶液组成双液原电池,连通后铜片上有固体沉积 原电池中Zn作正极,Cu作负极
B 向洁净试管中加入新制银氨溶液,滴入几滴乙醛,振荡,水浴加热,试管壁上出现银镜 乙醛有氧化性
C 向苯酚浊液中加入足量溶液,溶液由浑浊变澄清 苯酚的酸性比强
D 向溶液中先通入适量,无明显现象,再加入稀,有白色沉淀生成 稀有氧化性
2.(2023·广东卷)负载有和的活性炭,可选择性去除实现废酸的纯化,其工作原理如图。下列说法正确的是
A.作原电池正极
B.电子由经活性炭流向
C.表面发生的电极反应:
D.每消耗标准状况下的,最多去除
3.(2021·广东卷)火星大气中含有大量,一种有参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
A.负极上发生还原反应
B.在正极上得电子
C.阳离子由正极移向负极
D.将电能转化为化学能
4.(2021·山东卷)以KOH溶液为离子导体,分别组成CH3OH—O2、N2H4—O2、(CH3)2NNH2—O2清洁燃料电池,下列说法正确的是
A.放电过程中,K+均向负极移动
B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH3)2NNH2—O2燃料电池的理论放电量最大
D.消耗1molO2时,理论上N2H4—O2燃料电池气体产物的体积在标准状况下为11.2L
考点二 化学电源
5.(2024·全国甲卷)科学家使用研制了一种可充电电池(如图所示)。电池工作一段时间后,电极上检测到和少量。下列叙述正确的是
A.充电时,向阳极方向迁移
B.充电时,会发生反应
C.放电时,正极反应有
D.放电时,电极质量减少,电极生成了
6.(2024·新课标卷)一种可植入体内的微型电池工作原理如图所示,通过CuO催化消耗血糖发电,从而控制血糖浓度。当传感器检测到血糖浓度高于标准,电池启动。血糖浓度下降至标准,电池停止工作。(血糖浓度以葡萄糖浓度计)
电池工作时,下列叙述错误的是
A.电池总反应为
B.b电极上CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用
C.消耗18mg葡萄糖,理论上a电极有0.4mmol电子流入
D.两电极间血液中的在电场驱动下的迁移方向为b→a
7.(2024·安徽卷)我国学者研发出一种新型水系锌电池,其示意图如下。该电池分别以(局部结构如标注框内所示)形成的稳定超分子材料和为电极,以和混合液为电解质溶液。下列说法错误的是
A.标注框内所示结构中存在共价键和配位键
B.电池总反应为:
C.充电时,阴极被还原的主要来自
D.放电时,消耗,理论上转移电子
8.(2024·江苏卷)碱性锌锰电池的总反应为,电池构造示意图如图所示。下列有关说法正确的是
A.电池工作时,发生氧化反应
B.电池工作时,通过隔膜向正极移动
C.环境温度过低,不利于电池放电
D.反应中每生成,转移电子数为
9.(2024·河北卷)我国科技工作者设计了如图所示的可充电电池,以为电解质,电解液中加入1,3-丙二胺()以捕获,使放电时还原产物为。该设计克服了导电性差和释放能力差的障碍,同时改善了的溶剂化环境,提高了电池充放电循环性能。
下列说法错误的是
A.放电时,电池总反应为
B.充电时,多孔碳纳米管电极与电源正极连接
C.充电时,电子由电极流向阳极,向阴极迁移
D.放电时,每转移电子,理论上可转化
10.(2023·全国乙卷)室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。工作时,在硫电极发生反应:S8+e-→S,S+e-→S,2Na++S+2(1-)e-→Na2Sx
下列叙述错误的是
A.充电时Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为:2Na++S8+2e-→Na2Sx
D.炭化纤维素纸的作用是增强硫电极导电性能
11.(2023·新课标卷)一种以和为电极、水溶液为电解质的电池,其示意图如下所示。放电时,可插入层间形成。下列说法错误的是
A.放电时为正极
B.放电时由负极向正极迁移
C.充电总反应:
D.充电阳极反应:
12.(2023·海南卷)利用金属Al、海水及其中的溶解氧可组成电池,如图所示。下列说法正确的是
A.b电极为电池正极
B.电池工作时,海水中的向a电极移动
C.电池工作时,紧邻a电极区域的海水呈强碱性
D.每消耗1kgAl,电池最多向外提供37mol电子的电量
13.(2023·河北卷)我国科学家发明了一种以和为电极材料的新型电池,其内部结构如下图所示,其中①区、②区、③区电解质溶液的酸碱性不同。放电时,电极材料转化为。下列说法错误的是
A.充电时,b电极上发生还原反应
B.充电时,外电源的正极连接b电极
C.放电时,①区溶液中的向②区迁移
D.放电时,a电极的电极反应式为
14.(2023·福建卷)一种可在较高温下安全快充的铝-硫电池的工作原理如图,电解质为熔融氯铝酸盐(由和形成熔点为的共熔物),其中氯铝酸根起到结合或释放的作用。电池总反应:。下列说法错误的是
A.含个键
B.中同时连接2个原子的原子有个
C.充电时,再生单质至少转移电子
D.放电时间越长,负极附近熔融盐中n值小的浓度越高
15.(2023·山东卷)利用热再生氨电池可实现电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是
A.甲室电极为正极
B.隔膜为阳离子膜
C.电池总反应为:
D.扩散到乙室将对电池电动势产生影响
16.(2023·辽宁卷)某低成本储能电池原理如下图所示。下列说法正确的是
A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧通过质子交换膜移向左侧
D.充电总反应:
17.(2022·湖南卷)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误的是
A.海水起电解质溶液作用
B.N极仅发生的电极反应:
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
18.(2022·福建卷)一种化学“自充电”的锌-有机物电池,电解质为和水溶液。将电池暴露于空气中,某电极无需外接电源即能实现化学自充电,该电极充放电原理如下图所示。下列说法正确的是
A.化学自充电时,增大
B.化学自充电时,电能转化为化学能
C.化学自充电时,锌电极反应式:
D.放电时,外电路通过电子,正极材料损耗
19.(2022·全国乙卷)电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家研究了一种光照充电电池(如图所示)。光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应(Li2O2+2h+=2Li++O2)对电池进行充电。下列叙述错误的是
A.充电时,电池的总反应
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应
20.(2022·广东卷)科学家基于易溶于的性质,发展了一种无需离子交换膜的新型氯流电池,可作储能设备(如图)。充电时电极a的反应为: 。下列说法正确的是
A.充电时电极b是阴极
B.放电时溶液的减小
C.放电时溶液的浓度增大
D.每生成,电极a质量理论上增加
21.(2022·浙江卷)通过电解废旧锂电池中的可获得难溶性的和,电解示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。下列说法不正确的是
A.电极A为阴极,发生还原反应
B.电极B的电极发应:
C.电解一段时间后溶液中浓度保持不变
D.电解结束,可通过调节除去,再加入溶液以获得
22.(2022·辽宁卷)某储能电池原理如图。下列说法正确的是
A.放电时负极反应:
B.放电时透过多孔活性炭电极向中迁移
C.放电时每转移电子,理论上吸收
D.充电过程中,溶液浓度增大
23.(2021·河北卷)K—O2电池结构如图,a和b为两个电极,其中之一为单质钾片。关于该电池,下列说法错误的是
A.隔膜允许K+通过,不允许O2通过
B.放电时,电流由b电极沿导线流向a电极;充电时,b电极为阳极
C.产生1Ah电量时,生成KO2的质量与消耗O2的质量比值约为2.22
D.用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗0.9g水
24.(2021·浙江卷)某全固态薄膜锂离子电池截面结构如图所示,电极A为非晶硅薄膜,充电时得电子成为Li嵌入该薄膜材料中;电极B为薄膜;集流体起导电作用。下列说法不正确的是
A.充电时,集流体A与外接电源的负极相连
B.放电时,外电路通过电子时,薄膜电解质损失
C.放电时,电极B为正极,反应可表示为
D.电池总反应可表示为
25.(2020·新课标Ⅰ卷)科学家近年发明了一种新型Zn CO2水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
下列说法错误的是
A. 放电时,负极反应为
B. 放电时,1 mol CO2转化为HCOOH,转移的电子数为2 mol
C. 充电时,电池总反应为
D. 充电时,正极溶液中OH 浓度升高
26.(2020·新课标Ⅲ卷)一种高性能的碱性硼化钒(VB2)—空气电池如下图所示,其中在VB2电极发生反应:该电池工作时,下列说法错误的是
A. 负载通过0.04 mol电子时,有0.224 L(标准状况)O2参与反应
B. 正极区溶液的pH降低、负极区溶液的pH升高
C. 电池总反应为
D. 电流由复合碳电极经负载、VB2电极、KOH溶液回到复合碳电极
27.(2020·天津卷)熔融钠-硫电池性能优良,是具有应用前景的储能电池。下图中的电池反应为(x=5~3,难溶于熔融硫),下列说法错误的是
A. Na2S4的电子式为
B. 放电时正极反应为
C. Na和Na2Sx分别为电池的负极和正极
D. 该电池是以为隔膜的二次电池
考点三 多池和多室电化学装置
28.(2022·全国甲卷)一种水性电解液Zn-MnO2离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以Zn(OH)存在)。电池放电时,下列叙述错误的是
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO通过隔膜向Ⅱ区迁移
C. MnO2电极反应:MnO2+2e-+4H+=Mn2++2H2O
D.电池总反应:Zn+4OH-+MnO2+4H+=Zn(OH)+Mn2++2H2O
29.(2022·山东卷)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成,将废旧锂离子电池的正极材料转化为,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为
D.若甲室减少,乙室增加,则此时已进行过溶液转移
30.(2021·湖南卷)锌溴液流电池是一种先进的水溶液电解质电池,广泛应用于再生能源储能和智能电网的备用电源等。三单体串联锌溴液流电池工作原理如图所:
下列说法错误的是
A.放电时,N极为正极
B.放电时,左侧贮液器中的浓度不断减小
C.充电时,M极的电极反应式为
D.隔膜允许阳离子通过,也允许阴离子通过
31.(2020·山东卷)微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含 CH3COO-的溶液为例)。下列说法错误的是
A. 负极反应为
B. 隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C. 当电路中转移1mol电子时,模拟海水理论上除盐58.5g
D. 电池工作一段时间后,正、负极产生气体的物质的量之比为2:1
专题13 原电池 化学电源
考向 五年考情(2020-2024) 命题趋势
考点一 原电池的工作原理及应用 2024·贵州卷;2023·广东卷;2021·广东卷;2021·山东卷 纵观近5年高考选择题,可知对原电池和化学电源的考查主要方向是以新型电池为背景的综合性电化学装置分析,涉及电极的判断、电极反应式书写、电极产物的判断、电子的转移或电流的方向和溶液中离子的移动方向的判断、溶液pH的变化、离子交换膜作用以及有关计算等。
考点二 化学电源 2024·全国甲卷;2024·新课标卷;2024·安徽卷;2024·江苏卷;2024·河北卷;2023·全国乙卷;2023·新课标卷;2023·河北卷;2023·福建卷;2023·山东卷;2023·辽宁卷;2022·湖南卷;2022·福建卷;2022·全国乙卷;2022·广东卷等
考点三 多池和多室电化学装置 2022·全国甲卷;2022·山东卷;2021·湖南卷;2020·山东卷
考点一 原电池的工作原理及应用
1.(2024·贵州卷)根据下列实验操作及现象所推出的结论正确的是
选项 实验操作及现象 结论
A 将Zn和溶液与Cu和溶液组成双液原电池,连通后铜片上有固体沉积 原电池中Zn作正极,Cu作负极
B 向洁净试管中加入新制银氨溶液,滴入几滴乙醛,振荡,水浴加热,试管壁上出现银镜 乙醛有氧化性
C 向苯酚浊液中加入足量溶液,溶液由浑浊变澄清 苯酚的酸性比强
D 向溶液中先通入适量,无明显现象,再加入稀,有白色沉淀生成 稀有氧化性
【答案】D
【解析】A.将Zn和溶液与Cu和溶液组成双液原电池,Zn活泼做负极,电极反应为: ,Cu做正极,电极反应为:,连通后铜片上有固体沉积,A错误;
B.新制银氨溶液与乙醛反应,乙醛具有还原性被新制银氨溶液氧化,,试管壁上出现银镜,B错误;
C.向苯酚浊液中加入足量溶液,溶液由浑浊变澄清,说明苯酚与反应生成苯酚钠与,酸性: 苯酚,无法判断苯酚与的酸性大小,C错误;
D.向溶液中先通入适量,无明显现象,不能用弱酸制强酸,加入稀可以氧化,,则可以和Ba2+有白色沉淀生成,D正确;
故选D。
2.(2023·广东卷)负载有和的活性炭,可选择性去除实现废酸的纯化,其工作原理如图。下列说法正确的是
A.作原电池正极
B.电子由经活性炭流向
C.表面发生的电极反应:
D.每消耗标准状况下的,最多去除
【答案】B
【分析】在Pt得电子发生还原反应,Pt为正极,Ag失去电子与溶液中的Cl-反应,Ag为负极。
【解析】A.由分析可知,Ag失去电子与溶液中的Cl-反应生成AgCl,Ag为负极,A错误;
B.电子由负极经活性炭流向正极,B正确;
C.溶液为酸性,故表面发生的电极反应为,C错误;
D.每消耗标准状况下的,转移电子2mol,而失去2mol电子,故最多去除,D错误。
故选B。
3.(2021·广东卷)火星大气中含有大量,一种有参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
A.负极上发生还原反应
B.在正极上得电子
C.阳离子由正极移向负极
D.将电能转化为化学能
【答案】B
【解析】根据题干信息可知,放电时总反应为4Na+3CO2=2Na2CO3+C。
A.放电时负极上Na发生氧化反应失去电子生成Na+,故A错误;
B.放电时正极为CO2得到电子生成C,故B正确;
C.放电时阳离子移向还原电极,即阳离子由负极移向正极,故C错误;
D.放电时装置为原电池,能量转化关系为化学能转化为电能和化学能等,故D正确;
综上所述,符合题意的为B项,故答案为B。
4.(2021·山东卷)以KOH溶液为离子导体,分别组成CH3OH—O2、N2H4—O2、(CH3)2NNH2—O2清洁燃料电池,下列说法正确的是
A.放电过程中,K+均向负极移动
B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH3)2NNH2—O2燃料电池的理论放电量最大
D.消耗1molO2时,理论上N2H4—O2燃料电池气体产物的体积在标准状况下为11.2L
【答案】C
【分析】碱性环境下,甲醇燃料电池总反应为:2CH3OH+3O2+4KOH=2K2CO3+6H2O;N2H4-O2清洁燃料电池总反应为:N2H4+O2=N2+2H2O;偏二甲肼[(CH3)2NNH2]中C和N的化合价均为-2价,H元素化合价为+1价,所以根据氧化还原反应原理可推知其燃料电池的总反应为:(CH3)2NNH2+4O2+4KOH=2K2CO3+N2+6H2O,据此结合原电池的工作原理分析解答。
【解析】A.放电过程为原电池工作原理,所以钾离子均向正极移动,A错误;
B.根据上述分析可知,N2H4-O2清洁燃料电池的产物为氮气和水,其总反应中未消耗KOH,所以KOH的物质的量不变,其他两种燃料电池根据总反应可知,KOH的物质的量减小,B错误;
C.理论放电量与燃料的物质的量和转移电子数有关,设消耗燃料的质量均为mg,则甲醇、N2H4和(CH3)2NNH2放电量(物质的量表达式)分别是:、、,通过比较可知(CH3)2NNH2理论放电量最大,C正确;
D.根据转移电子数守恒和总反应式可知,消耗1molO2生成的氮气的物质的量为1mol,在标准状况下为22.4L,D错误;
故选C。
考点二 化学电源
5.(2024·全国甲卷)科学家使用研制了一种可充电电池(如图所示)。电池工作一段时间后,电极上检测到和少量。下列叙述正确的是
A.充电时,向阳极方向迁移
B.充电时,会发生反应
C.放电时,正极反应有
D.放电时,电极质量减少,电极生成了
【答案】C
【分析】Zn具有比较强的还原性,具有比较强的氧化性,自发的氧化还原反应发生在Zn与MnO2之间,所以电极为正极,Zn电极为负极,则充电时电极为阳极、Zn电极为阴极。
【解析】A.充电时该装置为电解池,电解池中阳离子向阴极迁移,即向阴极方向迁移,A不正确;
B.放电时,负极的电极反应为,则充电时阴极反应为Zn2++2e-=Zn,即充电时Zn元素化合价应降低,而选项中Zn元素化合价升高,B不正确;
C.放电时电极为正极,正极上检测到和少量,则正极上主要发生的电极反应是,C正确;
D.放电时,Zn电极质量减少0.65g(物质的量为0.010mol),电路中转移0.020mol电子,由正极的主要反应可知,若正极上只有生成,则生成的物质的量为0.020mol,但是正极上还有生成,因此,的物质的量小于0.020mol,D不正确;
综上所述,本题选C。
6.(2024·新课标卷)一种可植入体内的微型电池工作原理如图所示,通过CuO催化消耗血糖发电,从而控制血糖浓度。当传感器检测到血糖浓度高于标准,电池启动。血糖浓度下降至标准,电池停止工作。(血糖浓度以葡萄糖浓度计)
电池工作时,下列叙述错误的是
A.电池总反应为
B.b电极上CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用
C.消耗18mg葡萄糖,理论上a电极有0.4mmol电子流入
D.两电极间血液中的在电场驱动下的迁移方向为b→a
【答案】C
【分析】由题中信息可知,b电极为负极,发生反应,然后再发生;a电极为正极,发生反应,在这个过程中发生的总反应为。
【解析】A.由题中信息可知,当电池开始工作时,a电极为电池正极,血液中的在a电极上得电子生成,电极反应式为;b电极为电池负极, 在b电极上失电子转化成CuO,电极反应式为,然后葡萄糖被CuO氧化为葡萄糖酸,CuO被还原为,则电池总反应为,A正确;
B.b电极上CuO将葡萄糖被CuO氧化为葡萄糖酸后被还原为,在b电极上失电子转化成CuO,在这个过程中CuO的质量和化学性质保持不变,因此,CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用,B正确;
C.根据反应可知,参加反应时转移2 mol电子,的物质的量为0.1 mmol,则消耗18 mg葡萄糖时,理论上a电极有0.2 mmol电子流入,C错误;
D.原电池中阳离子从负极移向正极迁移,故迁移方向为b→a,D正确。
综上所述,本题选C。
7.(2024·安徽卷)我国学者研发出一种新型水系锌电池,其示意图如下。该电池分别以(局部结构如标注框内所示)形成的稳定超分子材料和为电极,以和混合液为电解质溶液。下列说法错误的是
A.标注框内所示结构中存在共价键和配位键
B.电池总反应为:
C.充电时,阴极被还原的主要来自
D.放电时,消耗,理论上转移电子
【答案】C
【解析】由图中信息可知,该新型水系锌电池的负极是锌、正极是超分子材料;负极的电极反应式为,则充电时,该电极为阴极,电极反应式为;正极上发生,则充电时,该电极为阳极,电极反应式为。标注框内所示结构属于配合物,配位体中存在碳碳单键、碳碳双键、碳氮单键、碳氮双键和碳氢键等多种共价键,还有由提供孤电子对、提供空轨道形成的配位键,A正确;由以上分析可知,该电池总反应为,B正确;充电时,阴极电极反应式为,被还原的Zn2+主要来自电解质溶液,C错误;放电时,负极的电极反应式为,因此消耗0.65 g Zn(物质的量为0.01mol),理论上转移0.02 mol电子,D正确。
8.(2024·江苏卷)碱性锌锰电池的总反应为,电池构造示意图如图所示。下列有关说法正确的是
A.电池工作时,发生氧化反应
B.电池工作时,通过隔膜向正极移动
C.环境温度过低,不利于电池放电
D.反应中每生成,转移电子数为
【答案】C
【分析】Zn为负极,电极反应式为:,MnO2为正极,电极反应式为:。
【解析】A.电池工作时,为正极,得到电子,发生还原反应,故A错误;
B.电池工作时,通过隔膜向负极移动,故B错误;
C.环境温度过低,化学反应速率下降,不利于电池放电,故C正确;
D.由电极反应式可知,反应中每生成,转移电子数为,故D错误;
故选C。
9.(2024·河北卷)我国科技工作者设计了如图所示的可充电电池,以为电解质,电解液中加入1,3-丙二胺()以捕获,使放电时还原产物为。该设计克服了导电性差和释放能力差的障碍,同时改善了的溶剂化环境,提高了电池充放电循环性能。
下列说法错误的是
A.放电时,电池总反应为
B.充电时,多孔碳纳米管电极与电源正极连接
C.充电时,电子由电极流向阳极,向阴极迁移
D.放电时,每转移电子,理论上可转化
【答案】C
【分析】放电时CO2转化为MgC2O4,碳元素化合价由+4价降低为+3价,发生还原反应,所以放电时,多孔碳纳米管电极为正极、电极为负极,则充电时多孔碳纳米管电极为阳极、电极为阴极:
定位:二次电池,放电时阳离子向正极移动,充电时阳离子向阴极移动。 电极过程电极反应式电极放电充电多孔碳纳米管电极放电充电
【解析】A.根据以上分析,放电时正极反应式为、负极反应式为,将放电时正、负电极反应式相加,可得放电时电池总反应:,故A正确;
B.充电时,多孔碳纳米管电极上发生失电子的氧化反应,则多孔碳纳米管在充电时是阳极,与电源正极连接,故B正确;
C.充电时,电极为阴极,电子从电源负极经外电路流向电极,同时向阴极迁移,故C错误;
D.根据放电时的电极反应式可知,每转移电子,有参与反应,因此每转移电子,理论上可转化,故D正确;
故答案为:C。
10.(2023·全国乙卷)室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。工作时,在硫电极发生反应:S8+e-→S,S+e-→S,2Na++S+2(1-)e-→Na2Sx
下列叙述错误的是
A.充电时Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为:2Na++S8+2e-→Na2Sx
D.炭化纤维素纸的作用是增强硫电极导电性能
【答案】A
【分析】由题意可知放电时硫电极得电子,硫电极为原电池正极,钠电极为原电池负极。
【解析】A.充电时为电解池装置,阳离子移向阴极,即钠电极,故充电时,Na+由硫电极迁移至钠电极,A错误;
B.放电时Na在a电极失去电子,失去的电子经外电路流向b电极,硫黄粉在b电极上得电子与a电极释放出的Na+结合得到Na2Sx,电子在外电路的流向为a→b,B正确;
C.由题给的的一系列方程式相加可以得到放电时正极的反应式为2Na++S8+2e-→Na2Sx,C正确;
D.炭化纤维素纸中含有大量的炭,炭具有良好的导电性,可以增强硫电极的导电性能,D正确;
故答案选A。
11.(2023·新课标卷)一种以和为电极、水溶液为电解质的电池,其示意图如下所示。放电时,可插入层间形成。下列说法错误的是
A.放电时为正极
B.放电时由负极向正极迁移
C.充电总反应:
D.充电阳极反应:
【答案】C
【分析】由题中信息可知,该电池中Zn为负极、为正极,电池的总反应为。
【解析】A.由题信息可知,放电时,可插入层间形成,发生了还原反应,则放电时为正极,A说法正确;
B.Zn为负极,放电时Zn失去电子变为,阳离子向正极迁移,则放电时由负极向正极迁移,B说法正确;
C.电池在放电时的总反应为,则其在充电时的总反应为,C说法不正确;
D.充电阳极上被氧化为,则阳极的电极反应为,D说法正确;
综上所述,本题选C。
12.(2023·海南卷)利用金属Al、海水及其中的溶解氧可组成电池,如图所示。下列说法正确的是
A.b电极为电池正极
B.电池工作时,海水中的向a电极移动
C.电池工作时,紧邻a电极区域的海水呈强碱性
D.每消耗1kgAl,电池最多向外提供37mol电子的电量
【答案】A
【分析】铝为活泼金属,发生氧化反应为负极,则石墨为正极;
【解析】A.由分析可知,b电极为电池正极,A正确;
B.电池工作时,阳离子向正极移动,故海水中的向b电极移动,B错误;
C.电池工作时,a电极反应为铝失去电子生成铝离子,铝离子水解显酸性,C错误;
D.由C分析可知,每消耗1kgAl(为),电池最多向外提供mol电子的电量,D错误;
故选A。
13.(2023·河北卷)我国科学家发明了一种以和为电极材料的新型电池,其内部结构如下图所示,其中①区、②区、③区电解质溶液的酸碱性不同。放电时,电极材料转化为。下列说法错误的是
A.充电时,b电极上发生还原反应
B.充电时,外电源的正极连接b电极
C.放电时,①区溶液中的向②区迁移
D.放电时,a电极的电极反应式为
【答案】B
【分析】放电时,电极材料转化为,电极反应 -2ne-= +2nK+,是原电池的负极,阳离子增多需要通过阳离子交换膜进入②区;二氧化锰得到电子变成锰离子,是原电池的正极,电极反应:,阳离子减少,多余的阴离子需要通过阴离子交换膜进入②区,故③为碱性溶液是电极,①为酸性溶液是二氧化锰电极。
【解析】A.充电时,b电极上得到电子,发生还原反应,A正确;
B.充电时,外电源的正极连接a电极相连,电极失去电子,电极反应为,B错误;
C.放电时,①区溶液中多余的向②区迁移,C正确;
D.放电时,a电极的电极反应式为,D正确;
故选:B。
14.(2023·福建卷)一种可在较高温下安全快充的铝-硫电池的工作原理如图,电解质为熔融氯铝酸盐(由和形成熔点为的共熔物),其中氯铝酸根起到结合或释放的作用。电池总反应:。下列说法错误的是
A.含个键
B.中同时连接2个原子的原子有个
C.充电时,再生单质至少转移电子
D.放电时间越长,负极附近熔融盐中n值小的浓度越高
【答案】D
【分析】放电时铝失去电子生成铝离子做负极,硫单质得到电子做正极,充电时铝离子得到电子生成铝发生在阴极,硫离子失去电子生成硫单质发生在阳极,依此解题。
【解析】A.的结构为,所以含个键,A正确;
B.由的结构可知同时连接2个原子的原子有个,B正确;
C.由总反应可知充电时,再生单质需由铝离子得到电子生成,所以至少转移电子,C正确;
D.由总反应可知放电时间越长,负极铝失去电子生成的铝离子越多所以n值大的浓度越高,D错误;
故选D。
15.(2023·山东卷)利用热再生氨电池可实现电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是
A.甲室电极为正极
B.隔膜为阳离子膜
C.电池总反应为:
D.扩散到乙室将对电池电动势产生影响
【答案】CD
【解析】A. 向甲室加入足量氨水后电池开始工作,则甲室电极溶解,变为铜离子与氨气形成,因此甲室电极为负极,故A错误;
B. 再原电池内电路中阳离子向正极移动,若隔膜为阳离子膜,电极溶解生成的铜离子要向右侧移动,通入氨气要消耗铜离子,显然左侧阳离子不断减小,明显不利于电池反应正常进行,故B错误;
C. 左侧负极是,正极是,则电池总反应为:,故C正确;
D. 扩散到乙室会与铜离子反应生成,铜离子浓度降低,铜离子得电子能力减弱,因此将对电池电动势产生影响,故D正确。
综上所述,答案为CD。
16.(2023·辽宁卷)某低成本储能电池原理如下图所示。下列说法正确的是
A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧通过质子交换膜移向左侧
D.充电总反应:
【答案】B
【分析】该储能电池放电时,Pb为负极,失电子结合硫酸根离子生成PbSO4,则多孔碳电极为正极,正极上Fe3+得电子转化为Fe2+,充电时,多孔碳电极为阳极,Fe2+失电子生成Fe3+,PbSO4电极为阴极,PbSO4得电子生成Pb和硫酸。
【解析】A.放电时负极上Pb失电子结合硫酸根离子生成PbSO4附着在负极上,负极质量增大,A错误;
B.储能过程中,该装置为电解池,将电能转化为化学能,B正确;
C.放电时,右侧为正极,电解质溶液中的阳离子向正极移动,左侧的H+通过质子交换膜移向右侧,C错误;
D.充电时,总反应为PbSO4+2Fe2+=Pb++2Fe3+,D错误;
故答案选B。
17.(2022·湖南卷)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误的是
A.海水起电解质溶液作用
B.N极仅发生的电极反应:
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
【答案】B
【解析】锂海水电池的总反应为2Li+2H2O═2LiOH+H2↑, M极上Li失去电子发生氧化反应,则M电极为负极,电极反应为Li-e-=Li+,N极为正极,电极反应为2H2O+2e-=2OH-+H2↑,同时氧气也可以在N极得电子,电极反应为O2+4e-+2H2O=4OH-。
A.海水中含有丰富的电解质,如氯化钠、氯化镁等,可作为电解质溶液,故A正确;
B.由上述分析可知,N为正极,电极反应为2H2O+2e-=2OH-+H2↑,和反应O2+4e-+2H2O=4OH-,故B错误;
C.Li为活泼金属,易与水反应,玻璃陶瓷的作用是防止水和Li反应,并能传导离子,故C正确;
D.该电池不可充电,属于一次电池,故D正确;
答案选B。
18.(2022·福建卷)一种化学“自充电”的锌-有机物电池,电解质为和水溶液。将电池暴露于空气中,某电极无需外接电源即能实现化学自充电,该电极充放电原理如下图所示。下列说法正确的是
A.化学自充电时,增大
B.化学自充电时,电能转化为化学能
C.化学自充电时,锌电极反应式:
D.放电时,外电路通过电子,正极材料损耗
【答案】A
【解析】A.由图可知,化学自充电时,消耗O2,该反应为O2+2H2O+4e-=4OH-,增大,故A正确;
B.化学自充电时,无需外接电源即能实现化学自充电,该过程不是电能转化为化学能,故B错误;
C.由图可知,化学自充电时,锌电极作阴极,该电极的电极反应式为O2+2H2O+4e-=4OH-,故C错误;
D.放电时,1mol转化为 ,消耗2mol K+,外电路通过电子时,正极物质增加0.02mol K+,增加的质量为0.02mol×39g/mol =0.78g,故D错误;
故选A。
19.(2022·全国乙卷)电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家研究了一种光照充电电池(如图所示)。光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应(Li2O2+2h+=2Li++O2)对电池进行充电。下列叙述错误的是
A.充电时,电池的总反应
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应
【答案】C
【解析】充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应(Li2O2+2h+=2Li++O2),则充电时总反应为Li2O2=2Li+O2,结合图示,充电时金属Li电极为阴极,光催化电极为阳极;则放电时金属Li电极为负极,光催化电极为正极;据此作答。
A.光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应对电池进行充电,结合阴极反应和阳极反应,充电时电池的总反应为Li2O2=2Li+O2,A正确;
B.充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空穴有关,故充电效率与光照产生的电子和空穴量有关,B正确;
C.放电时,金属Li电极为负极,光催化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;
D.放电时总反应为2Li+O2=Li2O2,正极反应为O2+2Li++2e-=Li2O2,D正确;
答案选C。
20.(2022·广东卷)科学家基于易溶于的性质,发展了一种无需离子交换膜的新型氯流电池,可作储能设备(如图)。充电时电极a的反应为: 。下列说法正确的是
A.充电时电极b是阴极
B.放电时溶液的减小
C.放电时溶液的浓度增大
D.每生成,电极a质量理论上增加
【答案】C
【解析】A.由充电时电极a的反应可知,充电时电极a发生还原反应,所以电极a是阴极,则电极b是阳极,故A错误;
B.放电时电极反应和充电时相反,则由放电时电极a的反应为可知,NaCl溶液的pH不变,故B错误;
C.放电时负极反应为,正极反应为,反应后Na+和Cl-浓度都增大,则放电时NaCl溶液的浓度增大,故C正确;
D.充电时阳极反应为,阴极反应为,由得失电子守恒可知,每生成1molCl2,电极a质量理论上增加23g/mol2mol=46g,故D错误;
答案选C。
21.(2022·浙江卷)通过电解废旧锂电池中的可获得难溶性的和,电解示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。下列说法不正确的是
A.电极A为阴极,发生还原反应
B.电极B的电极发应:
C.电解一段时间后溶液中浓度保持不变
D.电解结束,可通过调节除去,再加入溶液以获得
【答案】C
【解析】A.由电解示意图可知,电极B上Mn2+转化为了MnO2,锰元素化合价升高,失电子,则电极B为阳极,电极A为阴极,得电子,发生还原反应,A正确;
B.由电解示意图可知,电极B上Mn2+失电子转化为了MnO2,电极反应式为:2H2O+Mn2+-2e-=MnO2+4H+,B正确;
C.电极A为阴极, LiMn2O4得电子,电极反应式为:2LiMn2O4+6e-+16H+=2Li++4Mn2++8H2O,依据得失电子守恒,电解池总反应为:2LiMn2O4+4H+=2Li++Mn2++3MnO2+2H2O,反应生成了Mn2+,Mn2+浓度增大,C错误;
D.电解池总反应为:2LiMn2O4+4H+=2Li++Mn2++3MnO2+2H2O,电解结束后,可通过调节溶液pH将锰离子转化为沉淀除去,然后再加入碳酸钠溶液,从而获得碳酸锂,D正确;
答案选C。
22.(2022·辽宁卷)某储能电池原理如图。下列说法正确的是
A.放电时负极反应:
B.放电时透过多孔活性炭电极向中迁移
C.放电时每转移电子,理论上吸收
D.充电过程中,溶液浓度增大
【答案】A
【分析】放电时负极反应:,正极反应:Cl2+2e-=2Cl-,消耗氯气,放电时,阴离子移向负极,充电时阳极:2Cl--2e-=Cl2,由此解析。
【解析】A. 放电时负极失电子,发生氧化反应,电极反应:,故A正确;
B. 放电时,阴离子移向负极,放电时透过多孔活性炭电极向NaCl中迁移,故B错误;
C. 放电时每转移电子,正极:Cl2+2e-=2Cl-,理论上释放,故C错误;
D. 充电过程中,阳极:2Cl--2e-=Cl2,消耗氯离子,溶液浓度减小,故D错误;
故选A。
23.(2021·河北卷)K—O2电池结构如图,a和b为两个电极,其中之一为单质钾片。关于该电池,下列说法错误的是
A.隔膜允许K+通过,不允许O2通过
B.放电时,电流由b电极沿导线流向a电极;充电时,b电极为阳极
C.产生1Ah电量时,生成KO2的质量与消耗O2的质量比值约为2.22
D.用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗0.9g水
【答案】D
【分析】由图可知,a电极为原电池的负极,单质钾片失去电子发生氧化反应生成钾离子,电极反应式为K—e-=K+,b电极为正极,在钾离子作用下,氧气在正极得到电子发生还原反应生成超氧化钾;据以上分析解答。
【解析】A.金属性强的金属钾易与氧气反应,为防止钾与氧气反应,电池所选择隔膜应允许通过,不允许通过,故A正确;
B.由分析可知,放电时,a为负极,b为正极,电流由b电极沿导线流向a电极,充电时,b电极应与直流电源的正极相连,做电解池的为阳极,故B正确;
C.由分析可知,生成1mol超氧化钾时,消耗1mol氧气,两者的质量比值为1mol×71g/mol:1mol×32g/mol≈2.22:1,故C正确;
D.铅酸蓄电池充电时的总反应方程式为2PbSO4+2H2O=PbO2+Pb+2H2SO4,反应消耗2mol水,转移2mol电子,由得失电子数目守恒可知,耗钾时,铅酸蓄电池消耗水的质量为×18g/mol=1.8g,故D错误;
故选D。
24.(2021·浙江卷)某全固态薄膜锂离子电池截面结构如图所示,电极A为非晶硅薄膜,充电时得电子成为Li嵌入该薄膜材料中;电极B为薄膜;集流体起导电作用。下列说法不正确的是
A.充电时,集流体A与外接电源的负极相连
B.放电时,外电路通过电子时,薄膜电解质损失
C.放电时,电极B为正极,反应可表示为
D.电池总反应可表示为
【答案】B
【分析】由题中信息可知,该电池充电时得电子成为Li嵌入电极A中,可知电极A在充电时作阴极,故其在放电时作电池的负极,而电极B是电池的正极。
【解析】A.由图可知,集流体A与电极A相连,充电时电极A作阴极,故充电时集流体A与外接电源的负极相连,A说法正确;
B.放电时,外电路通过a mol电子时,内电路中有a mol 通过LiPON薄膜电解质从负极迁移到正极,但是LiPON薄膜电解质没有损失,B说法不正确;
C.放电时,电极B为正极,发生还原反应,反应可表示为,C说法正确;
D.电池放电时,嵌入在非晶硅薄膜中的锂失去电子变成,正极上得到电子和变为,故电池总反应可表示为,D说法正确。
综上所述,相关说法不正确的是B,本题选B。
25.(2020·新课标Ⅰ卷)科学家近年发明了一种新型Zn CO2水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
下列说法错误的是
A. 放电时,负极反应为
B. 放电时,1 mol CO2转化为HCOOH,转移的电子数为2 mol
C. 充电时,电池总反应为
D. 充电时,正极溶液中OH 浓度升高
【答案】D
【解析】由题可知,放电时,CO2转化为HCOOH,即CO2发生还原反应,故放电时右侧电极为正极,左侧电极为负极,Zn发生氧化反应生成;充电时,右侧为阳极,H2O发生氧化反应生成O2,左侧为阴极,发生还原反应生成Zn,以此分析解答。放电时,负极上Zn发生氧化反应,电极反应式为:,故A正确;放电时,CO2转化为HCOOH,C元素化合价降低2,则1molCO2转化为HCOOH时,转移电子数为2mol,故B正确;充电时,阳极上H2O转化为O2,负极上转化为Zn,电池总反应为:,故C正确;充电时,正极即为阳极,电极反应式为:,溶液中H+浓度增大,溶液中c(H+) c(OH-)=KW,温度不变时,KW不变,因此溶液中OH-浓度降低,故D错误。
26.(2020·新课标Ⅲ卷)一种高性能的碱性硼化钒(VB2)—空气电池如下图所示,其中在VB2电极发生反应:该电池工作时,下列说法错误的是
A. 负载通过0.04 mol电子时,有0.224 L(标准状况)O2参与反应
B. 正极区溶液的pH降低、负极区溶液的pH升高
C. 电池总反应为
D. 电流由复合碳电极经负载、VB2电极、KOH溶液回到复合碳电极
【答案】B
【解析】根据图示的电池结构,左侧VB2发生失电子的反应生成和,反应的电极方程式如题干所示,右侧空气中的氧气发生得电子的反应生成OH-,反应的电极方程式为O2+4e-+2H2O=4OH-,电池的总反应方程式为4VB2+11O2+20OH-+6H2O=8+4,据此分析。当负极通过0.04mol电子时,正极也通过0.04mol电子,根据正极的电极方程式,通过0.04mol电子消耗0.01mol氧气,在标况下为0.224L,A正确;反应过程中正极生成大量的OH-使正极区pH升高,负极消耗OH-使负极区OH-浓度减小pH降低,B错误;根据分析,电池的总反应为4VB2+11O2+20OH-+6H2O=8+4,C正确;电池中,电子由VB2电极经负载流向复合碳电极,电流流向与电子流向相反,则电流流向为复合碳电极→负载→VB2电极→KOH溶液→复合碳电极,D正确。
27.(2020·天津卷)熔融钠-硫电池性能优良,是具有应用前景的储能电池。下图中的电池反应为(x=5~3,难溶于熔融硫),下列说法错误的是
A. Na2S4的电子式为
B. 放电时正极反应为
C. Na和Na2Sx分别为电池的负极和正极
D. 该电池是以为隔膜的二次电池
【答案】C
【解析】根据电池反应:可知,放电时,钠作负极,发生氧化反应,电极反应为:Na-e-= Na+,硫作正极,发生还原反应,电极反应为,据此分析。Na2S4属于离子化合物,4个硫原子间形成三对共用电子对,电子式为,故A正确;放电时发生的是原电池反应,正极发生还原反应,电极反应为:,故B正确;放电时,Na为电池的负极,正极为硫单质,故C错误;放电时,该电池是以钠作负极,硫作正极的原电池,充电时,是电解池,为隔膜,起到电解质溶液的作用,该电池为二次电池,故D正确;答案选C
考点三 多池和多室电化学装置
28.(2022·全国甲卷)一种水性电解液Zn-MnO2离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以Zn(OH)存在)。电池放电时,下列叙述错误的是
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO通过隔膜向Ⅱ区迁移
C. MnO2电极反应:MnO2+2e-+4H+=Mn2++2H2O
D.电池总反应:Zn+4OH-+MnO2+4H+=Zn(OH)+Mn2++2H2O
【答案】A
【解析】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为Zn-2e-+4OH-=Zn(OH),Ⅰ区MnO2为电池的正极,电极反应为MnO2+2e-+4H+=Mn2++2H2O;电池在工作过程中,由于两个离子选择隔膜没有指明的阳离子隔膜还是阴离子隔膜,故两个离子隔膜均可以通过阴、阳离子,因此可以得到Ⅰ区消耗H+,生成Mn2+,Ⅱ区的K+向Ⅰ区移动或Ⅰ区的SO向Ⅱ区移动,Ⅲ区消耗OH-,生成Zn(OH),Ⅱ区的SO向Ⅲ区移动或Ⅲ区的K+向Ⅱ区移动。据此分析答题。
A.根据分析,Ⅱ区的K+只能向Ⅰ区移动,A错误;
B.根据分析,Ⅰ区的SO向Ⅱ区移动,B正确;
C.MnO2电极的电极反应式为MnO2+2e-+4H+=Mn2++2H2O,C正确;
D.电池的总反应为Zn+4OH-+MnO2+4H+=Zn(OH)+Mn2++2H2O,D正确;
故答案选A。
29.(2022·山东卷)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成,将废旧锂离子电池的正极材料转化为,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为
D.若甲室减少,乙室增加,则此时已进行过溶液转移
【答案】BD
【解析】由于乙室中两个电极的电势差比甲室大,所以乙室是原电池,甲室是电解池,然后根据原电池、电解池反应原理分析解答。
A.电池工作时,甲室中细菌上乙酸盐的阴离子失去电子被氧化为CO2气体,Co2+在另一个电极上得到电子,被还原产生Co单质,CH3COO-失去电子后,Na+通过阳膜进入阴极室,溶液变为NaCl溶液,溶液由碱性变为中性,溶液pH减小,A错误;
B.对于乙室,正极上LiCoO2得到电子,被还原为Co2+,同时得到Li+,其中的O与溶液中的H+结合H2O,因此电池工作一段时间后应该补充盐酸,B正确;
C.电解质溶液为酸性,不可能大量存在OH-,乙室电极反应式为:LiCoO2+e-+4H+=Li++Co2++2H2O,C错误;
D.若甲室Co2+减少200 mg,电子转移物质的量为n(e-)= ,乙室Co2+增加300 mg,转移电子的物质的量为n(e-)=,说明此时已进行过溶液转移,D正确;
故合理选项是BD。
30.(2021·湖南卷)锌溴液流电池是一种先进的水溶液电解质电池,广泛应用于再生能源储能和智能电网的备用电源等。三单体串联锌溴液流电池工作原理如图所:
下列说法错误的是
A.放电时,N极为正极
B.放电时,左侧贮液器中的浓度不断减小
C.充电时,M极的电极反应式为
D.隔膜允许阳离子通过,也允许阴离子通过
【答案】B
【分析】由图可知,放电时,N电极为电池的正极,溴在正极上得到电子发生还原反应生成溴离子,电极反应式为Br2+2e—=2Br—,M电极为负极,锌失去电子发生氧化反应生成锌离子,电极反应式为Zn—2e—=Zn2+,正极放电生成的溴离子通过离子交换膜进入左侧,同时锌离子通过交换膜进入右侧,维持两侧溴化锌溶液的浓度保持不变;充电时,M电极与直流电源的负极相连,做电解池的阴极,N电极与直流电源的正极相连,做阳极。
【解析】A.由分析可知,放电时,N电极为电池的正极,故A正确;
B.由分析可知,放电或充电时,左侧储液器和右侧储液器中溴化锌的浓度维持不变,故B错误;
C.由分析可知,充电时,M电极与直流电源的负极相连,做电解池的阴极,锌离子在阴极上得到电子发生还原反应生成锌,电极反应式为Zn2++2e—=Zn,故C正确;
D.由分析可知,放电或充电时,交换膜允许锌离子和溴离子通过,维持两侧溴化锌溶液的浓度保持不变,故D正确;
故选B。
31.(2020·山东卷)微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含 CH3COO-的溶液为例)。下列说法错误的是
A. 负极反应为
B. 隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C. 当电路中转移1mol电子时,模拟海水理论上除盐58.5g
D. 电池工作一段时间后,正、负极产生气体的物质的量之比为2:1
【答案】B
【解析】据图可知a极上CH3COOˉ转化为CO2和H+,C元素被氧化,所以a极为该原电池的负极,则b极为正极。a极为负极,CH3COOˉ失电子被氧化成CO2和H+,结合电荷守恒可得电极反应式为CH3COOˉ+2H2O-8eˉ=2CO2↑+7H+,故A正确;为了实现海水的淡化,模拟海水中的氯离子需要移向负极,即a极,则隔膜1为阴离子交换膜,钠离子需要移向正极,即b极,则隔膜2为阳离子交换膜,故B错误;
当电路中转移1mol电子时,根据电荷守恒可知,海水中会有1molClˉ移向负极,同时有1molNa+移向正极,即除去1molNaCl,质量为58.5g,故C正确;b极为正极,水溶液为酸性,所以氢离子得电子产生氢气,电极反应式为2H++2eˉ=H2↑,所以当转移8mol电子时,正极产生4mol气体,根据负极反应式可知负极产生2mol气体,物质的量之比为4:2=2:1,故D正确;故答案为B。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
