人教版九年级上册(新)6.3 二氧化碳和一氧化碳 课件(共24张PPT)
文档属性
| 名称 | 人教版九年级上册(新)6.3 二氧化碳和一氧化碳 课件(共24张PPT) |
|
|
| 格式 | ppt | ||
| 文件大小 | 3.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-02-27 00:00:00 | ||
图片预览





文档简介
(共24张PPT)
课题3 二氧化碳和一氧化碳
搜索
颜色 味道 状态 可燃性 助燃性 相对分子质量
氧气
(O2) 无色 无味 气体 不具有 具有 32
二氧化碳(CO2) 无色 无味 气体 不具有 不具有 44
知识复习-氧气和二氧化碳的性质
实验室制取氧气和二氧化碳
O2
CO2
2KMnO4 K2MnO4+MnO2+O2
加热
↑
2H2O2 2H2O+O2
MnO2
↑
2KClO3 2KCl+3O2
加热
↑
MnO2
CaCO3+2HCl=CaCl2+CO2↑+H2O
一、二氧化碳
二、一氧化碳
3
4
1
实验
探究
点燃阶梯上的两只蜡烛,再放入烧内,沿杯壁倒入二氧化碳气体,观察先后发生的现象
二氧化碳的研究
2
实验
现象
下面的蜡烛先熄灭,上面的蜡烛后熄灭
实验
结论
二氧化碳不能燃烧;也不能支持燃烧;密度比空气大。
实验假设
为什么要用一块玻璃片挡住,而不直接倾倒气体呢?
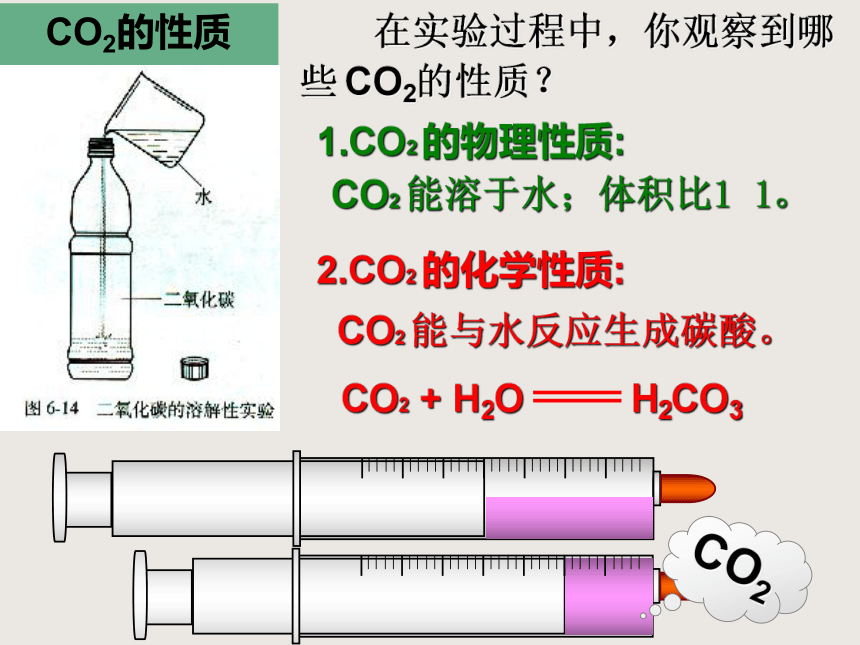
CO2的性质
在实验过程中,你观察到哪些 CO2的性质?
1.CO2 的物理性质:
CO2 能溶于水;体积比1∶1。
2.CO2 的化学性质:
CO2 能与水反应生成碳酸。
CO2
CO2 + H2O H2CO3
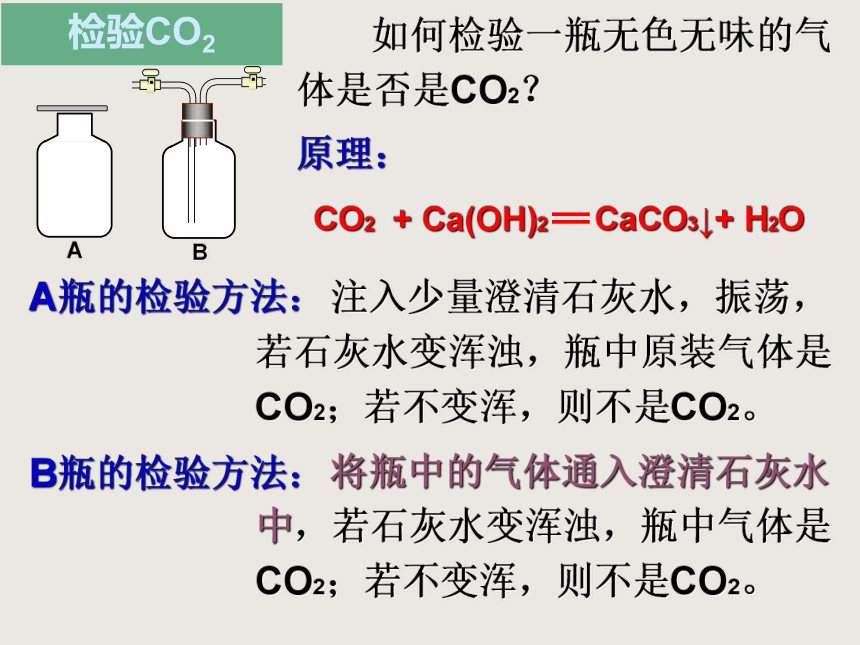
检验CO2
如何检验一瓶无色无味的气体是否是CO2?
·
·
A
B
原理:
A瓶的检验方法:
CO2 + Ca(OH)2 CaCO3↓+ H2O
B瓶的检验方法:
注入少量澄清石灰水,振荡,若石灰水变浑浊,瓶中原装气体是CO2;若不变浑,则不是CO2。
将瓶中的气体通入澄清石灰水中,若石灰水变浑浊,瓶中气体是CO2;若不变浑,则不是CO2。
石灰水中与CO2反应的物质是什么? 液体中的白色浑浊物质是什么?
Ca(OH)2 + CO2 = CaCO3↓+ H2O
Ca(OH)2
CaCO3↓
CO2
H2O
在搬进新建的房屋时,为了使墙壁表面快点变干变硬,可以在屋内生一个炭火盆。请问这是为什么?
为什么刚开始生炭火盆时,墙壁反而会变得更潮湿呢?
为什么盛放石灰水的试剂瓶的瓶壁会变得模糊不清呢?可以用什么物质来洗涤呢?
干冰的介绍
在一定条件下,二氧化碳气体会变成固体,固体二氧化碳叫 “干冰”。
干冰
CO2的用途
消防灭火
化工原料
光合作用
CO2对人体健康的影响
空气中CO2的体积分数/% 对人体健康的影响
1 使人感到气闷、头昏、心悸
4~5 使人感到气喘、头痛、眩晕
10 使人神志不清、呼吸停止,以致死亡
温室效应(Greenhouse effect)
大气中的二氧化碳气体能像温室的玻璃或塑料薄膜那样,使地面吸收的太阳光的能量不易散失,从而使全球变暖,这种现象叫“温室效应”。
二氧化碳对环境的影响
温室效应的危害
全球变暖,冰川融化,海平面升高,淹没许多城市。
病毒增加,气候反常
土地沙漠化,农业减产。
能产生温室效应的气体
二氧化碳、臭氧、甲烷、氟氯代烷等。
减缓温室效应的措施
节约能源,减少使用煤、石油、天然气等化石燃料;更多地利用太阳能、风能、地热等;大力植树造林,严禁乱砍滥伐森林等。
总结--CO2的性质
二、CO2对生活和环境的影响。
⒈CO2的物理性质:
⒉CO2的化学性质:
⑴通常CO2是无色无味的气体,能溶于水,密度比空气大
⑵干冰是CO2固体,能升华,吸收大量的热。
⑴CO2不能燃烧,也不支持燃烧。
⑵CO2能与水化合。
CO2 + H2O H2CO3
⑶CO2能与碱液反应。
CO2 + Ca(OH)2 CaCO3↓+ H2O
⑷CO2具有氧化性。
CO2不能供呼吸。
CO2 + C 2CO
高 温
⑴CO2具有广泛的用途。
⑵“温室效应”
第二
课时
讨论
1、有人用炉火取暖,为了防止发生煤气中毒,在火炉上放一盆水,这样行吗?为什么?
2、 还有人说,一闻到它的气味,就打开门窗跑到外面去。这样行吗?为什么?
3、一旦发生CO中毒,应怎样处理?
1.CO具有可燃性
2CO + O2 2CO2
点燃
现象:火焰呈蓝色,放出大量的热,产生能使澄清石灰水变浑浊 的气体。
应用:作气体燃料,如水煤气(CO和H2的混合气体)
注意事项:CO和H2是可燃的气体,使用时要注意安全,点燃前一定要检验气体的纯度。
C + O2 === CO2
点燃
C + CO2 === 2CO
高温
2CO + O2 === 2CO2
点燃
你知道一个通风良好的煤炉中发生了哪些化学反应吗?
站在煤炉旁闻到的刺鼻气味是什么物质?
S + O2 SO2
点燃
烟道
排出尾气
如图所示,向氧化铜中通入一氧化碳,黑色的氧化铜变成了红色的铜,澄清的石灰水变浑浊。
CO+CuO Cu+CO2
△
2.一氧化碳的还原性
实验步骤:
1. 连接装置
2. 检查装置的气密性。
3. 添加药品。
4.点燃加热尾气的酒精灯。
5.通入CO,排除串联装置中的空气。
6.点燃酒精灯,加热CuO。
7.熄灭酒精灯,停止加热CuO。
8.继续通入CO,直到玻璃管冷却为止,是为了防止生成的铜重新被氧化为氧化铜。
9.停止点燃尾气。
实验现象:
黑色固体变成红色
导管口有气泡冒出
澄清石灰水变浑浊
右端气体发生蓝色火焰
实验注意:
1.先通入CO一会儿 ,防止玻璃管内的空气没有排尽,加热时发生爆炸。
2.继续通入CO到玻璃管冷却为止,是为了防止生成的铜重新被氧化为氧化铜。
3.澄清石灰水的作用是检验CO2,并吸收CO2气体。
3.用酒精灯点燃是进行尾气处理:防止一氧化碳污染空气,使人中毒。
二氧化碳(CO2) 一氧化碳(CO)
物
理
性
质 色态
密度 比空气的密度大
(向上排空气法收集) 比空气的密度略小
(不可用排空气法收集)
溶 解 性 能溶于水
(不可用排水法收集) 难溶于水
(用排水法收集)
化
学
性
质 毒性 无 有剧毒
可燃性
既不能燃烧,也不支持燃烧
2CO + O2 ===2 CO2
与水反应 CO2 + H2O ===H2CO3 不反应
与澄清石灰水反应 CO2 + Ca(OH)2 ===CaCO3 +H2O 不反应
还原性 无 CO + CuO === Cu + CO2
转化关系 CO2 +C ===2CO 2CO + O2 ===2 CO2
点燃
△
都是无色无味的气体
高温
点燃
方法一:分别通入紫色石蕊溶液中,使紫色石蕊变成红色的通入的是CO2,无变化的是CO。
方法二:分别通入澄清石灰水中,使澄清石灰水变浑浊的是CO2 ,无变化的是CO。
方法三:分别通过灼热的氧化铜,使黑色固体变成红色的通入的是CO ,无变化的是CO2 。
方法四:用燃着的木条分别伸入瓶中,使燃着的木条熄灭的是CO2,能燃烧的是CO。
你能想到有哪些方法区别CO2和CO?
谢谢!
常见题型之———— 除杂质
下表中各物质都含有少量杂质(括号内的物质),用
适当的物质分别除去杂质,写出反应的化学方程式。
物质 除杂质的试剂 反应的化学方程式
Cu(CuO)
CO(CO2)
CO2(CO)
注:除杂质时要遵守“不增(不增加新的杂质)、不减(不减少被提纯的物质)、易分离”三原则。
CO
石灰水
氧化铜
CO + CuO === Cu + CO2
课题3 二氧化碳和一氧化碳
搜索
颜色 味道 状态 可燃性 助燃性 相对分子质量
氧气
(O2) 无色 无味 气体 不具有 具有 32
二氧化碳(CO2) 无色 无味 气体 不具有 不具有 44
知识复习-氧气和二氧化碳的性质
实验室制取氧气和二氧化碳
O2
CO2
2KMnO4 K2MnO4+MnO2+O2
加热
↑
2H2O2 2H2O+O2
MnO2
↑
2KClO3 2KCl+3O2
加热
↑
MnO2
CaCO3+2HCl=CaCl2+CO2↑+H2O
一、二氧化碳
二、一氧化碳
3
4
1
实验
探究
点燃阶梯上的两只蜡烛,再放入烧内,沿杯壁倒入二氧化碳气体,观察先后发生的现象
二氧化碳的研究
2
实验
现象
下面的蜡烛先熄灭,上面的蜡烛后熄灭
实验
结论
二氧化碳不能燃烧;也不能支持燃烧;密度比空气大。
实验假设
为什么要用一块玻璃片挡住,而不直接倾倒气体呢?
CO2的性质
在实验过程中,你观察到哪些 CO2的性质?
1.CO2 的物理性质:
CO2 能溶于水;体积比1∶1。
2.CO2 的化学性质:
CO2 能与水反应生成碳酸。
CO2
CO2 + H2O H2CO3
检验CO2
如何检验一瓶无色无味的气体是否是CO2?
·
·
A
B
原理:
A瓶的检验方法:
CO2 + Ca(OH)2 CaCO3↓+ H2O
B瓶的检验方法:
注入少量澄清石灰水,振荡,若石灰水变浑浊,瓶中原装气体是CO2;若不变浑,则不是CO2。
将瓶中的气体通入澄清石灰水中,若石灰水变浑浊,瓶中气体是CO2;若不变浑,则不是CO2。
石灰水中与CO2反应的物质是什么? 液体中的白色浑浊物质是什么?
Ca(OH)2 + CO2 = CaCO3↓+ H2O
Ca(OH)2
CaCO3↓
CO2
H2O
在搬进新建的房屋时,为了使墙壁表面快点变干变硬,可以在屋内生一个炭火盆。请问这是为什么?
为什么刚开始生炭火盆时,墙壁反而会变得更潮湿呢?
为什么盛放石灰水的试剂瓶的瓶壁会变得模糊不清呢?可以用什么物质来洗涤呢?
干冰的介绍
在一定条件下,二氧化碳气体会变成固体,固体二氧化碳叫 “干冰”。
干冰
CO2的用途
消防灭火
化工原料
光合作用
CO2对人体健康的影响
空气中CO2的体积分数/% 对人体健康的影响
1 使人感到气闷、头昏、心悸
4~5 使人感到气喘、头痛、眩晕
10 使人神志不清、呼吸停止,以致死亡
温室效应(Greenhouse effect)
大气中的二氧化碳气体能像温室的玻璃或塑料薄膜那样,使地面吸收的太阳光的能量不易散失,从而使全球变暖,这种现象叫“温室效应”。
二氧化碳对环境的影响
温室效应的危害
全球变暖,冰川融化,海平面升高,淹没许多城市。
病毒增加,气候反常
土地沙漠化,农业减产。
能产生温室效应的气体
二氧化碳、臭氧、甲烷、氟氯代烷等。
减缓温室效应的措施
节约能源,减少使用煤、石油、天然气等化石燃料;更多地利用太阳能、风能、地热等;大力植树造林,严禁乱砍滥伐森林等。
总结--CO2的性质
二、CO2对生活和环境的影响。
⒈CO2的物理性质:
⒉CO2的化学性质:
⑴通常CO2是无色无味的气体,能溶于水,密度比空气大
⑵干冰是CO2固体,能升华,吸收大量的热。
⑴CO2不能燃烧,也不支持燃烧。
⑵CO2能与水化合。
CO2 + H2O H2CO3
⑶CO2能与碱液反应。
CO2 + Ca(OH)2 CaCO3↓+ H2O
⑷CO2具有氧化性。
CO2不能供呼吸。
CO2 + C 2CO
高 温
⑴CO2具有广泛的用途。
⑵“温室效应”
第二
课时
讨论
1、有人用炉火取暖,为了防止发生煤气中毒,在火炉上放一盆水,这样行吗?为什么?
2、 还有人说,一闻到它的气味,就打开门窗跑到外面去。这样行吗?为什么?
3、一旦发生CO中毒,应怎样处理?
1.CO具有可燃性
2CO + O2 2CO2
点燃
现象:火焰呈蓝色,放出大量的热,产生能使澄清石灰水变浑浊 的气体。
应用:作气体燃料,如水煤气(CO和H2的混合气体)
注意事项:CO和H2是可燃的气体,使用时要注意安全,点燃前一定要检验气体的纯度。
C + O2 === CO2
点燃
C + CO2 === 2CO
高温
2CO + O2 === 2CO2
点燃
你知道一个通风良好的煤炉中发生了哪些化学反应吗?
站在煤炉旁闻到的刺鼻气味是什么物质?
S + O2 SO2
点燃
烟道
排出尾气
如图所示,向氧化铜中通入一氧化碳,黑色的氧化铜变成了红色的铜,澄清的石灰水变浑浊。
CO+CuO Cu+CO2
△
2.一氧化碳的还原性
实验步骤:
1. 连接装置
2. 检查装置的气密性。
3. 添加药品。
4.点燃加热尾气的酒精灯。
5.通入CO,排除串联装置中的空气。
6.点燃酒精灯,加热CuO。
7.熄灭酒精灯,停止加热CuO。
8.继续通入CO,直到玻璃管冷却为止,是为了防止生成的铜重新被氧化为氧化铜。
9.停止点燃尾气。
实验现象:
黑色固体变成红色
导管口有气泡冒出
澄清石灰水变浑浊
右端气体发生蓝色火焰
实验注意:
1.先通入CO一会儿 ,防止玻璃管内的空气没有排尽,加热时发生爆炸。
2.继续通入CO到玻璃管冷却为止,是为了防止生成的铜重新被氧化为氧化铜。
3.澄清石灰水的作用是检验CO2,并吸收CO2气体。
3.用酒精灯点燃是进行尾气处理:防止一氧化碳污染空气,使人中毒。
二氧化碳(CO2) 一氧化碳(CO)
物
理
性
质 色态
密度 比空气的密度大
(向上排空气法收集) 比空气的密度略小
(不可用排空气法收集)
溶 解 性 能溶于水
(不可用排水法收集) 难溶于水
(用排水法收集)
化
学
性
质 毒性 无 有剧毒
可燃性
既不能燃烧,也不支持燃烧
2CO + O2 ===2 CO2
与水反应 CO2 + H2O ===H2CO3 不反应
与澄清石灰水反应 CO2 + Ca(OH)2 ===CaCO3 +H2O 不反应
还原性 无 CO + CuO === Cu + CO2
转化关系 CO2 +C ===2CO 2CO + O2 ===2 CO2
点燃
△
都是无色无味的气体
高温
点燃
方法一:分别通入紫色石蕊溶液中,使紫色石蕊变成红色的通入的是CO2,无变化的是CO。
方法二:分别通入澄清石灰水中,使澄清石灰水变浑浊的是CO2 ,无变化的是CO。
方法三:分别通过灼热的氧化铜,使黑色固体变成红色的通入的是CO ,无变化的是CO2 。
方法四:用燃着的木条分别伸入瓶中,使燃着的木条熄灭的是CO2,能燃烧的是CO。
你能想到有哪些方法区别CO2和CO?
谢谢!
常见题型之———— 除杂质
下表中各物质都含有少量杂质(括号内的物质),用
适当的物质分别除去杂质,写出反应的化学方程式。
物质 除杂质的试剂 反应的化学方程式
Cu(CuO)
CO(CO2)
CO2(CO)
注:除杂质时要遵守“不增(不增加新的杂质)、不减(不减少被提纯的物质)、易分离”三原则。
CO
石灰水
氧化铜
CO + CuO === Cu + CO2
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
