5.1 化学反应中的质量守恒 课件(共26张PPT) 2024-2025学年化学鲁教版九年级上册
文档属性
| 名称 | 5.1 化学反应中的质量守恒 课件(共26张PPT) 2024-2025学年化学鲁教版九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-20 00:00:00 | ||
图片预览






文档简介
(共26张PPT)
5.1 化学反应中的质量守恒
1.认识质量守恒定律的含义,并通过实验探究验证质量守恒定律;
2.会用微粒的观点对质量守恒定律作出解释;
3.能用质量守恒定律解释常见的化学反应中的质量关系。
想一想:在化学反应过程中,
反应物和生成物的质量是如何变化的呢
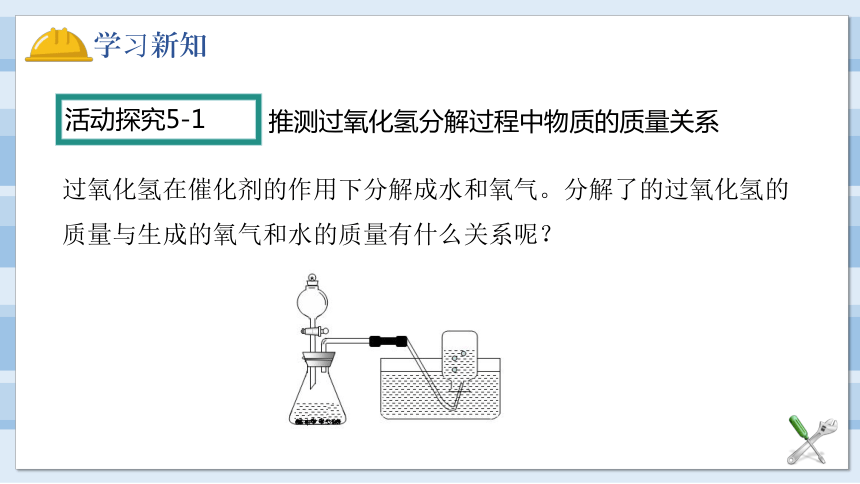
活动探究5-1
推测过氧化氢分解过程中物质的质量关系
过氧化氢在催化剂的作用下分解成水和氧气。分解了的过氧化氢的质量与生成的氧气和水的质量有什么关系呢?
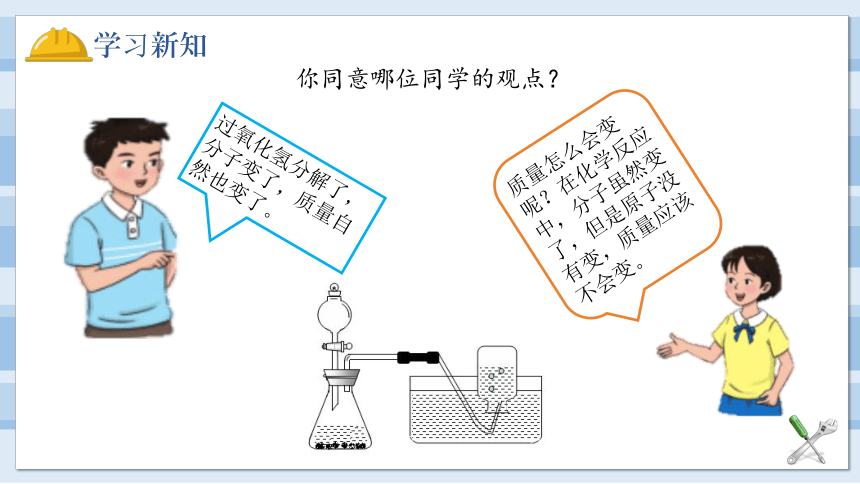
你同意哪位同学的观点?
过氧化氢分解了,分子变了,质量自然也变了。
质量怎么会变呢?在化学反应中,分子虽然变了,但是原子没有变,质量应该不会变。
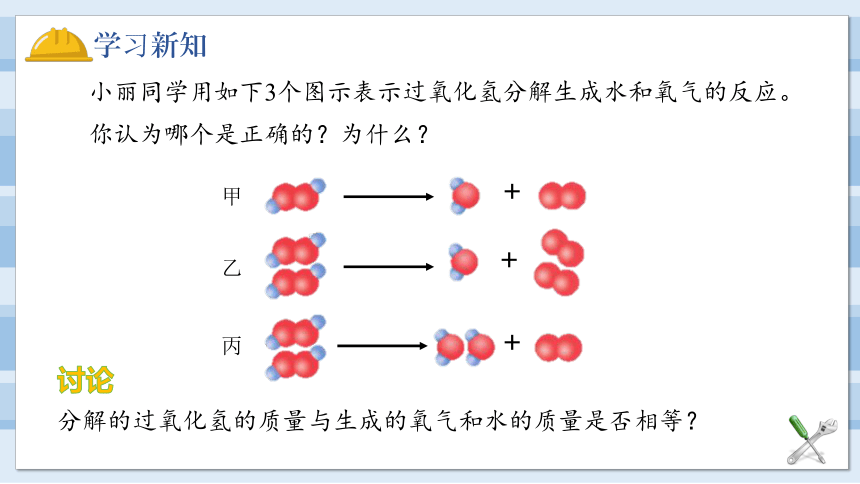
小丽同学用如下3个图示表示过氧化氢分解生成水和氧气的反应。你认为哪个是正确的?为什么?
分解的过氧化氢的质量与生成的氧气和水的质量是否相等?
甲
乙
丙
+
+
+
讨论
你的推测:物质在化学反应前后质量
不变
如何设计实验来验证这一推测是否正确?
活动探究5-2
探究化学反应前后物质的质量有无变化
氢氧化钠(NaOH)溶液和硫酸铜(CuSO4)溶液反应,生成氢氧化铜(Cu(OH)2)和硫酸钠(Na2SO4)
氢氧化钠+ 硫酸铜 氢氧化铜+ 硫酸钠
NaOH CuSO4 Cu(OH)2 Na2SO4
实验1
实验步骤 实验现象
将盛有硫酸铜溶液的小烧杯和盛有氢氧化钠溶液的小试管放在托盘天平中称量,记录数据。
把小试管中的氢氧化钠倒入盛有硫酸铜的小烧杯中,发生反应。 一段时间后,放回天平,观察天平是否平衡。
结论
反应前各物质的总质量=反应后各物质的总质量
有蓝色絮状沉淀产生,
天平平衡
活动探究5-2
探究化学反应前后物质的质量有无变化
盐酸(HCl)和大理石(CaCO3)反应生成二氧化碳、水和氯化钙(CaCl2)
碳酸钙 + 盐酸 → 氯化钙 + 二氧化碳 + 水
CaCO3 HCl CaCl2 CO2 H2O
实验2
实验步骤 实验现象
将盛有稀盐酸的小试管、盛有几块石灰石锥形瓶、气球一起放到天平上,称量,记录数据。 将石灰石和稀盐酸混合 一段时间后,放回天平,观察天平是否平衡。
结论
反应前各物质的总质量=反应后各物质的总质量
有气泡产生,
天平平衡
白磷在空气中燃烧,生成五氧化二磷(P2O5)
磷 + 氧气 五氧化二磷
P O2 P2O5
实验3
实验步骤 实验现象
将盛有少量白磷和细沙并带有玻璃棒(事先固定在橡皮塞上)的锥形瓶放在托盘天平上称量,记录数据。 将玻璃棒在酒精灯上烧热,迅速移入锥形瓶中塞紧橡皮塞。观察现象。 一段时间后,放回天平,观察天平是否平衡。
结论
反应前各物质的总质量=反应后各物质的总质量
点燃
有白烟产生,
天平平衡
质量守恒定律
化学反应后生成的各物质的质量总和,等于参加化
学反应的各物质的质量总和。
1.定义:
适用范围
所有反应物、所有生成物
未参加反应的不算
不能推广到其他物理量
点睛
化学变化只能改变物质的种类,不能改变物质的质量
任何化学反应前后物质的总质量不变
实验2:有气体生成的反应
实验3:有气体参加的反应
实验1:既没有气体参加反应,也没有气体生成的反应
必须在密闭容器中进行
拓展提高
科学史话
质量守恒定律的发现
1、1673年,英国化学家波义耳在密闭容器中加热金属汞,然后打开容器盖称量,固体物质的质量增加了
2、1756年,俄国化学家罗蒙诺索夫把金属放在密闭容器里煅烧,生成白色的氧化锡,容器里的物质的总质量在煅烧前后并没有发生变化。
3、1777年,法国化学家拉瓦锡在密闭容器中煅烧多种金属与非金属,发现化学反应前后各物质的质量相等。
思考
质量守恒定律的发现史给了你什么启示?
交流共享
为什么在化学反应前后,
物质的总质量没有发生变化?
分 子
破裂
原 子
新分子
重新组合
以氢气和氧气生成水为例
破裂
重新组合
化学反应前后,原子的种类没有改变、原子的数目没有增减、原子的质量也没有改变。
从微观认识化学反应
在化学反应前后,原子的种类和原子的数目没有改变,原子的质量没有变化,因此质量守恒。
2.质量守恒的实质:
原子的种类没有改变
原子的数目没有增减
原子的质量没有变化
——元素种类不变
元素质量不变
质量守恒
微观
宏观
蜡烛燃烧后质量变小,这违背质量守恒定律吗?
(1)解释一些化学反应的现象
3.质量守恒定律的应用:
X物质燃烧后的产物有CO2和H2O,根据质量守恒定律可知,该物质的组成中一定含有
元素和 元素,可能含有 元素.
C
H
O
(2)推断物质的组成元素
(3)计算物质的质量
在化学反应A+2B = C+ 2D中,5gA和8gB 恰好完全反应,生成6gD。若反应生成14gC,则参加反应的A的质量为( )
A.18g
B.10g
C.12g
D.16g
B
质量守恒定律
1.参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
2.实质:在化学反应前后,原子(元素)的种类和原子的数目没有改变,原子的质量没有变化。
3.应用:
(1)解释一些实验事实
(2)推测一些物质的组成
(3)进行有关的计算
1、下列现象不能用质量守恒定律解释的是( )
A.温度上升冰融化成水,变化前后的物质质量不变
B.木炭燃烧成为灰烬,灰烬的质量比木炭的质量小
C.氢氧化钠溶液和硫酸铜溶液反应,反应前后各物质的质量总和相等
D.镁条在氧气中燃烧生成固体氧化镁,反应后固体的质量增加
A
2、蜡烛在氧气中燃烧生成二氧化碳和水。
下列有关叙述正确的是( )。
A.蜡烛燃烧前后质量不变
B.蜡烛减少的质量等于生成的二氧化碳和水的质量之和
C.生成的二氧化碳和水的质量之和等于蜡烛燃烧的质量与氧气消耗的质量之和
D.通过生成物的元素组成推测,蜡烛中一定只含C、H两种元素
AC
3、通过白磷燃烧反应来验证质量守恒定律的实验装置气球如右图所示,下列说法错误的是( )。
A.实验过程中气球先变大后变瘪
B.白磷燃烧结束,锥形瓶应冷却后再称量
C.瓶底的细沙起隔热作用,防止瓶底炸裂
D.实验过程中托盘天平始终保持平衡
D
C
4、在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下:
物质 甲 乙 丙 丁
反应前的质量/g 20 50 80 30
反应后的质量/g 10 100 10 x
请根据质量守恒定律判断x的值为( )
A.50 B.40 C.60 D.70
成语“点石成金”,本意为古代术士的一种法术,即能使石头(主要成分CaCO3)变成黄金(Au) ;现比喻能化腐朽为神奇。有人说他能把石灰石变成黄金,请你用化学知识说明石灰石不能变成黄金的道理。
答:在化学反应中元素的种类不变。石灰石的主要成分是碳酸钙,它是由钙元素、碳元素、氧元素组成的。黄金是由金元素组成的,因此石灰石不可能变成黄金。
拓展
5.1 化学反应中的质量守恒
1.认识质量守恒定律的含义,并通过实验探究验证质量守恒定律;
2.会用微粒的观点对质量守恒定律作出解释;
3.能用质量守恒定律解释常见的化学反应中的质量关系。
想一想:在化学反应过程中,
反应物和生成物的质量是如何变化的呢
活动探究5-1
推测过氧化氢分解过程中物质的质量关系
过氧化氢在催化剂的作用下分解成水和氧气。分解了的过氧化氢的质量与生成的氧气和水的质量有什么关系呢?
你同意哪位同学的观点?
过氧化氢分解了,分子变了,质量自然也变了。
质量怎么会变呢?在化学反应中,分子虽然变了,但是原子没有变,质量应该不会变。
小丽同学用如下3个图示表示过氧化氢分解生成水和氧气的反应。你认为哪个是正确的?为什么?
分解的过氧化氢的质量与生成的氧气和水的质量是否相等?
甲
乙
丙
+
+
+
讨论
你的推测:物质在化学反应前后质量
不变
如何设计实验来验证这一推测是否正确?
活动探究5-2
探究化学反应前后物质的质量有无变化
氢氧化钠(NaOH)溶液和硫酸铜(CuSO4)溶液反应,生成氢氧化铜(Cu(OH)2)和硫酸钠(Na2SO4)
氢氧化钠+ 硫酸铜 氢氧化铜+ 硫酸钠
NaOH CuSO4 Cu(OH)2 Na2SO4
实验1
实验步骤 实验现象
将盛有硫酸铜溶液的小烧杯和盛有氢氧化钠溶液的小试管放在托盘天平中称量,记录数据。
把小试管中的氢氧化钠倒入盛有硫酸铜的小烧杯中,发生反应。 一段时间后,放回天平,观察天平是否平衡。
结论
反应前各物质的总质量=反应后各物质的总质量
有蓝色絮状沉淀产生,
天平平衡
活动探究5-2
探究化学反应前后物质的质量有无变化
盐酸(HCl)和大理石(CaCO3)反应生成二氧化碳、水和氯化钙(CaCl2)
碳酸钙 + 盐酸 → 氯化钙 + 二氧化碳 + 水
CaCO3 HCl CaCl2 CO2 H2O
实验2
实验步骤 实验现象
将盛有稀盐酸的小试管、盛有几块石灰石锥形瓶、气球一起放到天平上,称量,记录数据。 将石灰石和稀盐酸混合 一段时间后,放回天平,观察天平是否平衡。
结论
反应前各物质的总质量=反应后各物质的总质量
有气泡产生,
天平平衡
白磷在空气中燃烧,生成五氧化二磷(P2O5)
磷 + 氧气 五氧化二磷
P O2 P2O5
实验3
实验步骤 实验现象
将盛有少量白磷和细沙并带有玻璃棒(事先固定在橡皮塞上)的锥形瓶放在托盘天平上称量,记录数据。 将玻璃棒在酒精灯上烧热,迅速移入锥形瓶中塞紧橡皮塞。观察现象。 一段时间后,放回天平,观察天平是否平衡。
结论
反应前各物质的总质量=反应后各物质的总质量
点燃
有白烟产生,
天平平衡
质量守恒定律
化学反应后生成的各物质的质量总和,等于参加化
学反应的各物质的质量总和。
1.定义:
适用范围
所有反应物、所有生成物
未参加反应的不算
不能推广到其他物理量
点睛
化学变化只能改变物质的种类,不能改变物质的质量
任何化学反应前后物质的总质量不变
实验2:有气体生成的反应
实验3:有气体参加的反应
实验1:既没有气体参加反应,也没有气体生成的反应
必须在密闭容器中进行
拓展提高
科学史话
质量守恒定律的发现
1、1673年,英国化学家波义耳在密闭容器中加热金属汞,然后打开容器盖称量,固体物质的质量增加了
2、1756年,俄国化学家罗蒙诺索夫把金属放在密闭容器里煅烧,生成白色的氧化锡,容器里的物质的总质量在煅烧前后并没有发生变化。
3、1777年,法国化学家拉瓦锡在密闭容器中煅烧多种金属与非金属,发现化学反应前后各物质的质量相等。
思考
质量守恒定律的发现史给了你什么启示?
交流共享
为什么在化学反应前后,
物质的总质量没有发生变化?
分 子
破裂
原 子
新分子
重新组合
以氢气和氧气生成水为例
破裂
重新组合
化学反应前后,原子的种类没有改变、原子的数目没有增减、原子的质量也没有改变。
从微观认识化学反应
在化学反应前后,原子的种类和原子的数目没有改变,原子的质量没有变化,因此质量守恒。
2.质量守恒的实质:
原子的种类没有改变
原子的数目没有增减
原子的质量没有变化
——元素种类不变
元素质量不变
质量守恒
微观
宏观
蜡烛燃烧后质量变小,这违背质量守恒定律吗?
(1)解释一些化学反应的现象
3.质量守恒定律的应用:
X物质燃烧后的产物有CO2和H2O,根据质量守恒定律可知,该物质的组成中一定含有
元素和 元素,可能含有 元素.
C
H
O
(2)推断物质的组成元素
(3)计算物质的质量
在化学反应A+2B = C+ 2D中,5gA和8gB 恰好完全反应,生成6gD。若反应生成14gC,则参加反应的A的质量为( )
A.18g
B.10g
C.12g
D.16g
B
质量守恒定律
1.参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
2.实质:在化学反应前后,原子(元素)的种类和原子的数目没有改变,原子的质量没有变化。
3.应用:
(1)解释一些实验事实
(2)推测一些物质的组成
(3)进行有关的计算
1、下列现象不能用质量守恒定律解释的是( )
A.温度上升冰融化成水,变化前后的物质质量不变
B.木炭燃烧成为灰烬,灰烬的质量比木炭的质量小
C.氢氧化钠溶液和硫酸铜溶液反应,反应前后各物质的质量总和相等
D.镁条在氧气中燃烧生成固体氧化镁,反应后固体的质量增加
A
2、蜡烛在氧气中燃烧生成二氧化碳和水。
下列有关叙述正确的是( )。
A.蜡烛燃烧前后质量不变
B.蜡烛减少的质量等于生成的二氧化碳和水的质量之和
C.生成的二氧化碳和水的质量之和等于蜡烛燃烧的质量与氧气消耗的质量之和
D.通过生成物的元素组成推测,蜡烛中一定只含C、H两种元素
AC
3、通过白磷燃烧反应来验证质量守恒定律的实验装置气球如右图所示,下列说法错误的是( )。
A.实验过程中气球先变大后变瘪
B.白磷燃烧结束,锥形瓶应冷却后再称量
C.瓶底的细沙起隔热作用,防止瓶底炸裂
D.实验过程中托盘天平始终保持平衡
D
C
4、在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下:
物质 甲 乙 丙 丁
反应前的质量/g 20 50 80 30
反应后的质量/g 10 100 10 x
请根据质量守恒定律判断x的值为( )
A.50 B.40 C.60 D.70
成语“点石成金”,本意为古代术士的一种法术,即能使石头(主要成分CaCO3)变成黄金(Au) ;现比喻能化腐朽为神奇。有人说他能把石灰石变成黄金,请你用化学知识说明石灰石不能变成黄金的道理。
答:在化学反应中元素的种类不变。石灰石的主要成分是碳酸钙,它是由钙元素、碳元素、氧元素组成的。黄金是由金元素组成的,因此石灰石不可能变成黄金。
拓展
同课章节目录
