5.1降低化学反应活化能的酶(第1课时课件)(共27张PPT、1份视频)
文档属性
| 名称 | 5.1降低化学反应活化能的酶(第1课时课件)(共27张PPT、1份视频) |

|
|
| 格式 | pptx | ||
| 文件大小 | 18.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 生物学 | ||
| 更新时间 | 2024-10-21 00:00:00 | ||
图片预览






文档简介
(共27张PPT)
降低化学反应活化能的酶(1)
第1节
问题探讨
讨论
斯帕兰扎尼在研究鹰的消化作用
1.为什么要将肉块放在金属笼内?
便于取出实验材料(肉块),排除物理消化对肉块的影响,确定其是否发生了化学消化。
2.是什么物质使肉块消失了?
3.怎样才能证明你的推测?
是胃内的化学物质将肉块分解了。
收集胃内的化学物质,看看这些物质在体外是否也能将肉块分解。
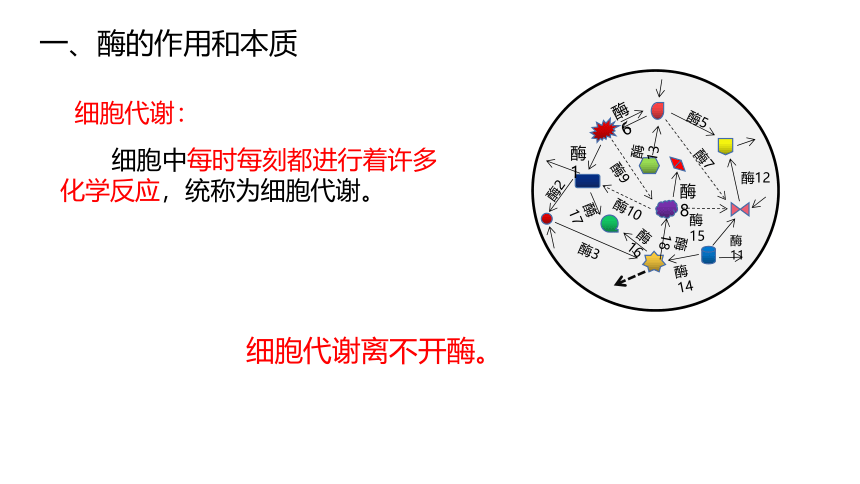
一、酶的作用和本质
细胞代谢:
细胞中每时每刻都进行着许多化学反应,统称为细胞代谢。
细胞代谢离不开酶。
酶1
酶2
酶3
酶11
酶5
酶6
酶12
酶8
酶9
酶10
酶14
酶7
酶13
酶15
酶16
酶17
酶18
(一)酶在细胞代谢中的作用
1.探究·实践:比较过氧化氢在不同条件下的分解
①实验原理
细胞代谢是细胞生命活动的基础,但细胞代谢中也会产生代谢废物,甚至会产生对细胞有害的物质,如过氧化氢,细胞中有过氧化氢酶,能将过氧化氢及时分解为氧气和水。新鲜肝脏中有较多的过氧化氢酶。
2H2O2
2H2O + O2 ↑
不同条件
②实验目的
通过比较过氧化氢在不同条件下的分解的快慢,了解过氧化氢酶的作用。
1.不同温度
2.加FeCl3
3.加过氧化氢酶.
③材料用具
新鲜的质量分数为20%的肝脏(如猪肝、鸡肝)研磨液
质量分数为3%的FeCl3溶液
新配制的体积分数为3%的过氧化氢溶液
a.材料:
b.用具:
量筒、试管、滴管、试管架、卫生香、火柴、酒精灯、试管夹、大烧杯、三脚架、石棉网、温度计。
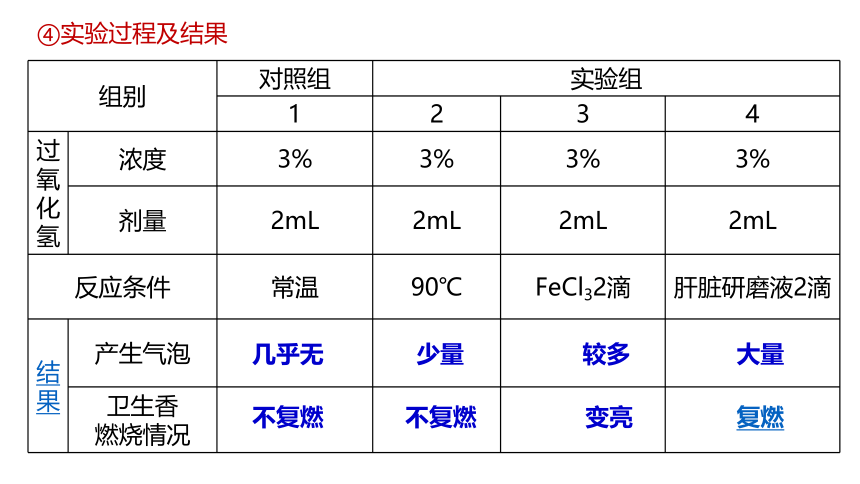
组别 对照组 实验组
1 2 3 4
过氧化氢 浓度 3% 3% 3% 3%
剂量 2mL 2mL 2mL 2mL
反应条件 常温 90℃ FeCl32滴 肝脏研磨液2滴
结果 产生气泡
卫生香 燃烧情况
④实验过程及结果
几乎无
少量
较多
大量
不复燃
不复燃
变亮
复燃
3号
4号
1号
2号
不明显
少量
较多
大量
观察产生气泡的多少
观察卫生香的燃烧情况
3号
4号
变亮
复燃不明显
复燃明显
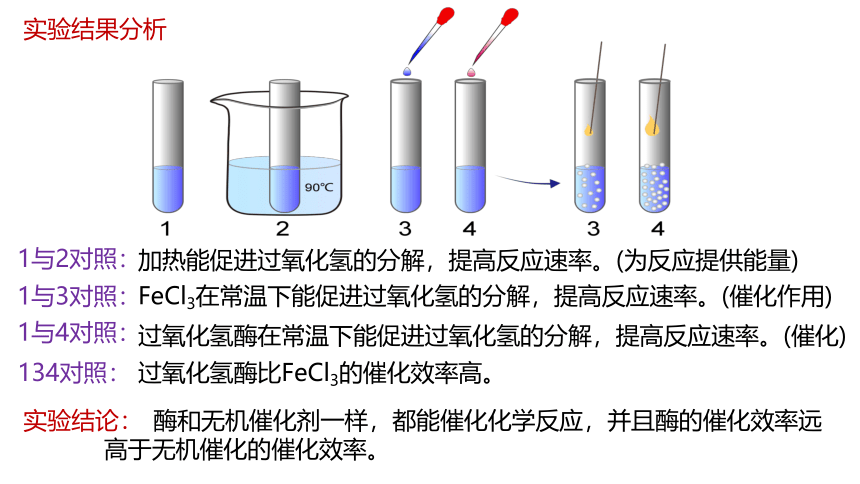
1与2对照:
加热能促进过氧化氢的分解,提高反应速率。(为反应提供能量)
1与3对照:
FeCl3在常温下能促进过氧化氢的分解,提高反应速率。(催化作用)
1与4对照:
过氧化氢酶在常温下能促进过氧化氢的分解,提高反应速率。(催化)
实验结果分析
134对照:
过氧化氢酶比FeCl3的催化效率高。
实验结论:
酶和无机催化剂一样,都能催化化学反应,并且酶的催化效率远高于无机催化的催化效率。
注意事项
1.新鲜肝脏,防止过氧化氢酶被细菌分解。
2.肝脏要制成研磨液。
----充分接触保证酶的催化效率。
3.胶头滴管不能混用。
4.H2O2有腐蚀性,要小心,不能触及皮肤。
5.卫生香不要触及气泡或者液面。
活化能:分子从常态转变为容易发生化学反应的活跃状态所需要的能量。
初态
终态
过渡态
活化能(EA)
活化能越低,反应越容易进行
酶与无机催化剂催化的机理相同,都能降低化学反应的活化能,但是酶降低活化能的作用更显著,催化效率更高。
加热、Fe3+、H2O2酶使H2O2分解加快本质
加热:
为反应物分子提供能量(活化能),使其达到活跃状态
Fe3+:
降低化学反应的活化能
酶:
更显著地降低化学反应的活化能(作用机理)
图中①表示:
无催化剂时化学反应所需的活化能。
图中②表示:
无机催化剂催化时化学反应所需的活化能。
图中④表示:
酶催化时化学反应所需的活化能。
③表示:
无机催化剂降低的活化能
⑤表示:
酶降低的活化能
常见有机化学反应的条件
高温 高压
强酸 强碱
剧烈条件
细胞内外的环境
常温
常压
水溶液环境
pH接近中性
温和
注意
①酶与无机催化剂的催化机理相同,都是降低化学反应的活化能。
②酶和无机催化剂反应前后数量和性质不发生改变,一段时间内可以重复利用。
③酶与无机催化剂都不改变反应的平衡点,只是缩短了到达平衡点的时间。如下图所示。
控制变量(单一变量)
变量:实验过程中的变化因素
自变量:人为控制的对实验对象进行处理的因素
因变量:因自变量改变而变化的变量
讨论:无关变量对实验结果有没有影响?该实验的无关变量还有哪些?
无关变量:实验过程中存在的其他一些会对实验结果造成影响的可变因素
(适宜且相等)
自变量
因变量
无关变量
对照实验:除作为自变量的因素外,其余无关变量都保持一致,并将结果进行比较的实验。
设计对照实验
对照实验一般要设置对照组和实验组
对照组
实验组
空白对照
目的是排除无关变量的干扰
对照的类型:
空白对照、自身对照、条件对照...
3.对照实验设计的一般步骤
对照实验的目的是排除无关变量的干扰,从而确定自变量与因变量的关系。
自变量
因变量
无关变量
(适宜且相等)
(控制)
(检测)
一般步骤:
第一步:分组编号,统一处理;
第二步:分组施加自变量
第三步:一段时间后,检测因变量
根据实验目的和器材,分析实验的自变量,找出主要的无关变量,明确因变量的检测方法。
仔细阅读本节的“思考·讨论”,总结每个科学家所研究的内容,体会巴斯德、李比希、毕希纳、萨姆纳的观点之间的逻辑关系;并解决·讨论题。
(二)酶的本质
巴斯德之前:发酵是纯化学反应,与生命活动无关。
发酵与活细胞有关,发酵是整个细胞而不是细胞中某种物质其作用
引起发酵的是细胞中的某些物质,但这些物质只有在酵母细胞死亡并裂解后才能发挥作用
酵母细胞中的某些物质能够在酵母细胞破碎后继续起到催化作用,就像在活酵母细胞中一样。
巴斯德
李比希
毕希纳
①对酵母菌发酵的探索
发现了起催化作用的物质——酶
②对酶本质的探索
萨姆纳:从刀豆中提纯脲酶,并证明其化学本质是蛋白质
发现少数RNA具有催化功能,称为核酶。
萨姆纳之后
科学家们获得胃蛋白酶,胰蛋白酶等许多酶的结晶,并证明这些酶的化学本质是蛋白质。
切赫、奥特曼
发现了绝大多数酶是蛋白质,少数RNA。
3.萨姆纳历时9年才证明脲酶是蛋白质,并因此荣获诺贝尔化学奖。你认为他取得成功靠的是什么样的精神品质?
4.请给酶下一个比较完整的定义。
萨姆纳历时9年,用正确的科学方法,坚持不懈、百折不饶的科学精神,将酶提纯出来。成功属于不畏艰苦的人。
酶是活细胞产生的具有催化作用的有机物。
讨论
酶的作用及本质
1.酶的作用:催化
2.来源:细胞产生
3.本质:蛋白质或RNA(少)
脂肪酶、淀粉酶、DNA酶都是蛋白质
4.原料(或水解产物):氨基酸或核糖核苷酸
5.合成场所:细胞内的核糖体或细胞核
6.发挥作用场所:细胞内、外
7.作用机理:降低反应所需的活化能
课后习题
一、概念检测
1.酶对细胞代谢起着非常重要的作用,可以降低化学反应的活化能。下列关于酶的作用特点及本质的叙述,正确的是( )
A.酶不能脱离生物体起作用B.酶只有释放到细胞外才起作用
C.所有的酶都是蛋白质 D.酶是具有催化作用的有机物
2.酶和无机催化剂都能催化化学反应。与无机催化剂相比,酶具有的特点是( )
A.能为反应物提供能量B.能降低化学反应的活化能
C.能在温和条件下催化化学反应D.催化化学反应更高效
D
D
二、拓展应用1.在本节“探究·实践”中,有同学在原有实验的基础上增加了5号和6号试管,向其中分别加入2mL过氧化氢溶液后,再向5号试管内加入2滴煮沸过的肝脏研磨液,向6号试管内加入2滴蒸馏水。这样做的目的是什么?
本小节“探究·实践”涉及的自变量并非只有 个,而是包括温度和催化剂两个变量,1号试管中仅放置了过氧化氢溶液,可以起到对照作用。2号试管与 1 号试管的区别在于温度,3号试管和4号试管与 1 号试管的区别在于多了催化剂 3号试管与 4号试管之间也可以起相互对照作用。加入 2 滴煮沸过的肝脏研磨液的 5号试管,可以与加入新鲜的肝脏研磨液的 4号试管做对照;同理,加入 2 滴蒸馏水的 6 号试管可以作为 3 号试管和 4 号试管的对照组。
3.给你一份某种酶的结晶,你能设计实验检测它是不是蛋白质吗 请简略写出实验步骤。想一想,在萨姆纳之前,为什么很难鉴定酶的本质
可用第2章中学过的检测蛋白质的方法。在萨姆纳之前,之所以很难鉴定酶的本质,主要是因为细胞中酶的提取和纯化非常困难。
酶是一种生物催化剂;
酶显著降低了化学反应的活化能。
学会确定自变量,控制无关变量,观察和检测因变量;
学会设置对照组,明确对照组在实验中的意义。
小 结
绝大多数酶是蛋白质,还有少量的RNA。
1.酶的作用
2.酶的化学本质
3.学习设计对照实验
降低化学反应活化能的酶(1)
第1节
问题探讨
讨论
斯帕兰扎尼在研究鹰的消化作用
1.为什么要将肉块放在金属笼内?
便于取出实验材料(肉块),排除物理消化对肉块的影响,确定其是否发生了化学消化。
2.是什么物质使肉块消失了?
3.怎样才能证明你的推测?
是胃内的化学物质将肉块分解了。
收集胃内的化学物质,看看这些物质在体外是否也能将肉块分解。
一、酶的作用和本质
细胞代谢:
细胞中每时每刻都进行着许多化学反应,统称为细胞代谢。
细胞代谢离不开酶。
酶1
酶2
酶3
酶11
酶5
酶6
酶12
酶8
酶9
酶10
酶14
酶7
酶13
酶15
酶16
酶17
酶18
(一)酶在细胞代谢中的作用
1.探究·实践:比较过氧化氢在不同条件下的分解
①实验原理
细胞代谢是细胞生命活动的基础,但细胞代谢中也会产生代谢废物,甚至会产生对细胞有害的物质,如过氧化氢,细胞中有过氧化氢酶,能将过氧化氢及时分解为氧气和水。新鲜肝脏中有较多的过氧化氢酶。
2H2O2
2H2O + O2 ↑
不同条件
②实验目的
通过比较过氧化氢在不同条件下的分解的快慢,了解过氧化氢酶的作用。
1.不同温度
2.加FeCl3
3.加过氧化氢酶.
③材料用具
新鲜的质量分数为20%的肝脏(如猪肝、鸡肝)研磨液
质量分数为3%的FeCl3溶液
新配制的体积分数为3%的过氧化氢溶液
a.材料:
b.用具:
量筒、试管、滴管、试管架、卫生香、火柴、酒精灯、试管夹、大烧杯、三脚架、石棉网、温度计。
组别 对照组 实验组
1 2 3 4
过氧化氢 浓度 3% 3% 3% 3%
剂量 2mL 2mL 2mL 2mL
反应条件 常温 90℃ FeCl32滴 肝脏研磨液2滴
结果 产生气泡
卫生香 燃烧情况
④实验过程及结果
几乎无
少量
较多
大量
不复燃
不复燃
变亮
复燃
3号
4号
1号
2号
不明显
少量
较多
大量
观察产生气泡的多少
观察卫生香的燃烧情况
3号
4号
变亮
复燃不明显
复燃明显
1与2对照:
加热能促进过氧化氢的分解,提高反应速率。(为反应提供能量)
1与3对照:
FeCl3在常温下能促进过氧化氢的分解,提高反应速率。(催化作用)
1与4对照:
过氧化氢酶在常温下能促进过氧化氢的分解,提高反应速率。(催化)
实验结果分析
134对照:
过氧化氢酶比FeCl3的催化效率高。
实验结论:
酶和无机催化剂一样,都能催化化学反应,并且酶的催化效率远高于无机催化的催化效率。
注意事项
1.新鲜肝脏,防止过氧化氢酶被细菌分解。
2.肝脏要制成研磨液。
----充分接触保证酶的催化效率。
3.胶头滴管不能混用。
4.H2O2有腐蚀性,要小心,不能触及皮肤。
5.卫生香不要触及气泡或者液面。
活化能:分子从常态转变为容易发生化学反应的活跃状态所需要的能量。
初态
终态
过渡态
活化能(EA)
活化能越低,反应越容易进行
酶与无机催化剂催化的机理相同,都能降低化学反应的活化能,但是酶降低活化能的作用更显著,催化效率更高。
加热、Fe3+、H2O2酶使H2O2分解加快本质
加热:
为反应物分子提供能量(活化能),使其达到活跃状态
Fe3+:
降低化学反应的活化能
酶:
更显著地降低化学反应的活化能(作用机理)
图中①表示:
无催化剂时化学反应所需的活化能。
图中②表示:
无机催化剂催化时化学反应所需的活化能。
图中④表示:
酶催化时化学反应所需的活化能。
③表示:
无机催化剂降低的活化能
⑤表示:
酶降低的活化能
常见有机化学反应的条件
高温 高压
强酸 强碱
剧烈条件
细胞内外的环境
常温
常压
水溶液环境
pH接近中性
温和
注意
①酶与无机催化剂的催化机理相同,都是降低化学反应的活化能。
②酶和无机催化剂反应前后数量和性质不发生改变,一段时间内可以重复利用。
③酶与无机催化剂都不改变反应的平衡点,只是缩短了到达平衡点的时间。如下图所示。
控制变量(单一变量)
变量:实验过程中的变化因素
自变量:人为控制的对实验对象进行处理的因素
因变量:因自变量改变而变化的变量
讨论:无关变量对实验结果有没有影响?该实验的无关变量还有哪些?
无关变量:实验过程中存在的其他一些会对实验结果造成影响的可变因素
(适宜且相等)
自变量
因变量
无关变量
对照实验:除作为自变量的因素外,其余无关变量都保持一致,并将结果进行比较的实验。
设计对照实验
对照实验一般要设置对照组和实验组
对照组
实验组
空白对照
目的是排除无关变量的干扰
对照的类型:
空白对照、自身对照、条件对照...
3.对照实验设计的一般步骤
对照实验的目的是排除无关变量的干扰,从而确定自变量与因变量的关系。
自变量
因变量
无关变量
(适宜且相等)
(控制)
(检测)
一般步骤:
第一步:分组编号,统一处理;
第二步:分组施加自变量
第三步:一段时间后,检测因变量
根据实验目的和器材,分析实验的自变量,找出主要的无关变量,明确因变量的检测方法。
仔细阅读本节的“思考·讨论”,总结每个科学家所研究的内容,体会巴斯德、李比希、毕希纳、萨姆纳的观点之间的逻辑关系;并解决·讨论题。
(二)酶的本质
巴斯德之前:发酵是纯化学反应,与生命活动无关。
发酵与活细胞有关,发酵是整个细胞而不是细胞中某种物质其作用
引起发酵的是细胞中的某些物质,但这些物质只有在酵母细胞死亡并裂解后才能发挥作用
酵母细胞中的某些物质能够在酵母细胞破碎后继续起到催化作用,就像在活酵母细胞中一样。
巴斯德
李比希
毕希纳
①对酵母菌发酵的探索
发现了起催化作用的物质——酶
②对酶本质的探索
萨姆纳:从刀豆中提纯脲酶,并证明其化学本质是蛋白质
发现少数RNA具有催化功能,称为核酶。
萨姆纳之后
科学家们获得胃蛋白酶,胰蛋白酶等许多酶的结晶,并证明这些酶的化学本质是蛋白质。
切赫、奥特曼
发现了绝大多数酶是蛋白质,少数RNA。
3.萨姆纳历时9年才证明脲酶是蛋白质,并因此荣获诺贝尔化学奖。你认为他取得成功靠的是什么样的精神品质?
4.请给酶下一个比较完整的定义。
萨姆纳历时9年,用正确的科学方法,坚持不懈、百折不饶的科学精神,将酶提纯出来。成功属于不畏艰苦的人。
酶是活细胞产生的具有催化作用的有机物。
讨论
酶的作用及本质
1.酶的作用:催化
2.来源:细胞产生
3.本质:蛋白质或RNA(少)
脂肪酶、淀粉酶、DNA酶都是蛋白质
4.原料(或水解产物):氨基酸或核糖核苷酸
5.合成场所:细胞内的核糖体或细胞核
6.发挥作用场所:细胞内、外
7.作用机理:降低反应所需的活化能
课后习题
一、概念检测
1.酶对细胞代谢起着非常重要的作用,可以降低化学反应的活化能。下列关于酶的作用特点及本质的叙述,正确的是( )
A.酶不能脱离生物体起作用B.酶只有释放到细胞外才起作用
C.所有的酶都是蛋白质 D.酶是具有催化作用的有机物
2.酶和无机催化剂都能催化化学反应。与无机催化剂相比,酶具有的特点是( )
A.能为反应物提供能量B.能降低化学反应的活化能
C.能在温和条件下催化化学反应D.催化化学反应更高效
D
D
二、拓展应用1.在本节“探究·实践”中,有同学在原有实验的基础上增加了5号和6号试管,向其中分别加入2mL过氧化氢溶液后,再向5号试管内加入2滴煮沸过的肝脏研磨液,向6号试管内加入2滴蒸馏水。这样做的目的是什么?
本小节“探究·实践”涉及的自变量并非只有 个,而是包括温度和催化剂两个变量,1号试管中仅放置了过氧化氢溶液,可以起到对照作用。2号试管与 1 号试管的区别在于温度,3号试管和4号试管与 1 号试管的区别在于多了催化剂 3号试管与 4号试管之间也可以起相互对照作用。加入 2 滴煮沸过的肝脏研磨液的 5号试管,可以与加入新鲜的肝脏研磨液的 4号试管做对照;同理,加入 2 滴蒸馏水的 6 号试管可以作为 3 号试管和 4 号试管的对照组。
3.给你一份某种酶的结晶,你能设计实验检测它是不是蛋白质吗 请简略写出实验步骤。想一想,在萨姆纳之前,为什么很难鉴定酶的本质
可用第2章中学过的检测蛋白质的方法。在萨姆纳之前,之所以很难鉴定酶的本质,主要是因为细胞中酶的提取和纯化非常困难。
酶是一种生物催化剂;
酶显著降低了化学反应的活化能。
学会确定自变量,控制无关变量,观察和检测因变量;
学会设置对照组,明确对照组在实验中的意义。
小 结
绝大多数酶是蛋白质,还有少量的RNA。
1.酶的作用
2.酶的化学本质
3.学习设计对照实验
同课章节目录
- 第1章 走近细胞
- 第1节 细胞是生命活动的基本单位
- 第2节 细胞的多样性和统一性
- 第2章 组成细胞的分子
- 第1节 细胞中的元素和化合物
- 第2节 细胞中的无机物
- 第3节 细胞中的糖类和脂质
- 第4节 蛋白质是生命活动的主要承担者
- 第5节 核酸是遗传信息的携带者
- 第3章 细胞的基本结构
- 第1节 细胞膜的结构和功能
- 第2节 细胞器之间的分工合作
- 第3节 细胞核的结构和功能
- 第4章 细胞的物质输入和输出
- 第1节 被动运输
- 第2节 主动运输与胞吞、胞吐
- 第5章 细胞的能量供应和利用
- 第1节 降低化学反应活化能的酶
- 第2节 细胞的能量“货币”ATP
- 第3节 细胞呼吸的原理和应用
- 第4节 光合作用与能量转化
- 第6章 细胞的生命历程
- 第1节 细胞的增殖
- 第2节 细胞的分化
- 第3节 细胞的衰老和死亡
