新人教版选修3-3《第8章 气体》2015年单元测试卷(山东省潍坊市高密三中)(创新班)(解析版)
文档属性
| 名称 | 新人教版选修3-3《第8章 气体》2015年单元测试卷(山东省潍坊市高密三中)(创新班)(解析版) |

|
|
| 格式 | zip | ||
| 文件大小 | 82.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2016-03-01 00:00:00 | ||
图片预览



文档简介
新人教版选修3-3《第8章 气体》2015年单元测试卷(山东省潍坊市高密三中)(创新班)
一、选择题(共9小题,每小题3分,满分27分)
1.关于理想气体,下列说法正确的是( )
A.温度极低的气体也是理想气体
B.压强极大的气体也遵从气体实验定律
C.理想气体是对实际气体的抽象化模型
D.理想气体实际并不存在
2.对一定质量的气体,通过一定的方法得到了分子数目f与速率v的两条关系图线,如图所示,下列说法正确的是( )
A.曲线Ⅰ对应的温度T1高于曲线Ⅱ对应的温度T2
B.曲线Ⅰ对应的温度T1可能等于曲线Ⅱ对应的温度T2
C.曲线Ⅰ对应的温度T1低于曲线Ⅱ对应的温度T2
D.无法判断两曲线对应的温度关系
3.一定质量的理想气体处于某一平衡状态,此时其压强为P0,经历下列四种过程后可能使气体压强恢复到P0( )
A.先保持体积不变,降低压强,再保持温度不变,使体积膨胀
B.先保持体积不变,使气体升温,再保持温度不变,使体积膨胀
C.先保持温度不变,压缩体积,再保持体积不变,使气体升温
D.先保持温度不变,使体积膨胀,再保持体积不变,使气体升温
4.甲、乙两个相同的密闭容器中分别装有等质量的同种气体,已知甲、乙容器中气体的压强分别为p甲、P乙,且p甲<p乙.则( )
A.甲容器中气体的温度高于乙容器中气体的温度
B.甲容器中气体的温度低于乙容器中气体的温度
C.甲容器中气体分子的平均动能小于乙容器中气体分子的平均动能
D.甲容器中气体分子的平均动能大于乙容器中气体分子的平均动能
5.如图所示,一定质量的理想气体,由状态A沿直线AB变化到B,在此过程中.气体分子的平均速率的变化情况是( )
A.不断增大 B.不断减小 C.先减小后增大 D.先增大后减小
6.一定质量的某种理想气体的压强为p,热力学温度为T,单位体积里气体分子数为n,则( )
A.p增大,n一定增大 B.T减小,n一定增大
C.增大时,n一定增大 D.增大时,n一定减小
7.如图所示,一定质量的某种气体的等压线,等压线上的a、b两个状态比较,下列说法正确的是( )
A.在相同时间内撞在单位面积上的分子数b状态较多
B.在相同时间内撞在单位面积上的分子数a状态较多
C.在相同时间内撞在相同面积上的分子数两状态一样多
D.单位体积的分子数两状态一样多
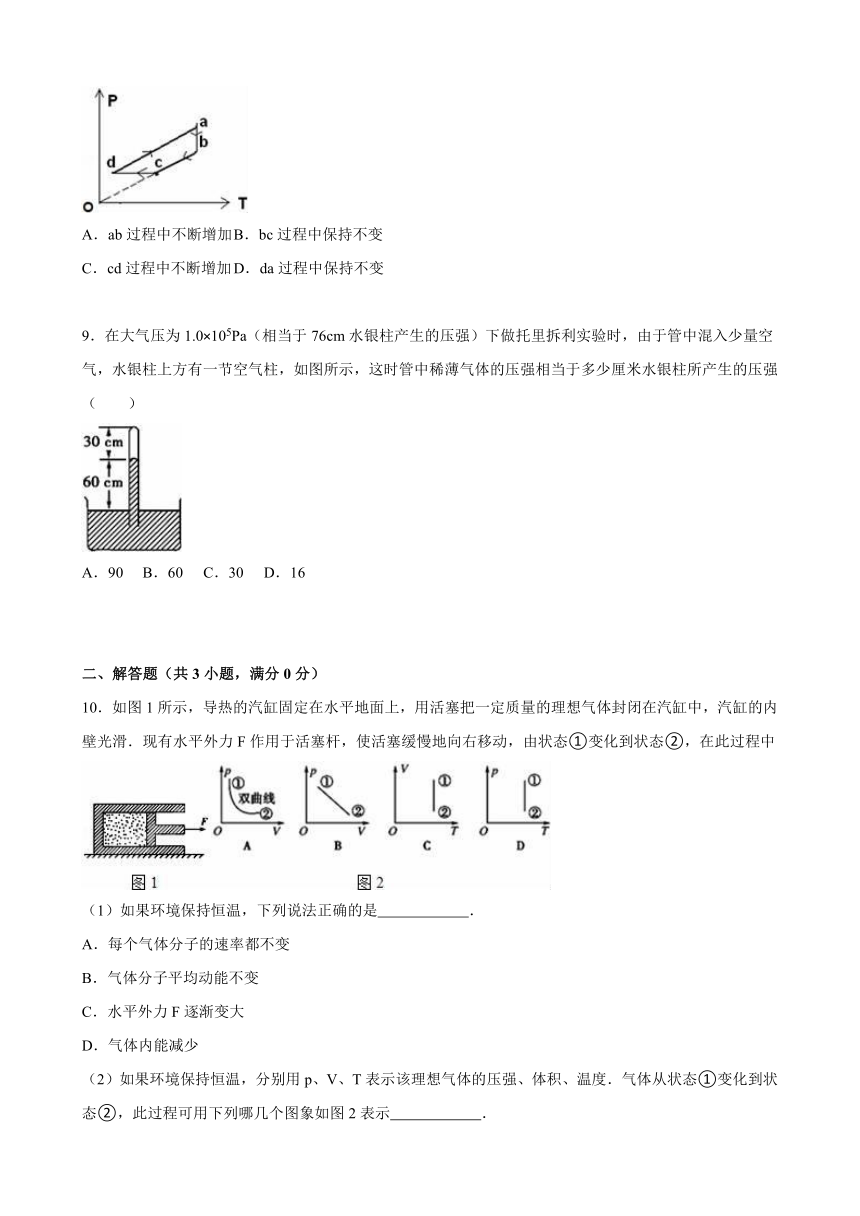
8.一定质量理想气体的状态经历了如图所示 ( http: / / www.21cnjy.com )的ab、bc、cd、da四个过程,其中bc的延长线通过原点,cd垂直于ab且与水平轴平行,da与bc平行,则气体体积在( )
A.ab过程中不断增加 B.bc过程中保持不变
C.cd过程中不断增加 D.da过程中保持不变
9.在大气压为1.0×105Pa(相当于7 ( http: / / www.21cnjy.com )6cm水银柱产生的压强)下做托里拆利实验时,由于管中混入少量空气,水银柱上方有一节空气柱,如图所示,这时管中稀薄气体的压强相当于多少厘米水银柱所产生的压强( )
A.90 B.60 C.30 D.16
二、解答题(共3小题,满分0分)
10.如图1所示,导热的汽缸固定在水平地面 ( http: / / www.21cnjy.com )上,用活塞把一定质量的理想气体封闭在汽缸中,汽缸的内壁光滑.现有水平外力F作用于活塞杆,使活塞缓慢地向右移动,由状态①变化到状态②,在此过程中
(1)如果环境保持恒温,下列说法正确的是 .
A.每个气体分子的速率都不变
B.气体分子平均动能不变
C.水平外力F逐渐变大
D.气体内能减少
(2)如果环境保持恒温,分 ( http: / / www.21cnjy.com )别用p、V、T表示该理想气体的压强、体积、温度.气体从状态①变化到状态②,此过程可用下列哪几个图象如图2表示 .
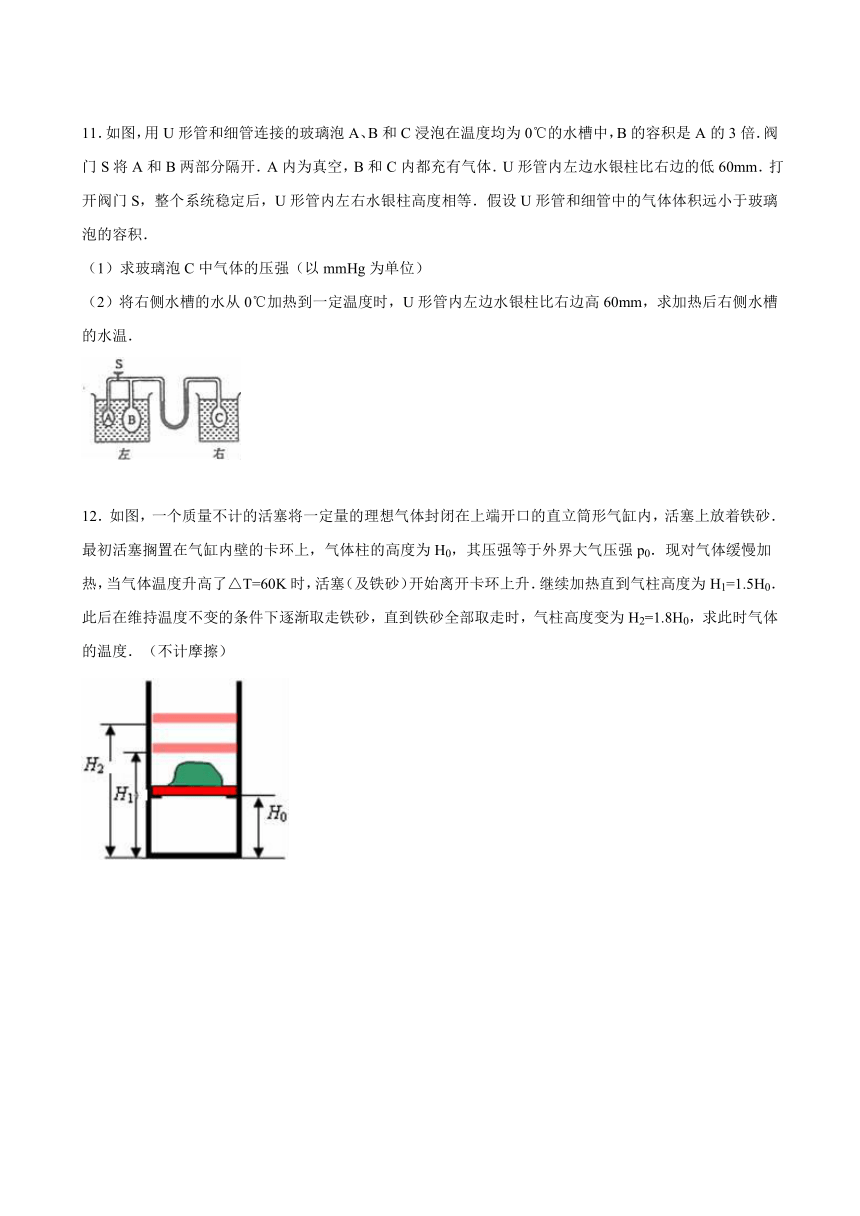
11.如图,用U形管和细管连接的玻璃泡 ( http: / / www.21cnjy.com )A、B和C浸泡在温度均为0℃的水槽中,B的容积是A的3倍.阀门S将A和B两部分隔开.A内为真空,B和C内都充有气体.U形管内左边水银柱比右边的低60mm.打开阀门S,整个系统稳定后,U形管内左右水银柱高度相等.假设U形管和细管中的气体体积远小于玻璃泡的容积.
(1)求玻璃泡C中气体的压强(以mmHg为单位)
(2)将右侧水槽的水从0℃加热到一定温度时,U形管内左边水银柱比右边高60mm,求加热后右侧水槽的水温.
12.如图,一个质量不计的活塞将一 ( http: / / www.21cnjy.com )定量的理想气体封闭在上端开口的直立筒形气缸内,活塞上放着铁砂.最初活塞搁置在气缸内壁的卡环上,气体柱的高度为H0,其压强等于外界大气压强p0.现对气体缓慢加热,当气体温度升高了△T=60K时,活塞(及铁砂)开始离开卡环上升.继续加热直到气柱高度为H1=1.5H0.此后在维持温度不变的条件下逐渐取走铁砂,直到铁砂全部取走时,气柱高度变为H2=1.8H0,求此时气体的温度.(不计摩擦)
新人教版选修3-3《第8章 气体》2015年单元测试卷(山东省潍坊市高密三中)(创新班)
参考答案与试题解析
一、选择题(共9小题,每小题3分,满分27分)
1.关于理想气体,下列说法正确的是( )
A.温度极低的气体也是理想气体
B.压强极大的气体也遵从气体实验定律
C.理想气体是对实际气体的抽象化模型
D.理想气体实际并不存在
【考点】理想气体.
【分析】只要实际气体的压强不是很高,温度不是很大,都可以近视的当成理想气体来处理,理想气体是一个理想化模型.
【解答】解:只要实际气体的压强不是 ( http: / / www.21cnjy.com )很高,温度不是很大,都可以近视的当成理想气体来处理,理想气体是物理学上为了简化为题而引入的一个理想化模型,在现实生活中不存在;通常状况下,严格遵从气态方程的气体,叫做理想气体,故CD正确.
故选:CD.
【点评】本题考查了理想气体的定义,记住:严格遵从气态方程的气体,叫做理想气体即可.
2.对一定质量的气体,通过一定的方法得到了分子数目f与速率v的两条关系图线,如图所示,下列说法正确的是( )
A.曲线Ⅰ对应的温度T1高于曲线Ⅱ对应的温度T2
B.曲线Ⅰ对应的温度T1可能等于曲线Ⅱ对应的温度T2
C.曲线Ⅰ对应的温度T1低于曲线Ⅱ对应的温度T2
D.无法判断两曲线对应的温度关系
【考点】温度是分子平均动能的标志.
【分析】根据温度是分子平均动能的标志,分析温度的变化,由气态方程分析体积的变化.由热力学第一定律分析热量的变化.
【解答】解:由图知气体在状态1时分子平均速率较小,则知气体在状态1时温度较低.故C正确.
故选:C
【点评】对于物理学中的基本概念和规律要深入理解,理解其实质,不能只是停留在表面上,同时要通过练习加强理解.
3.一定质量的理想气体处于某一平衡状态,此时其压强为P0,经历下列四种过程后可能使气体压强恢复到P0( )
A.先保持体积不变,降低压强,再保持温度不变,使体积膨胀
B.先保持体积不变,使气体升温,再保持温度不变,使体积膨胀
C.先保持温度不变,压缩体积,再保持体积不变,使气体升温
D.先保持温度不变,使体积膨胀,再保持体积不变,使气体升温
【考点】理想气体的状态方程.
【专题】理想气体状态方程专题.
【分析】根据理想气体状态方程分析四种途径压强的变化情况,判断经过每种途径后压强能否仍为P0.
【解答】解:A、先保持体积不变,降低压强,再保持温度不变,使体积膨胀时,根据气态方程可知,压强减小,故A错误;
B、先保持体积不变,使气体升温,再保持温度不变,让体积膨胀.根据气态方程得知,压强先增大,后减小,故B正确;
C、先保持温度不变,使体积膨胀,再保持体积不变,使气体升温,根据气态方程可知,压强一直增加,故C错误;
D、先保持温度不变,使体积膨胀,再保持体积不变,使气体升温,根据气态方程可知,压强先减小后增加,故D正确;
故选BD.
【点评】要使气体的压强能回到原来的压强P0,必须先增大后减小,或先减小后增大.本题也可以根据气体实验定律判断.
4.甲、乙两个相同的密闭容器中分别装有等质量的同种气体,已知甲、乙容器中气体的压强分别为p甲、P乙,且p甲<p乙.则( )
A.甲容器中气体的温度高于乙容器中气体的温度
B.甲容器中气体的温度低于乙容器中气体的温度
C.甲容器中气体分子的平均动能小于乙容器中气体分子的平均动能
D.甲容器中气体分子的平均动能大于乙容器中气体分子的平均动能
【考点】气体的体积、温度、压强之间的关系;温度是分子平均动能的标志.
【专题】常规题型;理想气体状态方程专题.
【分析】根据气体状态方程=C和已知的变化量去判断其它的物理量.
温度是分子平均动能变化的标志.
【解答】解:A、根据气体状态方程=C,由于甲、乙两个相同的密闭容器中分别装有等质量的同种气体,
所以常量C和体积V相等.
已知甲、乙容器中气体的压强分别为p甲、P乙,且p甲<p乙,所以T甲<T乙,故A错误,B正确.
C、由于温度是分子热运动平均动能的标志,所以甲容器中气体分子的平均动能小于乙容器中气体分子的平均动能,故C正确,D错误.
故选BC.
【点评】描述气体的各个参量间存在相互依存关系 ( http: / / www.21cnjy.com ),当气体的状态发生变化时气体的压强、体积和温度中至少有两个参量同时发生变化,有时三个同时发生变化.
当温度升高时,气体分子平均运动的剧烈程度增加,即分子运动的平均动能增大.
5.如图所示,一定质量的理想气体,由状态A沿直线AB变化到B,在此过程中.气体分子的平均速率的变化情况是( )
A.不断增大 B.不断减小 C.先减小后增大 D.先增大后减小
【考点】理想气体的状态方程.
【专题】理想气体状态方程专题.
【分析】根据气体状态方程=C和已知的变化量去判断其它的物理量.对于一定质量的理想气体,温度升高,那么气体的内能增加.
【解答】解:根据pV=CT ( http: / / www.21cnjy.com ),可知C不变,pV越大,T越高.状态在(2,2)处温度最高,在A和B状态时,pV乘积相等,说明在AB处的温度相等,所以从A到B的过程中,温度先升高,后又减小到初始温度,温度是分子平均动能的标志,所以在这个过程中,气体分子的平均动能先增大后减小,气体分子的平均速率也是先增大后减小,所以D正确.
故选D.
【点评】等容变化应该是双 ( http: / / www.21cnjy.com )曲线的一部分,根据图象的变化的过程,分析PV乘积的变化,从而得到温度T的变化规律,就可以得到气体分子的平均速率的变化情况.
6.一定质量的某种理想气体的压强为p,热力学温度为T,单位体积里气体分子数为n,则( )
A.p增大,n一定增大 B.T减小,n一定增大
C.增大时,n一定增大 D.增大时,n一定减小
【考点】理想气体的状态方程.
【专题】理想气体状态方程专题.
【分析】单位体积内的分子数等于分子总数 ( http: / / www.21cnjy.com )与体积之比.气体的质量一定,分子总数一定,根据气态方程分析体积如何变化,即可判断单位体积内分子如何变化.
【解答】解:A、当P增大时,根据气态方 ( http: / / www.21cnjy.com )程=c,可知气体的体积不一定减小,还与温度的变化情况有关,所以单位体积内的分子数不一定增大,故A错误.
B、当T减小时,根据气态方程=c,可知气体的体积不一定减小,还与压强的变化情况有关,所以单位体积内的分子数不一定增大,故B错误.
C、D、当的比值增大时,根据气态方程=c,可知气体的体积一定减小,所以单位体积内的分子数一定增大,故C正确,D错误.
故选:C.
【点评】对于气体图象问题,要深刻理解,必须掌握气态方程,可结合图象的数学意义分析参量的变化.
7.如图所示,一定质量的某种气体的等压线,等压线上的a、b两个状态比较,下列说法正确的是( )
A.在相同时间内撞在单位面积上的分子数b状态较多
B.在相同时间内撞在单位面积上的分子数a状态较多
C.在相同时间内撞在相同面积上的分子数两状态一样多
D.单位体积的分子数两状态一样多
【考点】理想气体的状态方程.
【专题】理想气体状态方程专题.
【分析】在相同时间内撞在单位面积上的分子数与分子密集程度有关,即与单位体积内的分子数目有关.
【解答】解:由V﹣T图象可以看出b ( http: / / www.21cnjy.com )状态的体积大于a状态的体积,则b状态的分子密集程度小于a状态的分子密集程度,故a状态下在相同时间内撞在单位面积上的分子数a状态较多;
故选:B.
【点评】从微观上说,气体的压强与单位时间 ( http: / / www.21cnjy.com )内撞击单位面积的分子数和分子平均动能有关,a状态的温度较低,则分子平均动能较小,而二者压强相等,故a状态在相同时间内撞在单位面积上的分子数较多.
8.一定质量理想气体的状态经历了如图 ( http: / / www.21cnjy.com )所示的ab、bc、cd、da四个过程,其中bc的延长线通过原点,cd垂直于ab且与水平轴平行,da与bc平行,则气体体积在( )
A.ab过程中不断增加 B.bc过程中保持不变
C.cd过程中不断增加 D.da过程中保持不变
【考点】理想气体的状态方程.
【专题】理想气体状态方程专题.
【分析】ab过程气体发生等温过程,由玻 ( http: / / www.21cnjy.com )意耳定律分析体积的变化;bc过程,根据b、c两点与绝对零度连线,分析其斜率变化,判断体积变化,斜率越大,体积越小;cd过程是等压变化,由盖 吕萨克定律分析体积的变化.
【解答】解:A、ab过程气体发生等温过程,压强减小,由玻意耳定律分析可知,气体的体积变大,故A正确.
B、bc过程,b与绝对零度﹣2 ( http: / / www.21cnjy.com )73℃连线的斜率等于c与绝对零度﹣273℃连线的斜率,则b状态气体的体积等于c状态气体的体积,则bc过程中体积不变.故B正确.
C、cd过程是等压变化,温度降低,由盖 吕萨克定律分析可知体积减小;故C错误.
D、过d点的斜率大于过a点的斜率,则d点的体积小于a点的体积,da过程体积增大.故D错误.
故选:AB.
【点评】本题中对于等值变化,根据玻意耳定律和盖 吕萨克定律分析体积的变化,而另外两个过程,抓住过绝对零度的直线表示等容变化进行分析.
9.在大气压为1.0×105Pa(相当 ( http: / / www.21cnjy.com )于76cm水银柱产生的压强)下做托里拆利实验时,由于管中混入少量空气,水银柱上方有一节空气柱,如图所示,这时管中稀薄气体的压强相当于多少厘米水银柱所产生的压强( )
A.90 B.60 C.30 D.16
【考点】封闭气体压强.
【专题】定性思想;推理法;气体的压强专题.
【分析】知道大气压能支持的水银柱高,利用液体压强公式求的P=P0﹣h即可求得.
【解答】解:60cm高的水银柱产生的压强是 ( http: / / www.21cnjy.com )60cmHg,而大气的压强相当于76cm水银柱产生的压强,所以被封闭气体的压强为P=P0﹣h=76﹣60cmHg=16cmHg
故选:D
【点评】此题考查气体的压强的计算,难度不大,可以结合水银柱的受力平衡进行解答,也可以由液体产生的压强的公式进行计算.
二、解答题(共3小题,满分0分)
10.如图1所示,导热的汽缸 ( http: / / www.21cnjy.com )固定在水平地面上,用活塞把一定质量的理想气体封闭在汽缸中,汽缸的内壁光滑.现有水平外力F作用于活塞杆,使活塞缓慢地向右移动,由状态①变化到状态②,在此过程中
(1)如果环境保持恒温,下列说法正确的是 BC .
A.每个气体分子的速率都不变
B.气体分子平均动能不变
C.水平外力F逐渐变大
D.气体内能减少
(2)如果环境保持恒温,分别用p、V、 ( http: / / www.21cnjy.com )T表示该理想气体的压强、体积、温度.气体从状态①变化到状态②,此过程可用下列哪几个图象如图2表示 A .
【考点】理想气体的状态方程.
【专题】定性思想;推理法;理想气体状态方程专题.
【分析】(1)封闭气体等温膨胀过程,温 ( http: / / www.21cnjy.com )度是分子平均动能的标志且理想气体的内能只与温度有关,以活塞为研究对象根据受力平衡判断水平外力F的变化.
(2)如果环境保持恒温,气体做等温变化,然后结合理想气体的状态方程,逐个选项分析即可.
【解答】解:(1)A、封闭气体等温膨胀过 ( http: / / www.21cnjy.com )程,温度是分子热运动平均动能的标志,是大量分子运动的统计规律,故分子热运动的平均动能不变,不是每个分子动能都不变,故A错误;
B、气体等温膨胀,温度不变,则气体分子的平均动能不变,故B正确;
C、温度不变,体积增大,根据=C,则压强P减小,以活塞为研究对象,根据平衡条件:P0S=PS+F,
得:F=P0S﹣PS,压强P减小,则F增大,故C正确;
D、理想气体的内能只与温度有关,温度不变,则内能不变,故D错误.
故选:BC.
(2)如果环境保持恒温,气体做等温变化;
A、双曲线的方程:PV=恒量,故A正确,B错误;
C、①到②的过程体积减小,与题意相悖,故C错误;
D、①到②的过程温度不变,压强减小,根据玻意耳定律,气体的体积增大,故D错误.
故选:A
故答案为:(1)BC;(2)A
【点评】本题的突破口是:题目中说“导热”的汽缸且环境保持恒温,即得出气体做等温变化.然后会根据理想气体状态方程判断压强P的变化.
11.如图,用U形管和细管连接的玻璃泡A、B ( http: / / www.21cnjy.com )和C浸泡在温度均为0℃的水槽中,B的容积是A的3倍.阀门S将A和B两部分隔开.A内为真空,B和C内都充有气体.U形管内左边水银柱比右边的低60mm.打开阀门S,整个系统稳定后,U形管内左右水银柱高度相等.假设U形管和细管中的气体体积远小于玻璃泡的容积.
(1)求玻璃泡C中气体的压强(以mmHg为单位)
(2)将右侧水槽的水从0℃加热到一定温度时,U形管内左边水银柱比右边高60mm,求加热后右侧水槽的水温.
【考点】理想气体的状态方程;封闭气体压强.
【专题】理想气体状态方程专题.
【分析】以B内封闭气体为研究对象,做等温变化,根据玻意耳定律求出B内的压强,然后求出C内压强;
以C中封闭气体为研究对象,根据等容变化列方程求解.
【解答】解:(i)加热前C中压强始终不变,B内封闭气体初状态:PB=PC+60,打开阀门后PB′=PC
由题意:VB′=
由玻意尔定律PBVB=PB′VB′
得:PB′=180mmHg PC=PB′=180mmHg
(ii)C内封闭气体做等容变化,加热后压强PC′=PC+60mmHg
得:T′=364K
答:(1)玻璃泡C中气体的压强为180mmHg
(2)加热后右侧水槽的水温364K.
【点评】本题考查了理想气体状态方程的应用,关键是正确分析ABC中气体压强的关系
12.如图,一个质量不计的活塞将一定 ( http: / / www.21cnjy.com )量的理想气体封闭在上端开口的直立筒形气缸内,活塞上放着铁砂.最初活塞搁置在气缸内壁的卡环上,气体柱的高度为H0,其压强等于外界大气压强p0.现对气体缓慢加热,当气体温度升高了△T=60K时,活塞(及铁砂)开始离开卡环上升.继续加热直到气柱高度为H1=1.5H0.此后在维持温度不变的条件下逐渐取走铁砂,直到铁砂全部取走时,气柱高度变为H2=1.8H0,求此时气体的温度.(不计摩擦)
【考点】理想气体的状态方程;气体压强的微观意义.
【专题】理想气体状态方程专题.
【分析】对气体缓慢加热至活塞(及铁砂)开始离开卡环而上升的过程气体做等容变化;
继续加热直到气柱高度为H1=1.5H0.为等压变化;
此后在维持温度不变的条件下缓慢取走铁砂,发生等温变化.
【解答】解:对气体缓慢加热至活塞(及铁砂)开始离开卡环而上升的过程,体积不变,
初状态:P1=P0,T1=T
末状态:P2=?,T2=T+60K
根据理想气体状态方程:
=
解得:P2=P0…①
继续加热直到气柱高度为H1=1.5H0.此过程做等压变化:
=
得:T′=1.5(T+60)K…②
此后在维持温度不变的条件下缓慢取走铁砂,气体做等温变化,
初状态:压强为P2,体积为1.5H0S
取走细砂后末状态:压强为P0,体积为1.8H0S
P2 1.5H0=P0 1.8H0
得:P2=1.2P0…③
③代入①得:T=300K…④
④代入②得:T′=540K
答:直到铁砂全部取走时,气柱高度变为H2=1.8H0,此时气体的温度540k.
【点评】本题关键是确定气体发生了几个阶段的变化,找出气体各变化的初末状态参量后分过程根据气体实验定律的方程列式求解.
一、选择题(共9小题,每小题3分,满分27分)
1.关于理想气体,下列说法正确的是( )
A.温度极低的气体也是理想气体
B.压强极大的气体也遵从气体实验定律
C.理想气体是对实际气体的抽象化模型
D.理想气体实际并不存在
2.对一定质量的气体,通过一定的方法得到了分子数目f与速率v的两条关系图线,如图所示,下列说法正确的是( )
A.曲线Ⅰ对应的温度T1高于曲线Ⅱ对应的温度T2
B.曲线Ⅰ对应的温度T1可能等于曲线Ⅱ对应的温度T2
C.曲线Ⅰ对应的温度T1低于曲线Ⅱ对应的温度T2
D.无法判断两曲线对应的温度关系
3.一定质量的理想气体处于某一平衡状态,此时其压强为P0,经历下列四种过程后可能使气体压强恢复到P0( )
A.先保持体积不变,降低压强,再保持温度不变,使体积膨胀
B.先保持体积不变,使气体升温,再保持温度不变,使体积膨胀
C.先保持温度不变,压缩体积,再保持体积不变,使气体升温
D.先保持温度不变,使体积膨胀,再保持体积不变,使气体升温
4.甲、乙两个相同的密闭容器中分别装有等质量的同种气体,已知甲、乙容器中气体的压强分别为p甲、P乙,且p甲<p乙.则( )
A.甲容器中气体的温度高于乙容器中气体的温度
B.甲容器中气体的温度低于乙容器中气体的温度
C.甲容器中气体分子的平均动能小于乙容器中气体分子的平均动能
D.甲容器中气体分子的平均动能大于乙容器中气体分子的平均动能
5.如图所示,一定质量的理想气体,由状态A沿直线AB变化到B,在此过程中.气体分子的平均速率的变化情况是( )
A.不断增大 B.不断减小 C.先减小后增大 D.先增大后减小
6.一定质量的某种理想气体的压强为p,热力学温度为T,单位体积里气体分子数为n,则( )
A.p增大,n一定增大 B.T减小,n一定增大
C.增大时,n一定增大 D.增大时,n一定减小
7.如图所示,一定质量的某种气体的等压线,等压线上的a、b两个状态比较,下列说法正确的是( )
A.在相同时间内撞在单位面积上的分子数b状态较多
B.在相同时间内撞在单位面积上的分子数a状态较多
C.在相同时间内撞在相同面积上的分子数两状态一样多
D.单位体积的分子数两状态一样多
8.一定质量理想气体的状态经历了如图所示 ( http: / / www.21cnjy.com )的ab、bc、cd、da四个过程,其中bc的延长线通过原点,cd垂直于ab且与水平轴平行,da与bc平行,则气体体积在( )
A.ab过程中不断增加 B.bc过程中保持不变
C.cd过程中不断增加 D.da过程中保持不变
9.在大气压为1.0×105Pa(相当于7 ( http: / / www.21cnjy.com )6cm水银柱产生的压强)下做托里拆利实验时,由于管中混入少量空气,水银柱上方有一节空气柱,如图所示,这时管中稀薄气体的压强相当于多少厘米水银柱所产生的压强( )
A.90 B.60 C.30 D.16
二、解答题(共3小题,满分0分)
10.如图1所示,导热的汽缸固定在水平地面 ( http: / / www.21cnjy.com )上,用活塞把一定质量的理想气体封闭在汽缸中,汽缸的内壁光滑.现有水平外力F作用于活塞杆,使活塞缓慢地向右移动,由状态①变化到状态②,在此过程中
(1)如果环境保持恒温,下列说法正确的是 .
A.每个气体分子的速率都不变
B.气体分子平均动能不变
C.水平外力F逐渐变大
D.气体内能减少
(2)如果环境保持恒温,分 ( http: / / www.21cnjy.com )别用p、V、T表示该理想气体的压强、体积、温度.气体从状态①变化到状态②,此过程可用下列哪几个图象如图2表示 .
11.如图,用U形管和细管连接的玻璃泡 ( http: / / www.21cnjy.com )A、B和C浸泡在温度均为0℃的水槽中,B的容积是A的3倍.阀门S将A和B两部分隔开.A内为真空,B和C内都充有气体.U形管内左边水银柱比右边的低60mm.打开阀门S,整个系统稳定后,U形管内左右水银柱高度相等.假设U形管和细管中的气体体积远小于玻璃泡的容积.
(1)求玻璃泡C中气体的压强(以mmHg为单位)
(2)将右侧水槽的水从0℃加热到一定温度时,U形管内左边水银柱比右边高60mm,求加热后右侧水槽的水温.
12.如图,一个质量不计的活塞将一 ( http: / / www.21cnjy.com )定量的理想气体封闭在上端开口的直立筒形气缸内,活塞上放着铁砂.最初活塞搁置在气缸内壁的卡环上,气体柱的高度为H0,其压强等于外界大气压强p0.现对气体缓慢加热,当气体温度升高了△T=60K时,活塞(及铁砂)开始离开卡环上升.继续加热直到气柱高度为H1=1.5H0.此后在维持温度不变的条件下逐渐取走铁砂,直到铁砂全部取走时,气柱高度变为H2=1.8H0,求此时气体的温度.(不计摩擦)
新人教版选修3-3《第8章 气体》2015年单元测试卷(山东省潍坊市高密三中)(创新班)
参考答案与试题解析
一、选择题(共9小题,每小题3分,满分27分)
1.关于理想气体,下列说法正确的是( )
A.温度极低的气体也是理想气体
B.压强极大的气体也遵从气体实验定律
C.理想气体是对实际气体的抽象化模型
D.理想气体实际并不存在
【考点】理想气体.
【分析】只要实际气体的压强不是很高,温度不是很大,都可以近视的当成理想气体来处理,理想气体是一个理想化模型.
【解答】解:只要实际气体的压强不是 ( http: / / www.21cnjy.com )很高,温度不是很大,都可以近视的当成理想气体来处理,理想气体是物理学上为了简化为题而引入的一个理想化模型,在现实生活中不存在;通常状况下,严格遵从气态方程的气体,叫做理想气体,故CD正确.
故选:CD.
【点评】本题考查了理想气体的定义,记住:严格遵从气态方程的气体,叫做理想气体即可.
2.对一定质量的气体,通过一定的方法得到了分子数目f与速率v的两条关系图线,如图所示,下列说法正确的是( )
A.曲线Ⅰ对应的温度T1高于曲线Ⅱ对应的温度T2
B.曲线Ⅰ对应的温度T1可能等于曲线Ⅱ对应的温度T2
C.曲线Ⅰ对应的温度T1低于曲线Ⅱ对应的温度T2
D.无法判断两曲线对应的温度关系
【考点】温度是分子平均动能的标志.
【分析】根据温度是分子平均动能的标志,分析温度的变化,由气态方程分析体积的变化.由热力学第一定律分析热量的变化.
【解答】解:由图知气体在状态1时分子平均速率较小,则知气体在状态1时温度较低.故C正确.
故选:C
【点评】对于物理学中的基本概念和规律要深入理解,理解其实质,不能只是停留在表面上,同时要通过练习加强理解.
3.一定质量的理想气体处于某一平衡状态,此时其压强为P0,经历下列四种过程后可能使气体压强恢复到P0( )
A.先保持体积不变,降低压强,再保持温度不变,使体积膨胀
B.先保持体积不变,使气体升温,再保持温度不变,使体积膨胀
C.先保持温度不变,压缩体积,再保持体积不变,使气体升温
D.先保持温度不变,使体积膨胀,再保持体积不变,使气体升温
【考点】理想气体的状态方程.
【专题】理想气体状态方程专题.
【分析】根据理想气体状态方程分析四种途径压强的变化情况,判断经过每种途径后压强能否仍为P0.
【解答】解:A、先保持体积不变,降低压强,再保持温度不变,使体积膨胀时,根据气态方程可知,压强减小,故A错误;
B、先保持体积不变,使气体升温,再保持温度不变,让体积膨胀.根据气态方程得知,压强先增大,后减小,故B正确;
C、先保持温度不变,使体积膨胀,再保持体积不变,使气体升温,根据气态方程可知,压强一直增加,故C错误;
D、先保持温度不变,使体积膨胀,再保持体积不变,使气体升温,根据气态方程可知,压强先减小后增加,故D正确;
故选BD.
【点评】要使气体的压强能回到原来的压强P0,必须先增大后减小,或先减小后增大.本题也可以根据气体实验定律判断.
4.甲、乙两个相同的密闭容器中分别装有等质量的同种气体,已知甲、乙容器中气体的压强分别为p甲、P乙,且p甲<p乙.则( )
A.甲容器中气体的温度高于乙容器中气体的温度
B.甲容器中气体的温度低于乙容器中气体的温度
C.甲容器中气体分子的平均动能小于乙容器中气体分子的平均动能
D.甲容器中气体分子的平均动能大于乙容器中气体分子的平均动能
【考点】气体的体积、温度、压强之间的关系;温度是分子平均动能的标志.
【专题】常规题型;理想气体状态方程专题.
【分析】根据气体状态方程=C和已知的变化量去判断其它的物理量.
温度是分子平均动能变化的标志.
【解答】解:A、根据气体状态方程=C,由于甲、乙两个相同的密闭容器中分别装有等质量的同种气体,
所以常量C和体积V相等.
已知甲、乙容器中气体的压强分别为p甲、P乙,且p甲<p乙,所以T甲<T乙,故A错误,B正确.
C、由于温度是分子热运动平均动能的标志,所以甲容器中气体分子的平均动能小于乙容器中气体分子的平均动能,故C正确,D错误.
故选BC.
【点评】描述气体的各个参量间存在相互依存关系 ( http: / / www.21cnjy.com ),当气体的状态发生变化时气体的压强、体积和温度中至少有两个参量同时发生变化,有时三个同时发生变化.
当温度升高时,气体分子平均运动的剧烈程度增加,即分子运动的平均动能增大.
5.如图所示,一定质量的理想气体,由状态A沿直线AB变化到B,在此过程中.气体分子的平均速率的变化情况是( )
A.不断增大 B.不断减小 C.先减小后增大 D.先增大后减小
【考点】理想气体的状态方程.
【专题】理想气体状态方程专题.
【分析】根据气体状态方程=C和已知的变化量去判断其它的物理量.对于一定质量的理想气体,温度升高,那么气体的内能增加.
【解答】解:根据pV=CT ( http: / / www.21cnjy.com ),可知C不变,pV越大,T越高.状态在(2,2)处温度最高,在A和B状态时,pV乘积相等,说明在AB处的温度相等,所以从A到B的过程中,温度先升高,后又减小到初始温度,温度是分子平均动能的标志,所以在这个过程中,气体分子的平均动能先增大后减小,气体分子的平均速率也是先增大后减小,所以D正确.
故选D.
【点评】等容变化应该是双 ( http: / / www.21cnjy.com )曲线的一部分,根据图象的变化的过程,分析PV乘积的变化,从而得到温度T的变化规律,就可以得到气体分子的平均速率的变化情况.
6.一定质量的某种理想气体的压强为p,热力学温度为T,单位体积里气体分子数为n,则( )
A.p增大,n一定增大 B.T减小,n一定增大
C.增大时,n一定增大 D.增大时,n一定减小
【考点】理想气体的状态方程.
【专题】理想气体状态方程专题.
【分析】单位体积内的分子数等于分子总数 ( http: / / www.21cnjy.com )与体积之比.气体的质量一定,分子总数一定,根据气态方程分析体积如何变化,即可判断单位体积内分子如何变化.
【解答】解:A、当P增大时,根据气态方 ( http: / / www.21cnjy.com )程=c,可知气体的体积不一定减小,还与温度的变化情况有关,所以单位体积内的分子数不一定增大,故A错误.
B、当T减小时,根据气态方程=c,可知气体的体积不一定减小,还与压强的变化情况有关,所以单位体积内的分子数不一定增大,故B错误.
C、D、当的比值增大时,根据气态方程=c,可知气体的体积一定减小,所以单位体积内的分子数一定增大,故C正确,D错误.
故选:C.
【点评】对于气体图象问题,要深刻理解,必须掌握气态方程,可结合图象的数学意义分析参量的变化.
7.如图所示,一定质量的某种气体的等压线,等压线上的a、b两个状态比较,下列说法正确的是( )
A.在相同时间内撞在单位面积上的分子数b状态较多
B.在相同时间内撞在单位面积上的分子数a状态较多
C.在相同时间内撞在相同面积上的分子数两状态一样多
D.单位体积的分子数两状态一样多
【考点】理想气体的状态方程.
【专题】理想气体状态方程专题.
【分析】在相同时间内撞在单位面积上的分子数与分子密集程度有关,即与单位体积内的分子数目有关.
【解答】解:由V﹣T图象可以看出b ( http: / / www.21cnjy.com )状态的体积大于a状态的体积,则b状态的分子密集程度小于a状态的分子密集程度,故a状态下在相同时间内撞在单位面积上的分子数a状态较多;
故选:B.
【点评】从微观上说,气体的压强与单位时间 ( http: / / www.21cnjy.com )内撞击单位面积的分子数和分子平均动能有关,a状态的温度较低,则分子平均动能较小,而二者压强相等,故a状态在相同时间内撞在单位面积上的分子数较多.
8.一定质量理想气体的状态经历了如图 ( http: / / www.21cnjy.com )所示的ab、bc、cd、da四个过程,其中bc的延长线通过原点,cd垂直于ab且与水平轴平行,da与bc平行,则气体体积在( )
A.ab过程中不断增加 B.bc过程中保持不变
C.cd过程中不断增加 D.da过程中保持不变
【考点】理想气体的状态方程.
【专题】理想气体状态方程专题.
【分析】ab过程气体发生等温过程,由玻 ( http: / / www.21cnjy.com )意耳定律分析体积的变化;bc过程,根据b、c两点与绝对零度连线,分析其斜率变化,判断体积变化,斜率越大,体积越小;cd过程是等压变化,由盖 吕萨克定律分析体积的变化.
【解答】解:A、ab过程气体发生等温过程,压强减小,由玻意耳定律分析可知,气体的体积变大,故A正确.
B、bc过程,b与绝对零度﹣2 ( http: / / www.21cnjy.com )73℃连线的斜率等于c与绝对零度﹣273℃连线的斜率,则b状态气体的体积等于c状态气体的体积,则bc过程中体积不变.故B正确.
C、cd过程是等压变化,温度降低,由盖 吕萨克定律分析可知体积减小;故C错误.
D、过d点的斜率大于过a点的斜率,则d点的体积小于a点的体积,da过程体积增大.故D错误.
故选:AB.
【点评】本题中对于等值变化,根据玻意耳定律和盖 吕萨克定律分析体积的变化,而另外两个过程,抓住过绝对零度的直线表示等容变化进行分析.
9.在大气压为1.0×105Pa(相当 ( http: / / www.21cnjy.com )于76cm水银柱产生的压强)下做托里拆利实验时,由于管中混入少量空气,水银柱上方有一节空气柱,如图所示,这时管中稀薄气体的压强相当于多少厘米水银柱所产生的压强( )
A.90 B.60 C.30 D.16
【考点】封闭气体压强.
【专题】定性思想;推理法;气体的压强专题.
【分析】知道大气压能支持的水银柱高,利用液体压强公式求的P=P0﹣h即可求得.
【解答】解:60cm高的水银柱产生的压强是 ( http: / / www.21cnjy.com )60cmHg,而大气的压强相当于76cm水银柱产生的压强,所以被封闭气体的压强为P=P0﹣h=76﹣60cmHg=16cmHg
故选:D
【点评】此题考查气体的压强的计算,难度不大,可以结合水银柱的受力平衡进行解答,也可以由液体产生的压强的公式进行计算.
二、解答题(共3小题,满分0分)
10.如图1所示,导热的汽缸 ( http: / / www.21cnjy.com )固定在水平地面上,用活塞把一定质量的理想气体封闭在汽缸中,汽缸的内壁光滑.现有水平外力F作用于活塞杆,使活塞缓慢地向右移动,由状态①变化到状态②,在此过程中
(1)如果环境保持恒温,下列说法正确的是 BC .
A.每个气体分子的速率都不变
B.气体分子平均动能不变
C.水平外力F逐渐变大
D.气体内能减少
(2)如果环境保持恒温,分别用p、V、 ( http: / / www.21cnjy.com )T表示该理想气体的压强、体积、温度.气体从状态①变化到状态②,此过程可用下列哪几个图象如图2表示 A .
【考点】理想气体的状态方程.
【专题】定性思想;推理法;理想气体状态方程专题.
【分析】(1)封闭气体等温膨胀过程,温 ( http: / / www.21cnjy.com )度是分子平均动能的标志且理想气体的内能只与温度有关,以活塞为研究对象根据受力平衡判断水平外力F的变化.
(2)如果环境保持恒温,气体做等温变化,然后结合理想气体的状态方程,逐个选项分析即可.
【解答】解:(1)A、封闭气体等温膨胀过 ( http: / / www.21cnjy.com )程,温度是分子热运动平均动能的标志,是大量分子运动的统计规律,故分子热运动的平均动能不变,不是每个分子动能都不变,故A错误;
B、气体等温膨胀,温度不变,则气体分子的平均动能不变,故B正确;
C、温度不变,体积增大,根据=C,则压强P减小,以活塞为研究对象,根据平衡条件:P0S=PS+F,
得:F=P0S﹣PS,压强P减小,则F增大,故C正确;
D、理想气体的内能只与温度有关,温度不变,则内能不变,故D错误.
故选:BC.
(2)如果环境保持恒温,气体做等温变化;
A、双曲线的方程:PV=恒量,故A正确,B错误;
C、①到②的过程体积减小,与题意相悖,故C错误;
D、①到②的过程温度不变,压强减小,根据玻意耳定律,气体的体积增大,故D错误.
故选:A
故答案为:(1)BC;(2)A
【点评】本题的突破口是:题目中说“导热”的汽缸且环境保持恒温,即得出气体做等温变化.然后会根据理想气体状态方程判断压强P的变化.
11.如图,用U形管和细管连接的玻璃泡A、B ( http: / / www.21cnjy.com )和C浸泡在温度均为0℃的水槽中,B的容积是A的3倍.阀门S将A和B两部分隔开.A内为真空,B和C内都充有气体.U形管内左边水银柱比右边的低60mm.打开阀门S,整个系统稳定后,U形管内左右水银柱高度相等.假设U形管和细管中的气体体积远小于玻璃泡的容积.
(1)求玻璃泡C中气体的压强(以mmHg为单位)
(2)将右侧水槽的水从0℃加热到一定温度时,U形管内左边水银柱比右边高60mm,求加热后右侧水槽的水温.
【考点】理想气体的状态方程;封闭气体压强.
【专题】理想气体状态方程专题.
【分析】以B内封闭气体为研究对象,做等温变化,根据玻意耳定律求出B内的压强,然后求出C内压强;
以C中封闭气体为研究对象,根据等容变化列方程求解.
【解答】解:(i)加热前C中压强始终不变,B内封闭气体初状态:PB=PC+60,打开阀门后PB′=PC
由题意:VB′=
由玻意尔定律PBVB=PB′VB′
得:PB′=180mmHg PC=PB′=180mmHg
(ii)C内封闭气体做等容变化,加热后压强PC′=PC+60mmHg
得:T′=364K
答:(1)玻璃泡C中气体的压强为180mmHg
(2)加热后右侧水槽的水温364K.
【点评】本题考查了理想气体状态方程的应用,关键是正确分析ABC中气体压强的关系
12.如图,一个质量不计的活塞将一定 ( http: / / www.21cnjy.com )量的理想气体封闭在上端开口的直立筒形气缸内,活塞上放着铁砂.最初活塞搁置在气缸内壁的卡环上,气体柱的高度为H0,其压强等于外界大气压强p0.现对气体缓慢加热,当气体温度升高了△T=60K时,活塞(及铁砂)开始离开卡环上升.继续加热直到气柱高度为H1=1.5H0.此后在维持温度不变的条件下逐渐取走铁砂,直到铁砂全部取走时,气柱高度变为H2=1.8H0,求此时气体的温度.(不计摩擦)
【考点】理想气体的状态方程;气体压强的微观意义.
【专题】理想气体状态方程专题.
【分析】对气体缓慢加热至活塞(及铁砂)开始离开卡环而上升的过程气体做等容变化;
继续加热直到气柱高度为H1=1.5H0.为等压变化;
此后在维持温度不变的条件下缓慢取走铁砂,发生等温变化.
【解答】解:对气体缓慢加热至活塞(及铁砂)开始离开卡环而上升的过程,体积不变,
初状态:P1=P0,T1=T
末状态:P2=?,T2=T+60K
根据理想气体状态方程:
=
解得:P2=P0…①
继续加热直到气柱高度为H1=1.5H0.此过程做等压变化:
=
得:T′=1.5(T+60)K…②
此后在维持温度不变的条件下缓慢取走铁砂,气体做等温变化,
初状态:压强为P2,体积为1.5H0S
取走细砂后末状态:压强为P0,体积为1.8H0S
P2 1.5H0=P0 1.8H0
得:P2=1.2P0…③
③代入①得:T=300K…④
④代入②得:T′=540K
答:直到铁砂全部取走时,气柱高度变为H2=1.8H0,此时气体的温度540k.
【点评】本题关键是确定气体发生了几个阶段的变化,找出气体各变化的初末状态参量后分过程根据气体实验定律的方程列式求解.
