山西省运城市盐湖区第五高级中学2024-2025学年高一上学期月考试卷(含答案)
文档属性
| 名称 | 山西省运城市盐湖区第五高级中学2024-2025学年高一上学期月考试卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 134.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-22 00:00:00 | ||
图片预览


文档简介
山西运城2024-2025学年度盐湖五中高一化学月考卷
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
第I卷(选择题42分)
一、选择题(共42分)
1.思超同学炒菜时不小心把少许食盐洒在炉火上,可看到
A.黄绿色火焰 B.黄色火焰 C.紫红色火焰 D.洋红色火焰
2.将一小块钠放到下列稀溶液中,既有气体又有沉淀生成的是
A.氯化钠 B.硝酸钡 C.氢氧化钠 D.硫酸铜
3.下列关于钠的说法中,正确的是
A.实验后剩余的钠粒,不能放回原试剂瓶中
B.钠着火后,可用泡沫灭火器来灭火
C.钠的化学性质比较活泼,少量的钠可以保存在与钠不反应的煤油中
D.已知金属锂的密度比煤油小,则少量的金属锂可以保存在煤油中
4.一小块金属钠长时间置于空气中,可能有下列现象,这些现象出现的先后顺序是
①变成白色粉末 ②变暗 ③变潮湿 ④变成白色晶体
A.②③④① B.①②③④ C.②③①④ D.③②④①
5.下列物质在空气中加热时质量会增加的是
A. B. C.NaOH D.
6.下列关于钠的化合物的叙述不正确的是
A.热稳定性
B.与都能和水反应生成碱,它们都是碱性氧化物
C.过氧化钠放到酚酞溶液中会使溶液先红色后褪色
D.中阴、阳离子的个数比为
7.下列反应的离子方程式书写正确的是
A.过氧化钠与水的反应:
B.钠与水反应:
C.溶液与溶液反应:
D.氢氧化钠溶液与过量的碳酸氢钙溶液反应:
8.下列说法中不正确的是
A.Na2CO3 和NaHCO3均可与HNO3反应 B.Na2CO3、NaHCO3均易溶于水
C.Na2CO3的热稳定性比NaHCO3弱 D.Na2CO3能与石灰水反应
9.除去碳酸钠粉末中的少量碳酸氢钠的最佳实验方法是
A.加盐酸 B.加热至恒重 C.通入 D.加入氢氧化钠溶液
10.在酸性溶液中,下列离子能大量共存的是
A.、、、
B.、、、
C.、、、
D.、、、
11.某兴趣小组实验室制取后的废液中的溶质是和。某同学取一定质量的该废液于烧杯中,并向其中逐滴加入溶液充分反应。下列图像是滴加过程中他对烧杯中物质变化情况的分析(溶液呈中性),其中错误的是
A.B.
C.D.
12.实验室模拟并改进侯氏制碱法制备的实验流程如下图
下列说法错误的是
A.实验室制备的可用饱和溶液洗气
B.生成的总反应的离子方程式为
C.流程中可循环使用的试剂仅为
D.母液中含有较多,可作肥料
13.下表中,对陈述I、II的正确性及两者间是否具有因果关系的判断都正确的是
选项 陈述I 陈述II 判断
A 小苏打可用于治疗胃酸过多 可与盐酸反应 I对,II对,无
B 与过氧化钠反应 着火不能用灭火 I对,II错,无
C 碳酸钠、碳酸氢钠能用澄清石灰水鉴别 能与澄清石灰水反应生成白色沉淀,而不能 I对,II对,有
D 过氧化钠用于航天员的供氧剂 能和反应生成 I对,II对,有
A.A B.B C.C D.D
14.现加热的碳酸钠和碳酸氢钠的混合固体使碳酸氢钠完全分解,固体质量变为,则原混合固体中碳酸钠的质量分数为
A. B. C. D.
第II卷(非选择题58分)
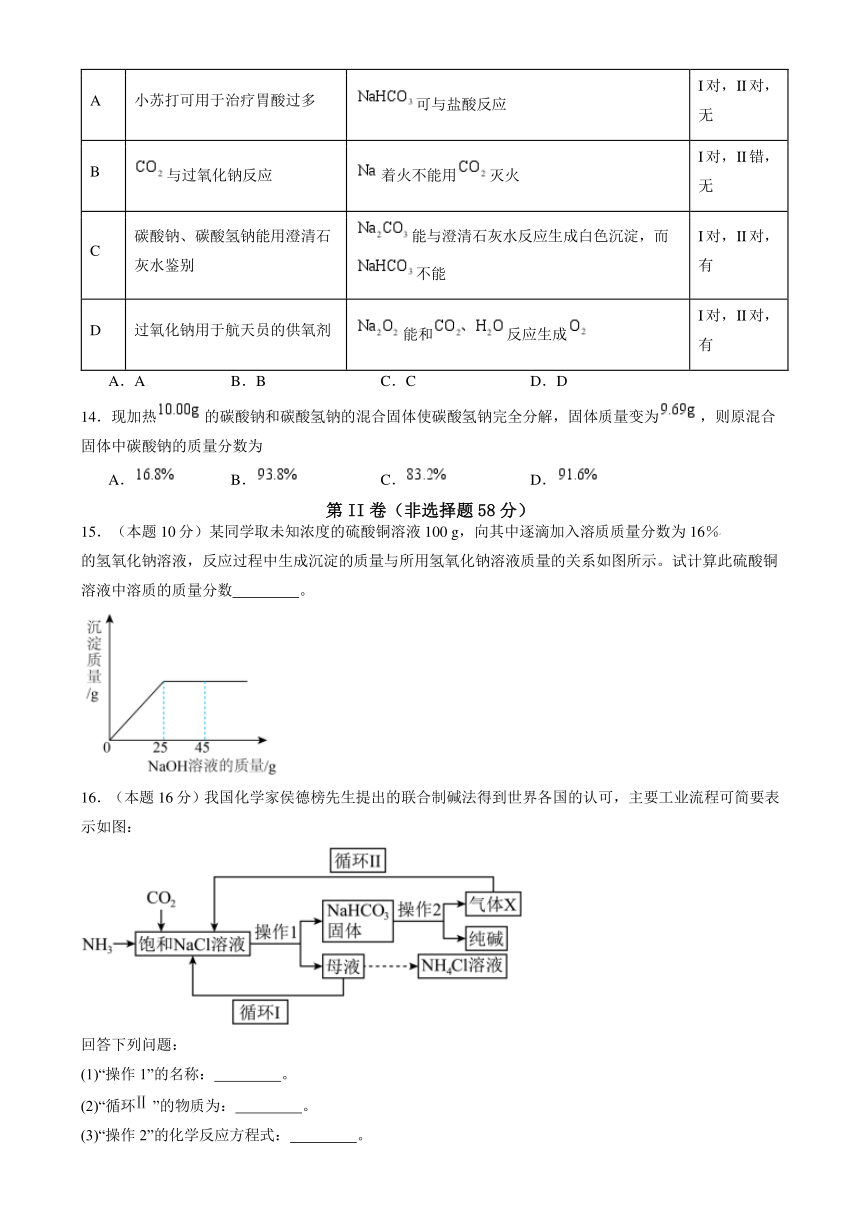
15.(本题10分)某同学取未知浓度的硫酸铜溶液100 g,向其中逐滴加入溶质质量分数为16%
的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示。试计算此硫酸铜溶液中溶质的质量分数 。
16.(本题16分)我国化学家侯德榜先生提出的联合制碱法得到世界各国的认可,主要工业流程可简要表示如图:
回答下列问题:
(1)“操作1”的名称: 。
(2)“循环”的物质为: 。
(3)“操作2”的化学反应方程式: 。
(4)流程中产生NaHCO3固体的化学方程式: 。
(5)下列说法不正确的是___________。
A.由“操作1”可知,在相同温度下碳酸氢钠溶解度比NaCl大
B.侯德榜联合制碱法得到的主要产品是烧碱,副产物是NH4Cl
C.应该向“饱和NaCl溶液”中先通入足量NH3,再通入足量CO2
D.使原料氯化钠的利用率从70%提高到90%以上,主要设计了“循环”
17.(本题16分)将化学物质通过它们的转化关系归纳成思维导图,是学习元素及其化合物的基本方法。物质A~H的转化关系如图所示,其中A、B、C为单质,其他均为化合物,A为密度最小的气体,F是造成温室效应的主要气体之一,E为淡黄色固体。回答下列问题:
(1)化合物E的化学式为 ,G的化学式为 ,化合物E中阴、阳离子的个数比为 。
(2)E与F反应的化学方程式为 ,现实应用可用作 。
(3)反应③的化学方程式为 ,据此判断 (填是或否)碱性氧化物。
(4)C与D反应的化学方程式为 。
18.(本题16分)某课外活动小组为了探究钠与MgSO4溶液的反应,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒金属钠,再从U形管左端加入MgSO4溶液,一段时间后加热铜丝。回答下列问题:
(1)实验室的钠保存在 中,从试剂瓶取出后剩余的Na能否放回原试剂瓶? (填“能”或“否”)。
(2)U形管中出现的现象是___________(填字母)。
A.有气泡生成,钠熔化成小球
B.钠在煤油面上四处游动
C.溶液中有银白色金属生成
D.溶液变浑浊
(3)写出钠与MgSO4溶液反应的离子方程式: 。
(4)铜丝的变化现象是 。
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 B D C A D B D C B A
题号 11 12 13 14
答案 C C D D
15.8%
16.(1)过滤
(2)CO2
(3)2NaHCO3Na2CO3+CO2↑+H2O
(4)NH3+CO2+NaCl+H2O=NaHCO3↓+NH4Cl
(5)AB
17.(1) Na2O2 NaOH 1:2
(2) 2Na2O2+2CO2=2Na2CO3+O2 呼吸面罩或供氧剂
(3) 2Na2O2+2H2O=4NaOH+O2↑ 否
(4)2Na+2H2O=2NaOH+H2↑
18.(1) 煤油 能
(2)AD
(3)
(4)黑色变为红色
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
第I卷(选择题42分)
一、选择题(共42分)
1.思超同学炒菜时不小心把少许食盐洒在炉火上,可看到
A.黄绿色火焰 B.黄色火焰 C.紫红色火焰 D.洋红色火焰
2.将一小块钠放到下列稀溶液中,既有气体又有沉淀生成的是
A.氯化钠 B.硝酸钡 C.氢氧化钠 D.硫酸铜
3.下列关于钠的说法中,正确的是
A.实验后剩余的钠粒,不能放回原试剂瓶中
B.钠着火后,可用泡沫灭火器来灭火
C.钠的化学性质比较活泼,少量的钠可以保存在与钠不反应的煤油中
D.已知金属锂的密度比煤油小,则少量的金属锂可以保存在煤油中
4.一小块金属钠长时间置于空气中,可能有下列现象,这些现象出现的先后顺序是
①变成白色粉末 ②变暗 ③变潮湿 ④变成白色晶体
A.②③④① B.①②③④ C.②③①④ D.③②④①
5.下列物质在空气中加热时质量会增加的是
A. B. C.NaOH D.
6.下列关于钠的化合物的叙述不正确的是
A.热稳定性
B.与都能和水反应生成碱,它们都是碱性氧化物
C.过氧化钠放到酚酞溶液中会使溶液先红色后褪色
D.中阴、阳离子的个数比为
7.下列反应的离子方程式书写正确的是
A.过氧化钠与水的反应:
B.钠与水反应:
C.溶液与溶液反应:
D.氢氧化钠溶液与过量的碳酸氢钙溶液反应:
8.下列说法中不正确的是
A.Na2CO3 和NaHCO3均可与HNO3反应 B.Na2CO3、NaHCO3均易溶于水
C.Na2CO3的热稳定性比NaHCO3弱 D.Na2CO3能与石灰水反应
9.除去碳酸钠粉末中的少量碳酸氢钠的最佳实验方法是
A.加盐酸 B.加热至恒重 C.通入 D.加入氢氧化钠溶液
10.在酸性溶液中,下列离子能大量共存的是
A.、、、
B.、、、
C.、、、
D.、、、
11.某兴趣小组实验室制取后的废液中的溶质是和。某同学取一定质量的该废液于烧杯中,并向其中逐滴加入溶液充分反应。下列图像是滴加过程中他对烧杯中物质变化情况的分析(溶液呈中性),其中错误的是
A.B.
C.D.
12.实验室模拟并改进侯氏制碱法制备的实验流程如下图
下列说法错误的是
A.实验室制备的可用饱和溶液洗气
B.生成的总反应的离子方程式为
C.流程中可循环使用的试剂仅为
D.母液中含有较多,可作肥料
13.下表中,对陈述I、II的正确性及两者间是否具有因果关系的判断都正确的是
选项 陈述I 陈述II 判断
A 小苏打可用于治疗胃酸过多 可与盐酸反应 I对,II对,无
B 与过氧化钠反应 着火不能用灭火 I对,II错,无
C 碳酸钠、碳酸氢钠能用澄清石灰水鉴别 能与澄清石灰水反应生成白色沉淀,而不能 I对,II对,有
D 过氧化钠用于航天员的供氧剂 能和反应生成 I对,II对,有
A.A B.B C.C D.D
14.现加热的碳酸钠和碳酸氢钠的混合固体使碳酸氢钠完全分解,固体质量变为,则原混合固体中碳酸钠的质量分数为
A. B. C. D.
第II卷(非选择题58分)
15.(本题10分)某同学取未知浓度的硫酸铜溶液100 g,向其中逐滴加入溶质质量分数为16%
的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示。试计算此硫酸铜溶液中溶质的质量分数 。
16.(本题16分)我国化学家侯德榜先生提出的联合制碱法得到世界各国的认可,主要工业流程可简要表示如图:
回答下列问题:
(1)“操作1”的名称: 。
(2)“循环”的物质为: 。
(3)“操作2”的化学反应方程式: 。
(4)流程中产生NaHCO3固体的化学方程式: 。
(5)下列说法不正确的是___________。
A.由“操作1”可知,在相同温度下碳酸氢钠溶解度比NaCl大
B.侯德榜联合制碱法得到的主要产品是烧碱,副产物是NH4Cl
C.应该向“饱和NaCl溶液”中先通入足量NH3,再通入足量CO2
D.使原料氯化钠的利用率从70%提高到90%以上,主要设计了“循环”
17.(本题16分)将化学物质通过它们的转化关系归纳成思维导图,是学习元素及其化合物的基本方法。物质A~H的转化关系如图所示,其中A、B、C为单质,其他均为化合物,A为密度最小的气体,F是造成温室效应的主要气体之一,E为淡黄色固体。回答下列问题:
(1)化合物E的化学式为 ,G的化学式为 ,化合物E中阴、阳离子的个数比为 。
(2)E与F反应的化学方程式为 ,现实应用可用作 。
(3)反应③的化学方程式为 ,据此判断 (填是或否)碱性氧化物。
(4)C与D反应的化学方程式为 。
18.(本题16分)某课外活动小组为了探究钠与MgSO4溶液的反应,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒金属钠,再从U形管左端加入MgSO4溶液,一段时间后加热铜丝。回答下列问题:
(1)实验室的钠保存在 中,从试剂瓶取出后剩余的Na能否放回原试剂瓶? (填“能”或“否”)。
(2)U形管中出现的现象是___________(填字母)。
A.有气泡生成,钠熔化成小球
B.钠在煤油面上四处游动
C.溶液中有银白色金属生成
D.溶液变浑浊
(3)写出钠与MgSO4溶液反应的离子方程式: 。
(4)铜丝的变化现象是 。
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 B D C A D B D C B A
题号 11 12 13 14
答案 C C D D
15.8%
16.(1)过滤
(2)CO2
(3)2NaHCO3Na2CO3+CO2↑+H2O
(4)NH3+CO2+NaCl+H2O=NaHCO3↓+NH4Cl
(5)AB
17.(1) Na2O2 NaOH 1:2
(2) 2Na2O2+2CO2=2Na2CO3+O2 呼吸面罩或供氧剂
(3) 2Na2O2+2H2O=4NaOH+O2↑ 否
(4)2Na+2H2O=2NaOH+H2↑
18.(1) 煤油 能
(2)AD
(3)
(4)黑色变为红色
同课章节目录
