苏教版高中化学必修一专题2从海水中获得的化学物质 专题优化总结 课件(共35张PPT)
文档属性
| 名称 | 苏教版高中化学必修一专题2从海水中获得的化学物质 专题优化总结 课件(共35张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-03-01 00:00:00 | ||
图片预览







文档简介
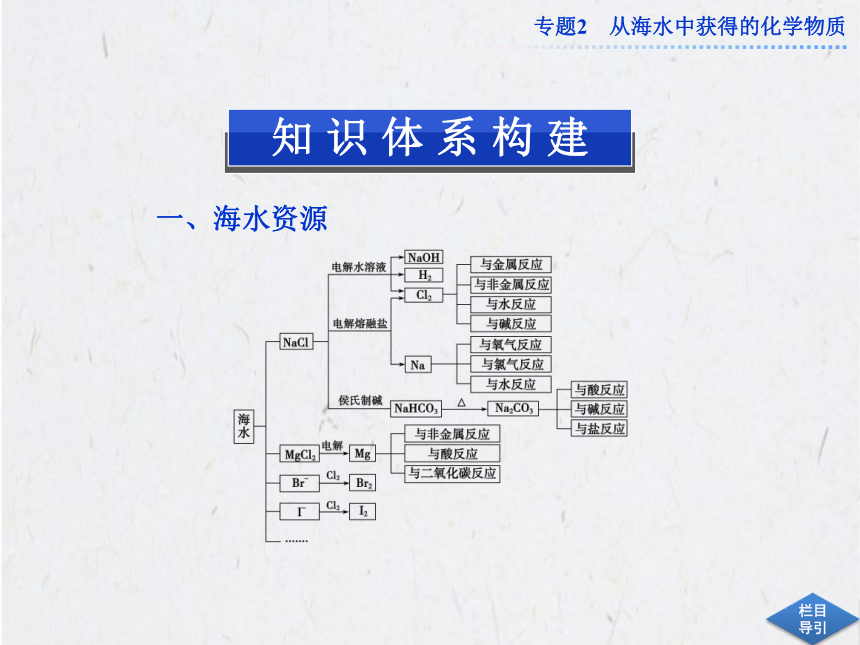
课件35张PPT。专题优化总结专题2 从海水中获得的化学物质一、海水资源
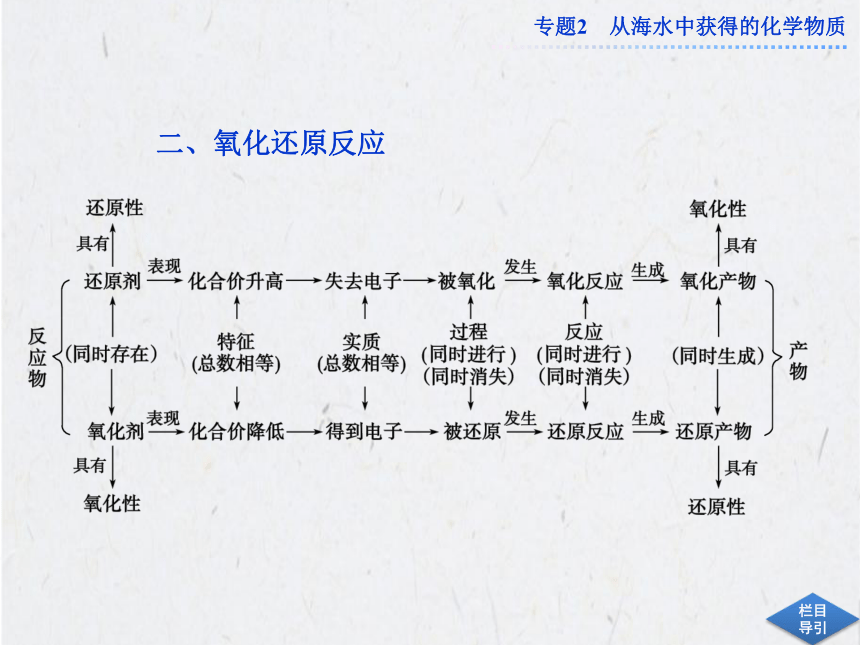
二、氧化还原反应
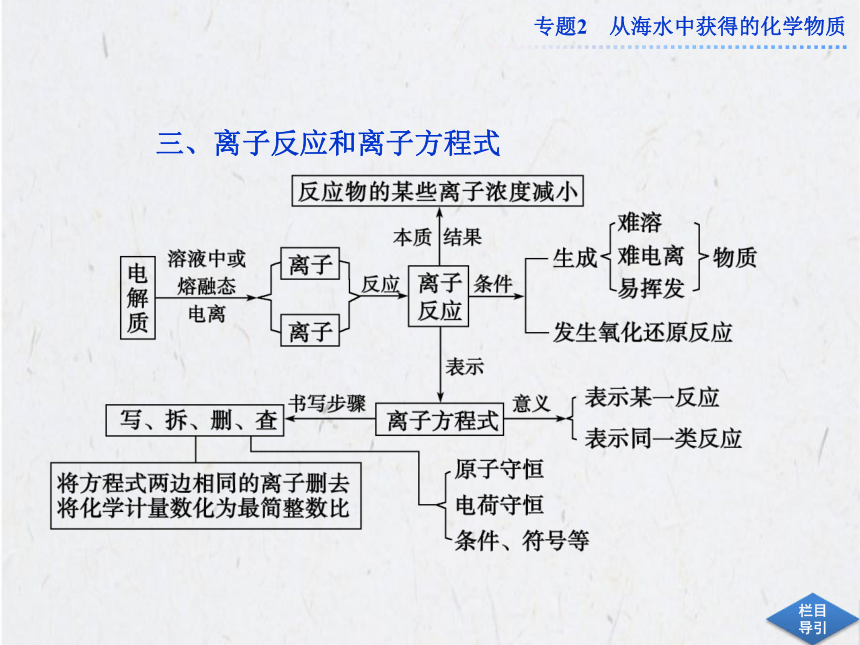
三、离子反应和离子方程式
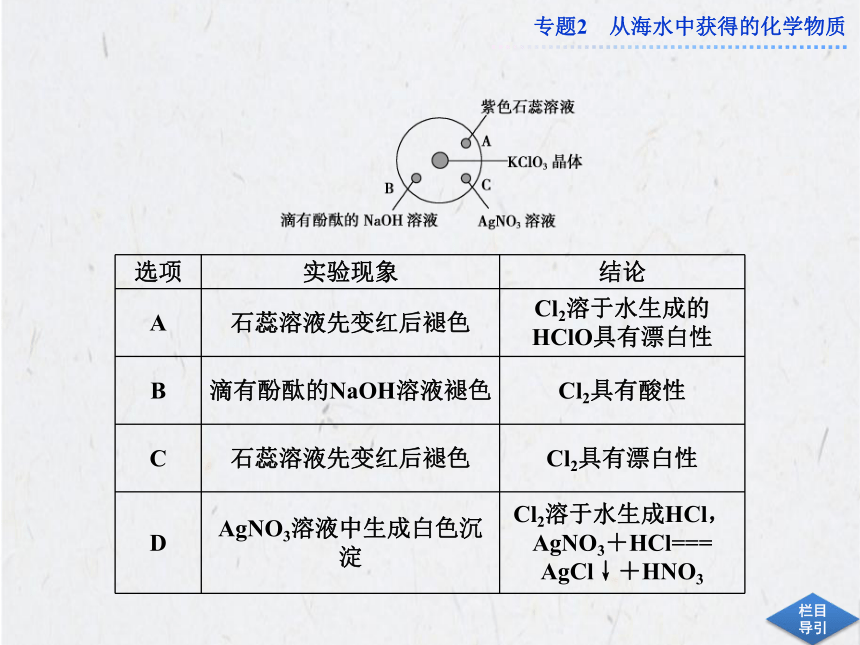
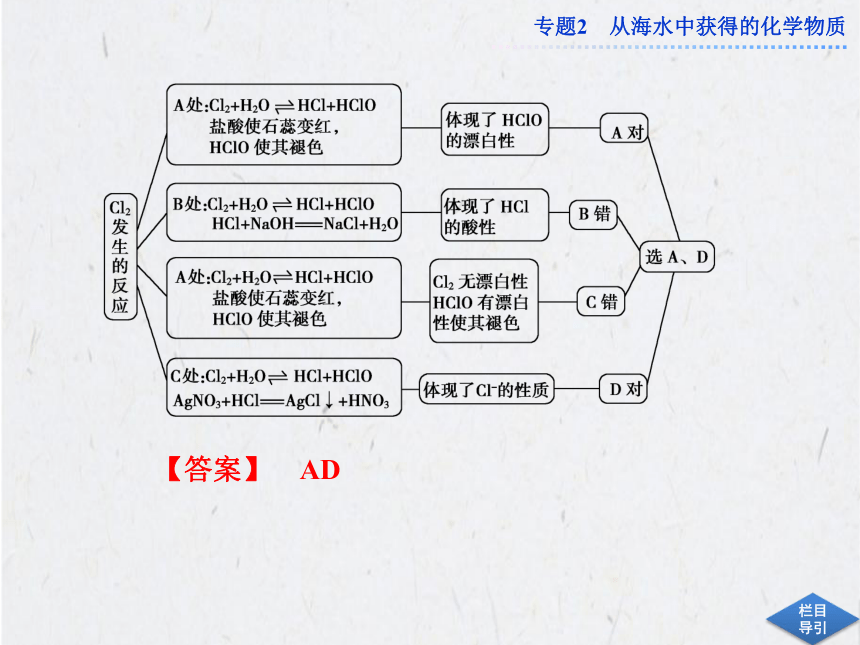
已知KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O。如下图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表实验现象和得出的结论都完全正确的是( )
【解析】 浓盐酸滴在KClO3晶体(即固体)上,会发生反应生成Cl2:KClO3+6HCl(浓)
===KCl+3H2O+3Cl2↑,生成的Cl2在培养皿和表面皿形成的气室中扩散,接触到
A、B、C三处的试剂,均发生反应。
【答案】 AD
巩固练习
1.向某无色溶液中通入一定量的氯气后,溶液变成橙黄色,再向溶液中滴加一定量的四氯化碳后,充分振荡,溶液分层,下层呈橙红色,则原溶液中一定含有的离子为( )
A.Cl- B.Br-
C.I- D.Fe2+
解析:选B。CCl4萃取Br2后在下层为橙红色.
a g镁在盛有b L(标准状况下)CO2和O2混合气体的密闭容器中燃烧。
(1)若反应容器中只有CO2剩余,则容器中的固体物质中一定含有________。
(2)若反应容器中有O2剩余,则容器中固体物质的质量为________g,
此时在b L CO2和O2的混合气体中氧气体积为V(O2),必须满足的条件是________。当容器中只有CO2剩余时,由反应①可知固体物质中一定没有Mg,一定有MgO,可能有C。当容器中有O2剩余时,肯定无Mg和C剩余,固体物质只有MgO。将反应①和③加和得反应②,设生成的MgO的质量为x,消耗的O2的物质的量为y。
巩固练习
2.将Na2CO3 、NaHCO3的混合物6.85 g充分加热后,固体的质量变为5.3 g,原混合物中NaHCO3的质量是________g。
解析:在加热前后,Na2CO3及其质量无变化,NaHCO3分解产生的CO2、H2O逸出而使固体的质量减小。因此,固体的质量由6.85 g变为5.3 g仅与NaHCO3有关。
答案:4.2
已知反应:
①2K2CrO4+H2SO4===K2Cr2O7+K2SO4+H2O
②Fe2(SO4)3+2HI===2FeSO4+I2+H2SO4
③□K2Cr2O7+□FeSO4+□H2SO4―→□Fe2(SO4)3+□Cr2(SO4)3+□K2SO4+□H2O
(1)上述三个反应中,属于氧化还原反应的是________(填序号);
(2)完成并配平反应③的化学方程式,标出电子转移的方向和数目;
(3)Fe2(SO4)3、K2Cr2O7、I2氧化性由强到弱的顺序为________________;
(4)若用K2Cr2O7与HI反应,每生成12.7 g I2,转移电子________个。
【解析】①中没有元素化合价的变化,所以是非氧化还原反应。氧化还原反应的配平是利用守恒原则,K2Cr2O7是氧化剂,其中Cr元素化合价由+6价降为+3价;FeSO4是还原剂,其中Fe元素化合价由+2价升为+3价,所以要满足氧化剂和还原剂的化合价升降总数相等,K2Cr2O7和FeSO4系数比是1∶6,然后利用其他各元素的原子守恒进行配平。根据强弱规律:氧化剂+还原剂―→还原产物+氧化产物,氧化性:氧化剂>氧化产物,得出氧化性:K2Cr2O7>Fe2(SO4)3>I2。碘元素的化合价由-1价升为0价,所以每生成1 mol I2即转移了2 mol 电子,因此每生成12.7 g I2 ,转移电子6.02×1022个。
【答案】 (1)②③
(2)1 6 7 3 1 1 7
(3)K2Cr2O7>Fe2(SO4)3>I2
(4)6.02×1022
【名师点睛】 对于氧化还原反应的配平、计算,通常是利用守恒原则解答:即化合价升降总数相等,包括氧化剂和还原剂之间、氧化产物和还原产物之间、氧化剂和氧化产物之间、还原剂和还原产物之间,具体由题目而定。
巩固练习
B.上述反应中,每生成1 mol AlN需转移3 mol电子
C.AlN中氮元素的化合价为+3
D.AlN的摩尔质量为41 g
离子反应在物质的检验鉴别、分离提纯、消除污染等方面有着广泛应用和重要意义。
(1)判断离子能否大量共存
离子能否大量共存即离子能否反应的问题。离子之间的反应类型很多,目前首先要掌握酸、碱、盐之间的复分解反应即离子互换反应能否发生,D.向次氯酸钙溶液中通入少量二氧化碳:
Ca2++2ClO-+CO2+H2O===2HClO+CaCO3↓
C项正确;少量二氧化碳与次氯酸钙溶液反应生成碳酸钙和次氯酸:Ca(ClO)2+CO2+H2O===CaCO3↓+2HClO,D项正确。
【答案】 A
巩固练习
C.锌与盐酸的反应:
Zn+2H++2Cl-===Zn2++2Cl-+H2↑
D.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:
Fe3++3H2O===Fe(OH)3↓+3H+
二、氧化还原反应
三、离子反应和离子方程式
已知KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O。如下图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表实验现象和得出的结论都完全正确的是( )
【解析】 浓盐酸滴在KClO3晶体(即固体)上,会发生反应生成Cl2:KClO3+6HCl(浓)
===KCl+3H2O+3Cl2↑,生成的Cl2在培养皿和表面皿形成的气室中扩散,接触到
A、B、C三处的试剂,均发生反应。
【答案】 AD
巩固练习
1.向某无色溶液中通入一定量的氯气后,溶液变成橙黄色,再向溶液中滴加一定量的四氯化碳后,充分振荡,溶液分层,下层呈橙红色,则原溶液中一定含有的离子为( )
A.Cl- B.Br-
C.I- D.Fe2+
解析:选B。CCl4萃取Br2后在下层为橙红色.
a g镁在盛有b L(标准状况下)CO2和O2混合气体的密闭容器中燃烧。
(1)若反应容器中只有CO2剩余,则容器中的固体物质中一定含有________。
(2)若反应容器中有O2剩余,则容器中固体物质的质量为________g,
此时在b L CO2和O2的混合气体中氧气体积为V(O2),必须满足的条件是________。当容器中只有CO2剩余时,由反应①可知固体物质中一定没有Mg,一定有MgO,可能有C。当容器中有O2剩余时,肯定无Mg和C剩余,固体物质只有MgO。将反应①和③加和得反应②,设生成的MgO的质量为x,消耗的O2的物质的量为y。
巩固练习
2.将Na2CO3 、NaHCO3的混合物6.85 g充分加热后,固体的质量变为5.3 g,原混合物中NaHCO3的质量是________g。
解析:在加热前后,Na2CO3及其质量无变化,NaHCO3分解产生的CO2、H2O逸出而使固体的质量减小。因此,固体的质量由6.85 g变为5.3 g仅与NaHCO3有关。
答案:4.2
已知反应:
①2K2CrO4+H2SO4===K2Cr2O7+K2SO4+H2O
②Fe2(SO4)3+2HI===2FeSO4+I2+H2SO4
③□K2Cr2O7+□FeSO4+□H2SO4―→□Fe2(SO4)3+□Cr2(SO4)3+□K2SO4+□H2O
(1)上述三个反应中,属于氧化还原反应的是________(填序号);
(2)完成并配平反应③的化学方程式,标出电子转移的方向和数目;
(3)Fe2(SO4)3、K2Cr2O7、I2氧化性由强到弱的顺序为________________;
(4)若用K2Cr2O7与HI反应,每生成12.7 g I2,转移电子________个。
【解析】①中没有元素化合价的变化,所以是非氧化还原反应。氧化还原反应的配平是利用守恒原则,K2Cr2O7是氧化剂,其中Cr元素化合价由+6价降为+3价;FeSO4是还原剂,其中Fe元素化合价由+2价升为+3价,所以要满足氧化剂和还原剂的化合价升降总数相等,K2Cr2O7和FeSO4系数比是1∶6,然后利用其他各元素的原子守恒进行配平。根据强弱规律:氧化剂+还原剂―→还原产物+氧化产物,氧化性:氧化剂>氧化产物,得出氧化性:K2Cr2O7>Fe2(SO4)3>I2。碘元素的化合价由-1价升为0价,所以每生成1 mol I2即转移了2 mol 电子,因此每生成12.7 g I2 ,转移电子6.02×1022个。
【答案】 (1)②③
(2)1 6 7 3 1 1 7
(3)K2Cr2O7>Fe2(SO4)3>I2
(4)6.02×1022
【名师点睛】 对于氧化还原反应的配平、计算,通常是利用守恒原则解答:即化合价升降总数相等,包括氧化剂和还原剂之间、氧化产物和还原产物之间、氧化剂和氧化产物之间、还原剂和还原产物之间,具体由题目而定。
巩固练习
B.上述反应中,每生成1 mol AlN需转移3 mol电子
C.AlN中氮元素的化合价为+3
D.AlN的摩尔质量为41 g
离子反应在物质的检验鉴别、分离提纯、消除污染等方面有着广泛应用和重要意义。
(1)判断离子能否大量共存
离子能否大量共存即离子能否反应的问题。离子之间的反应类型很多,目前首先要掌握酸、碱、盐之间的复分解反应即离子互换反应能否发生,D.向次氯酸钙溶液中通入少量二氧化碳:
Ca2++2ClO-+CO2+H2O===2HClO+CaCO3↓
C项正确;少量二氧化碳与次氯酸钙溶液反应生成碳酸钙和次氯酸:Ca(ClO)2+CO2+H2O===CaCO3↓+2HClO,D项正确。
【答案】 A
巩固练习
C.锌与盐酸的反应:
Zn+2H++2Cl-===Zn2++2Cl-+H2↑
D.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:
Fe3++3H2O===Fe(OH)3↓+3H+
