鲁科版高中化学选修5第2章第3节醛和酮 糖类 课件(共35张PPT)
文档属性
| 名称 | 鲁科版高中化学选修5第2章第3节醛和酮 糖类 课件(共35张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 552.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-03-01 00:00:00 | ||
图片预览









文档简介
课件35张PPT。第3节 醛和酮 糖类
第三节课堂互动讲练知能优化训练课前自主学案学习目标探究整合应用1.了解醛、酮在自然界的存在,能列举几种常见醛、酮并写出其结构式。
2.能根据醛、酮的结构特点推测其分子发生反应的部位及反应类型。
3.掌握醛、酮的加成反应。
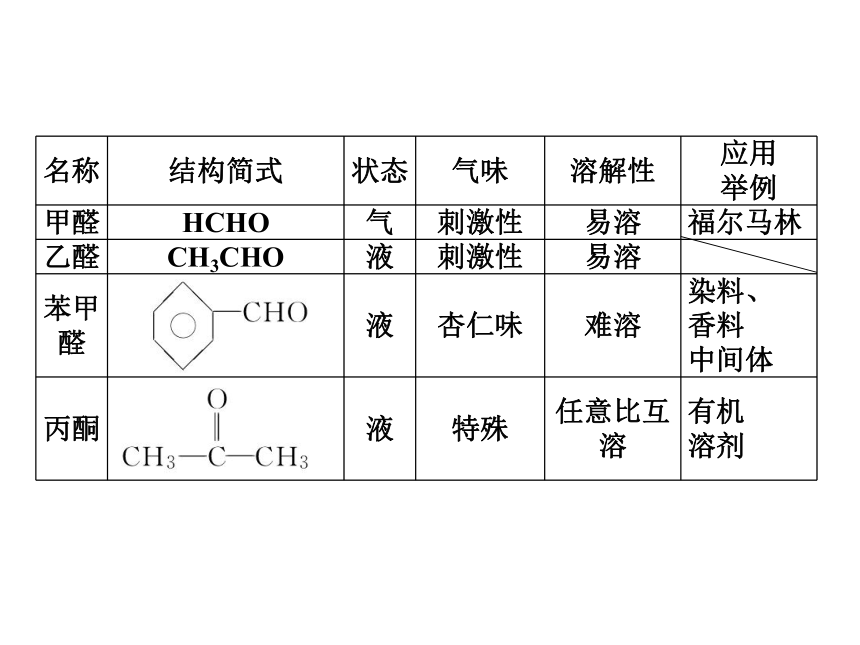
4.正确判断醛、酮的氧化反应和还原反应。课前自主学案一、常见的醛、酮
1.醛和酮
(1)概念
①醛:______碳原子( )分别与___原子和_____
(或___原子)相连的化合物。
②酮:_____与两个_____相连的化合物。
(2)饱和一元脂肪醛、酮的通式为:________,分子中碳原子数相同的饱和一元脂肪醛和饱和一元脂肪酮互为_____________。
2.常见的醛、酮羰基氢烃基氢羰基烃基CnH2nO同分异构体思考感悟
1.醛基的结构式为 ,书写结构简式时应注意什么?
【提示】 醛基是羰基与氢原子相连,在写其结构简式时要突出羰基与氢原子的关系,可以写成—CHO,但不能写成—COH或CHO—。二、醛、酮的化学性质
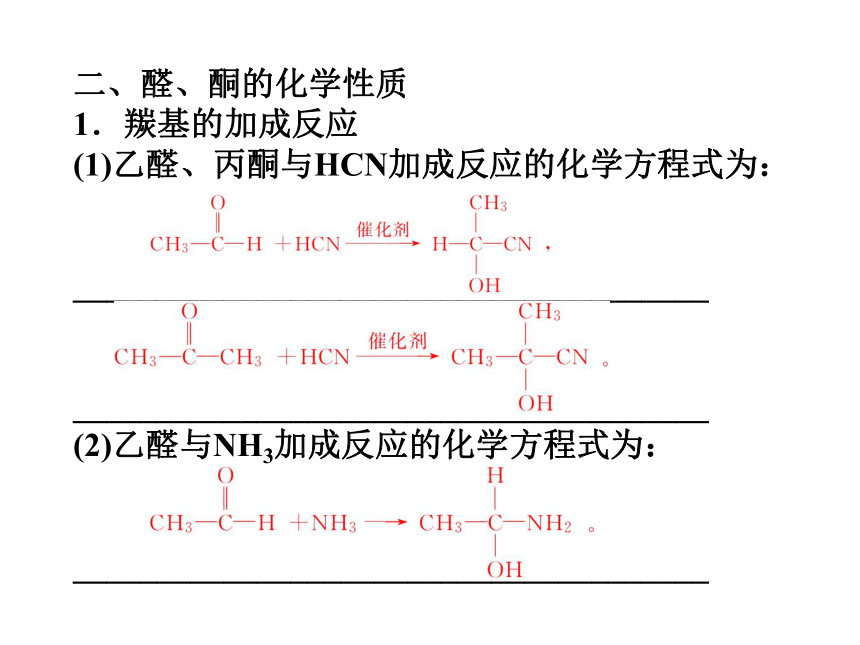
1.羰基的加成反应
(1)乙醛、丙酮与HCN加成反应的化学方程式为:
______________________________________
______________________________________
(2)乙醛与NH3加成反应的化学方程式为:
______________________________________2.氧化反应和还原反应
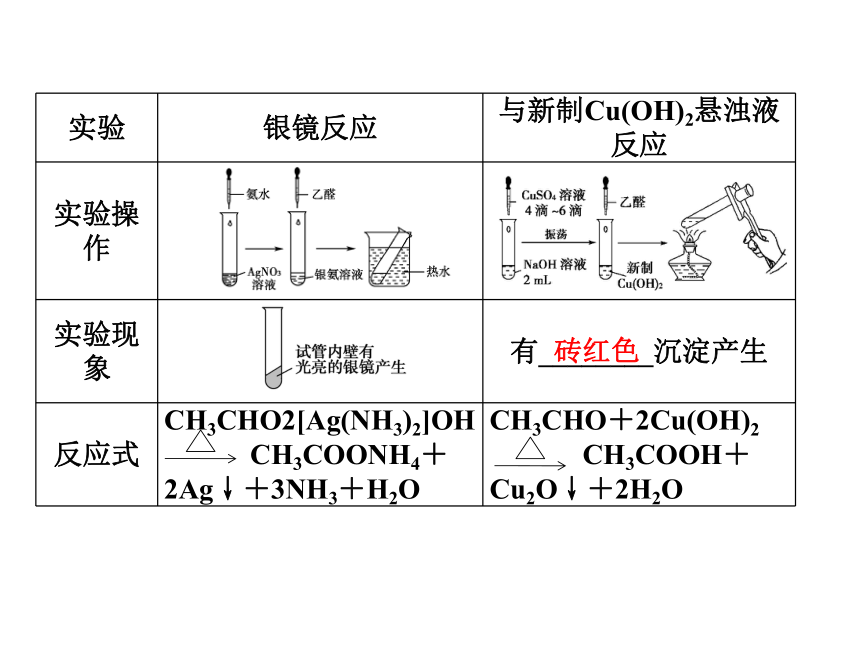
(1)氧化反应
①醛能被O2催化氧化,也能被弱氧化剂
_____________________________氧化。
②酮对一般的氧化剂比较稳定,一般也不会被O2氧化,它只能被很强的氧化剂氧化,氧化时碳碳单键断裂。银氨溶液、新制氢氧化铜悬浊液砖红色羰基醇思考感悟
2.(1)乙醛能使酸性KMnO4溶液或溴水退色吗?为什么?
(2)如何鉴别醛和酮?
【提示】 (1)能。银氨溶液、新制Cu(OH)2悬浊液的氧化性是很弱的,乙醛能被弱氧化剂氧化,原因是乙醛具有较强的还原性。由此推知,乙醛也易被酸性KMnO4溶液中的KMnO4、溴水中的Br2等强氧化剂氧化,KMnO4、Br2被还原而使溶液退色。
(2)醛能发生银镜反应,也能被新制Cu(OH)2悬浊液氧化,而酮不具有上述性质,因此可用银氨溶液或新制Cu(OH)2悬浊液来鉴别醛和酮。解析:选B。由醛的定义知羰基碳两端必须连有氢原子和烃基(氢原子)知,B不为醛。2.下列物质可用于杀菌消毒的是( )
①苯酚 ②次氯酸 ③福尔马林 ④双氧水
A.只有①③ B.只有②④
C.只有①②④ D.全部
解析:选D。苯酚可制“来苏水”、药皂等用来杀菌消毒;次氯酸、双氧水具有强氧化性,可用于杀菌消毒;35%~45%的甲醛水溶液即为福尔马林,用于杀菌防腐。3.(2011年烟台高二检测)下列有关银镜反应的说法中正确的是( )
A.配制银氨溶液时氨水必须过量
B.1 mol甲醛发生银镜反应最多生成2 mol Ag
C.银镜反应通常采用水浴加热
D.银镜反应后的试管一般用浓硝酸洗涤
解析:选C。银氨溶液必须随配随用,不可久置,否则会生成易爆物质——Ag3N。在配制过程中滴加氨水使产生的沉淀恰好溶解,要防止氨水过量。1 mol甲醛发生银镜反应最多可以生成4 mol Ag。生成的银镜用少量稀硝酸洗去,再用水洗净,通常不用浓硝酸。课堂互动讲练银镜反应和与新制Cu(OH)2悬浊液的反应是检验醛基和鉴别醛基与酮羰基的方法。
实验时必须注意以下几点:
1.银镜反应
(1)试管必须洁净。试管先用热的烧碱溶液洗涤,再用蒸馏水洗涤;
(2)银氨溶液应现用现配,不可久置;
(3)银氨溶液的配制,是向AgNO3溶液中滴加稀氨水,直到生成的沉淀恰好完全溶解为止。氨水不能过量,因为氨水过量或浓度过大,根据化学平衡原理[Ag(NH3)2]+??Ag++2NH3,电离出的Ag+浓度降低,不利于银镜的生成,而且易产生易爆物;
(4)实验必须在水浴中进行,温度控制在60 ℃~70 ℃,不能直接加热煮沸;
(5)试管加热过程中,不可振荡;
(6)当银镜生成后,试管内的液体应及时处理,不可久置,试管用稀硝酸洗涤。
2.与新制Cu(OH)2悬浊液的反应
(1)所用Cu(OH)2必须是新制的,在制备Cu(OH)2时,NaOH溶液必须明显过量;
(2)加热时须将混合溶液加热至沸腾,才有明显的砖红色沉淀产生;
(3)加热煮沸时间不能过久,过久将出现黑色沉淀,原因是Cu(OH)2受热分解为CuO。
特别提醒:1.只要有机物的分子中含有 ,就能发生银镜反应,就能被新制的Cu(OH)2悬浊液氧化。
2.乙醛被银氨溶液氧化,产物写成羧酸铵,被新制Cu(OH)2悬浊液氧化,产物写成羧酸。 柠檬醛的结构简式为:请设计实验证明柠檬醛的分子结构中含有醛基和碳碳双键:
(1)检验柠檬醛分子结构中含有醛基的方法是________________________________________,
有关反应的化学方程式为________________________________________________________________________。(2)检验柠檬醛分子结构中含有碳碳双键的方法是____________________________________________
__________________________________________,
有关反应的化学方程式为______________________________________________________________________________________。
【解析】 检验醛基用银氨溶液或新制Cu(OH)2悬浊液作检验试剂;检验碳碳双键用溴水或高锰酸钾酸性溶液,但因醛基有较强的还原性,会使高锰酸钾酸性溶液和溴水退色,故检验碳碳双键之前需先将醛基氧化。【答案】 (1)取少量柠檬醛加入到新制银氨溶液中,水浴加热,有银镜出现,证明柠檬醛分子结构中含有醛基[用新制Cu(OH)2悬浊液检测也可]
(2)取上层溶液少许,用稀硫酸酸化,再加到溴水中,溴水退色,证明柠檬醛分子结构中含有碳碳双键【规律方法】 检验碳碳双键可以用溴水或KMnO4酸性溶液;检验醛基用银氨溶液或新制Cu(OH)2悬浊液。但由于醛基也能使溴水和KMnO4酸性溶液退色,对碳碳双键的检验造成了干扰,因此,能否排除干扰是解答此类问题正误的关键。只有将醛基全部氧化成羧基后,才能检验出碳碳双键的存在。解析:选A。因为一般情况下1 mol一元醛通常可以还原得到2 mol Ag,现得到0.4 mol Ag,故醛为0.2 mol,该醛的摩尔质量为3 g/0.2 mol=15 g·mol-1,此题似乎无解。但1 mol甲醛可以得到4 mol Ag,即3 g甲醛可得到43.2 g(0.4 mol)Ag,符合题意。注:“√”代表“能”,“×”代表“不能”。
特别提醒:1.醛能使溴水退色,并不是加成反应所致,反应实质是Br2氧化醛类物质,而自身因被还原而使溶液退色。
2.直馏汽油、苯、CCl4、己烷等分别与溴水混合,则能通过萃取作用使溴水中的溴进入非极性有机溶剂而使溴水退色,但属于物理变化。 为了鉴别己烯、甲苯和乙醛这三种无色液体,可以使用下列哪组试剂( )
A.新制Cu(OH)2悬浊液和溴水
B.酸性KMnO4溶液和溴水
C.银氨溶液和酸性KMnO4溶液
D.FeCl3溶液和银氨溶液
【思路点拨】【解析】 先加入新制的Cu(OH)2悬浊液,鉴别出乙醛;再加入溴水,鉴别出己烯(溴水退色)和甲苯[溴水退色但分层,且有机层(上层)显红棕色]。
【答案】 A 茉莉醛具有浓郁的茉莉花香,其结构简式如下所示:
关于茉莉醛的下列叙述错误的是( )
A.在加热和催化剂作用下,能被氢气还原
B.能被酸性高锰酸钾溶液氧化
C.在一定条件下能与溴发生取代反应
D.不能与氢溴酸发生加成反应解析:选D。茉莉醛中含有—CHO、苯环和
三种官能团,含有—CH2(CH2)3CH3烃基,因此能发生取代、还原、氧化、加成反应,与氢溴酸在一定条件下可发生加成反应。探究整合应用银镜反应实验探究
【举例】 用如图所示装置进行实验,将A逐渐滴入B中:(1)①若B是生石灰,实验中观察到C溶液先形成沉淀,然后沉淀溶解,当溶液恰好澄清时,关闭E,然后往烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜,则A是________,C是________与乙醛的混合液(均写化学式)。写出装置Ⅱ中反应的离子方程式:___________________________________________。
②仪器D在此实验中的作用是___________________________________________。
(2)已知在75 ℃左右,用HgSO4做催化剂,乙炔可水化为乙醛,但HgSO4遇到某些特定物质常会发生催化剂中毒而失去催化作用,H2S就是其中一种。现用乙炔水化法,只用块状电石、浓硫酸、水、NaOH溶液、HgO粉末5种物质制乙醛,并且装置Ⅱ进行银镜反应。请回答下列问题:
①若B为电石,则A是_____________________。
②在装置Ⅰ和Ⅱ间添加装置Ⅲ(内装氧化汞、水和浓硫酸制备乙醛)的同时还应添加装置Ⅳ,请画出Ⅳ的装置图并指出所装的药品和Ⅳ所处的位置______________。
③装置Ⅲ中对F加热的方法叫________,所选用温度计G的量程表示正确的是________(填代号)。
A.0 ℃~50 ℃ B.0 ℃~100 ℃
C.0 ℃~200 ℃ D.50 ℃~100 ℃ E.0 ℃~360 ℃
④此时,装置Ⅱ中除烧杯中加入热水外,C的溶质是________(填名称)。(2)
①此时装置Ⅰ为制乙炔装置,
A中所盛为水。②装置Ⅳ的作
用为除去由Ⅰ装置导出的气流
中混有的H2S杂质,以防止催
化剂中毒,故而应添加一个洗气装置Ⅳ(内盛NaOH溶液),位置处在装置Ⅲ之前。如图所示。
第三节课堂互动讲练知能优化训练课前自主学案学习目标探究整合应用1.了解醛、酮在自然界的存在,能列举几种常见醛、酮并写出其结构式。
2.能根据醛、酮的结构特点推测其分子发生反应的部位及反应类型。
3.掌握醛、酮的加成反应。
4.正确判断醛、酮的氧化反应和还原反应。课前自主学案一、常见的醛、酮
1.醛和酮
(1)概念
①醛:______碳原子( )分别与___原子和_____
(或___原子)相连的化合物。
②酮:_____与两个_____相连的化合物。
(2)饱和一元脂肪醛、酮的通式为:________,分子中碳原子数相同的饱和一元脂肪醛和饱和一元脂肪酮互为_____________。
2.常见的醛、酮羰基氢烃基氢羰基烃基CnH2nO同分异构体思考感悟
1.醛基的结构式为 ,书写结构简式时应注意什么?
【提示】 醛基是羰基与氢原子相连,在写其结构简式时要突出羰基与氢原子的关系,可以写成—CHO,但不能写成—COH或CHO—。二、醛、酮的化学性质
1.羰基的加成反应
(1)乙醛、丙酮与HCN加成反应的化学方程式为:
______________________________________
______________________________________
(2)乙醛与NH3加成反应的化学方程式为:
______________________________________2.氧化反应和还原反应
(1)氧化反应
①醛能被O2催化氧化,也能被弱氧化剂
_____________________________氧化。
②酮对一般的氧化剂比较稳定,一般也不会被O2氧化,它只能被很强的氧化剂氧化,氧化时碳碳单键断裂。银氨溶液、新制氢氧化铜悬浊液砖红色羰基醇思考感悟
2.(1)乙醛能使酸性KMnO4溶液或溴水退色吗?为什么?
(2)如何鉴别醛和酮?
【提示】 (1)能。银氨溶液、新制Cu(OH)2悬浊液的氧化性是很弱的,乙醛能被弱氧化剂氧化,原因是乙醛具有较强的还原性。由此推知,乙醛也易被酸性KMnO4溶液中的KMnO4、溴水中的Br2等强氧化剂氧化,KMnO4、Br2被还原而使溶液退色。
(2)醛能发生银镜反应,也能被新制Cu(OH)2悬浊液氧化,而酮不具有上述性质,因此可用银氨溶液或新制Cu(OH)2悬浊液来鉴别醛和酮。解析:选B。由醛的定义知羰基碳两端必须连有氢原子和烃基(氢原子)知,B不为醛。2.下列物质可用于杀菌消毒的是( )
①苯酚 ②次氯酸 ③福尔马林 ④双氧水
A.只有①③ B.只有②④
C.只有①②④ D.全部
解析:选D。苯酚可制“来苏水”、药皂等用来杀菌消毒;次氯酸、双氧水具有强氧化性,可用于杀菌消毒;35%~45%的甲醛水溶液即为福尔马林,用于杀菌防腐。3.(2011年烟台高二检测)下列有关银镜反应的说法中正确的是( )
A.配制银氨溶液时氨水必须过量
B.1 mol甲醛发生银镜反应最多生成2 mol Ag
C.银镜反应通常采用水浴加热
D.银镜反应后的试管一般用浓硝酸洗涤
解析:选C。银氨溶液必须随配随用,不可久置,否则会生成易爆物质——Ag3N。在配制过程中滴加氨水使产生的沉淀恰好溶解,要防止氨水过量。1 mol甲醛发生银镜反应最多可以生成4 mol Ag。生成的银镜用少量稀硝酸洗去,再用水洗净,通常不用浓硝酸。课堂互动讲练银镜反应和与新制Cu(OH)2悬浊液的反应是检验醛基和鉴别醛基与酮羰基的方法。
实验时必须注意以下几点:
1.银镜反应
(1)试管必须洁净。试管先用热的烧碱溶液洗涤,再用蒸馏水洗涤;
(2)银氨溶液应现用现配,不可久置;
(3)银氨溶液的配制,是向AgNO3溶液中滴加稀氨水,直到生成的沉淀恰好完全溶解为止。氨水不能过量,因为氨水过量或浓度过大,根据化学平衡原理[Ag(NH3)2]+??Ag++2NH3,电离出的Ag+浓度降低,不利于银镜的生成,而且易产生易爆物;
(4)实验必须在水浴中进行,温度控制在60 ℃~70 ℃,不能直接加热煮沸;
(5)试管加热过程中,不可振荡;
(6)当银镜生成后,试管内的液体应及时处理,不可久置,试管用稀硝酸洗涤。
2.与新制Cu(OH)2悬浊液的反应
(1)所用Cu(OH)2必须是新制的,在制备Cu(OH)2时,NaOH溶液必须明显过量;
(2)加热时须将混合溶液加热至沸腾,才有明显的砖红色沉淀产生;
(3)加热煮沸时间不能过久,过久将出现黑色沉淀,原因是Cu(OH)2受热分解为CuO。
特别提醒:1.只要有机物的分子中含有 ,就能发生银镜反应,就能被新制的Cu(OH)2悬浊液氧化。
2.乙醛被银氨溶液氧化,产物写成羧酸铵,被新制Cu(OH)2悬浊液氧化,产物写成羧酸。 柠檬醛的结构简式为:请设计实验证明柠檬醛的分子结构中含有醛基和碳碳双键:
(1)检验柠檬醛分子结构中含有醛基的方法是________________________________________,
有关反应的化学方程式为________________________________________________________________________。(2)检验柠檬醛分子结构中含有碳碳双键的方法是____________________________________________
__________________________________________,
有关反应的化学方程式为______________________________________________________________________________________。
【解析】 检验醛基用银氨溶液或新制Cu(OH)2悬浊液作检验试剂;检验碳碳双键用溴水或高锰酸钾酸性溶液,但因醛基有较强的还原性,会使高锰酸钾酸性溶液和溴水退色,故检验碳碳双键之前需先将醛基氧化。【答案】 (1)取少量柠檬醛加入到新制银氨溶液中,水浴加热,有银镜出现,证明柠檬醛分子结构中含有醛基[用新制Cu(OH)2悬浊液检测也可]
(2)取上层溶液少许,用稀硫酸酸化,再加到溴水中,溴水退色,证明柠檬醛分子结构中含有碳碳双键【规律方法】 检验碳碳双键可以用溴水或KMnO4酸性溶液;检验醛基用银氨溶液或新制Cu(OH)2悬浊液。但由于醛基也能使溴水和KMnO4酸性溶液退色,对碳碳双键的检验造成了干扰,因此,能否排除干扰是解答此类问题正误的关键。只有将醛基全部氧化成羧基后,才能检验出碳碳双键的存在。解析:选A。因为一般情况下1 mol一元醛通常可以还原得到2 mol Ag,现得到0.4 mol Ag,故醛为0.2 mol,该醛的摩尔质量为3 g/0.2 mol=15 g·mol-1,此题似乎无解。但1 mol甲醛可以得到4 mol Ag,即3 g甲醛可得到43.2 g(0.4 mol)Ag,符合题意。注:“√”代表“能”,“×”代表“不能”。
特别提醒:1.醛能使溴水退色,并不是加成反应所致,反应实质是Br2氧化醛类物质,而自身因被还原而使溶液退色。
2.直馏汽油、苯、CCl4、己烷等分别与溴水混合,则能通过萃取作用使溴水中的溴进入非极性有机溶剂而使溴水退色,但属于物理变化。 为了鉴别己烯、甲苯和乙醛这三种无色液体,可以使用下列哪组试剂( )
A.新制Cu(OH)2悬浊液和溴水
B.酸性KMnO4溶液和溴水
C.银氨溶液和酸性KMnO4溶液
D.FeCl3溶液和银氨溶液
【思路点拨】【解析】 先加入新制的Cu(OH)2悬浊液,鉴别出乙醛;再加入溴水,鉴别出己烯(溴水退色)和甲苯[溴水退色但分层,且有机层(上层)显红棕色]。
【答案】 A 茉莉醛具有浓郁的茉莉花香,其结构简式如下所示:
关于茉莉醛的下列叙述错误的是( )
A.在加热和催化剂作用下,能被氢气还原
B.能被酸性高锰酸钾溶液氧化
C.在一定条件下能与溴发生取代反应
D.不能与氢溴酸发生加成反应解析:选D。茉莉醛中含有—CHO、苯环和
三种官能团,含有—CH2(CH2)3CH3烃基,因此能发生取代、还原、氧化、加成反应,与氢溴酸在一定条件下可发生加成反应。探究整合应用银镜反应实验探究
【举例】 用如图所示装置进行实验,将A逐渐滴入B中:(1)①若B是生石灰,实验中观察到C溶液先形成沉淀,然后沉淀溶解,当溶液恰好澄清时,关闭E,然后往烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜,则A是________,C是________与乙醛的混合液(均写化学式)。写出装置Ⅱ中反应的离子方程式:___________________________________________。
②仪器D在此实验中的作用是___________________________________________。
(2)已知在75 ℃左右,用HgSO4做催化剂,乙炔可水化为乙醛,但HgSO4遇到某些特定物质常会发生催化剂中毒而失去催化作用,H2S就是其中一种。现用乙炔水化法,只用块状电石、浓硫酸、水、NaOH溶液、HgO粉末5种物质制乙醛,并且装置Ⅱ进行银镜反应。请回答下列问题:
①若B为电石,则A是_____________________。
②在装置Ⅰ和Ⅱ间添加装置Ⅲ(内装氧化汞、水和浓硫酸制备乙醛)的同时还应添加装置Ⅳ,请画出Ⅳ的装置图并指出所装的药品和Ⅳ所处的位置______________。
③装置Ⅲ中对F加热的方法叫________,所选用温度计G的量程表示正确的是________(填代号)。
A.0 ℃~50 ℃ B.0 ℃~100 ℃
C.0 ℃~200 ℃ D.50 ℃~100 ℃ E.0 ℃~360 ℃
④此时,装置Ⅱ中除烧杯中加入热水外,C的溶质是________(填名称)。(2)
①此时装置Ⅰ为制乙炔装置,
A中所盛为水。②装置Ⅳ的作
用为除去由Ⅰ装置导出的气流
中混有的H2S杂质,以防止催
化剂中毒,故而应添加一个洗气装置Ⅳ(内盛NaOH溶液),位置处在装置Ⅲ之前。如图所示。
