2.2 课时3 反应条件对化学平衡的影响 课件 (共18张PPT)2024-2025学年高二化学鲁科版(2019)选择性必修1
文档属性
| 名称 | 2.2 课时3 反应条件对化学平衡的影响 课件 (共18张PPT)2024-2025学年高二化学鲁科版(2019)选择性必修1 |

|
|
| 格式 | pptx | ||
| 文件大小 | 32.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-24 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
反应条件对化学平衡的影响
第2章 化学反应的方向、限度与速率
了解温度、浓度等因素对化学平衡的影响,并能判断平衡移动的方向。
在工业生产中,人们会遇到各种各样的可逆反应,如合成氨的反应:
N2(g)+3H2(g) 2NH3(g)
高温、高压
催化剂
该反应在一定条件下已经达到平衡状态,但是产率不够理想,改变外界条件是否可以改变它的平衡状态呢?
温度、浓度、压强
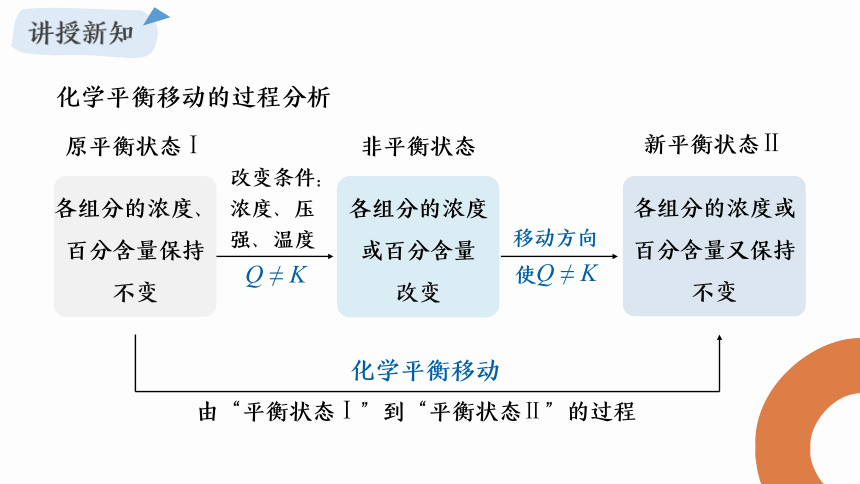
化学平衡移动的过程分析
原平衡状态Ⅰ
各组分的浓度、百分含量保持
不变
改变条件:浓度、压强、温度
非平衡状态
各组分的浓度或百分含量
改变
Q ≠ K
移动方向
使Q ≠ K
新平衡状态Ⅱ
各组分的浓度或百分含量又保持
不变
化学平衡移动
由“平衡状态Ⅰ”到“平衡状态Ⅱ”的过程
条件改变
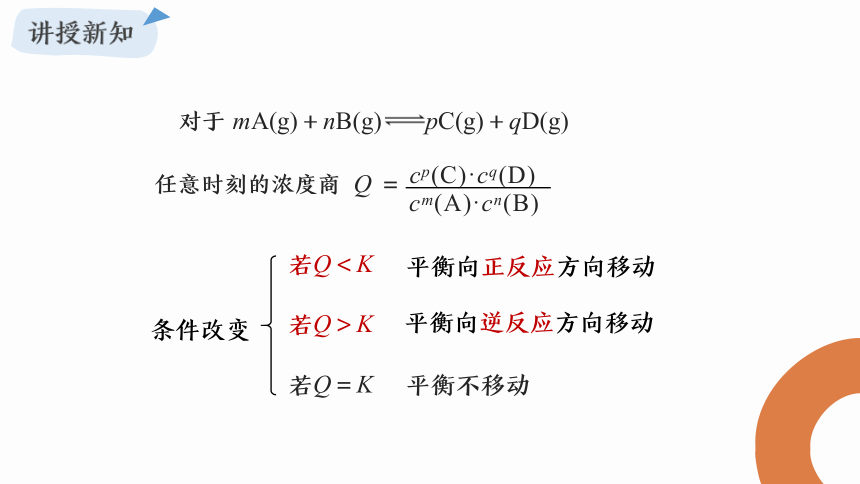
若Q<K
若Q>K
若Q=K
mA(g)+nB(g) pC(g)+qD(g)
任意时刻的浓度商
Q =
cp(C)·cq(D)
cm(A)·cn(B)
平衡向正反应方向移动
平衡向逆反应方向移动
平衡不移动
对于
红棕色
无色
2NO2 (g) N2O4(g)
ΔH < 0
一、温度对化学平衡的影响
二氧化氮平衡球
T / K K /(mol-1·L)
333 0.601
298 6.80
根据信息,预测温度改变对化学平衡移动有怎样的影响。
平衡状态Ⅰ(Q1=K1)
298K
平衡状态Ⅱ(Q2=K2)
333K
Q1 >
K2
333K
【实验现象】
浸到冰水中时混合物颜色_____,
浸到热水中时混合物颜色_____。
变浅
变深
平衡正向移动
平衡逆向移动
降低温度
颜色变浅
升高温度
颜色变深
视频
小结:温度对化学平衡的影响是通过改变化学平衡常数实现的!
归纳:温度对化学平衡的影响
a A(g)+b B(g) c C(g)+d D(g)
升高温度,平衡向吸热方向移动
降低温度,平衡向放热方向移动
反应焓变 温度变化 平衡常数K 移动方向
ΔH < 0 (放热反应) 升高 变小
降低 变大
ΔH >0 (吸热反应) 升高 变大
降低 变小
吸热方向(逆向)
放热方向(正向)
吸热方向(正向)
放热方向(逆向)
二、浓度对化学平衡的影响
a A(g)+b B(g) c C(g)+d D(g)
a
c (A) c (B)
Q =
c
c (C) c (D)
d
b
= K
一定条件下,对任意可逆反应:
增大反应物浓度,或减小反应产物浓度
减小反应物浓度,或增大反应产物浓度
Q <
K
平衡正向移动
Q >
K
平衡逆向移动
Q和K的相对大小与平衡移动的关系图
Q
Q
Q
K
K
K
QQ=K
Q>K
平衡正移
平衡逆移
增大反应物浓度
减小反应产物浓度
减小反应物浓度
增大反应产物浓度
三、压强对化学平衡的影响
N2(g)+3H2(g) 2NH3(g)
高温、高压
催化剂
ΔH<0
如果压缩体积增大压强,K、Q如何变化?平衡如何移动?
Q=
c2 (NH3)
c(N2) c3 (H2)
K=
c 2 (NH3)
c (N2) c 3 (H2)
平
平
平
K不变, Q变?
各物质浓度同等程度增大
压缩体积
压强增大
Q<K
平衡正向移动
若是针对气体减小的反应呢?
归纳:压强对化学平衡的影响
1)对于Δvg≠0的反应:增大压强,化学平衡向气体分子数减小的方向移动;减小压强,化学平衡向气体分子数增大的方向移动。
2)对于Δvg=0的反应:压强改变,平衡不移动。
注:对于只涉及固体或液体的反应,压强对平衡体系的影响极其微弱,可以不予考虑。
四、勒·夏特列原理——平衡移动原理
“如果改变影响平衡的条件之一(如温度、压强、以及参加反应的化学物质的浓度),平衡向着能够减弱这种改变的方向移动。”
勒 夏特列
(1)对于C(s)+CO2(g)??2CO(g),在某温度下达到平衡,缩小容器的体积,平衡不移动( )
(2)有气体参与的反应,改变压强,平衡一定发生移动( )
(3)增大压强可使2SO2(g)+O2(g) 2SO3(g)平衡向正向移动,原因是增大压强,v正增大,v逆减小( )
(4)恒容容器中充入He,可使N2(g)+3H2(g)??2NH3(g)平衡向正向移动( )
1.判断下列叙述的正误
2.在密闭容器中,反应:xA(g)+yB(g)??zC(g),在一定条件下达到平衡状态,保持温度不变,改变下列条件,分析解答下列问题:
(1)若x+y>z,缩小体积,增大压强,则平衡向________方向移动。
(2)若保持体积不变,通入He气,则平衡________移动。
(3)若保持压强不变,通入He气,平衡向正反应方向移动,则x、y、z的关系为________。
(4)若x+y=z,恒容条件下充入He气,则平衡________移动。
正反应
不
x+y<z
不
惰性气体对化学平衡的影响
(1)恒温、恒容条件
原平衡体系
惰性气体
体系中各组
分浓度不变
Q = K
平衡不移动
(2)恒温、恒压条件
原平衡体系
平衡体系容
器容积增大
惰性气体
各组分浓度
同比例减小
减压
反应
条件
对化
学平
衡的
影响
温度
浓度
压强
升高温度,平衡向吸热方向移动
降低温度,平衡向放热方向移动
改变浓度,若Q < K,平衡正向移动
改变浓度,若Q > K,平衡逆向移动
改变压强,若Q < K,平衡正向移动
改变压强,若Q > K,平衡逆向移动
勒·夏特列原理
反应条件对化学平衡的影响
第2章 化学反应的方向、限度与速率
了解温度、浓度等因素对化学平衡的影响,并能判断平衡移动的方向。
在工业生产中,人们会遇到各种各样的可逆反应,如合成氨的反应:
N2(g)+3H2(g) 2NH3(g)
高温、高压
催化剂
该反应在一定条件下已经达到平衡状态,但是产率不够理想,改变外界条件是否可以改变它的平衡状态呢?
温度、浓度、压强
化学平衡移动的过程分析
原平衡状态Ⅰ
各组分的浓度、百分含量保持
不变
改变条件:浓度、压强、温度
非平衡状态
各组分的浓度或百分含量
改变
Q ≠ K
移动方向
使Q ≠ K
新平衡状态Ⅱ
各组分的浓度或百分含量又保持
不变
化学平衡移动
由“平衡状态Ⅰ”到“平衡状态Ⅱ”的过程
条件改变
若Q<K
若Q>K
若Q=K
mA(g)+nB(g) pC(g)+qD(g)
任意时刻的浓度商
Q =
cp(C)·cq(D)
cm(A)·cn(B)
平衡向正反应方向移动
平衡向逆反应方向移动
平衡不移动
对于
红棕色
无色
2NO2 (g) N2O4(g)
ΔH < 0
一、温度对化学平衡的影响
二氧化氮平衡球
T / K K /(mol-1·L)
333 0.601
298 6.80
根据信息,预测温度改变对化学平衡移动有怎样的影响。
平衡状态Ⅰ(Q1=K1)
298K
平衡状态Ⅱ(Q2=K2)
333K
Q1 >
K2
333K
【实验现象】
浸到冰水中时混合物颜色_____,
浸到热水中时混合物颜色_____。
变浅
变深
平衡正向移动
平衡逆向移动
降低温度
颜色变浅
升高温度
颜色变深
视频
小结:温度对化学平衡的影响是通过改变化学平衡常数实现的!
归纳:温度对化学平衡的影响
a A(g)+b B(g) c C(g)+d D(g)
升高温度,平衡向吸热方向移动
降低温度,平衡向放热方向移动
反应焓变 温度变化 平衡常数K 移动方向
ΔH < 0 (放热反应) 升高 变小
降低 变大
ΔH >0 (吸热反应) 升高 变大
降低 变小
吸热方向(逆向)
放热方向(正向)
吸热方向(正向)
放热方向(逆向)
二、浓度对化学平衡的影响
a A(g)+b B(g) c C(g)+d D(g)
a
c (A) c (B)
Q =
c
c (C) c (D)
d
b
= K
一定条件下,对任意可逆反应:
增大反应物浓度,或减小反应产物浓度
减小反应物浓度,或增大反应产物浓度
Q <
K
平衡正向移动
Q >
K
平衡逆向移动
Q和K的相对大小与平衡移动的关系图
Q
Q
Q
K
K
K
Q
Q>K
平衡正移
平衡逆移
增大反应物浓度
减小反应产物浓度
减小反应物浓度
增大反应产物浓度
三、压强对化学平衡的影响
N2(g)+3H2(g) 2NH3(g)
高温、高压
催化剂
ΔH<0
如果压缩体积增大压强,K、Q如何变化?平衡如何移动?
Q=
c2 (NH3)
c(N2) c3 (H2)
K=
c 2 (NH3)
c (N2) c 3 (H2)
平
平
平
K不变, Q变?
各物质浓度同等程度增大
压缩体积
压强增大
Q<K
平衡正向移动
若是针对气体减小的反应呢?
归纳:压强对化学平衡的影响
1)对于Δvg≠0的反应:增大压强,化学平衡向气体分子数减小的方向移动;减小压强,化学平衡向气体分子数增大的方向移动。
2)对于Δvg=0的反应:压强改变,平衡不移动。
注:对于只涉及固体或液体的反应,压强对平衡体系的影响极其微弱,可以不予考虑。
四、勒·夏特列原理——平衡移动原理
“如果改变影响平衡的条件之一(如温度、压强、以及参加反应的化学物质的浓度),平衡向着能够减弱这种改变的方向移动。”
勒 夏特列
(1)对于C(s)+CO2(g)??2CO(g),在某温度下达到平衡,缩小容器的体积,平衡不移动( )
(2)有气体参与的反应,改变压强,平衡一定发生移动( )
(3)增大压强可使2SO2(g)+O2(g) 2SO3(g)平衡向正向移动,原因是增大压强,v正增大,v逆减小( )
(4)恒容容器中充入He,可使N2(g)+3H2(g)??2NH3(g)平衡向正向移动( )
1.判断下列叙述的正误
2.在密闭容器中,反应:xA(g)+yB(g)??zC(g),在一定条件下达到平衡状态,保持温度不变,改变下列条件,分析解答下列问题:
(1)若x+y>z,缩小体积,增大压强,则平衡向________方向移动。
(2)若保持体积不变,通入He气,则平衡________移动。
(3)若保持压强不变,通入He气,平衡向正反应方向移动,则x、y、z的关系为________。
(4)若x+y=z,恒容条件下充入He气,则平衡________移动。
正反应
不
x+y<z
不
惰性气体对化学平衡的影响
(1)恒温、恒容条件
原平衡体系
惰性气体
体系中各组
分浓度不变
Q = K
平衡不移动
(2)恒温、恒压条件
原平衡体系
平衡体系容
器容积增大
惰性气体
各组分浓度
同比例减小
减压
反应
条件
对化
学平
衡的
影响
温度
浓度
压强
升高温度,平衡向吸热方向移动
降低温度,平衡向放热方向移动
改变浓度,若Q < K,平衡正向移动
改变浓度,若Q > K,平衡逆向移动
改变压强,若Q < K,平衡正向移动
改变压强,若Q > K,平衡逆向移动
勒·夏特列原理
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
