金属的腐蚀与防护 -2025年高考化学考向分析(共21张PPT)
文档属性
| 名称 | 金属的腐蚀与防护 -2025年高考化学考向分析(共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-27 00:00:00 | ||
图片预览






文档简介
(共21张PPT)
2025年高考化学考向分析
金属的腐蚀与防护
1.(传统文化)(2024河北秦皇岛联考)1965年越王勾践
宝剑出土时冰冷发亮,剑刃仍然锋利,经分析剑身有铜锡
合金等物质,镀了一层含铬的超级稀有金属,经测试剑花
D
A.墓坑填青灰泥与白膏泥密封性好,环境干燥,避免电化学腐蚀
B.棺椁坚固严密,剑出土时带着剑鞘,减少剑与空气接触
C.剑身镀了一层含铬的超级稀有金属,增强抗腐蚀性
D.涂硫黄粉产生黑色的硫化铜等稳定物质
纹黑色部分是因为曾用硫黄粉末处理过。为什么越王勾践宝剑在地下保存了2 000多年
仍能比较完好,下列有关分析错误的是( )
【解析】 墓坑填青灰泥与白膏泥密封性好,具有很好的防水性,从而保证墓坑相
对干燥,避免发生电化学腐蚀。
棺椁坚固严密、剑出土时带着剑鞘,都能有效避免剑体与空气接触,减缓腐蚀速
率。
由信息可知剑身镀了一层含铬的超级稀有金属,可增强剑身的抗腐蚀性。
硫黄粉与铜发生反应生成硫化亚铜。
2.(2022广东)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌
铁片放入酸化的 溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐
蚀的是( )
D
A.加入 溶液产生沉淀 B.加入淀粉碘化钾溶液无蓝色出现
C.加入溶液无红色出现 D.加入 溶液无蓝色沉淀生成
【解析】 在溶液中无论铁片是否被腐蚀,溶液中都有,加入 溶液均
会出现白色沉淀。
淀粉碘化钾溶液与溶液在本实验中只能检测溶液中是否有 ,但无论
是否被腐蚀,都不会有 。
若铁片被腐蚀,则溶液中含有,加入溶液会生成 蓝
色沉淀。
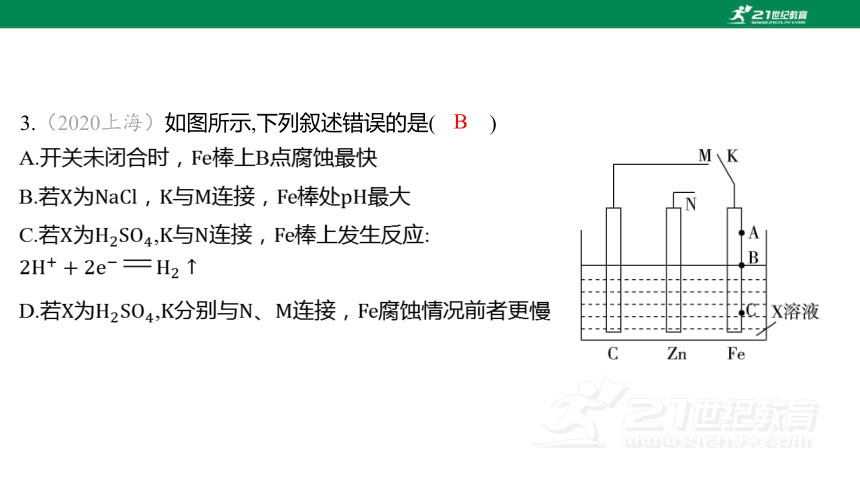
3.(2020上海)如图所示,下列叙述错误的是( )
B
A.开关未闭合时, 棒上B点腐蚀最快
B.若为,与连接,棒处 最大
C.若为,与连接, 棒上发生反应:
D.若为,分别与、连接, 腐蚀情况前者更慢
【解析】 开关未闭合时, 棒上B点同时与空气、
接触,腐蚀最快。
若为,与连接,形成原电池, 棒作负极,
电极反应为 ,C棒作正极,电极反应为
,故C棒处 最大。
若为,与连接,形成原电池, 棒为正极,
电极反应为 。
若为,与连接时,棒为正极,被保护,与连接时, 棒为负极,
被腐蚀,故 腐蚀情况前者更慢。
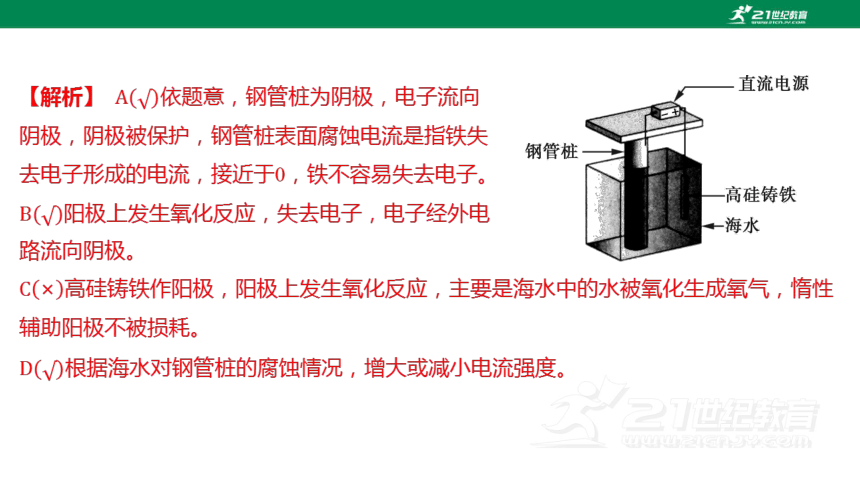
4.(2023上海七宝中学月考)支撑海港码头基础的钢管桩,常用外加电流的阴极保护法
进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的
是( )
C
A.通入保护电流使钢管桩表面腐蚀电流接近于零
B.通电后外电路电子被强制从高硅铸铁流出,流入
钢管桩
C.高硅铸铁的作用是作为损耗阳极材料和传递电流
D.通入的保护电流应该根据环境条件变化进行调整
【解析】 依题意,钢管桩为阴极,电子流向
阴极,阴极被保护,钢管桩表面腐蚀电流是指铁失
去电子形成的电流,接近于0,铁不容易失去电子。
阳极上发生氧化反应,失去电子,电子经外电
路流向阴极。
高硅铸铁作阳极,阳极上发生氧化反应,主要是海水中的水被氧化生成氧气,惰性
辅助阳极不被损耗。
根据海水对钢管桩的腐蚀情况,增大或减小电流强度。
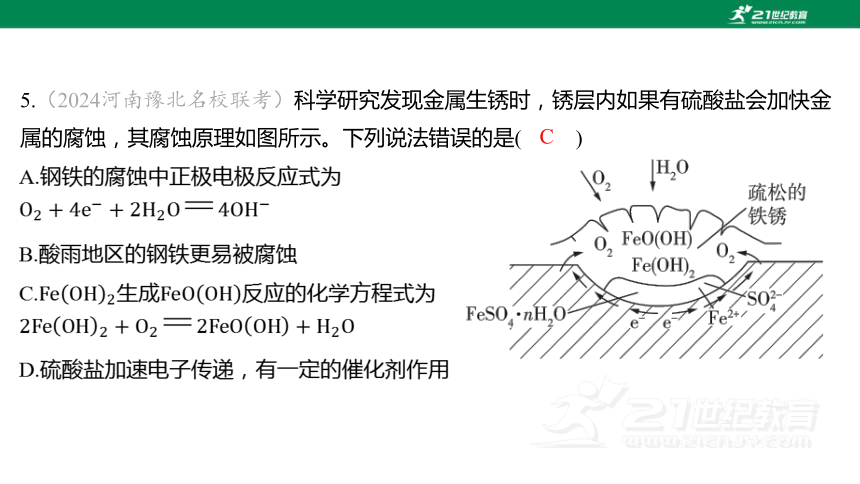
5.(2024河南豫北名校联考)科学研究发现金属生锈时,锈层内如果有硫酸盐会加快金
属的腐蚀,其腐蚀原理如图所示。下列说法错误的是( )
C
A.钢铁的腐蚀中正极电极反应式为
B.酸雨地区的钢铁更易被腐蚀
C.生成 反应的化学方程式为
D.硫酸盐加速电子传递,有一定的催化剂作用
【解析】 由题图可知钢铁发生吸氧腐蚀,
作负极,电极反应式为 ,C
作正极,氧气在正极得电子,电极反应式为
。
酸雨地区吸收的水中溶有电解质,溶液导
电性增强,钢铁更易被腐蚀。
不稳定,易被氧气氧化生成 ,题给化学方程式原子不守恒、得失
电子不守恒,正确的化学方程式为 。
根据题干信息“锈层内如果有硫酸盐会加快金属的腐蚀”,知硫酸盐能增加导电性,
加速电子传递,有一定的催化剂作用。
1.(2022上海)浓硫酸贮存罐的钝化金属保护法
示意图如图,其原理是利用可钝化的金属与直流
电源相连,控制合适的电压,使金属贮存罐表面形
成致密的钝化膜,以有效减缓金属腐蚀。下列选
项错误的是( )
C
A.金属贮存罐可用钢制材料 B.电子沿导线流入辅助电极
C.贮存浓硫酸的金属罐与电源负极相连 D.电压高到一定程度有可能会加剧腐蚀
【解析】 .
钢的主要成分是铁,铁遇冷的浓硫酸发生钝化,因
此金属贮存罐可用钢制材料。
贮存浓硫酸的金属罐为阳极,连接电源正极,辅助电极是阴极,电子沿导线
流入辅助电极。
电压过高时,有可能会加剧腐蚀。
2.(2024四川南充模拟)某研究小组利用图1装置探究铁粉腐蚀原理。挤压胶头滴管将
醋酸溶液滴入铁粉与碳粉的均匀混合物中,容器内的压强随时间的变化如图2所示。下
列说法正确的是( )
D
A.铁腐蚀过程中化学能全部转化为电能 B.该实验中铁粉只发生电化学腐蚀
C.段压强增大只是因为产生了 D. 段铁粉发生吸氧腐蚀
【解析】 .
铁腐蚀过程中化学能转化为电能、热能。
铁粉与醋酸接触,也会发生化学腐蚀。
铁粉的腐蚀反应属于放热反应,能引起压强增大,因此 装置内压强逐渐增
大,可能是因为产生了氢气,也可能是因为温度上升。
之后容器内压强减小,说明装置内气体分子数目减小,氧气被消耗,发生吸氧
腐蚀。
3.(2024内蒙古赤峰联考)硫酸盐还原菌 在地球上分布很
广泛,通过多种相互作用发挥诸多潜力,但在水体中,会促
使许多金属及合金发生腐蚀。某种 合金在硫酸盐还原菌存
在条件下腐蚀的机理如图所示,对于该反应机理相关信息分
析错误的是 ( )
A
①升高温度会加速硫酸盐还原菌 对金属的腐蚀
②硫酸盐还原菌 对金属的腐蚀作用是在有氧环境下进行的
③在硫酸盐还原菌作用下,腐蚀后最终会生成
④电化学腐蚀中负极反应式为
⑤当在的作用下转化为时,理论上正极反应会消耗 水
A.①②③ B.①②⑤ C.②③④ D.②③⑤
【解析】 ①高温下蛋白质容易变性,使硫酸盐还原菌
失去生理活性,会减弱其对金属的腐蚀,错误。
②根据示意图可知,过程中并没有氧气参与,硫酸盐还原菌
对金属的腐蚀作用是在无氧环境下进行的,错误。
③根据示意图可知,硫酸盐被硫酸盐还原菌还原成,腐蚀后生成的 最
终与反应生成 ,错误。
④电化学腐蚀中负极铁失去电子被氧化,电极反应式为 ,正确。
⑤在的作用下转化为时需要 可视为与
结合变成,根据示意图可知,水在正极发生还原反应,生成
和,所以理论上正极反应会消耗 水,正确。
4.(新情境)(2023山东省实验中学月考)利用小粒径零价
铁 的电化学腐蚀处理三氯乙烯( ),进行水体修
复的过程如图。、、 等共存物的存在会影响水体修
复效果,定义单位时间内释放电子的物质的量为 ,其中
A
A.上述反应仅②③④在正极发生
B.单位时间内,三氯乙烯脱去时,
C.④的电极反应式为
D.增大单位体积水体中小微粒的投入量,可使 增大
用于有效腐蚀的电子的物质的量为 。下列说法错误的是 ( )
【解析】 由题图中反应前后元素化合价变化可知,反
应①②③④均为得电子化合价降低的反应,均应在正极发生。
三氯乙烯中碳元素的化合价可看作 ,乙烯中碳元素化
合价可看作,转化为 时,得到
电子,脱去氯原子,所以脱去 时
。
第一步 根据题目信息写出谁变成谁,确认得失电子数,注意变 价元素原子守恒
(1个价个价 )
第二步 根据信息用 调平电荷
第三步 看补,用 检查
增大单位体积水体中小微粒 的投入量,可以增大小
微粒和正极的接触面积,加快 释放电子的速率,可使
增大。
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
2025年高考化学考向分析
金属的腐蚀与防护
1.(传统文化)(2024河北秦皇岛联考)1965年越王勾践
宝剑出土时冰冷发亮,剑刃仍然锋利,经分析剑身有铜锡
合金等物质,镀了一层含铬的超级稀有金属,经测试剑花
D
A.墓坑填青灰泥与白膏泥密封性好,环境干燥,避免电化学腐蚀
B.棺椁坚固严密,剑出土时带着剑鞘,减少剑与空气接触
C.剑身镀了一层含铬的超级稀有金属,增强抗腐蚀性
D.涂硫黄粉产生黑色的硫化铜等稳定物质
纹黑色部分是因为曾用硫黄粉末处理过。为什么越王勾践宝剑在地下保存了2 000多年
仍能比较完好,下列有关分析错误的是( )
【解析】 墓坑填青灰泥与白膏泥密封性好,具有很好的防水性,从而保证墓坑相
对干燥,避免发生电化学腐蚀。
棺椁坚固严密、剑出土时带着剑鞘,都能有效避免剑体与空气接触,减缓腐蚀速
率。
由信息可知剑身镀了一层含铬的超级稀有金属,可增强剑身的抗腐蚀性。
硫黄粉与铜发生反应生成硫化亚铜。
2.(2022广东)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌
铁片放入酸化的 溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐
蚀的是( )
D
A.加入 溶液产生沉淀 B.加入淀粉碘化钾溶液无蓝色出现
C.加入溶液无红色出现 D.加入 溶液无蓝色沉淀生成
【解析】 在溶液中无论铁片是否被腐蚀,溶液中都有,加入 溶液均
会出现白色沉淀。
淀粉碘化钾溶液与溶液在本实验中只能检测溶液中是否有 ,但无论
是否被腐蚀,都不会有 。
若铁片被腐蚀,则溶液中含有,加入溶液会生成 蓝
色沉淀。
3.(2020上海)如图所示,下列叙述错误的是( )
B
A.开关未闭合时, 棒上B点腐蚀最快
B.若为,与连接,棒处 最大
C.若为,与连接, 棒上发生反应:
D.若为,分别与、连接, 腐蚀情况前者更慢
【解析】 开关未闭合时, 棒上B点同时与空气、
接触,腐蚀最快。
若为,与连接,形成原电池, 棒作负极,
电极反应为 ,C棒作正极,电极反应为
,故C棒处 最大。
若为,与连接,形成原电池, 棒为正极,
电极反应为 。
若为,与连接时,棒为正极,被保护,与连接时, 棒为负极,
被腐蚀,故 腐蚀情况前者更慢。
4.(2023上海七宝中学月考)支撑海港码头基础的钢管桩,常用外加电流的阴极保护法
进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的
是( )
C
A.通入保护电流使钢管桩表面腐蚀电流接近于零
B.通电后外电路电子被强制从高硅铸铁流出,流入
钢管桩
C.高硅铸铁的作用是作为损耗阳极材料和传递电流
D.通入的保护电流应该根据环境条件变化进行调整
【解析】 依题意,钢管桩为阴极,电子流向
阴极,阴极被保护,钢管桩表面腐蚀电流是指铁失
去电子形成的电流,接近于0,铁不容易失去电子。
阳极上发生氧化反应,失去电子,电子经外电
路流向阴极。
高硅铸铁作阳极,阳极上发生氧化反应,主要是海水中的水被氧化生成氧气,惰性
辅助阳极不被损耗。
根据海水对钢管桩的腐蚀情况,增大或减小电流强度。
5.(2024河南豫北名校联考)科学研究发现金属生锈时,锈层内如果有硫酸盐会加快金
属的腐蚀,其腐蚀原理如图所示。下列说法错误的是( )
C
A.钢铁的腐蚀中正极电极反应式为
B.酸雨地区的钢铁更易被腐蚀
C.生成 反应的化学方程式为
D.硫酸盐加速电子传递,有一定的催化剂作用
【解析】 由题图可知钢铁发生吸氧腐蚀,
作负极,电极反应式为 ,C
作正极,氧气在正极得电子,电极反应式为
。
酸雨地区吸收的水中溶有电解质,溶液导
电性增强,钢铁更易被腐蚀。
不稳定,易被氧气氧化生成 ,题给化学方程式原子不守恒、得失
电子不守恒,正确的化学方程式为 。
根据题干信息“锈层内如果有硫酸盐会加快金属的腐蚀”,知硫酸盐能增加导电性,
加速电子传递,有一定的催化剂作用。
1.(2022上海)浓硫酸贮存罐的钝化金属保护法
示意图如图,其原理是利用可钝化的金属与直流
电源相连,控制合适的电压,使金属贮存罐表面形
成致密的钝化膜,以有效减缓金属腐蚀。下列选
项错误的是( )
C
A.金属贮存罐可用钢制材料 B.电子沿导线流入辅助电极
C.贮存浓硫酸的金属罐与电源负极相连 D.电压高到一定程度有可能会加剧腐蚀
【解析】 .
钢的主要成分是铁,铁遇冷的浓硫酸发生钝化,因
此金属贮存罐可用钢制材料。
贮存浓硫酸的金属罐为阳极,连接电源正极,辅助电极是阴极,电子沿导线
流入辅助电极。
电压过高时,有可能会加剧腐蚀。
2.(2024四川南充模拟)某研究小组利用图1装置探究铁粉腐蚀原理。挤压胶头滴管将
醋酸溶液滴入铁粉与碳粉的均匀混合物中,容器内的压强随时间的变化如图2所示。下
列说法正确的是( )
D
A.铁腐蚀过程中化学能全部转化为电能 B.该实验中铁粉只发生电化学腐蚀
C.段压强增大只是因为产生了 D. 段铁粉发生吸氧腐蚀
【解析】 .
铁腐蚀过程中化学能转化为电能、热能。
铁粉与醋酸接触,也会发生化学腐蚀。
铁粉的腐蚀反应属于放热反应,能引起压强增大,因此 装置内压强逐渐增
大,可能是因为产生了氢气,也可能是因为温度上升。
之后容器内压强减小,说明装置内气体分子数目减小,氧气被消耗,发生吸氧
腐蚀。
3.(2024内蒙古赤峰联考)硫酸盐还原菌 在地球上分布很
广泛,通过多种相互作用发挥诸多潜力,但在水体中,会促
使许多金属及合金发生腐蚀。某种 合金在硫酸盐还原菌存
在条件下腐蚀的机理如图所示,对于该反应机理相关信息分
析错误的是 ( )
A
①升高温度会加速硫酸盐还原菌 对金属的腐蚀
②硫酸盐还原菌 对金属的腐蚀作用是在有氧环境下进行的
③在硫酸盐还原菌作用下,腐蚀后最终会生成
④电化学腐蚀中负极反应式为
⑤当在的作用下转化为时,理论上正极反应会消耗 水
A.①②③ B.①②⑤ C.②③④ D.②③⑤
【解析】 ①高温下蛋白质容易变性,使硫酸盐还原菌
失去生理活性,会减弱其对金属的腐蚀,错误。
②根据示意图可知,过程中并没有氧气参与,硫酸盐还原菌
对金属的腐蚀作用是在无氧环境下进行的,错误。
③根据示意图可知,硫酸盐被硫酸盐还原菌还原成,腐蚀后生成的 最
终与反应生成 ,错误。
④电化学腐蚀中负极铁失去电子被氧化,电极反应式为 ,正确。
⑤在的作用下转化为时需要 可视为与
结合变成,根据示意图可知,水在正极发生还原反应,生成
和,所以理论上正极反应会消耗 水,正确。
4.(新情境)(2023山东省实验中学月考)利用小粒径零价
铁 的电化学腐蚀处理三氯乙烯( ),进行水体修
复的过程如图。、、 等共存物的存在会影响水体修
复效果,定义单位时间内释放电子的物质的量为 ,其中
A
A.上述反应仅②③④在正极发生
B.单位时间内,三氯乙烯脱去时,
C.④的电极反应式为
D.增大单位体积水体中小微粒的投入量,可使 增大
用于有效腐蚀的电子的物质的量为 。下列说法错误的是 ( )
【解析】 由题图中反应前后元素化合价变化可知,反
应①②③④均为得电子化合价降低的反应,均应在正极发生。
三氯乙烯中碳元素的化合价可看作 ,乙烯中碳元素化
合价可看作,转化为 时,得到
电子,脱去氯原子,所以脱去 时
。
第一步 根据题目信息写出谁变成谁,确认得失电子数,注意变 价元素原子守恒
(1个价个价 )
第二步 根据信息用 调平电荷
第三步 看补,用 检查
增大单位体积水体中小微粒 的投入量,可以增大小
微粒和正极的接触面积,加快 释放电子的速率,可使
增大。
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
同课章节目录
