盐类水解 -2025年高考化学考向分析(共118张PPT)
文档属性
| 名称 | 盐类水解 -2025年高考化学考向分析(共118张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 14.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-27 00:00:00 | ||
图片预览











文档简介
(共118张PPT)
2025年高考化学考向分析
盐类水解
盐类水解的影响因素及应用
1.(2023北京)下列过程与水解反应无关的是( )
B
A.热的纯碱溶液去除油脂
B.重油在高温、高压和催化剂作用下转化为小分子烃
C.蛋白质在酶的作用下转化为氨基酸
D.向沸水中滴入饱和溶液制备 胶体
【解析】 纯碱溶液因碳酸根离子的水解显碱性,油脂在碱性、加热条件下会发生
水解反应,生成易溶于水的高级脂肪酸盐和甘油,故可用热的纯碱溶液去除油脂,不符
合题意。
重油在高温、高压和催化剂作用下生成小分子烃的反应为裂化或裂解反应,符合
题意。
蛋白质在酶的作用下发生水解反应生成氨基酸,不符合题意。
向沸水中滴加饱和氯化铁溶液,发生水解反应生成 胶体,不符合题意。
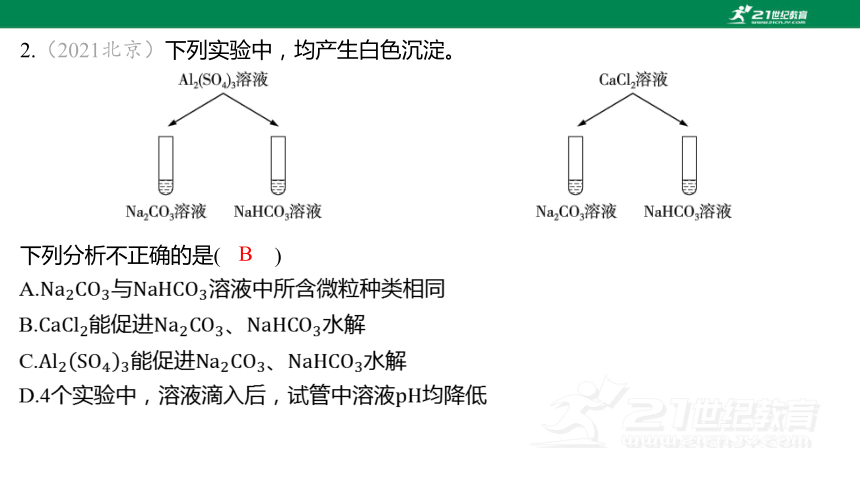
2.(2021北京)下列实验中,均产生白色沉淀。
下列分析不正确的是( )
B
A.与 溶液中所含微粒种类相同
B.能促进、 水解
C.能促进、 水解
D.4个实验中,溶液滴入后,试管中溶液 均降低
【解析】 溶液、溶液中均存在、、、 、
、、 ,故含有的微粒种类相同。
在溶液中存在电离平衡:,加入后,和 反
应生成沉淀,促进 的电离平衡正向移动,而不是促进水解。
与、都能发生相互促进的水解反应。(与 水解相互促进:
;与 水解相互促进:
(泡沫灭火器的反应原理))
个实验最终都会降低和 的浓度,而溶液显碱性来自两种离子的水解,
当这两种离子浓度降低了,水解出的浓度自然也会降低, 减小。
杰哥补充
很多同学一定有疑惑,不是说与不会生成沉淀吗?为什么在这个题目中
与会反应产生白色沉淀呢?其实,与 在某些条件下是不会沉淀的,但在
某些条件下会反应形成沉淀,这个取决于溶液的 、温度、离子浓度等。举个例子,
对而言,当偏高,平衡正移, 浓度会升高,使溶液的
,那自然就会有 沉淀生成啦!因此在学化学的时候,一
定要灵活,遇到题目信息与自己所学知识不相同时,以题目信息为主,并且要运用高中
知识点去解释、探究可能的原因噢
3.(2023安徽合肥质检)某化学兴趣小组测定了溶液的 随温度的
变化,结果如图所示。下列叙述正确的是( )
D
A.溶液呈碱性的原因是
B.溶液中:
C.图1表明升温过程中的水解程度减小, 减小
D.由图2可推知降低温度时,水的电离平衡逆向移动
【解析】 的水解分步进行,且以第一步为主:
。
方法一 全部是离子,找电荷守恒, 溶液中存在电荷守恒:
,溶液显碱性, ,则
。
方法二 不含和,找元素质量守恒, 溶液中存在元素质量守
恒:,则 。
碳酸钠水解吸热,升高温度促进水解,溶液 增大,但温度升高,水的电
离平衡也正向移动,水的离子积增大, 降低,综合两者作用,温度对水的电离平衡
的影响程度大于对碳酸根离子水解程度的影响,故升温的整体结果是溶液 减小。
降低温度,的水解程度减小,溶液中减小,溶液 减小,但温度降
低,水的电离平衡逆向移动,水的离子积减小, 增大,综合两者作用,温度对水的
电离平衡的影响程度大于对碳酸根离子水解程度的影响,故降温的整体结果是溶液
增大。
溶液中粒子浓度大小的比较
大招17 对应练习
解题觉醒
溶液中粒子浓度的大小比较,根据所给关系式,可以分为两种:
若给的是等式关系,判断依据:全部是离子找电荷守恒;不含与 找元素质量守
恒;含与且不含、 等不水解的离子找质子守恒;以上三点都不符合时往
往是电荷守恒与元素质量守恒凑出来的。
若给的是大小顺序关系,第一步:先考虑出现的粒子,强电解质拆成离子,弱电解质不
拆;第二步:比粒子的个数,此时不考虑水解和电离;第三步,考虑粒子的电离和水解。
4.(2023江苏)室温下,用含少量的溶液制备 的过程如图所示。已
知, 。下列说法正确的是( )
C
A.溶液中:
B.“除镁”得到的上层清液中:
C.溶液中:
D.“沉锰”后的滤液中:
【解析】 全部是离子,找电荷守恒,
溶液中存在电荷守恒:
。
加入溶液除镁,生成沉淀,上层澄清液为 的饱和溶液,又
,因此
。
含与且不含、等不水解的离子找质子守恒, 溶
液中存在质子守恒: ,故
。
全部是离子,找电荷守恒,但“沉锰” 后的滤液中还存在(【提醒】除镁步骤一般
加入的是过量)、等,因此选项中的电荷守恒还少了、 等。
5.(2023浙江6月选考)草酸 是二元弱酸。某小组做如下两组实验:
实验Ⅰ:往溶液中滴加 溶液。
实验Ⅱ:往溶液中滴加 溶液。
已知:的电离常数,, ,
溶液混合后体积变化忽略不计,下列说法正确的是( )
D
A.实验Ⅰ可选用甲基橙作指示剂,指示反应终点
B.实验Ⅰ中溶液时,存在
C.实验Ⅱ中发生反应
D.实验Ⅱ中溶液时,溶液中
【解析】 和完全中和生成,溶液由于 水解
而显碱性,指示剂应选择在碱性范围变色的酚酞才能减小实验误差。
实验Ⅰ中溶液时,恰好反应一半的 ,混合溶液的溶质为
等浓度的和,, ,
,, 的电离程度大于
的水解程度,因此存在 。
往溶液中滴加 溶液,由于一开始
滴入的溶液量很少,溶液中有大量 ,若发生
,则生成的会和反应生成 ,因此发生
的离子反应为 ( 【杰哥补充】
的平衡常数 ,
该反应平衡常数很大,可确定反应几乎完全向右进行)。
当滴加的溶液时,由于过量,生成 沉淀之后溶液中
还有剩余的钙离子,其浓度为
,溶液中
。
6.(2023吉林长春质监)关于常温时的下列溶液,说法正确的是( )
C
A.氨水加水稀释后,电离程度增大, 增大
B. 相等的醋酸和氯化铵溶液中,阳离子物质的量浓度之和相等
C.溶液中:
D.醋酸钠溶液中:
【解析】 加水稀释促进 电离(【点拨】越稀越电离),但溶液体积增大,
溶液体积增大使浓度减小的程度大于加水稀释促进电离使 浓度增大的程度
(【点拨】平衡移动是有限的,只能减弱外界条件引起的改变,并不能抵消这种改变),
故整体分析结果是浓度减小, 减小。
醋酸中的阳离子只有氢离子,氯化铵溶液中的阳离子有氢离子和铵根离子, 相
等的醋酸和氯化铵溶液中氢离子浓度相同,故氯化铵溶液中的阳离子总浓度比醋酸中的
大。
全部是离子,找电荷守恒, 溶液中存在电荷守恒:
,又 溶液显碱性,
,故 。
醋酸根离子会水解, 醋酸钠溶液中
。
7.(2023河南模拟)为二元弱酸, ,
,设溶液中 (总)
。室温下用 溶液滴定
溶液至终点。滴定过程得到的下列溶液中微粒的物质
的量浓度关系一定正确的是( )
D
A. 溶液:
B.(总)的溶液:
C.的溶液:
D.(总)的溶液:
【解析】 题给式子既不是单纯的电荷守恒,也不是单纯的元素质量守恒,所以写
出电荷守恒式与元素质量守恒式后,检查是否能组合出题目的等式。电荷守恒为
,元素质量守恒为
,两式整理得
。
根据元素质量守恒可知,溶液符合(总)。 既存在电离
平衡又存在水解平衡,水解的离子方程式为 ,
的水解常数,可知 的电离程度大于水解程度,则
。
滴入 溶液后,溶液中的电荷守恒为
,室温下 表示
,则 (总)
,由于溶液体积变大,(总) ,则
。
根据元素质量守恒可知,溶液符合(总)。题给式子含 与
且不含等不水解的离子,初步判定为质子守恒。 溶液为单一溶液,可
以依据两种方法来写质子守恒。
方法一:用电荷守恒和元素质量守恒推导出
质子守恒,电荷守恒为
,
元素质量守恒为
,
联立两式消去 得
。方法二:
8.(1) [同浓度的盐溶液中同种离子的浓度大小比较]现有 的五种溶液,
、 、、、 ,
由大到小的顺序为______________________。
(2) [同的盐溶液中同种离子的浓度大小比较]现有 相同的4种溶液,
、、、, 由大到小的顺序为
_________________。
【解析】 (1)
略小 于 的 溶液 电离出的,少部分水解,最终
浓度略小于
略小 于 的 溶 液 在水中发生水解:
在水中发生水解:
水解出的会抑制的水解, 水解程度减小
的 溶液 在水中不水解,对 的水解既不促进也不抑制
略小 于 的 溶 液 在水中发生水解:
在水中发生水解:
水解出的会与水解出的 反应,两种
离子的水解平衡都正向移动与 的水解互相
促进, 水解程度增大
远小 于 的 氨水 是弱碱,只会电离出很少量的
(约电离),远小于
由以上分析可知,溶液中由大到小的顺序为 。
续表
(2)
原理解释 杰哥“调味料”判断法
溶液显酸性的原因是 在水中 发生水解:,和 在水中不水解,不 影响溶液酸碱性,因此 相同的 和溶液中 浓 度相同 把 想象成是酸性“调味料”,当
溶液酸性相同相同 时,则溶液
所含的酸性“调味料”浓度一样
原理解释 杰哥“调味料”判断法
在水中水解使溶液显酸性: ; 在水中水解也使溶液显酸 性: ; 由于也会提供,与 溶液相比, 相同时 溶液所含的 浓 度较低 和 都是因为水解使溶液显
酸性的“调味料”,比起只有 一
种“调味料”的 来说,
中既有 又有
,当酸性相同相同 时,
溶液所含 浓度会
比较小
续表
原理解释 杰哥“调味料”判断法
在水中电离:,电离出是溶液显酸性的主要原因,且会大幅抑制 的水解,在相同时, 浓度 是最小的 能直接电离出 ,是酸性非
常强的“调味料”,与
溶液相比, 的酸性是水解得来
的,比起 的电离而言弱得
多,因此酸性相同相同 时,
溶液所含 浓度会小得
多
综上所述,由大到小的顺序为 。
续表
滴定过程中溶液粒子浓度变化
大招18 对应练习
解题觉醒
抓特殊点:“起始”点、“恰好反应一半”点、“中性”点、“恰好完全反应”点、“过量”点。
9.(图像创新)(2023海南中学检测)已知。初始温度 时,向
氨水中滴加稀硫酸,测得混合溶液的温度、 随加
入稀硫酸的体积 的变化关系如图所示。下列说法正确的是( )
D
A.、、三点对应 的水解平衡常数:
B.水的电离程度:
C.点对应溶液中:
D.若,则 点对应溶液中
【解析】
.
的水解过程吸热,温度越高, 的水解平衡常数越
大,温度:,则、、三点对应 的水解
平衡常数: 。
点对应溶液的溶质为、 点对应溶液的溶质为
和、点对应溶液的溶质为 和
,由于促进水的电离,和 均
会抑制水的电离,故 点水的电离程度最大。
根据电荷守恒, 溶液中
, 水解使溶液呈酸
性,,则 。
若,则和 的物质的量相等,此时的
溶液为 溶液,根据电荷守恒有
(【易错】注意与弱酸
的区别,是强酸,溶液中只存在 ),根据元素质量
守恒有 ,联立两式消去
可得 。
10.(2023福建龙岩质检)按如图1装置,常温下
分别向 溶液和
溶液中逐滴滴加
的稀盐酸,测得压强随盐酸体积的变
化曲线如图2所示,已知:碳酸的
; 。下列说法
正确的是( )
C
A.为 溶液的反应曲线
B.点溶液中的数量级为
C.到点之间的离子浓度大小关系:
D.水的电离程度:
【解析】
11.(2023湖南)常温下,用浓度为的 标准溶液滴定浓度均为
的和的混合溶液,滴定过程中溶液的 随
的变化曲线如图所示。下列说法错误的是( )
D
A.约为
B.点:
C.点:
D.水的电离程度:
【解析】
.
抓开始滴定的起始点,由上述分析可知, 点溶
液溶质组成为等物质的量的和, 不影响溶
液酸碱性,因此点可视为 (【提醒】体积加
倍,浓度减半)溶液的 ,溶液
,根据 ,
此时溶液中 ,因此
。
,表示加入的 溶液体积和混合酸的体积相
等,由于、、浓度都相同,且 会
部分电离出 ,根据元素质量守恒有
。
抓反应一半的点,由上述分析可知, 点溶液中
含有及等物质的量的和, 不影
响溶液酸碱性,而点溶液显酸性,说明 的
电离程度大于 的水解程度,因此溶液中
。
抓恰好完全反应的点, 点时酸碱恰好完全中和,
生成可促进水电离的可水解的盐 ,且没有会抑制水
电离的酸或碱,因此 点是中和过程中,水电离程度最大的
点;点相比点又多加了,过量的 会抑制水的电
离导致水的电离程度降低,因此水的电离程度: 。
12.(2023黑龙江哈尔滨质监) 时,向
(二元弱酸)溶液中滴加
溶液,溶液与加入 溶液体积的关
系如图所示。下列说法正确的是( )
C
A. 点对应的溶液中:
B.点对应的溶液中:
C.、、、四点中, 点对应的溶液中水的电离程度最大
D.、、、 四点对应的溶液中均有:
【解析】
.
加入溶液前,溶液的浓度为,加入 溶液后,溶液体积增大,
故点对应的溶液中: 。
点对应溶液的溶质为,此时溶液 ,
说明 的电离程度大于水解程度,
。
酸、碱抑制水的电离,可水解的正盐促进水的电离,可
水解的酸式盐若酸式酸根离子的电离程度大于水解程度则抑
制水的电离、若酸式酸根离子的电离程度小于水解程度则促
进水的电离。过程中,未加氢氧化钠溶液时, 电
离出 ,抑制水的电离,加入氢氧化钠溶液,酸逐渐被中
和为盐,对水的抑制程度减弱; 过程中,抑制水电离
的的量逐渐减少(【点拨】 的电离程度大于水解程
度)、促进水电离的 的量逐渐增多,水的电离程度逐渐
增大,故、、、四点中, 点对应的溶液中水的电离程
度最大。
全部是离子,找电荷守恒,、、、 四点,根据电
荷守恒可得 。
13.(2023天津南开中学模拟)常温下,已知醋酸的电离常数 ,向
溶液中逐滴加入的 溶液,溶液中水电
离的随加入溶液体积的变化关系如图所示。已知 。下列说法正
确的是( )
B
A.、两点对应溶液的 相同
B. 点对应溶液中:
C. 点对应溶液中,
D.点坐标为
【解析】
半反应点:点对应溶液的溶质为等浓度的和, 的水解
常数为,则 的电离程度大于
的水解程度,溶液呈酸性,抑制水的电离,则 点对应溶液中
(√)]
过量点:点对应溶液的溶质为等浓度的和 ,溶液呈碱性,抑制水的
电离,由物料守恒知
( )]
14.(图像创新)(2023山东泰安模拟,双选)
时,用 溶液滴定同浓度的
溶液,被滴定分数、 及微粒分
布分数,表示 、
或 的关系如图所示。
下列说法错误的是( )
CD
A.时,第一步电离平衡常数
B.点溶液中:
C.、、、四点溶液中水的电离程度:
D.点溶液中:
【解析】
时,点溶液中,约为4,代入 第一步电离平衡常数
得 。
点溶液中,,则 ,结合电荷守恒
,可得
。
过程中,抑制水电离的的量逐渐减少、抑制水电离的 的量逐渐增多,
水的电离程度逐渐增大;过程中,抑制水电离的 的量逐渐减少、促进水电离
的的量逐渐增多,水的电离程度逐渐增大,故、、、四点中, 点对应的溶液
中水的电离程度最大。
分析题图可知点溶液中, ,
,且点时被滴定分数大于1,因此 。
电解质溶液图像——对数图像分析
大招19 对应练习
解题觉醒
第一步,确定坐标轴的含义。
第二步,明晰曲线的变化趋势。
第三步,抓特殊点。
第四步,作出判断。
15.(方式创新·学科融合)(2023辽宁大连双基测试)常温下用 标准溶液滴定
等浓度的三元酸溶液,得到与、或 或
的关系分别如图1、图2所示。下列说法错误的是( )
A.当时,
B.,对应
C.到 滴定过程中,水的电离程度逐渐增大
D.用标准液滴定 溶液时,可选用酚酞作指示剂
√
【解析】 根据,得 ,
同理,,。根据 ,代入
图2中三个点的坐标值,可以计算出, ,
,,, 。
当时,, ,
。
由得,若,则 ,即
;由得 ,若
,则,即 。
,对应 。
到滴定过程中,溶液中溶质逐渐由转变为, 的水解
程度小于 的,水解促进水的电离,则水的电离程度逐渐增大。
用标准液滴定溶液(呈酸性),达到滴定终点时得到 溶液,分
析题图1可知滴定终点时溶液的约为10,在酚酞的 变色范围之内,可选用酚酞作指
示剂。
16.(2023湖北武汉调研) 在水中存在两种平衡:
;。在
时,与的关系如图所示,表示或浓度的负对数 。下列
说法错误的是( )
D
A.曲线①代表与 的关系
B.点坐标为
C. 的
D.向的溶液中加入
至时,元素以 形式存在
【解析】
由上述分析知A项正确。
曲线②上时和点时对应的 相等,即
,解得,故 点
,坐标为 。
曲线①上时,,所以
,同理, ,则
。
结合C项分析,时, ,
,均远小于,结合
原子守恒可知,此时元素主要以 形式存在。
17.(2023湖南郴州质监) 时,向二元
弱酸溶液中滴加 溶液(忽略温度
变化),所得混合溶液的 与粒子浓度变
化如图所示。下列说法错误的是( )
D
A.随着溶液的滴加, 增大
B.溶液中水的电离程度:
C.点对应的溶液中:
D.当溶液的时,
【解析】
时,向二元弱酸溶液中滴加溶液,溶液酸性减弱, 减小,
不变,增大, 增大。
随着溶液的加入,抑制水电离的 逐渐减少,促进水电离的可水解的盐逐
渐增多,,水的电离程度增强,水的电离程度: 。
点时 ,溶液中存在电荷守恒:
,则
,溶液呈酸性, ,转化
可得 。
当溶液的时, ,
, ,
, ,
。
18.(2023山东济南统考,双选)已知 属于难溶于水、可溶
于酸的盐。常温下,用调节浊液的,测得在不同 条件
下,体系中为或与 的关系如图所示。下
列说法错误的是( )
BC
A.的数量级为
B.代表与 的变化曲线
C. 点溶液显碱性
D.点的溶液中存在:
【解析】
19.(2023山东,双选)在含的溶液中,一定 范围内,存在平衡关系:
;; ;
;,平衡常数依次为、、、、 。
已知、,、随 的变化关系如图所示,下列
说法错误的是( )
BD
A.线表示 的变化情况
B.随增大, 先增大后减小
C.
D.溶液中元素与元素的物质的量之比始终为
【解析】
.
线(即图中的)表示 的变化情况。
由题目信息“在含 的溶液中”,可知在一定
范围内,该溶液为 的饱和溶液,
始终符合沉淀溶解平衡,因此
维持不变。
点存在 和
,且 ,因此
,
由题图中点坐标可知对应的是,即 。
若溶液只含,溶液中元素与元素的物质的量之比始终为 ,但由于溶液
有额外加入去改变,因此溶液中元素与 元素的物质的量之比并没有始终维持
。
电解质溶液图像——分布分数图像分析
大招20 对应练习
解题觉醒
分析图像:定曲线、读浓度、找交点、可替换。
20.(2023湖北) 为某邻苯二酚类配体,其
,。常温下构建(Ⅲ) 溶液
体系,其中 ,
。体系中含 物种的组分
分布系数 与 的关系如图所示,分布系数
,已知, 。下列
说法正确的是( )
C
A.当时,体系中
B.在之间,含的物种主要为
C.的平衡常数的 约为14
D.当时,参与配位的
【解析】 当 时,
,含 的粒子
在强酸性环境中主要以存在,此时 约
为,因此 ;②常温下
时,; 的
,即 ,可知
,求出溶液中
约为 。由以上分析可知:体系中
。
在 之间,
;
溶液中,,即 时
;同理,即 时,
,据此可以画出 体系的分布系数图
为 ,7.46和12.4取中间
值为,可知附近的分布系数远大于
和,利用守恒可知,此时
(所含 的浓度)
( 所含 的浓
度),可知 的浓
度大于、的浓度,因此 在
之间,含的物种主要为 。
的平衡常数表达式为
,分析题图可知,当 时,
,此时
。时体系中含的物种主要为 ,
考虑有部分结合形成配离子、,此时 可求出近似值约为
;已知 、
,欲求 ,可利用
,将
、 代入计算出
,因此选项所求, 。
当时, ,参与配位
的 。
21.(2024湖南师大附中入学考)在含初始浓度为 的溶液中滴加一定浓
度的氨水,含微粒存在下列转化: ;
。
、、的分布分数 与 的关系如图所示。下列推断
不正确的是( )
已知:的分布分数 。
A.曲线表示与 的关系
B.反应①的平衡常数
C. 点银元素的2个物种浓度相等,均为
D.当 时,含 微粒的主
要存在形式是
【解析】 图像分析较小时,含微粒的主要存在形式是;随着 增大,
先发生反应①生成逐渐减小、 逐渐增大;随着
继续增大,发生反应②生成 逐渐减小、
逐渐增大。
√
识图结果
由上述分析知A项正确。
曲线、相交于点,此时,则 、
,而 的平衡常数
,由 与题给两个反应的
关系可知,,则 。
点时,因同时还存在 ,且加入氨水,溶液体
积增大,结合元素质量守恒可知, 。
分析题图可知,当 时,即时,含 微粒
的主要存在形式是 。
22.(2023河北石家庄质检)已知常温下水溶液中、、、、 的分布分数
随变化曲线如图1;溶液中 和
的关系如图2。用 溶液滴定
溶液,下列说法错误的是( )
D
A.曲线表示
B.的水解平衡常数
C.滴定过程中溶液会变浑浊
D.滴定过程中始终存在:
【解析】 随增大,溶液中、减少, 、
增多, 先增多后减少,结合粒子分布分数的
计算公式可确定题图1中各曲线含义。
由上述分析知A项正确。
时 ,则
。
难溶,滴定过程中会生成 沉淀。
若滴定过程中 不沉淀,则溶液中存在电荷守恒:
,元素质量守恒:
,两式联立得:
,但生成 沉淀。
23.(2023山东潍坊二模,双选)常温下,
用测定溶液中的 时,
含微粒的分布系数及平均配位数
与的关系如图所示。与 的
配合物存在如下平衡:
AD
A.,
B.在点:
C.在点:
D.若点,
。下列说法错误的是( )
【解析】 随着的增大,含 微粒依次发生转
化: 。根据
曲线交点处,相应粒子的浓度相同,可以计算出对应平
衡常数等于对应交点处的值,即 ,
,, 。
由上述分析可知,, 。
在点,, ,则
。
在点, ,平均配位数
,, ,根据电荷
守恒可知, ,
则 ,
。
点时, ,平均配位数
,,, ,结
合电荷守恒可知
,则
,
;
根据、 ,则
,点时,则 ,
,故 。
1.(2020全国Ⅰ)以酚酞为指示剂,用的
溶液滴定未知浓度的二元酸溶液。溶液中, 、
分布系数 随滴加溶液体积 的变化关系如图所示。
[比如的分布系数:
下列叙述正确的是( )
C
A.曲线①代表,曲线②代表
B.溶液的浓度为
C.的电离常数
D.滴定终点时,溶液中
【解析】
2.(2023重庆联考)用一定浓度的 溶液分别滴定体积均
为,浓度均为的、 和
三种溶液,滴定过程中三种溶液的电导率如图所示。
(已知:溶液电导率越大,导电能力越强)下列说法错误的
是( )
D
A.曲线①②③分别代表、和
B.的浓度为
C.、、、四点中, 点水的电离程度最小
D.点对应的溶液中粒子浓度大小关系:
【解析】 三种碱溶液浓度都是 ,
是二元强碱, 是一元强碱,它们均完全电离,
而 是一元弱碱,在溶液中存在电离平衡,因此溶液
中的离子浓度: ,故曲线①②
③分别代表、和 在滴定过程中的电
导率曲线。
曲线①代表在滴定过程中的电导率曲线,点时电导率最小, 点表示的是硫
酸与恰好完全反应,反应为 ,由于二者消
耗的体积相同,二者反应的物质的量之比是,所以的浓度与 相同,均
为 。
点时恰好被中和得到 ,该
盐是强酸弱碱盐,水解使溶液显酸性,水的电离受到促进作
用,点时恰好被中和得到 ,该盐是强酸
强碱盐,不水解,水的电离不受影响,点时 恰好被
完全中和产生, 是强酸强碱盐,不水解,
溶液显中性,水的电离不受影响,点是、
等浓度的混合溶液,过量的酸电离产生 ,使水的电离受到
抑制,所以、、、四点中,水的电离程度点最大, 点
最小。
根据电荷守恒可知溶液中离子浓度关系为
。
3.(2023广东深圳一调)常温下,乙二胺 的水溶液中,
、和的分布分数与 的关
系如图所示。已知: 。
下列说法不正确的是( )
C
A. 溶液显酸性
B.曲线可表示
C.
的平衡常数
D. 溶液中:
【解析】 类比“”,乙二胺可看作二元碱,随着 的减
小,逐渐减少、 先增加后
减少、 逐渐增多。
根据上述分析可知, 是二元弱碱,
属于强酸弱碱盐,
水解使溶液显酸性。
由上述分析知B项正确。
表示 的第一
步电离,则其平衡常数为 。
,
即 的电离程度大于其水解程度(【技法】
可通过最大时对应溶液的 作出判
断),所以 溶液中:
。
4.(图像创新)(2023辽宁)某废水处理过程中始终保
持饱和,即,通过调节 使
和形成硫化物而分离,体系中与 关系
如图所示,为、、和 的浓度,单位为
。已知 ,下列说法正确的是
( )
D
A.
B.③为与 的关系曲线
C.
D.
【解析】 图像读取 方法一
方法二 根据,可得 ,即
,和符合 的函
数关系,同理,, ,
即,和 符合
的函数关系,则④表示与 的关系曲线,③表
示与的关系曲线;根据 ,
可得 ,
,、符合 的
函数关系,同理、符合 的函数关系,
,则对应的轴截距小,②表示与 的关系曲线,
①表示与 的关系曲线。
曲线①和③的交点表示溶液中 ,则有
。
曲线③为与 的关系曲线。
曲线④代表与的关系曲线,由曲线④所给的坐标,可求出 和
,再根据题目已知条件 ,两个坐标选择其中一个即可求出
。
① 利用坐标、 ,
。
②利用坐标、 ,
。
D(√)欲求,需知道相同时和 各是多少,但题图中没有给
出相同下的和,由于题目给出 ,因此可以通过
,将 消掉,再利用曲线③的坐
标以及C选项的来求出 。
①利用坐标 ,
,因此 。
②利用坐标, ,
因此 。
5.(2023湖北武汉调研)常温下,用 盐
酸滴定溶液,溶液中 、
、的分布分数 [已知
随 变化的曲线及滴定曲
线如图。下列说法不正确的是( )
D
A.
B.点溶液中
C.滴定分析时, 点可用甲基橙作指示剂
D.忽略溶液体积变化, 点溶液中
【解析】
加入的盐酸体积为 时,所得溶液中
、、,说明此时
与恰好反应生成和,则 。
,又点时 ,
,则
。
点溶液 ,溶液呈酸性,故可用甲基橙
作指示剂。
点时所加盐酸体积为,溶液总体积为 ,
溶液中, ,
由电荷守恒可得
,点溶液呈酸性, ,则
,又由元素质量守
恒可得
(【点拨】根据点时 判断,在滴定过程中始终有
元素质量守恒关系式
),且 点时
,联立可得
。
6.(图像创新)(2023辽宁本溪高级中学
一模)时,将 气体缓慢通入
的氨水中,溶液的 、体系
中粒子浓度的对数 与反应物的物质
的量之比 的关系如图所
D
A.时,的电离平衡常数为
B.时,
C.所示溶液:
D.所示溶液:
示。若忽略通入气体后溶液体积的变化,下列有关说法错误的是( )
【解析】 抓特殊点 ,分
析题图可知,当溶液
时,
,则
,此时
,故
的电离平衡常数
。
时,溶液中的溶质为等浓度的和 ,分析题图可知此时溶液显
碱性,则一水合氨的电离程度大于铵根离子的水解程度,则此时溶液中的粒子浓度大小
顺序为 。
抓特殊点,所示溶液 ,
则 ,根据
的电离常数
,则
,
故 。
所示溶液中 ,且存在电荷守恒
,因,故 所示溶液中
,故假设错误。
7.(2023河北邯郸二模)某酸溶液中含有
粒子的分布分数与 的变化关系如图所示。下
列说法正确的是( )
C
A.已知亚磷酸的结构为,则可能为
B.向溶液中滴加少量 溶液,发生反应的
离子方程式为
C. 溶液中存在:
D. 溶液中存在:
【解析】 由题图各粒子的分布分数与
的变化关系可知,该酸应该为三元弱酸,亚磷酸的
结构为 ,含有两个羟基,为二元酸,所
以不可能为 。
向溶液中滴加少量 溶液,发生反应
的离子方程式应为 。
方法一 分析题图可知, 点时,
,所以 的电离常数
, 点时,
,则 ;
在 溶液中,存在电离平衡和水解平衡,
的水解常数
, ,则有
。
方法二 分析题图可知,溶液中 最大时,
溶液的为,溶液呈碱性,说明 的
水解程度大于电离程度,则有
。
全部是离子,找电荷守恒,在 溶液中,
存在电荷守恒:
。
8.(2023山东临沂检测)常温下,向一定浓度溶液中加入 ,保持溶液体
积和温度不变,测得与为、、 变化如图所示。下
列说法错误的是( )
A
A.常温下,
B. 点溶液中:
C. 溶液中:
D.点溶液中:
【解析】 向一定浓度溶液中加入 固体,
随着增大,减小、 减小、
增大,则 增大,
减小。
增大,则减小。又
,
则与呈线性关系,故曲线 表示
,曲线表示,曲线 表
示 。
,
,则
。
点溶液中 ,题给式子可
变形为
,
全部是离子,找电荷守恒,由电荷守恒有
,
则 。
第一步:先考虑出现的 粒子,强电解质拆成离 子,弱电解质不拆 先出现的是,是强电解质,拆成和
第二步:比粒子的个 数,此时不考虑水解和 电离 和的个数比为,可以判断出
第三 步:考 虑粒子 的电离 和水解 ① (主)
② (
,即 的电离
程度大于其水解程度)
的电离程度大于其水解程度,故( ,又水解、电
离的程度都很微弱,因此溶液最终微粒浓度大小顺序为
点时,溶液,溶液呈酸性,且
(【点拨】点对应 ,此时
续表
),则由电荷守恒
得
。
9.(2023湖北华中师大一附中测试)溶洞水体中的 与
空气中的保持平衡,水体中为、 、
或与 的关系如图所示。已知
,下列说法错误的是( )
D
A.
B.Ⅱ代表与 的关系曲线
C.
D.点溶液中,
【解析】 溶洞水体中的与空气中的 保持平衡,
故可认为保持不变,随着 增大,溶液碱性增强,
、的浓度增大,较小时 ,
较大时,故Ⅰ为与 的关系
曲线,Ⅱ为与的关系曲线,随着 增大,
减小,Ⅲ为与 的关系曲线。
由点,得 ,
由点得 ,
。
点时,,则,, 。
点溶液中,, ,则由
可求得 点
,
。
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
2025年高考化学考向分析
盐类水解
盐类水解的影响因素及应用
1.(2023北京)下列过程与水解反应无关的是( )
B
A.热的纯碱溶液去除油脂
B.重油在高温、高压和催化剂作用下转化为小分子烃
C.蛋白质在酶的作用下转化为氨基酸
D.向沸水中滴入饱和溶液制备 胶体
【解析】 纯碱溶液因碳酸根离子的水解显碱性,油脂在碱性、加热条件下会发生
水解反应,生成易溶于水的高级脂肪酸盐和甘油,故可用热的纯碱溶液去除油脂,不符
合题意。
重油在高温、高压和催化剂作用下生成小分子烃的反应为裂化或裂解反应,符合
题意。
蛋白质在酶的作用下发生水解反应生成氨基酸,不符合题意。
向沸水中滴加饱和氯化铁溶液,发生水解反应生成 胶体,不符合题意。
2.(2021北京)下列实验中,均产生白色沉淀。
下列分析不正确的是( )
B
A.与 溶液中所含微粒种类相同
B.能促进、 水解
C.能促进、 水解
D.4个实验中,溶液滴入后,试管中溶液 均降低
【解析】 溶液、溶液中均存在、、、 、
、、 ,故含有的微粒种类相同。
在溶液中存在电离平衡:,加入后,和 反
应生成沉淀,促进 的电离平衡正向移动,而不是促进水解。
与、都能发生相互促进的水解反应。(与 水解相互促进:
;与 水解相互促进:
(泡沫灭火器的反应原理))
个实验最终都会降低和 的浓度,而溶液显碱性来自两种离子的水解,
当这两种离子浓度降低了,水解出的浓度自然也会降低, 减小。
杰哥补充
很多同学一定有疑惑,不是说与不会生成沉淀吗?为什么在这个题目中
与会反应产生白色沉淀呢?其实,与 在某些条件下是不会沉淀的,但在
某些条件下会反应形成沉淀,这个取决于溶液的 、温度、离子浓度等。举个例子,
对而言,当偏高,平衡正移, 浓度会升高,使溶液的
,那自然就会有 沉淀生成啦!因此在学化学的时候,一
定要灵活,遇到题目信息与自己所学知识不相同时,以题目信息为主,并且要运用高中
知识点去解释、探究可能的原因噢
3.(2023安徽合肥质检)某化学兴趣小组测定了溶液的 随温度的
变化,结果如图所示。下列叙述正确的是( )
D
A.溶液呈碱性的原因是
B.溶液中:
C.图1表明升温过程中的水解程度减小, 减小
D.由图2可推知降低温度时,水的电离平衡逆向移动
【解析】 的水解分步进行,且以第一步为主:
。
方法一 全部是离子,找电荷守恒, 溶液中存在电荷守恒:
,溶液显碱性, ,则
。
方法二 不含和,找元素质量守恒, 溶液中存在元素质量守
恒:,则 。
碳酸钠水解吸热,升高温度促进水解,溶液 增大,但温度升高,水的电
离平衡也正向移动,水的离子积增大, 降低,综合两者作用,温度对水的电离平衡
的影响程度大于对碳酸根离子水解程度的影响,故升温的整体结果是溶液 减小。
降低温度,的水解程度减小,溶液中减小,溶液 减小,但温度降
低,水的电离平衡逆向移动,水的离子积减小, 增大,综合两者作用,温度对水的
电离平衡的影响程度大于对碳酸根离子水解程度的影响,故降温的整体结果是溶液
增大。
溶液中粒子浓度大小的比较
大招17 对应练习
解题觉醒
溶液中粒子浓度的大小比较,根据所给关系式,可以分为两种:
若给的是等式关系,判断依据:全部是离子找电荷守恒;不含与 找元素质量守
恒;含与且不含、 等不水解的离子找质子守恒;以上三点都不符合时往
往是电荷守恒与元素质量守恒凑出来的。
若给的是大小顺序关系,第一步:先考虑出现的粒子,强电解质拆成离子,弱电解质不
拆;第二步:比粒子的个数,此时不考虑水解和电离;第三步,考虑粒子的电离和水解。
4.(2023江苏)室温下,用含少量的溶液制备 的过程如图所示。已
知, 。下列说法正确的是( )
C
A.溶液中:
B.“除镁”得到的上层清液中:
C.溶液中:
D.“沉锰”后的滤液中:
【解析】 全部是离子,找电荷守恒,
溶液中存在电荷守恒:
。
加入溶液除镁,生成沉淀,上层澄清液为 的饱和溶液,又
,因此
。
含与且不含、等不水解的离子找质子守恒, 溶
液中存在质子守恒: ,故
。
全部是离子,找电荷守恒,但“沉锰” 后的滤液中还存在(【提醒】除镁步骤一般
加入的是过量)、等,因此选项中的电荷守恒还少了、 等。
5.(2023浙江6月选考)草酸 是二元弱酸。某小组做如下两组实验:
实验Ⅰ:往溶液中滴加 溶液。
实验Ⅱ:往溶液中滴加 溶液。
已知:的电离常数,, ,
溶液混合后体积变化忽略不计,下列说法正确的是( )
D
A.实验Ⅰ可选用甲基橙作指示剂,指示反应终点
B.实验Ⅰ中溶液时,存在
C.实验Ⅱ中发生反应
D.实验Ⅱ中溶液时,溶液中
【解析】 和完全中和生成,溶液由于 水解
而显碱性,指示剂应选择在碱性范围变色的酚酞才能减小实验误差。
实验Ⅰ中溶液时,恰好反应一半的 ,混合溶液的溶质为
等浓度的和,, ,
,, 的电离程度大于
的水解程度,因此存在 。
往溶液中滴加 溶液,由于一开始
滴入的溶液量很少,溶液中有大量 ,若发生
,则生成的会和反应生成 ,因此发生
的离子反应为 ( 【杰哥补充】
的平衡常数 ,
该反应平衡常数很大,可确定反应几乎完全向右进行)。
当滴加的溶液时,由于过量,生成 沉淀之后溶液中
还有剩余的钙离子,其浓度为
,溶液中
。
6.(2023吉林长春质监)关于常温时的下列溶液,说法正确的是( )
C
A.氨水加水稀释后,电离程度增大, 增大
B. 相等的醋酸和氯化铵溶液中,阳离子物质的量浓度之和相等
C.溶液中:
D.醋酸钠溶液中:
【解析】 加水稀释促进 电离(【点拨】越稀越电离),但溶液体积增大,
溶液体积增大使浓度减小的程度大于加水稀释促进电离使 浓度增大的程度
(【点拨】平衡移动是有限的,只能减弱外界条件引起的改变,并不能抵消这种改变),
故整体分析结果是浓度减小, 减小。
醋酸中的阳离子只有氢离子,氯化铵溶液中的阳离子有氢离子和铵根离子, 相
等的醋酸和氯化铵溶液中氢离子浓度相同,故氯化铵溶液中的阳离子总浓度比醋酸中的
大。
全部是离子,找电荷守恒, 溶液中存在电荷守恒:
,又 溶液显碱性,
,故 。
醋酸根离子会水解, 醋酸钠溶液中
。
7.(2023河南模拟)为二元弱酸, ,
,设溶液中 (总)
。室温下用 溶液滴定
溶液至终点。滴定过程得到的下列溶液中微粒的物质
的量浓度关系一定正确的是( )
D
A. 溶液:
B.(总)的溶液:
C.的溶液:
D.(总)的溶液:
【解析】 题给式子既不是单纯的电荷守恒,也不是单纯的元素质量守恒,所以写
出电荷守恒式与元素质量守恒式后,检查是否能组合出题目的等式。电荷守恒为
,元素质量守恒为
,两式整理得
。
根据元素质量守恒可知,溶液符合(总)。 既存在电离
平衡又存在水解平衡,水解的离子方程式为 ,
的水解常数,可知 的电离程度大于水解程度,则
。
滴入 溶液后,溶液中的电荷守恒为
,室温下 表示
,则 (总)
,由于溶液体积变大,(总) ,则
。
根据元素质量守恒可知,溶液符合(总)。题给式子含 与
且不含等不水解的离子,初步判定为质子守恒。 溶液为单一溶液,可
以依据两种方法来写质子守恒。
方法一:用电荷守恒和元素质量守恒推导出
质子守恒,电荷守恒为
,
元素质量守恒为
,
联立两式消去 得
。方法二:
8.(1) [同浓度的盐溶液中同种离子的浓度大小比较]现有 的五种溶液,
、 、、、 ,
由大到小的顺序为______________________。
(2) [同的盐溶液中同种离子的浓度大小比较]现有 相同的4种溶液,
、、、, 由大到小的顺序为
_________________。
【解析】 (1)
略小 于 的 溶液 电离出的,少部分水解,最终
浓度略小于
略小 于 的 溶 液 在水中发生水解:
在水中发生水解:
水解出的会抑制的水解, 水解程度减小
的 溶液 在水中不水解,对 的水解既不促进也不抑制
略小 于 的 溶 液 在水中发生水解:
在水中发生水解:
水解出的会与水解出的 反应,两种
离子的水解平衡都正向移动与 的水解互相
促进, 水解程度增大
远小 于 的 氨水 是弱碱,只会电离出很少量的
(约电离),远小于
由以上分析可知,溶液中由大到小的顺序为 。
续表
(2)
原理解释 杰哥“调味料”判断法
溶液显酸性的原因是 在水中 发生水解:,和 在水中不水解,不 影响溶液酸碱性,因此 相同的 和溶液中 浓 度相同 把 想象成是酸性“调味料”,当
溶液酸性相同相同 时,则溶液
所含的酸性“调味料”浓度一样
原理解释 杰哥“调味料”判断法
在水中水解使溶液显酸性: ; 在水中水解也使溶液显酸 性: ; 由于也会提供,与 溶液相比, 相同时 溶液所含的 浓 度较低 和 都是因为水解使溶液显
酸性的“调味料”,比起只有 一
种“调味料”的 来说,
中既有 又有
,当酸性相同相同 时,
溶液所含 浓度会
比较小
续表
原理解释 杰哥“调味料”判断法
在水中电离:,电离出是溶液显酸性的主要原因,且会大幅抑制 的水解,在相同时, 浓度 是最小的 能直接电离出 ,是酸性非
常强的“调味料”,与
溶液相比, 的酸性是水解得来
的,比起 的电离而言弱得
多,因此酸性相同相同 时,
溶液所含 浓度会小得
多
综上所述,由大到小的顺序为 。
续表
滴定过程中溶液粒子浓度变化
大招18 对应练习
解题觉醒
抓特殊点:“起始”点、“恰好反应一半”点、“中性”点、“恰好完全反应”点、“过量”点。
9.(图像创新)(2023海南中学检测)已知。初始温度 时,向
氨水中滴加稀硫酸,测得混合溶液的温度、 随加
入稀硫酸的体积 的变化关系如图所示。下列说法正确的是( )
D
A.、、三点对应 的水解平衡常数:
B.水的电离程度:
C.点对应溶液中:
D.若,则 点对应溶液中
【解析】
.
的水解过程吸热,温度越高, 的水解平衡常数越
大,温度:,则、、三点对应 的水解
平衡常数: 。
点对应溶液的溶质为、 点对应溶液的溶质为
和、点对应溶液的溶质为 和
,由于促进水的电离,和 均
会抑制水的电离,故 点水的电离程度最大。
根据电荷守恒, 溶液中
, 水解使溶液呈酸
性,,则 。
若,则和 的物质的量相等,此时的
溶液为 溶液,根据电荷守恒有
(【易错】注意与弱酸
的区别,是强酸,溶液中只存在 ),根据元素质量
守恒有 ,联立两式消去
可得 。
10.(2023福建龙岩质检)按如图1装置,常温下
分别向 溶液和
溶液中逐滴滴加
的稀盐酸,测得压强随盐酸体积的变
化曲线如图2所示,已知:碳酸的
; 。下列说法
正确的是( )
C
A.为 溶液的反应曲线
B.点溶液中的数量级为
C.到点之间的离子浓度大小关系:
D.水的电离程度:
【解析】
11.(2023湖南)常温下,用浓度为的 标准溶液滴定浓度均为
的和的混合溶液,滴定过程中溶液的 随
的变化曲线如图所示。下列说法错误的是( )
D
A.约为
B.点:
C.点:
D.水的电离程度:
【解析】
.
抓开始滴定的起始点,由上述分析可知, 点溶
液溶质组成为等物质的量的和, 不影响溶
液酸碱性,因此点可视为 (【提醒】体积加
倍,浓度减半)溶液的 ,溶液
,根据 ,
此时溶液中 ,因此
。
,表示加入的 溶液体积和混合酸的体积相
等,由于、、浓度都相同,且 会
部分电离出 ,根据元素质量守恒有
。
抓反应一半的点,由上述分析可知, 点溶液中
含有及等物质的量的和, 不影
响溶液酸碱性,而点溶液显酸性,说明 的
电离程度大于 的水解程度,因此溶液中
。
抓恰好完全反应的点, 点时酸碱恰好完全中和,
生成可促进水电离的可水解的盐 ,且没有会抑制水
电离的酸或碱,因此 点是中和过程中,水电离程度最大的
点;点相比点又多加了,过量的 会抑制水的电
离导致水的电离程度降低,因此水的电离程度: 。
12.(2023黑龙江哈尔滨质监) 时,向
(二元弱酸)溶液中滴加
溶液,溶液与加入 溶液体积的关
系如图所示。下列说法正确的是( )
C
A. 点对应的溶液中:
B.点对应的溶液中:
C.、、、四点中, 点对应的溶液中水的电离程度最大
D.、、、 四点对应的溶液中均有:
【解析】
.
加入溶液前,溶液的浓度为,加入 溶液后,溶液体积增大,
故点对应的溶液中: 。
点对应溶液的溶质为,此时溶液 ,
说明 的电离程度大于水解程度,
。
酸、碱抑制水的电离,可水解的正盐促进水的电离,可
水解的酸式盐若酸式酸根离子的电离程度大于水解程度则抑
制水的电离、若酸式酸根离子的电离程度小于水解程度则促
进水的电离。过程中,未加氢氧化钠溶液时, 电
离出 ,抑制水的电离,加入氢氧化钠溶液,酸逐渐被中
和为盐,对水的抑制程度减弱; 过程中,抑制水电离
的的量逐渐减少(【点拨】 的电离程度大于水解程
度)、促进水电离的 的量逐渐增多,水的电离程度逐渐
增大,故、、、四点中, 点对应的溶液中水的电离程
度最大。
全部是离子,找电荷守恒,、、、 四点,根据电
荷守恒可得 。
13.(2023天津南开中学模拟)常温下,已知醋酸的电离常数 ,向
溶液中逐滴加入的 溶液,溶液中水电
离的随加入溶液体积的变化关系如图所示。已知 。下列说法正
确的是( )
B
A.、两点对应溶液的 相同
B. 点对应溶液中:
C. 点对应溶液中,
D.点坐标为
【解析】
半反应点:点对应溶液的溶质为等浓度的和, 的水解
常数为,则 的电离程度大于
的水解程度,溶液呈酸性,抑制水的电离,则 点对应溶液中
(√)]
过量点:点对应溶液的溶质为等浓度的和 ,溶液呈碱性,抑制水的
电离,由物料守恒知
( )]
14.(图像创新)(2023山东泰安模拟,双选)
时,用 溶液滴定同浓度的
溶液,被滴定分数、 及微粒分
布分数,表示 、
或 的关系如图所示。
下列说法错误的是( )
CD
A.时,第一步电离平衡常数
B.点溶液中:
C.、、、四点溶液中水的电离程度:
D.点溶液中:
【解析】
时,点溶液中,约为4,代入 第一步电离平衡常数
得 。
点溶液中,,则 ,结合电荷守恒
,可得
。
过程中,抑制水电离的的量逐渐减少、抑制水电离的 的量逐渐增多,
水的电离程度逐渐增大;过程中,抑制水电离的 的量逐渐减少、促进水电离
的的量逐渐增多,水的电离程度逐渐增大,故、、、四点中, 点对应的溶液
中水的电离程度最大。
分析题图可知点溶液中, ,
,且点时被滴定分数大于1,因此 。
电解质溶液图像——对数图像分析
大招19 对应练习
解题觉醒
第一步,确定坐标轴的含义。
第二步,明晰曲线的变化趋势。
第三步,抓特殊点。
第四步,作出判断。
15.(方式创新·学科融合)(2023辽宁大连双基测试)常温下用 标准溶液滴定
等浓度的三元酸溶液,得到与、或 或
的关系分别如图1、图2所示。下列说法错误的是( )
A.当时,
B.,对应
C.到 滴定过程中,水的电离程度逐渐增大
D.用标准液滴定 溶液时,可选用酚酞作指示剂
√
【解析】 根据,得 ,
同理,,。根据 ,代入
图2中三个点的坐标值,可以计算出, ,
,,, 。
当时,, ,
。
由得,若,则 ,即
;由得 ,若
,则,即 。
,对应 。
到滴定过程中,溶液中溶质逐渐由转变为, 的水解
程度小于 的,水解促进水的电离,则水的电离程度逐渐增大。
用标准液滴定溶液(呈酸性),达到滴定终点时得到 溶液,分
析题图1可知滴定终点时溶液的约为10,在酚酞的 变色范围之内,可选用酚酞作指
示剂。
16.(2023湖北武汉调研) 在水中存在两种平衡:
;。在
时,与的关系如图所示,表示或浓度的负对数 。下列
说法错误的是( )
D
A.曲线①代表与 的关系
B.点坐标为
C. 的
D.向的溶液中加入
至时,元素以 形式存在
【解析】
由上述分析知A项正确。
曲线②上时和点时对应的 相等,即
,解得,故 点
,坐标为 。
曲线①上时,,所以
,同理, ,则
。
结合C项分析,时, ,
,均远小于,结合
原子守恒可知,此时元素主要以 形式存在。
17.(2023湖南郴州质监) 时,向二元
弱酸溶液中滴加 溶液(忽略温度
变化),所得混合溶液的 与粒子浓度变
化如图所示。下列说法错误的是( )
D
A.随着溶液的滴加, 增大
B.溶液中水的电离程度:
C.点对应的溶液中:
D.当溶液的时,
【解析】
时,向二元弱酸溶液中滴加溶液,溶液酸性减弱, 减小,
不变,增大, 增大。
随着溶液的加入,抑制水电离的 逐渐减少,促进水电离的可水解的盐逐
渐增多,,水的电离程度增强,水的电离程度: 。
点时 ,溶液中存在电荷守恒:
,则
,溶液呈酸性, ,转化
可得 。
当溶液的时, ,
, ,
, ,
。
18.(2023山东济南统考,双选)已知 属于难溶于水、可溶
于酸的盐。常温下,用调节浊液的,测得在不同 条件
下,体系中为或与 的关系如图所示。下
列说法错误的是( )
BC
A.的数量级为
B.代表与 的变化曲线
C. 点溶液显碱性
D.点的溶液中存在:
【解析】
19.(2023山东,双选)在含的溶液中,一定 范围内,存在平衡关系:
;; ;
;,平衡常数依次为、、、、 。
已知、,、随 的变化关系如图所示,下列
说法错误的是( )
BD
A.线表示 的变化情况
B.随增大, 先增大后减小
C.
D.溶液中元素与元素的物质的量之比始终为
【解析】
.
线(即图中的)表示 的变化情况。
由题目信息“在含 的溶液中”,可知在一定
范围内,该溶液为 的饱和溶液,
始终符合沉淀溶解平衡,因此
维持不变。
点存在 和
,且 ,因此
,
由题图中点坐标可知对应的是,即 。
若溶液只含,溶液中元素与元素的物质的量之比始终为 ,但由于溶液
有额外加入去改变,因此溶液中元素与 元素的物质的量之比并没有始终维持
。
电解质溶液图像——分布分数图像分析
大招20 对应练习
解题觉醒
分析图像:定曲线、读浓度、找交点、可替换。
20.(2023湖北) 为某邻苯二酚类配体,其
,。常温下构建(Ⅲ) 溶液
体系,其中 ,
。体系中含 物种的组分
分布系数 与 的关系如图所示,分布系数
,已知, 。下列
说法正确的是( )
C
A.当时,体系中
B.在之间,含的物种主要为
C.的平衡常数的 约为14
D.当时,参与配位的
【解析】 当 时,
,含 的粒子
在强酸性环境中主要以存在,此时 约
为,因此 ;②常温下
时,; 的
,即 ,可知
,求出溶液中
约为 。由以上分析可知:体系中
。
在 之间,
;
溶液中,,即 时
;同理,即 时,
,据此可以画出 体系的分布系数图
为 ,7.46和12.4取中间
值为,可知附近的分布系数远大于
和,利用守恒可知,此时
(所含 的浓度)
( 所含 的浓
度),可知 的浓
度大于、的浓度,因此 在
之间,含的物种主要为 。
的平衡常数表达式为
,分析题图可知,当 时,
,此时
。时体系中含的物种主要为 ,
考虑有部分结合形成配离子、,此时 可求出近似值约为
;已知 、
,欲求 ,可利用
,将
、 代入计算出
,因此选项所求, 。
当时, ,参与配位
的 。
21.(2024湖南师大附中入学考)在含初始浓度为 的溶液中滴加一定浓
度的氨水,含微粒存在下列转化: ;
。
、、的分布分数 与 的关系如图所示。下列推断
不正确的是( )
已知:的分布分数 。
A.曲线表示与 的关系
B.反应①的平衡常数
C. 点银元素的2个物种浓度相等,均为
D.当 时,含 微粒的主
要存在形式是
【解析】 图像分析较小时,含微粒的主要存在形式是;随着 增大,
先发生反应①生成逐渐减小、 逐渐增大;随着
继续增大,发生反应②生成 逐渐减小、
逐渐增大。
√
识图结果
由上述分析知A项正确。
曲线、相交于点,此时,则 、
,而 的平衡常数
,由 与题给两个反应的
关系可知,,则 。
点时,因同时还存在 ,且加入氨水,溶液体
积增大,结合元素质量守恒可知, 。
分析题图可知,当 时,即时,含 微粒
的主要存在形式是 。
22.(2023河北石家庄质检)已知常温下水溶液中、、、、 的分布分数
随变化曲线如图1;溶液中 和
的关系如图2。用 溶液滴定
溶液,下列说法错误的是( )
D
A.曲线表示
B.的水解平衡常数
C.滴定过程中溶液会变浑浊
D.滴定过程中始终存在:
【解析】 随增大,溶液中、减少, 、
增多, 先增多后减少,结合粒子分布分数的
计算公式可确定题图1中各曲线含义。
由上述分析知A项正确。
时 ,则
。
难溶,滴定过程中会生成 沉淀。
若滴定过程中 不沉淀,则溶液中存在电荷守恒:
,元素质量守恒:
,两式联立得:
,但生成 沉淀。
23.(2023山东潍坊二模,双选)常温下,
用测定溶液中的 时,
含微粒的分布系数及平均配位数
与的关系如图所示。与 的
配合物存在如下平衡:
AD
A.,
B.在点:
C.在点:
D.若点,
。下列说法错误的是( )
【解析】 随着的增大,含 微粒依次发生转
化: 。根据
曲线交点处,相应粒子的浓度相同,可以计算出对应平
衡常数等于对应交点处的值,即 ,
,, 。
由上述分析可知,, 。
在点,, ,则
。
在点, ,平均配位数
,, ,根据电荷
守恒可知, ,
则 ,
。
点时, ,平均配位数
,,, ,结
合电荷守恒可知
,则
,
;
根据、 ,则
,点时,则 ,
,故 。
1.(2020全国Ⅰ)以酚酞为指示剂,用的
溶液滴定未知浓度的二元酸溶液。溶液中, 、
分布系数 随滴加溶液体积 的变化关系如图所示。
[比如的分布系数:
下列叙述正确的是( )
C
A.曲线①代表,曲线②代表
B.溶液的浓度为
C.的电离常数
D.滴定终点时,溶液中
【解析】
2.(2023重庆联考)用一定浓度的 溶液分别滴定体积均
为,浓度均为的、 和
三种溶液,滴定过程中三种溶液的电导率如图所示。
(已知:溶液电导率越大,导电能力越强)下列说法错误的
是( )
D
A.曲线①②③分别代表、和
B.的浓度为
C.、、、四点中, 点水的电离程度最小
D.点对应的溶液中粒子浓度大小关系:
【解析】 三种碱溶液浓度都是 ,
是二元强碱, 是一元强碱,它们均完全电离,
而 是一元弱碱,在溶液中存在电离平衡,因此溶液
中的离子浓度: ,故曲线①②
③分别代表、和 在滴定过程中的电
导率曲线。
曲线①代表在滴定过程中的电导率曲线,点时电导率最小, 点表示的是硫
酸与恰好完全反应,反应为 ,由于二者消
耗的体积相同,二者反应的物质的量之比是,所以的浓度与 相同,均
为 。
点时恰好被中和得到 ,该
盐是强酸弱碱盐,水解使溶液显酸性,水的电离受到促进作
用,点时恰好被中和得到 ,该盐是强酸
强碱盐,不水解,水的电离不受影响,点时 恰好被
完全中和产生, 是强酸强碱盐,不水解,
溶液显中性,水的电离不受影响,点是、
等浓度的混合溶液,过量的酸电离产生 ,使水的电离受到
抑制,所以、、、四点中,水的电离程度点最大, 点
最小。
根据电荷守恒可知溶液中离子浓度关系为
。
3.(2023广东深圳一调)常温下,乙二胺 的水溶液中,
、和的分布分数与 的关
系如图所示。已知: 。
下列说法不正确的是( )
C
A. 溶液显酸性
B.曲线可表示
C.
的平衡常数
D. 溶液中:
【解析】 类比“”,乙二胺可看作二元碱,随着 的减
小,逐渐减少、 先增加后
减少、 逐渐增多。
根据上述分析可知, 是二元弱碱,
属于强酸弱碱盐,
水解使溶液显酸性。
由上述分析知B项正确。
表示 的第一
步电离,则其平衡常数为 。
,
即 的电离程度大于其水解程度(【技法】
可通过最大时对应溶液的 作出判
断),所以 溶液中:
。
4.(图像创新)(2023辽宁)某废水处理过程中始终保
持饱和,即,通过调节 使
和形成硫化物而分离,体系中与 关系
如图所示,为、、和 的浓度,单位为
。已知 ,下列说法正确的是
( )
D
A.
B.③为与 的关系曲线
C.
D.
【解析】 图像读取 方法一
方法二 根据,可得 ,即
,和符合 的函
数关系,同理,, ,
即,和 符合
的函数关系,则④表示与 的关系曲线,③表
示与的关系曲线;根据 ,
可得 ,
,、符合 的
函数关系,同理、符合 的函数关系,
,则对应的轴截距小,②表示与 的关系曲线,
①表示与 的关系曲线。
曲线①和③的交点表示溶液中 ,则有
。
曲线③为与 的关系曲线。
曲线④代表与的关系曲线,由曲线④所给的坐标,可求出 和
,再根据题目已知条件 ,两个坐标选择其中一个即可求出
。
① 利用坐标、 ,
。
②利用坐标、 ,
。
D(√)欲求,需知道相同时和 各是多少,但题图中没有给
出相同下的和,由于题目给出 ,因此可以通过
,将 消掉,再利用曲线③的坐
标以及C选项的来求出 。
①利用坐标 ,
,因此 。
②利用坐标, ,
因此 。
5.(2023湖北武汉调研)常温下,用 盐
酸滴定溶液,溶液中 、
、的分布分数 [已知
随 变化的曲线及滴定曲
线如图。下列说法不正确的是( )
D
A.
B.点溶液中
C.滴定分析时, 点可用甲基橙作指示剂
D.忽略溶液体积变化, 点溶液中
【解析】
加入的盐酸体积为 时,所得溶液中
、、,说明此时
与恰好反应生成和,则 。
,又点时 ,
,则
。
点溶液 ,溶液呈酸性,故可用甲基橙
作指示剂。
点时所加盐酸体积为,溶液总体积为 ,
溶液中, ,
由电荷守恒可得
,点溶液呈酸性, ,则
,又由元素质量守
恒可得
(【点拨】根据点时 判断,在滴定过程中始终有
元素质量守恒关系式
),且 点时
,联立可得
。
6.(图像创新)(2023辽宁本溪高级中学
一模)时,将 气体缓慢通入
的氨水中,溶液的 、体系
中粒子浓度的对数 与反应物的物质
的量之比 的关系如图所
D
A.时,的电离平衡常数为
B.时,
C.所示溶液:
D.所示溶液:
示。若忽略通入气体后溶液体积的变化,下列有关说法错误的是( )
【解析】 抓特殊点 ,分
析题图可知,当溶液
时,
,则
,此时
,故
的电离平衡常数
。
时,溶液中的溶质为等浓度的和 ,分析题图可知此时溶液显
碱性,则一水合氨的电离程度大于铵根离子的水解程度,则此时溶液中的粒子浓度大小
顺序为 。
抓特殊点,所示溶液 ,
则 ,根据
的电离常数
,则
,
故 。
所示溶液中 ,且存在电荷守恒
,因,故 所示溶液中
,故假设错误。
7.(2023河北邯郸二模)某酸溶液中含有
粒子的分布分数与 的变化关系如图所示。下
列说法正确的是( )
C
A.已知亚磷酸的结构为,则可能为
B.向溶液中滴加少量 溶液,发生反应的
离子方程式为
C. 溶液中存在:
D. 溶液中存在:
【解析】 由题图各粒子的分布分数与
的变化关系可知,该酸应该为三元弱酸,亚磷酸的
结构为 ,含有两个羟基,为二元酸,所
以不可能为 。
向溶液中滴加少量 溶液,发生反应
的离子方程式应为 。
方法一 分析题图可知, 点时,
,所以 的电离常数
, 点时,
,则 ;
在 溶液中,存在电离平衡和水解平衡,
的水解常数
, ,则有
。
方法二 分析题图可知,溶液中 最大时,
溶液的为,溶液呈碱性,说明 的
水解程度大于电离程度,则有
。
全部是离子,找电荷守恒,在 溶液中,
存在电荷守恒:
。
8.(2023山东临沂检测)常温下,向一定浓度溶液中加入 ,保持溶液体
积和温度不变,测得与为、、 变化如图所示。下
列说法错误的是( )
A
A.常温下,
B. 点溶液中:
C. 溶液中:
D.点溶液中:
【解析】 向一定浓度溶液中加入 固体,
随着增大,减小、 减小、
增大,则 增大,
减小。
增大,则减小。又
,
则与呈线性关系,故曲线 表示
,曲线表示,曲线 表
示 。
,
,则
。
点溶液中 ,题给式子可
变形为
,
全部是离子,找电荷守恒,由电荷守恒有
,
则 。
第一步:先考虑出现的 粒子,强电解质拆成离 子,弱电解质不拆 先出现的是,是强电解质,拆成和
第二步:比粒子的个 数,此时不考虑水解和 电离 和的个数比为,可以判断出
第三 步:考 虑粒子 的电离 和水解 ① (主)
② (
,即 的电离
程度大于其水解程度)
的电离程度大于其水解程度,故( ,又水解、电
离的程度都很微弱,因此溶液最终微粒浓度大小顺序为
点时,溶液,溶液呈酸性,且
(【点拨】点对应 ,此时
续表
),则由电荷守恒
得
。
9.(2023湖北华中师大一附中测试)溶洞水体中的 与
空气中的保持平衡,水体中为、 、
或与 的关系如图所示。已知
,下列说法错误的是( )
D
A.
B.Ⅱ代表与 的关系曲线
C.
D.点溶液中,
【解析】 溶洞水体中的与空气中的 保持平衡,
故可认为保持不变,随着 增大,溶液碱性增强,
、的浓度增大,较小时 ,
较大时,故Ⅰ为与 的关系
曲线,Ⅱ为与的关系曲线,随着 增大,
减小,Ⅲ为与 的关系曲线。
由点,得 ,
由点得 ,
。
点时,,则,, 。
点溶液中,, ,则由
可求得 点
,
。
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
同课章节目录
