沉淀溶解平衡 -2025年高考化学考向分析(共88张PPT)
文档属性
| 名称 | 沉淀溶解平衡 -2025年高考化学考向分析(共88张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 10.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-27 00:00:00 | ||
图片预览








文档简介
(共88张PPT)
2025年高考化学考向分析
沉淀溶解平衡
沉淀溶解平衡及其影响因素
1.(生活情境)(2023山东青岛期末)牙釉质的主要成分为羟基磷酸钙 ,
在牙齿表面存在着如下平衡:
,已知
的 。下列说法错误的是( )
C
A.残留在牙齿上的糖会发酵产生 ,使羟基磷酸钙沉淀溶解平衡右移,破坏牙釉质
B.按时刷牙可减少食物残留,从而减少有机酸的产生,防止腐蚀牙齿
C.用含 的溶液漱口,可使平衡左移,保护牙齿
D.含氟牙膏使转化为更难溶的 ,促进牙齿表面矿物质的沉积,
修复牙釉质
【解析】 残留在牙齿上的糖会发酵产生,则将消耗,导致 减小,
使羟基磷酸钙沉淀溶解平衡右移,破坏牙釉质。
由A项分析可知,按时刷牙可减少食物残留,从而减少有机酸的产生,防止腐蚀牙
齿。
碱性太强,具有强腐蚀性,不能用含 的溶液漱口,否则将腐蚀口腔等
组织。
,含氟牙膏使 转化为更难溶的
,促进牙齿表面矿物质的沉积,修复牙釉质。
2.(2023天津中学期末)把足量熟石灰放入蒸馏水中,一段时间后达到平衡:
。下列叙述正确的是( )
D
A.给溶液加热,溶液的 升高
B.恒温下向溶液中加入,溶液的 升高
C.向溶液中加入溶液, 固体增多
D.向溶液中加入少量的固体, 固体增多
【解析】 氢氧化钙的溶解度随温度的升高而降低,所以给溶液加热,溶液的 降
低。
温度不变,溶解度不变,饱和溶液的 不变。
向溶液中加入溶液,能和反应生成 白色沉淀,
被消耗而减少。
向溶液中加入少量的固体, 的浓度增大,氢氧化钙的溶解平衡逆向移
动, 固体增多。
3.(2024浙江宁波九校联考)某温度下向含固体的 饱和溶液中加少量稀盐酸,
下列说法正确的是( )
C
A.的溶解度、均减小 B.的溶解度、 均不变
C.的溶解度减小、不变 D.的溶解度不变、 减小
【解析】 在含固体的 饱和溶液中存在沉淀溶解平衡:
,当加入少量稀盐酸时, 增大,平衡逆向移动,饱
和溶液中的减小,即溶解的质量减小、溶解度减小;的 只受温度影
响,温度不变,的 不变。
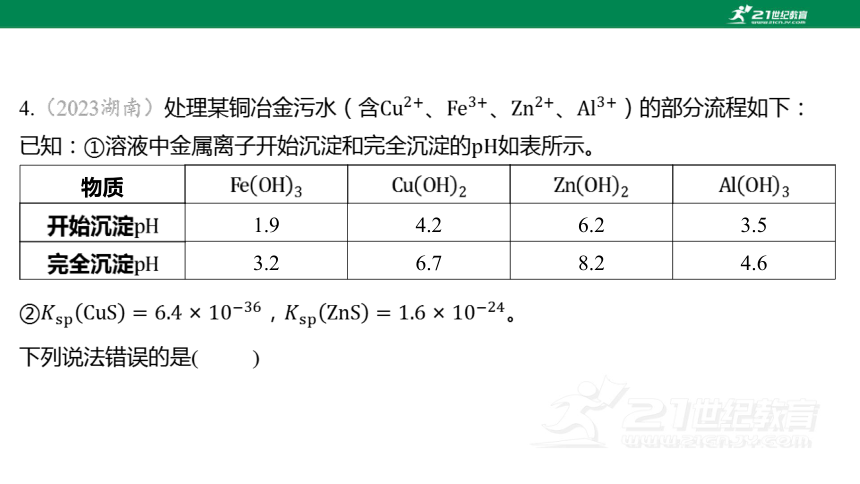
4.(2023湖南)处理某铜冶金污水(含、、、 )的部分流程如下:
已知:①溶液中金属离子开始沉淀和完全沉淀的 如表所示。
物质
开始沉淀 1.9 4.2 6.2 3.5
完全沉淀 3.2 6.7 8.2 4.6
, 。
下列说法错误的是( )
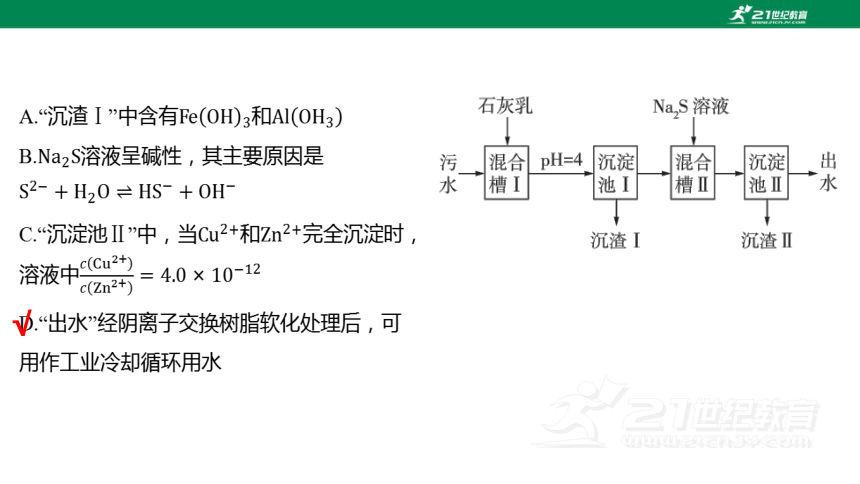
A.“沉渣Ⅰ”中含有和
B. 溶液呈碱性,其主要原因是
C.“沉淀池Ⅱ”中,当和 完全沉淀时,
溶液中
D.“出水”经阴离子交换树脂软化处理后,可
用作工业冷却循环用水
√
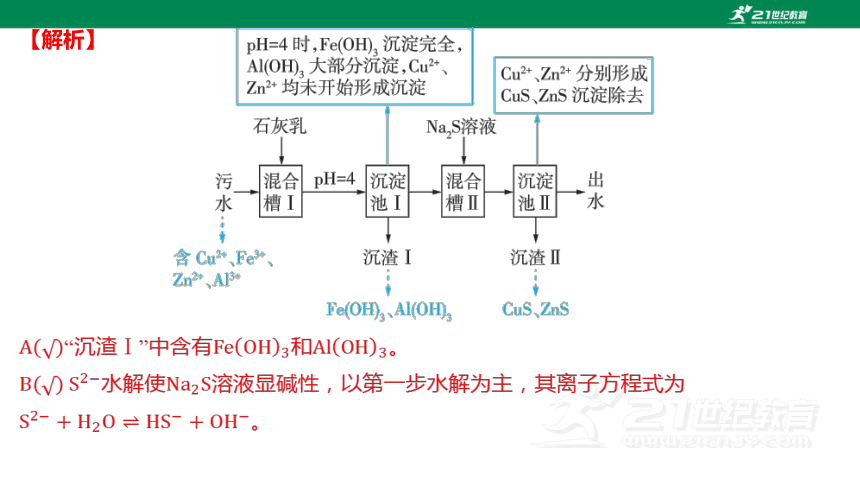
【解析】
.
“沉渣Ⅰ”中含有和 。
水解使 溶液显碱性,以第一步水解为主,其离子方程式为
。
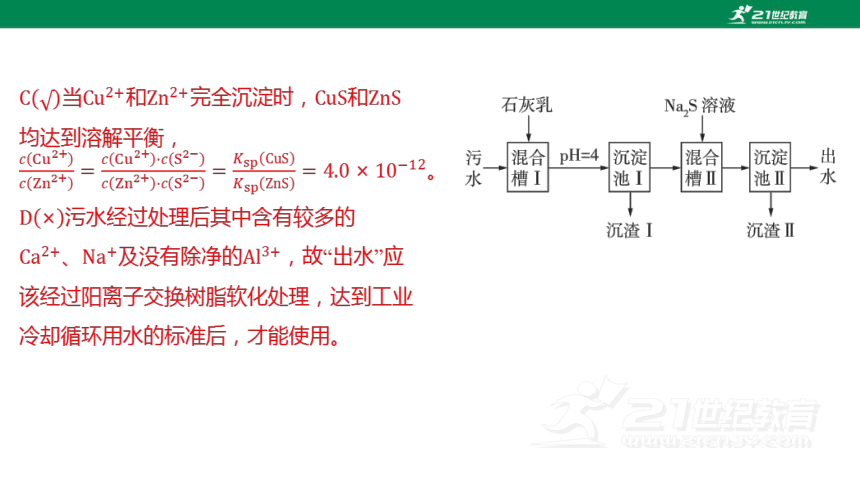
当和完全沉淀时,和
均达到溶解平衡,
。
污水经过处理后其中含有较多的
、及没有除净的 ,故“出水”应
该经过阳离子交换树脂软化处理,达到工业
冷却循环用水的标准后,才能使用。
5.已知常温下,几种难溶电解质的溶度积 如表所示,下列说法不正确的是( )
化学式
溶度积
B
A.在的悬浊液中加入少量固体, 增大
B.在的悬浊液中加入溶液后,不可能转化为
C.溶液中混入了一定量,可以通过向溶液中加入 的方法调节
溶液的,除去
D.向含一定浓度的和的溶液中加过量 溶液,完全反应后过滤,滤液中
【解析】 的悬浊液中存在沉淀溶解平衡:
,加入少量固体,与 反应生成
,溶液中浓度降低,促使溶解平衡正向移动, 增大。
在的悬浊液中加入溶液后,若溶液中 浓度够大,能使
,则可以转化为 。(【警示】对于难
溶电解质的相互转化,通常都是由溶度积大的向溶度积小的转化,但是对于溶度积相差
不大的,一定条件下,溶度积小的也可能向溶度积大的转化)
由题给数据知,完全沉淀时 ,此时
,不会形成沉淀,故向溶液中加入
调节溶液的,可达到除去溶液中的 杂质的目的。
加入过量溶液,则和都沉淀完全,过滤后的滤液为 和
的饱和溶液,、 均达到溶解平衡,故
。
6.(2024湖北部分学校联考,双选)分别进行下列操作,由现象得出的结论正确的是
( )
选项 操作 现象 结论
A 将稀硫酸和 反应生成的气体通入含 的 悬浊液中 出现黑色沉淀
B 向盛有 溶液的试 管中滴加 溶液,再 向其中滴加滴 溶液 先有白色沉淀生成,后又产生黄色沉淀
C 向悬浊液中滴入少量 溶液 固体变黑
D 将气体通入浓度均为 的 和 溶液中 先出现 黑色沉淀
【解析】 稀硫酸和反应生成的气体为,将通入含的 悬浊液
中,电离出的会直接和生成黑色的 沉淀,不能判断是否发生沉淀转
化,因此无法判断与 的大小。
向盛有溶液的试管中滴加 溶液,
并没有完全沉淀,因此再加入溶液,直接与 反应,没有发生沉淀转化,
因此无法判断与 的大小关系。
悬浊液表示已经达到饱和,向其中滴入少量 溶液,固体变黑,说明发
生沉淀转化:,可推知 。
溶解度小的物质先沉淀,由实验现象可知,溶解度小于;由于和 是
同类型的难溶电解质(都是型),因此溶解度小的也小, 。
沉淀溶解平衡图像
7.(2021全国甲)已知相同温度下, 。某温度下,饱和溶液
中、与 的关系如图所示。下列说法正确的是
( )
B
A.曲线①代表 的沉淀溶解曲线
B.该温度下的值为
C.加适量固体可使溶液由点变到 点
D. 时两溶液中
【解析】
结合上述分析,可知曲线①代表 的沉淀溶
解曲线,曲线②代表 的沉淀溶解曲线。
根据曲线①上横纵坐标均为5.0的点可知,溶解
平衡体系中 ,
则该温度下 。
加适量固体,溶液中 增大,由于温
度保持不变,即溶液中减小,可使溶液由 点
向 点移动。
当时, 点平衡时
, 点平衡时
,即两溶液中
。
8.(2022海南,双选)某元素的氢氧化物 在
水中的溶解反应为 、
。,
与的关系如图所示,为或 浓度的值。
下列说法错误的是( )
BD
A.曲线①代表与 的关系
B.的约为
C.向的溶液中加入 溶液至
,体系中元素主要以 存在
D.向 的溶液中加入等体积
的后,体系中元素主要以 存在
【解析】
由图像分析可知,曲线①代表与 的关系。
根据图像可知,时,,即 时,
,因此的 。
向的溶液中加入溶液至 ,根据图像分析可
知,时溶液中的、浓度均极小,则体系中元素 主要以
存在。
分析题图可知,当即 时,
,,即约为 。加入等体
积的后,先与反应,最后的依然大于, 大于
14,故反应后体系中元素主要还是以 存在。
9.(2023全国乙)一定温度下,和 的沉淀溶解平衡曲线如图所示。
下列说法正确的是( )
C
A.点条件下能生成 沉淀,也能生
成 沉淀
B.点时, ,
C. 的平衡
常数
D.向、均为 的混
合溶液中滴加溶液,先产生
沉淀
. .
.
【解析】
点位于和 沉淀溶解平衡曲
线的右上方,由上述分析知越往上、越往右
离子浓度越小,则点的离子积 必小于
或,因此 点不会有沉
淀生成。
由上述分析可知,
、
, 只与温度有关而与浓
度无关,因此点两者的 不相等。
的平衡
常数表达式为 ,将该表达式转
化为和两种难溶物溶度积有关的式子:
。
该混合溶液中形成 沉淀所需的
,
形成 沉淀所需的
,形成 所
需的较小,所以先产生 沉淀。
10.(2023新课标)向饱和溶液(有足量 固
体)中滴加氨水,发生反应
和 。
与 的关
系如图所示{其中代表、、 或
。
下列说法错误的是( )
A
A.曲线Ⅰ可视为溶解度随 浓度变化曲线
B.的溶度积常数
C.反应的平衡常数的值为
D.时,溶液中
【解析】
.
随着逐渐增大,结合 形成和,而 减
小会促使 平衡正向移动,增大溶解度的同时也增大了
浓度,溶解多少 溶液就会增加多少,因此 的溶解度曲线应与 的曲线吻
合,应该为曲线Ⅳ。
分析题图可知, 时,
、
,则 的溶度积常数
。
分析题图可知, 时,溶
液中和 的浓度分别为
和 ,则
的平
衡常数 。
分析题图可知, 时,溶
液中 。
11.(2023全国甲)如图所示为、和 在水中达沉淀溶解平衡时
的关系图{;可认为 离子沉
淀完全}。下列叙述正确的是( )
C
A.由点可求得
B.时 的溶解度为
C.浓度均为的和 可通过
分步沉淀进行分离
D.、 混合溶液中
时,二者不会同时沉
淀
【解析】 由点 可知,此时
,即
; ,
,则
(【提醒】题目没有
特别说明时,默认温度为 ),因此
。
方法一 由线上的点 可知,此时
, ,则
,因此,可知时
的溶解度为 。
方法二 由线上的点 可知,此时
,,即
时的溶解度为 。
分析题图可知, 约为2.8时,
,即 完全沉淀,
而此时 尚未开始沉淀,因此可通过调节溶
液的方法分步沉淀和 。
当时 完全沉
淀,分析题图可知此时约为 ,且
,此时 已经开始
沉淀了,选项中
,即
,会有
沉淀出现,因此、 可以同时沉淀。
12.(2023北京)利用平衡移动原理,分析一定温度下在不同的 体系中
的可能产物。
已知:①图1中曲线表示体系中各含碳粒子的物质的量分数与 的关系。
②图2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子
浓度关系符合[注:起始 ,
不同下 由图1得到]。
图1
图2
下列说法不正确的是( )
A.由图1,,
B.由图2,初始状态、 ,无沉淀生成
C.由图2,初始状态、 ,平衡后溶液中存在
D.由图1和图2,初始状态、 ,发生反应:
C
【解析】 分析题图1可知,时,与 物质的量分数相等,在同
一溶液中物质的量浓度也相等,即 。
分析题图2可知,初始状态、 对应的点在题图2中
和 的溶解平衡曲线下方,溶液中离子浓度偏小,此时
且,因此不会生成 或
沉淀。
分析题图2可知,、 对应的点位于曲线Ⅱ的上方,会生成
沉淀,根据元素质量守恒,溶液中
。
分析题图1可知,时,溶液中主要含碳微粒是 ;分析题图2可知,
、对应的点位于曲线Ⅱ的上方,会生成 沉淀,因此反应
的离子方程式为 。
13.(2022湖南)室温时,用的标准 溶
液滴定浓度相等的、和 混合溶液,通过电位
滴定法获得与 的关系曲线如图所示[忽略
沉淀对离子的吸附作用。若溶液中离子浓度小于
时,认为该离子沉淀完全。
, ,
]。下列说法正确的是( )
C
A.点:有白色沉淀生成 B.原溶液中的浓度为
C.当沉淀完全时,已经有部分沉淀 D.点:
【解析】 由于、、 是同类型的难溶电解质[都是
, 越小,在水中的溶解度也越小。
向浓度相等的、和 混合溶液中滴加硝酸银溶液,三种
离子沉淀的先后顺序为、、 。
先沉淀,是黄色的,所以点有黄色沉淀 生成。
当滴入硝酸银溶液时, 发生突变,说明
此时、、 沉淀完全,此时共消耗硝酸银的物质的量为
,又原溶液中、、 浓度相等,
则、和 均为
,故的浓度为 。
当沉淀完全时浓度为 ,溶液
中的
,
产生 沉淀的最小
,随着滴定的
进行,溶液体积增大,当完全沉淀时,加入 溶液的
体积小于 ,则混合液中
,故此时已经有部分 沉淀。
点加入了过量的硝酸银溶液,浓度最大;在 浓
度相同的条件下,越大,对应的阴离子浓度也越大,因此
点各离子浓度的大小顺序为 。
14.(2022山东)工业上以为原料生产 ,对其工艺条件进行研究。现有
含的、溶液,含的 、
溶液。在一定范围内,四种溶液中随 的变化关系如
图所示。下列说法错误的是( )
D
A.反应 的平衡常数
B.
C.曲线④代表含的 溶液的变化曲
线
D.对含且和初始浓度均为
的混合溶液, 时才发生沉淀转化
【解析】
反应 的平衡常数
。
由分析可知,曲线①代表含固体的 溶液的变化曲线,则
的溶度积 。温度不变,溶
度积不变,则溶液为7.7时,曲线②的 ,此时
,则 。
由图像分析可知,曲线④表示含固体的 溶液的变化曲线。
由图像分析可知,含且和初始浓度均为 的混合
溶液分别对应曲线②和曲线④,由曲线交点可知,当 时即可发生沉淀
转化。
的相关计算
15.(2023河南焦作期末)已知, ,
。某溶液中含有、和,浓度均为 ,
向该溶液中逐滴加入的 溶液时,三种阳离子产生沉淀的先后顺序为
( )
A
A.、、 B.、、
C.、、 D.、、
【解析】 根据溶度积的定义可知,三种离子沉淀时分别有
, ,
,溶液中、、的浓度均为 ,
则向该溶液中逐滴加入溶液产生沉淀时,所需 分别为
、 、
,所需 越小越先沉淀,所以这三种离子产生沉
淀的先后顺序为、、 。
16.(2023重庆名校联考)
(1) 工业上利用含的废液制备时,废液中除含 外,主要还含
、 等杂质离子,可以将杂质离子转化为相应氟化物沉淀而除去。写出加入
最先除去的杂质的离子方程式:________________________________________
[已知:; ;
。
(2) 已知:,,向 溶液中加入
和,当两种沉淀共存时, ___________。
(3) 已知在时,。时,向
溶液中加入固体,如要生成沉淀,则溶液的 最小是____[已知:
,, 。
9.2
【解析】 (1)、的组成类型相同,且,故 先将
废液中的转化为 沉淀而除去,离子方程式为
。(2)体系中存在、 沉淀,即
、 均处于沉淀溶解平衡状态,则
。(3)沉淀的 最小
最大最小最大,即刚开始沉淀时的 最小。当
时, ,则
,故, 。
17.(1) 在化学分析中采用为指示剂,以标准溶液滴定溶液中的 ,利
用与生成砖红色沉淀,指示到达滴定终点。当溶液中 恰好沉淀完全
(浓度等于时,溶液中为___________ ,此时溶液
中等于___________(已知、的分别为 和
)。
(2) (2021海南) 时,潮湿的石膏雕像表面会发生反应:
,其平衡常数 _______[已知
, 。
3 250
(3) 和 都是锂离子电池的
电极材料,可利用钛铁矿(主要成分为
,还含有少量、 等杂质)来
制备。工艺流程如下:
若“滤液②”中 ,加入
【答案】 恰好沉淀完全时,
, ,因此不会生成
沉淀
双氧水和磷酸(设溶液体积增加1倍),使 恰好沉淀完全即溶液中
,此时是否有 沉淀生成?(列式计算)。
、的分别为、 。
【解析】 (1)根据溶度积计算:
,故
。
(2)已知 ,
,
则该反应的 。
18.(1) 用废电池的锌皮制备 的过程中,需除去锌皮中的少量杂质铁:
化合物
近似值
其方法是:加稀和溶解,铁变为______,加碱调节至 为____时,铁刚好
沉淀完全(离子浓度小于 时,即可认为该离子沉淀完全);继续加碱至
为___时,锌开始沉淀(假定浓度为)。若上述过程不加 的后
果是____________________,原因是___________________________。
2.7
6
和分离不开
和的相近
(2) (2020全国Ⅲ改编)常温下,溶液中金属离子开始沉淀和完全沉淀的 如表所示。
金属离子
开始沉淀时的 7.2 3.7 2.2 7.5
沉淀完全时的 8.7 4.7 3.2 9.0
利用上述表格数据,计算的 _________________(列出计算式)。如果“转
化”后的溶液中浓度为,则“调”应控制的 是____。
6.2
(3) (2020山东改编)时相关物质的 如表所示。
物质
使用氨水调溶液的,使和完全沉淀,则 的理论最小值为____(当溶液中
某离子浓度 时,可认为该离子沉淀完全)。
4.9
【解析】 (1)锌皮中的少量杂质铁与稀反应生成,再被 氧化:
,最后变为。给出氢氧化物的 ,求阳离
子完全沉淀所需的 ,可以按照三步快速解出:
的, 时,求出
;
② ;
③常温下,,因此 。
浓度为,调节至 开始沉淀,此时符合
,可以按照三步快速解出:
①的, ,求出
; ;
③常温下,,因此 。
酸性条件下被氧化为,再通过调节溶液的可使、 两种元素分别以
和形式分离开来,若不加,由数据可知和的
近似值相同,因此会在相同 时一起沉淀,而无法达到分离的目的。
(2)本题有两组数据可以计算出的 。
数据开始沉淀时的为 ,可知
, ,
的 。
数据完全沉淀时的为 ,可知
, ,
的 。
已经求出的,当浓度为,欲求溶液的 ,可以按照三步快
速解出:
①的 ,
,求出 ;
② ;
③常温下,,因此 。
(3)和都属于型的难溶电解质, 表达式皆为
,因此越小溶解度越小,在 逐渐升高的过程中越优先沉淀。由数
据可知,,因此溶解度也是, 完全沉
淀时也必将完全沉淀。欲使和完全沉淀,则只需要计算使 完全沉淀时
溶液对应的即可。已知的,当浓度为 ,欲求溶液
的 ,可以按照三步快速解出:
的, ,求
出 ;
;
③常温下,,因此 。
当调节至,则和 皆完全沉淀。
1.(2023北京东城区综合练习)室温下,时刻向两个盛有 蒸馏水的烧杯中分别
加入、 蔗糖,搅拌,最终分别得到悬浊液和澄清溶液,溶解过程中分
散系的导电能力变化如图。
下列分析不正确的是( )
B
A.该实验可证明蔗糖不是电解质
B.该实验可证明碳酸钙是强电解质
C.当①中导电能力不变时,
达到平衡
D.时刻,①中再加 ,导电能力不变
【解析】 蔗糖溶解过程中分散系的导
电能力基本不变,说明蔗糖为非电解质。
由题图知,溶于水的碳酸钙发生了电离,
但不能判断其是否完全电离,故不能证明碳
酸钙属于强电解质。
碳酸钙溶解过程中分散系的导电能力增
强,当导电能力不变时,说明
达到平衡。
时刻,①中碳酸钙在水中已达到溶解平衡,再加 碳酸钙,溶液中的离子浓度
不变,导电能力不变。
2.(2023广东深圳二调)室温下,以氟磷灰石 为原料,经酸浸、转化可得
到、和。已知:,的、 、
。下列说法不正确的是( )
B
A. 的沉淀溶解平衡可表示为
B.酸浸过程中溶液时,
C. 溶液中存在:
D.向溶液中加入少量水稀释时, 的值增大
【解析】 氟磷灰石 在溶液中存在沉淀溶解平衡,可表示为
。
在溶液中分三步电离:, ,
,,, 。
时,由可知, ,
。
方法一 溶液中,根据电荷守恒可得:
,根据元素质量守恒
可得: ,两式联立消去
可得: 。
方法二 含与且不含、 等不水解的离子找质子守恒。
溶液中存在电离平衡:, ,向
溶液中加入少量水稀释时,由于为定值,减小,则 增大,
即 的值增大。
3.下列说法正确的是( )
选项 实验 现象 结论
A 向2支盛有 相同浓度银氨溶液的试管中 分别加入2滴相同浓度的和 溶液 一支试管中产生黄色 沉淀,另一支中无明 显现象
B 室温下,向浓度均为的 和 混合溶液中滴加 溶液 出现白色沉淀
C 将 溶液滴入 溶液 至不再有沉淀产生,再滴加 溶液 先有白色沉淀生成, 后变为浅蓝色沉淀 的溶度积比 的大
D 将稀硫酸与 反应产生的气体不断通入 与 的浊液中 白色沉淀逐渐变为黑 色沉淀
A
【解析】 根据题中描述可知黄色沉淀为 ,另一支试管中无明显现象,说明没有
析出,证明 。
和均为白色沉淀,根据该实验现象不能判断出二者的 的相对大小
关系。
对于组成类似(阴、阳离子个数比相同)的难溶电解质,溶度积大的易转化为溶
度积小的。
稀硫酸与反应可产生,通入与 的浊液中,虽然白色沉淀变成黑
色沉淀,但因溶液中存在,也可与 反应产生沉淀,不能说明
。
4.(2023湖北武汉部分学校调研)常温下,用
的溶液滴定 未知浓度的
溶液。溶液电导率、随滴入
溶液体积 的变化关系如图所示。
下列叙述错误的是( )
D
A.当时,溶液中的溶质为
B.该溶液的物质的量浓度是
C.该温度下的溶度积常数
D.当 时,溶液中
【解析】 随着的加入,发生反应:,
减小,增大;随着 的加入,溶液体积增大,溶液中离子浓度减小,
电导率先减小,当反应完全时,电导率达到最小值,再加 溶液,溶液中离
子浓度增大,电导率逐渐增大。
5.(2023河北石家庄期末检测)时,向的 溶液中通入氨气,
测得溶液的与 之间的变化曲线如图所示[已知:
,, ,忽略反应过程
中溶液体积的变化]。下列说法正确的是( )
C
A.的数量级是
B.点溶液中会产生 沉淀
C. 点溶液中存在:
D.点溶液中存在:
【解析】
6.(2023山东历城二中期末)常温下,将 粉
末置于盛有 蒸馏水的烧杯中,然后向烧杯中加入
固体(忽略溶液体积的变化)并充分搅拌,该过程
中几种离子的浓度变化曲线如图所示,下列说法不正确的
是( )
C
A.反应 的
B.相同温度下,在水中和在溶液中的 不变
C.曲线代表 浓度变化
D.锅炉水垢中的可先用溶液处理,使
转化为 后,再用酸除去
【解析】 .
反应 的
。
B(√) 只与温度有关,而与溶剂无关,故相同温度
下,在水中和在溶液中的 不变。
曲线代表 浓度变化。
锅炉水垢中的 微溶于水,不溶于酸,可根据沉
淀溶解平衡,先用溶液处理,使 转化为
,弃去沉淀转化后的溶液,再向其中加入盐酸,发
生反应: ,达到除
去锅炉水垢的目的。
7.(2023河北衡水中学模拟)时,和
的沉淀溶解平衡曲线如图所示。已知:
,,其中为
或 。下列说法正确的是( )
D
A.曲线Ⅰ代表 的沉淀溶解平衡曲线
B.点:,点:
C.点对应的溶液为过饱和溶液,有 沉
淀析出
D. 时,
的平
衡常数
【解析】 图像分析根据 的沉淀溶解平衡可
知, ,同理
;分析题图可知,斜率:
曲线Ⅰ Ⅱ,则曲线Ⅰ、Ⅱ分别代表、 的沉
淀溶解平衡曲线;
,
即 ,
,即 。
曲线Ⅰ代表 沉淀溶解平衡曲线。
根据图像可知,横轴和纵轴均表示浓度的负对数,
离子浓度越大,其负对数越小, 点:
。
点对应的溶液中, ,
则点对应的 溶液为不饱和溶液,溶液中没
有 析出。
的平衡常数 。
8.(方式创新·学科融合)(2023山东烟台二模)已知
、 。常温下,
难溶物 在不同浓度盐酸(足量)中恰好不再溶解时,
测得混合液中与 的关系如图所示。下列说
法错误的是( )
B
A.约为
B.点对应溶液中:
C.点对应溶液中:
D.直线上任一点均满足:
【解析】
. .
.
9.(生态环保)(2022全国乙)废旧铅蓄电
池的铅膏中主要含有、、 和
,还有少量、、 的盐或氧化物等,
为了保护环境、充分利用铅资源,通过下图
流程实现铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质
一定条件下,一些金属氢氧化物沉淀时的 如表所示:
金属氢氧化物
开始沉淀的 2.3 6.8 3.5 7.2
完全沉淀的 3.2 8.3 4.6 9.1
回答下列问题:
(1) 在“脱硫”中 转化反应的离子方
程式为_________________________________
______________________________,用沉淀
溶解平衡原理解释选择 的原因
____________________________________________________________________________________________________________________ 。
该反应的 ,
反应正向进行的程度很大,可以进行到底
(2) 在“脱硫”中,加入 不能使铅膏中
完全转化,原因是 ____________________________________________________________________________________________________________________________ 。
反应 的
,
反应正向进行的程度很小
(3) 在“酸浸”中,除加入醋酸,还要加入 。
(ⅰ) 能被 氧化的离子是______;
(ⅱ) 促进了金属在醋酸中转化为 ,其化学方程式为________________
_______________________;
(ⅲ) 也能使转化为, 的作用是__________。
作还原剂
(4) “酸浸”后溶液的约为 ,滤渣的
主要成分是__________________。
、
(5) “沉铅”的滤液中,金属离子有
____________。
、
【解析】 加入使 转化为
,便于后续的酸浸;通过酸浸,
铅元素全部转化为可溶性的 ,过滤
后在滤液中加入溶液,使 转化
为,加热分解得到 。
(1)的远小于的,易发生生成 的沉淀转化,且进行较为彻底。
(2)的大于的,生成 的沉淀转化的反应进行的程度也很小。
(3)(ⅰ)具有还原性,能被氧化;(ⅱ)能氧化,使其转化成,
再与结合生成 ,依据氧化还原反应的规律,即可写出反应的化学方程
式;(ⅲ)通过与、反应转化为,发生氧化还原反应, 化合价降
低, 作还原剂。(4)根据题给信息,
当时,、 完全转化为
、。(5)加入 溶液,
发生沉铅的反应为
,
故滤液中含有的金属离子有 以及未沉淀
的 。
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
2025年高考化学考向分析
沉淀溶解平衡
沉淀溶解平衡及其影响因素
1.(生活情境)(2023山东青岛期末)牙釉质的主要成分为羟基磷酸钙 ,
在牙齿表面存在着如下平衡:
,已知
的 。下列说法错误的是( )
C
A.残留在牙齿上的糖会发酵产生 ,使羟基磷酸钙沉淀溶解平衡右移,破坏牙釉质
B.按时刷牙可减少食物残留,从而减少有机酸的产生,防止腐蚀牙齿
C.用含 的溶液漱口,可使平衡左移,保护牙齿
D.含氟牙膏使转化为更难溶的 ,促进牙齿表面矿物质的沉积,
修复牙釉质
【解析】 残留在牙齿上的糖会发酵产生,则将消耗,导致 减小,
使羟基磷酸钙沉淀溶解平衡右移,破坏牙釉质。
由A项分析可知,按时刷牙可减少食物残留,从而减少有机酸的产生,防止腐蚀牙
齿。
碱性太强,具有强腐蚀性,不能用含 的溶液漱口,否则将腐蚀口腔等
组织。
,含氟牙膏使 转化为更难溶的
,促进牙齿表面矿物质的沉积,修复牙釉质。
2.(2023天津中学期末)把足量熟石灰放入蒸馏水中,一段时间后达到平衡:
。下列叙述正确的是( )
D
A.给溶液加热,溶液的 升高
B.恒温下向溶液中加入,溶液的 升高
C.向溶液中加入溶液, 固体增多
D.向溶液中加入少量的固体, 固体增多
【解析】 氢氧化钙的溶解度随温度的升高而降低,所以给溶液加热,溶液的 降
低。
温度不变,溶解度不变,饱和溶液的 不变。
向溶液中加入溶液,能和反应生成 白色沉淀,
被消耗而减少。
向溶液中加入少量的固体, 的浓度增大,氢氧化钙的溶解平衡逆向移
动, 固体增多。
3.(2024浙江宁波九校联考)某温度下向含固体的 饱和溶液中加少量稀盐酸,
下列说法正确的是( )
C
A.的溶解度、均减小 B.的溶解度、 均不变
C.的溶解度减小、不变 D.的溶解度不变、 减小
【解析】 在含固体的 饱和溶液中存在沉淀溶解平衡:
,当加入少量稀盐酸时, 增大,平衡逆向移动,饱
和溶液中的减小,即溶解的质量减小、溶解度减小;的 只受温度影
响,温度不变,的 不变。
4.(2023湖南)处理某铜冶金污水(含、、、 )的部分流程如下:
已知:①溶液中金属离子开始沉淀和完全沉淀的 如表所示。
物质
开始沉淀 1.9 4.2 6.2 3.5
完全沉淀 3.2 6.7 8.2 4.6
, 。
下列说法错误的是( )
A.“沉渣Ⅰ”中含有和
B. 溶液呈碱性,其主要原因是
C.“沉淀池Ⅱ”中,当和 完全沉淀时,
溶液中
D.“出水”经阴离子交换树脂软化处理后,可
用作工业冷却循环用水
√
【解析】
.
“沉渣Ⅰ”中含有和 。
水解使 溶液显碱性,以第一步水解为主,其离子方程式为
。
当和完全沉淀时,和
均达到溶解平衡,
。
污水经过处理后其中含有较多的
、及没有除净的 ,故“出水”应
该经过阳离子交换树脂软化处理,达到工业
冷却循环用水的标准后,才能使用。
5.已知常温下,几种难溶电解质的溶度积 如表所示,下列说法不正确的是( )
化学式
溶度积
B
A.在的悬浊液中加入少量固体, 增大
B.在的悬浊液中加入溶液后,不可能转化为
C.溶液中混入了一定量,可以通过向溶液中加入 的方法调节
溶液的,除去
D.向含一定浓度的和的溶液中加过量 溶液,完全反应后过滤,滤液中
【解析】 的悬浊液中存在沉淀溶解平衡:
,加入少量固体,与 反应生成
,溶液中浓度降低,促使溶解平衡正向移动, 增大。
在的悬浊液中加入溶液后,若溶液中 浓度够大,能使
,则可以转化为 。(【警示】对于难
溶电解质的相互转化,通常都是由溶度积大的向溶度积小的转化,但是对于溶度积相差
不大的,一定条件下,溶度积小的也可能向溶度积大的转化)
由题给数据知,完全沉淀时 ,此时
,不会形成沉淀,故向溶液中加入
调节溶液的,可达到除去溶液中的 杂质的目的。
加入过量溶液,则和都沉淀完全,过滤后的滤液为 和
的饱和溶液,、 均达到溶解平衡,故
。
6.(2024湖北部分学校联考,双选)分别进行下列操作,由现象得出的结论正确的是
( )
选项 操作 现象 结论
A 将稀硫酸和 反应生成的气体通入含 的 悬浊液中 出现黑色沉淀
B 向盛有 溶液的试 管中滴加 溶液,再 向其中滴加滴 溶液 先有白色沉淀生成,后又产生黄色沉淀
C 向悬浊液中滴入少量 溶液 固体变黑
D 将气体通入浓度均为 的 和 溶液中 先出现 黑色沉淀
【解析】 稀硫酸和反应生成的气体为,将通入含的 悬浊液
中,电离出的会直接和生成黑色的 沉淀,不能判断是否发生沉淀转
化,因此无法判断与 的大小。
向盛有溶液的试管中滴加 溶液,
并没有完全沉淀,因此再加入溶液,直接与 反应,没有发生沉淀转化,
因此无法判断与 的大小关系。
悬浊液表示已经达到饱和,向其中滴入少量 溶液,固体变黑,说明发
生沉淀转化:,可推知 。
溶解度小的物质先沉淀,由实验现象可知,溶解度小于;由于和 是
同类型的难溶电解质(都是型),因此溶解度小的也小, 。
沉淀溶解平衡图像
7.(2021全国甲)已知相同温度下, 。某温度下,饱和溶液
中、与 的关系如图所示。下列说法正确的是
( )
B
A.曲线①代表 的沉淀溶解曲线
B.该温度下的值为
C.加适量固体可使溶液由点变到 点
D. 时两溶液中
【解析】
结合上述分析,可知曲线①代表 的沉淀溶
解曲线,曲线②代表 的沉淀溶解曲线。
根据曲线①上横纵坐标均为5.0的点可知,溶解
平衡体系中 ,
则该温度下 。
加适量固体,溶液中 增大,由于温
度保持不变,即溶液中减小,可使溶液由 点
向 点移动。
当时, 点平衡时
, 点平衡时
,即两溶液中
。
8.(2022海南,双选)某元素的氢氧化物 在
水中的溶解反应为 、
。,
与的关系如图所示,为或 浓度的值。
下列说法错误的是( )
BD
A.曲线①代表与 的关系
B.的约为
C.向的溶液中加入 溶液至
,体系中元素主要以 存在
D.向 的溶液中加入等体积
的后,体系中元素主要以 存在
【解析】
由图像分析可知,曲线①代表与 的关系。
根据图像可知,时,,即 时,
,因此的 。
向的溶液中加入溶液至 ,根据图像分析可
知,时溶液中的、浓度均极小,则体系中元素 主要以
存在。
分析题图可知,当即 时,
,,即约为 。加入等体
积的后,先与反应,最后的依然大于, 大于
14,故反应后体系中元素主要还是以 存在。
9.(2023全国乙)一定温度下,和 的沉淀溶解平衡曲线如图所示。
下列说法正确的是( )
C
A.点条件下能生成 沉淀,也能生
成 沉淀
B.点时, ,
C. 的平衡
常数
D.向、均为 的混
合溶液中滴加溶液,先产生
沉淀
. .
.
【解析】
点位于和 沉淀溶解平衡曲
线的右上方,由上述分析知越往上、越往右
离子浓度越小,则点的离子积 必小于
或,因此 点不会有沉
淀生成。
由上述分析可知,
、
, 只与温度有关而与浓
度无关,因此点两者的 不相等。
的平衡
常数表达式为 ,将该表达式转
化为和两种难溶物溶度积有关的式子:
。
该混合溶液中形成 沉淀所需的
,
形成 沉淀所需的
,形成 所
需的较小,所以先产生 沉淀。
10.(2023新课标)向饱和溶液(有足量 固
体)中滴加氨水,发生反应
和 。
与 的关
系如图所示{其中代表、、 或
。
下列说法错误的是( )
A
A.曲线Ⅰ可视为溶解度随 浓度变化曲线
B.的溶度积常数
C.反应的平衡常数的值为
D.时,溶液中
【解析】
.
随着逐渐增大,结合 形成和,而 减
小会促使 平衡正向移动,增大溶解度的同时也增大了
浓度,溶解多少 溶液就会增加多少,因此 的溶解度曲线应与 的曲线吻
合,应该为曲线Ⅳ。
分析题图可知, 时,
、
,则 的溶度积常数
。
分析题图可知, 时,溶
液中和 的浓度分别为
和 ,则
的平
衡常数 。
分析题图可知, 时,溶
液中 。
11.(2023全国甲)如图所示为、和 在水中达沉淀溶解平衡时
的关系图{;可认为 离子沉
淀完全}。下列叙述正确的是( )
C
A.由点可求得
B.时 的溶解度为
C.浓度均为的和 可通过
分步沉淀进行分离
D.、 混合溶液中
时,二者不会同时沉
淀
【解析】 由点 可知,此时
,即
; ,
,则
(【提醒】题目没有
特别说明时,默认温度为 ),因此
。
方法一 由线上的点 可知,此时
, ,则
,因此,可知时
的溶解度为 。
方法二 由线上的点 可知,此时
,,即
时的溶解度为 。
分析题图可知, 约为2.8时,
,即 完全沉淀,
而此时 尚未开始沉淀,因此可通过调节溶
液的方法分步沉淀和 。
当时 完全沉
淀,分析题图可知此时约为 ,且
,此时 已经开始
沉淀了,选项中
,即
,会有
沉淀出现,因此、 可以同时沉淀。
12.(2023北京)利用平衡移动原理,分析一定温度下在不同的 体系中
的可能产物。
已知:①图1中曲线表示体系中各含碳粒子的物质的量分数与 的关系。
②图2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子
浓度关系符合[注:起始 ,
不同下 由图1得到]。
图1
图2
下列说法不正确的是( )
A.由图1,,
B.由图2,初始状态、 ,无沉淀生成
C.由图2,初始状态、 ,平衡后溶液中存在
D.由图1和图2,初始状态、 ,发生反应:
C
【解析】 分析题图1可知,时,与 物质的量分数相等,在同
一溶液中物质的量浓度也相等,即 。
分析题图2可知,初始状态、 对应的点在题图2中
和 的溶解平衡曲线下方,溶液中离子浓度偏小,此时
且,因此不会生成 或
沉淀。
分析题图2可知,、 对应的点位于曲线Ⅱ的上方,会生成
沉淀,根据元素质量守恒,溶液中
。
分析题图1可知,时,溶液中主要含碳微粒是 ;分析题图2可知,
、对应的点位于曲线Ⅱ的上方,会生成 沉淀,因此反应
的离子方程式为 。
13.(2022湖南)室温时,用的标准 溶
液滴定浓度相等的、和 混合溶液,通过电位
滴定法获得与 的关系曲线如图所示[忽略
沉淀对离子的吸附作用。若溶液中离子浓度小于
时,认为该离子沉淀完全。
, ,
]。下列说法正确的是( )
C
A.点:有白色沉淀生成 B.原溶液中的浓度为
C.当沉淀完全时,已经有部分沉淀 D.点:
【解析】 由于、、 是同类型的难溶电解质[都是
, 越小,在水中的溶解度也越小。
向浓度相等的、和 混合溶液中滴加硝酸银溶液,三种
离子沉淀的先后顺序为、、 。
先沉淀,是黄色的,所以点有黄色沉淀 生成。
当滴入硝酸银溶液时, 发生突变,说明
此时、、 沉淀完全,此时共消耗硝酸银的物质的量为
,又原溶液中、、 浓度相等,
则、和 均为
,故的浓度为 。
当沉淀完全时浓度为 ,溶液
中的
,
产生 沉淀的最小
,随着滴定的
进行,溶液体积增大,当完全沉淀时,加入 溶液的
体积小于 ,则混合液中
,故此时已经有部分 沉淀。
点加入了过量的硝酸银溶液,浓度最大;在 浓
度相同的条件下,越大,对应的阴离子浓度也越大,因此
点各离子浓度的大小顺序为 。
14.(2022山东)工业上以为原料生产 ,对其工艺条件进行研究。现有
含的、溶液,含的 、
溶液。在一定范围内,四种溶液中随 的变化关系如
图所示。下列说法错误的是( )
D
A.反应 的平衡常数
B.
C.曲线④代表含的 溶液的变化曲
线
D.对含且和初始浓度均为
的混合溶液, 时才发生沉淀转化
【解析】
反应 的平衡常数
。
由分析可知,曲线①代表含固体的 溶液的变化曲线,则
的溶度积 。温度不变,溶
度积不变,则溶液为7.7时,曲线②的 ,此时
,则 。
由图像分析可知,曲线④表示含固体的 溶液的变化曲线。
由图像分析可知,含且和初始浓度均为 的混合
溶液分别对应曲线②和曲线④,由曲线交点可知,当 时即可发生沉淀
转化。
的相关计算
15.(2023河南焦作期末)已知, ,
。某溶液中含有、和,浓度均为 ,
向该溶液中逐滴加入的 溶液时,三种阳离子产生沉淀的先后顺序为
( )
A
A.、、 B.、、
C.、、 D.、、
【解析】 根据溶度积的定义可知,三种离子沉淀时分别有
, ,
,溶液中、、的浓度均为 ,
则向该溶液中逐滴加入溶液产生沉淀时,所需 分别为
、 、
,所需 越小越先沉淀,所以这三种离子产生沉
淀的先后顺序为、、 。
16.(2023重庆名校联考)
(1) 工业上利用含的废液制备时,废液中除含 外,主要还含
、 等杂质离子,可以将杂质离子转化为相应氟化物沉淀而除去。写出加入
最先除去的杂质的离子方程式:________________________________________
[已知:; ;
。
(2) 已知:,,向 溶液中加入
和,当两种沉淀共存时, ___________。
(3) 已知在时,。时,向
溶液中加入固体,如要生成沉淀,则溶液的 最小是____[已知:
,, 。
9.2
【解析】 (1)、的组成类型相同,且,故 先将
废液中的转化为 沉淀而除去,离子方程式为
。(2)体系中存在、 沉淀,即
、 均处于沉淀溶解平衡状态,则
。(3)沉淀的 最小
最大最小最大,即刚开始沉淀时的 最小。当
时, ,则
,故, 。
17.(1) 在化学分析中采用为指示剂,以标准溶液滴定溶液中的 ,利
用与生成砖红色沉淀,指示到达滴定终点。当溶液中 恰好沉淀完全
(浓度等于时,溶液中为___________ ,此时溶液
中等于___________(已知、的分别为 和
)。
(2) (2021海南) 时,潮湿的石膏雕像表面会发生反应:
,其平衡常数 _______[已知
, 。
3 250
(3) 和 都是锂离子电池的
电极材料,可利用钛铁矿(主要成分为
,还含有少量、 等杂质)来
制备。工艺流程如下:
若“滤液②”中 ,加入
【答案】 恰好沉淀完全时,
, ,因此不会生成
沉淀
双氧水和磷酸(设溶液体积增加1倍),使 恰好沉淀完全即溶液中
,此时是否有 沉淀生成?(列式计算)。
、的分别为、 。
【解析】 (1)根据溶度积计算:
,故
。
(2)已知 ,
,
则该反应的 。
18.(1) 用废电池的锌皮制备 的过程中,需除去锌皮中的少量杂质铁:
化合物
近似值
其方法是:加稀和溶解,铁变为______,加碱调节至 为____时,铁刚好
沉淀完全(离子浓度小于 时,即可认为该离子沉淀完全);继续加碱至
为___时,锌开始沉淀(假定浓度为)。若上述过程不加 的后
果是____________________,原因是___________________________。
2.7
6
和分离不开
和的相近
(2) (2020全国Ⅲ改编)常温下,溶液中金属离子开始沉淀和完全沉淀的 如表所示。
金属离子
开始沉淀时的 7.2 3.7 2.2 7.5
沉淀完全时的 8.7 4.7 3.2 9.0
利用上述表格数据,计算的 _________________(列出计算式)。如果“转
化”后的溶液中浓度为,则“调”应控制的 是____。
6.2
(3) (2020山东改编)时相关物质的 如表所示。
物质
使用氨水调溶液的,使和完全沉淀,则 的理论最小值为____(当溶液中
某离子浓度 时,可认为该离子沉淀完全)。
4.9
【解析】 (1)锌皮中的少量杂质铁与稀反应生成,再被 氧化:
,最后变为。给出氢氧化物的 ,求阳离
子完全沉淀所需的 ,可以按照三步快速解出:
的, 时,求出
;
② ;
③常温下,,因此 。
浓度为,调节至 开始沉淀,此时符合
,可以按照三步快速解出:
①的, ,求出
; ;
③常温下,,因此 。
酸性条件下被氧化为,再通过调节溶液的可使、 两种元素分别以
和形式分离开来,若不加,由数据可知和的
近似值相同,因此会在相同 时一起沉淀,而无法达到分离的目的。
(2)本题有两组数据可以计算出的 。
数据开始沉淀时的为 ,可知
, ,
的 。
数据完全沉淀时的为 ,可知
, ,
的 。
已经求出的,当浓度为,欲求溶液的 ,可以按照三步快
速解出:
①的 ,
,求出 ;
② ;
③常温下,,因此 。
(3)和都属于型的难溶电解质, 表达式皆为
,因此越小溶解度越小,在 逐渐升高的过程中越优先沉淀。由数
据可知,,因此溶解度也是, 完全沉
淀时也必将完全沉淀。欲使和完全沉淀,则只需要计算使 完全沉淀时
溶液对应的即可。已知的,当浓度为 ,欲求溶液
的 ,可以按照三步快速解出:
的, ,求
出 ;
;
③常温下,,因此 。
当调节至,则和 皆完全沉淀。
1.(2023北京东城区综合练习)室温下,时刻向两个盛有 蒸馏水的烧杯中分别
加入、 蔗糖,搅拌,最终分别得到悬浊液和澄清溶液,溶解过程中分
散系的导电能力变化如图。
下列分析不正确的是( )
B
A.该实验可证明蔗糖不是电解质
B.该实验可证明碳酸钙是强电解质
C.当①中导电能力不变时,
达到平衡
D.时刻,①中再加 ,导电能力不变
【解析】 蔗糖溶解过程中分散系的导
电能力基本不变,说明蔗糖为非电解质。
由题图知,溶于水的碳酸钙发生了电离,
但不能判断其是否完全电离,故不能证明碳
酸钙属于强电解质。
碳酸钙溶解过程中分散系的导电能力增
强,当导电能力不变时,说明
达到平衡。
时刻,①中碳酸钙在水中已达到溶解平衡,再加 碳酸钙,溶液中的离子浓度
不变,导电能力不变。
2.(2023广东深圳二调)室温下,以氟磷灰石 为原料,经酸浸、转化可得
到、和。已知:,的、 、
。下列说法不正确的是( )
B
A. 的沉淀溶解平衡可表示为
B.酸浸过程中溶液时,
C. 溶液中存在:
D.向溶液中加入少量水稀释时, 的值增大
【解析】 氟磷灰石 在溶液中存在沉淀溶解平衡,可表示为
。
在溶液中分三步电离:, ,
,,, 。
时,由可知, ,
。
方法一 溶液中,根据电荷守恒可得:
,根据元素质量守恒
可得: ,两式联立消去
可得: 。
方法二 含与且不含、 等不水解的离子找质子守恒。
溶液中存在电离平衡:, ,向
溶液中加入少量水稀释时,由于为定值,减小,则 增大,
即 的值增大。
3.下列说法正确的是( )
选项 实验 现象 结论
A 向2支盛有 相同浓度银氨溶液的试管中 分别加入2滴相同浓度的和 溶液 一支试管中产生黄色 沉淀,另一支中无明 显现象
B 室温下,向浓度均为的 和 混合溶液中滴加 溶液 出现白色沉淀
C 将 溶液滴入 溶液 至不再有沉淀产生,再滴加 溶液 先有白色沉淀生成, 后变为浅蓝色沉淀 的溶度积比 的大
D 将稀硫酸与 反应产生的气体不断通入 与 的浊液中 白色沉淀逐渐变为黑 色沉淀
A
【解析】 根据题中描述可知黄色沉淀为 ,另一支试管中无明显现象,说明没有
析出,证明 。
和均为白色沉淀,根据该实验现象不能判断出二者的 的相对大小
关系。
对于组成类似(阴、阳离子个数比相同)的难溶电解质,溶度积大的易转化为溶
度积小的。
稀硫酸与反应可产生,通入与 的浊液中,虽然白色沉淀变成黑
色沉淀,但因溶液中存在,也可与 反应产生沉淀,不能说明
。
4.(2023湖北武汉部分学校调研)常温下,用
的溶液滴定 未知浓度的
溶液。溶液电导率、随滴入
溶液体积 的变化关系如图所示。
下列叙述错误的是( )
D
A.当时,溶液中的溶质为
B.该溶液的物质的量浓度是
C.该温度下的溶度积常数
D.当 时,溶液中
【解析】 随着的加入,发生反应:,
减小,增大;随着 的加入,溶液体积增大,溶液中离子浓度减小,
电导率先减小,当反应完全时,电导率达到最小值,再加 溶液,溶液中离
子浓度增大,电导率逐渐增大。
5.(2023河北石家庄期末检测)时,向的 溶液中通入氨气,
测得溶液的与 之间的变化曲线如图所示[已知:
,, ,忽略反应过程
中溶液体积的变化]。下列说法正确的是( )
C
A.的数量级是
B.点溶液中会产生 沉淀
C. 点溶液中存在:
D.点溶液中存在:
【解析】
6.(2023山东历城二中期末)常温下,将 粉
末置于盛有 蒸馏水的烧杯中,然后向烧杯中加入
固体(忽略溶液体积的变化)并充分搅拌,该过程
中几种离子的浓度变化曲线如图所示,下列说法不正确的
是( )
C
A.反应 的
B.相同温度下,在水中和在溶液中的 不变
C.曲线代表 浓度变化
D.锅炉水垢中的可先用溶液处理,使
转化为 后,再用酸除去
【解析】 .
反应 的
。
B(√) 只与温度有关,而与溶剂无关,故相同温度
下,在水中和在溶液中的 不变。
曲线代表 浓度变化。
锅炉水垢中的 微溶于水,不溶于酸,可根据沉
淀溶解平衡,先用溶液处理,使 转化为
,弃去沉淀转化后的溶液,再向其中加入盐酸,发
生反应: ,达到除
去锅炉水垢的目的。
7.(2023河北衡水中学模拟)时,和
的沉淀溶解平衡曲线如图所示。已知:
,,其中为
或 。下列说法正确的是( )
D
A.曲线Ⅰ代表 的沉淀溶解平衡曲线
B.点:,点:
C.点对应的溶液为过饱和溶液,有 沉
淀析出
D. 时,
的平
衡常数
【解析】 图像分析根据 的沉淀溶解平衡可
知, ,同理
;分析题图可知,斜率:
曲线Ⅰ Ⅱ,则曲线Ⅰ、Ⅱ分别代表、 的沉
淀溶解平衡曲线;
,
即 ,
,即 。
曲线Ⅰ代表 沉淀溶解平衡曲线。
根据图像可知,横轴和纵轴均表示浓度的负对数,
离子浓度越大,其负对数越小, 点:
。
点对应的溶液中, ,
则点对应的 溶液为不饱和溶液,溶液中没
有 析出。
的平衡常数 。
8.(方式创新·学科融合)(2023山东烟台二模)已知
、 。常温下,
难溶物 在不同浓度盐酸(足量)中恰好不再溶解时,
测得混合液中与 的关系如图所示。下列说
法错误的是( )
B
A.约为
B.点对应溶液中:
C.点对应溶液中:
D.直线上任一点均满足:
【解析】
. .
.
9.(生态环保)(2022全国乙)废旧铅蓄电
池的铅膏中主要含有、、 和
,还有少量、、 的盐或氧化物等,
为了保护环境、充分利用铅资源,通过下图
流程实现铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质
一定条件下,一些金属氢氧化物沉淀时的 如表所示:
金属氢氧化物
开始沉淀的 2.3 6.8 3.5 7.2
完全沉淀的 3.2 8.3 4.6 9.1
回答下列问题:
(1) 在“脱硫”中 转化反应的离子方
程式为_________________________________
______________________________,用沉淀
溶解平衡原理解释选择 的原因
____________________________________________________________________________________________________________________ 。
该反应的 ,
反应正向进行的程度很大,可以进行到底
(2) 在“脱硫”中,加入 不能使铅膏中
完全转化,原因是 ____________________________________________________________________________________________________________________________ 。
反应 的
,
反应正向进行的程度很小
(3) 在“酸浸”中,除加入醋酸,还要加入 。
(ⅰ) 能被 氧化的离子是______;
(ⅱ) 促进了金属在醋酸中转化为 ,其化学方程式为________________
_______________________;
(ⅲ) 也能使转化为, 的作用是__________。
作还原剂
(4) “酸浸”后溶液的约为 ,滤渣的
主要成分是__________________。
、
(5) “沉铅”的滤液中,金属离子有
____________。
、
【解析】 加入使 转化为
,便于后续的酸浸;通过酸浸,
铅元素全部转化为可溶性的 ,过滤
后在滤液中加入溶液,使 转化
为,加热分解得到 。
(1)的远小于的,易发生生成 的沉淀转化,且进行较为彻底。
(2)的大于的,生成 的沉淀转化的反应进行的程度也很小。
(3)(ⅰ)具有还原性,能被氧化;(ⅱ)能氧化,使其转化成,
再与结合生成 ,依据氧化还原反应的规律,即可写出反应的化学方程
式;(ⅲ)通过与、反应转化为,发生氧化还原反应, 化合价降
低, 作还原剂。(4)根据题给信息,
当时,、 完全转化为
、。(5)加入 溶液,
发生沉铅的反应为
,
故滤液中含有的金属离子有 以及未沉淀
的 。
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
同课章节目录
