山西省大同市2024-2025学年高一上学期10月联考试题 化学(含答案)
文档属性
| 名称 | 山西省大同市2024-2025学年高一上学期10月联考试题 化学(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-28 00:00:00 | ||
图片预览




文档简介
2024~2025学年高一10月质量检测卷
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟,
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版必修第一册第一章。
5.可能用到的相对原子质量:H1 C12 O16 Na23 Mg24 S32 Cl35.5
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1. 下列诗句中对所涉及物质的性质、现象或变化的描述错误的是
A. “钻石恒久远,一颗永流传”说明了常温下碳的化学性质稳定
B. “炉火照天地,红星乱紫烟”形象地描写了金属的冶炼过程
C. “掬月水在手,弄花香满衣”诗文中隐含着化学变化
D. “遥知不是雪,为有暗香来”说明了分子在不停地运动
2. 下列诺贝尔奖获奖原因中不属于化学研究范畴的是
A. 准晶体的发现 B. 核糖体结构和功能方面的研究
C. 量子点的发现和合成 D. 发现巨磁电阻效应
3. 图a~c分别为氯化钠在不同状态下的导电实验(X、Y均表示石墨电极,X与电源正极相连,Y与电源负极相连,Y极聚集大量电子)微观示意图。下列说法错误的是
A. 图示中●代表 B. 图a中氯化钠固体不能导电
C. 图b表示NaCl(熔融) D. 图c中水合氯离子应向Y极移动
4. 下列分散系能产生“丁达尔效应”的是
A. 葡萄糖溶液 B. 鸡蛋清溶液 C. 纳米级氯化钠 D. 油水混合物
5. 氢化钠(NaH)可在野外用作生氢剂,其中氢元素为-1价。NaH用作生氢剂时化学反应原理为:NaH + H2O = NaOH + H2↑。下列有关该反应的说法中,正确的是
A. H2O中的氢元素部分被还原 B. 该反应属于复分解反应
C. NaH是氧化剂 D. 该反应属于置换反应
6. 根据图示关系判断,下列化学反应中属于阴影区域的是
A. B.
C. D.
7. 构建知识网络是一种重要的学习方法。“—”表示相连的两种物质能发生反应,“→”表示一种物质能一步转化为另一种物质,x、y、z分别属于不同类别的化合物,则x、y、z可能是
A. NaOH,, B. KOH,,
C. ,,CuO D. NaOH,HCl,
8. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 的溶液中:,,,
B. 无色溶液中:,,,
C. 使紫色石蕊试液变红的溶液中:,,,
D. 苏打溶液中:,,,
9. 下列各物质的化学式、俗称(或名称)和物质类别均对应正确的一组是
选项 化学式 俗称(或名称) 物质类别
A 烧碱 盐
B 干冰 酸性氧化物
C 生石灰 酸
D 高锰酸钾 还原剂
A. A B. B C. C D. D
10. 关于反应,下列说法正确的是
A. 氧化性:
B. 每生成3个,转移6个电子
C. 氧化产物与还原产物的质量之比为5∶1
D. 该反应体现了HCl的酸性和强氧化性
11. 下列指定反应的离子方程式书写正确的是
A. 食醋去除水垢中的:
B. 氢氧化钠溶液中通入过量二氧化碳:
C 向足量盐酸中滴入氨水:
D. 向中加入少量稀盐酸:
12. 某混合溶液中所含离子个数如表,则可能为
所含离子
个数 4a a 2a 2a
A. B. C. D.
13. 城市污水中含有一定量的,,向污水中加入菌体和溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ.从而实现,的脱除,转化过程如图所示。下列说法正确的是
A. “过程Ⅰ”中为催化剂
B. 的氧化性强于
C. 高温条件更有利于该污水处理过程
D. “过程Ⅱ”中发生反应的离子方程式为
14. 向一定体积的溶液中逐滴加入溶液,测得混合溶液的导电能力随时间的变化曲线如下图所示。下列说法正确的是
A. AB段溶液的导电能力不断减弱,说明产物是非电解质
B. AB段反应的离子方程式为:
C. BC段溶液的导电能力不断增强,说明过量的发生电离
D. BC段溶液中:、、和可以大量共存
二、非选择题(本题共4小题,共58分)
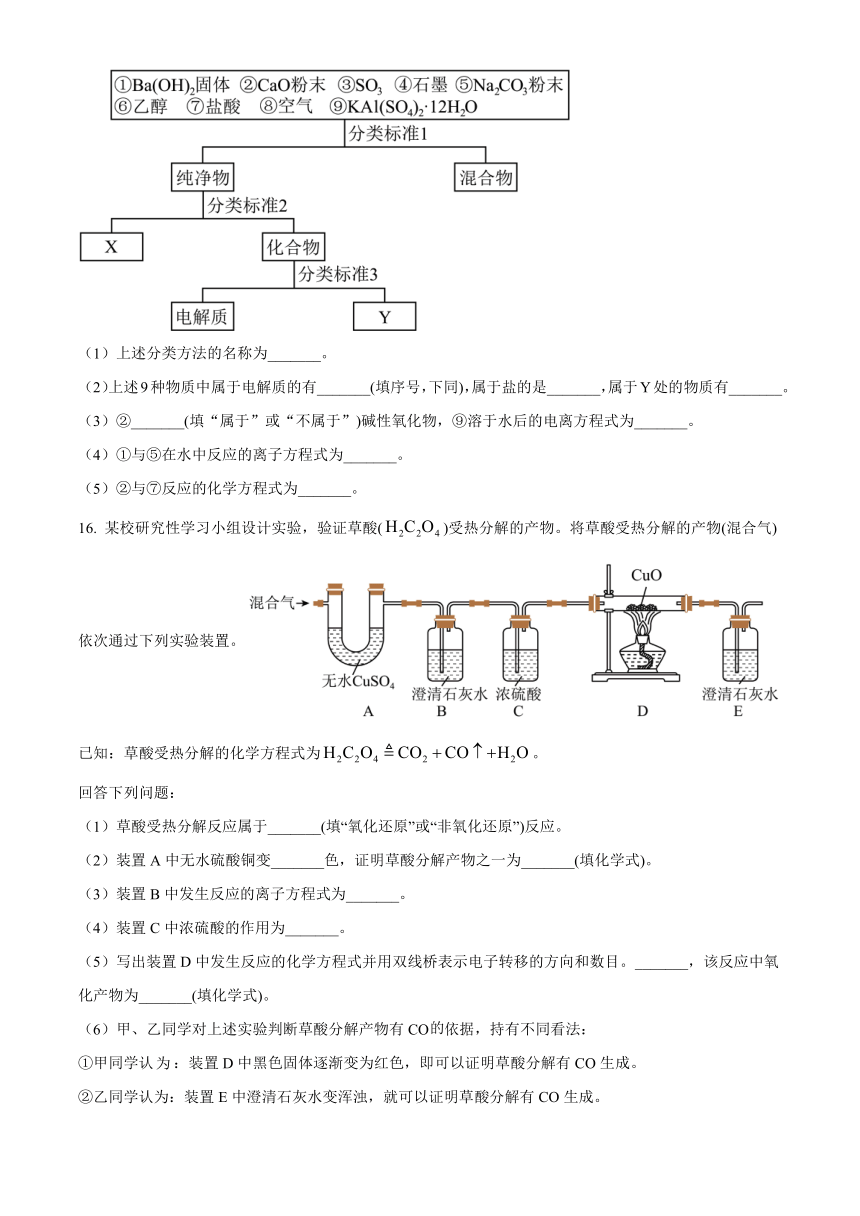
15. 用分类思想研究一类物质的通性和特殊性是学习化学的一种重要方法。按一定方法对下列物质进行的分类如图所示,回答下列问题:
(1)上述分类方法的名称为_______。
(2)上述9种物质中属于电解质的有_______(填序号,下同),属于盐的是_______,属于Y处的物质有_______。
(3)②_______(填“属于”或“不属于”)碱性氧化物,⑨溶于水后的电离方程式为_______。
(4)①与⑤在水中反应的离子方程式为_______。
(5)②与⑦反应的化学方程式为_______。
16. 某校研究性学习小组设计实验,验证草酸()受热分解的产物。将草酸受热分解的产物(混合气)依次通过下列实验装置。
已知:草酸受热分解的化学方程式为。
回答下列问题:
(1)草酸受热分解反应属于_______(填“氧化还原”或“非氧化还原”)反应。
(2)装置A中无水硫酸铜变_______色,证明草酸分解产物之一为_______(填化学式)。
(3)装置B中发生反应的离子方程式为_______。
(4)装置C中浓硫酸的作用为_______。
(5)写出装置D中发生反应的化学方程式并用双线桥表示电子转移的方向和数目。_______,该反应中氧化产物为_______(填化学式)。
(6)甲、乙同学对上述实验判断草酸分解产物有CO依据,持有不同看法:
①甲同学认:装置D中黑色固体逐渐变为红色,即可以证明草酸分解有CO生成。
②乙同学认为:装置E中澄清石灰水变浑浊,就可以证明草酸分解有CO生成。
你认为以上分析正确的同学是_______(填“甲同学”或“乙同学”)。
(7)为排除未反应完全的的干扰,应在装置B后增加一个广口瓶,新增的广口瓶中所加入的试剂为_______(填名称)。
17. Ⅰ.X、Y、Z三种可溶性盐,其阳离子分别是、、中的某一种,阴离子分别是、、中的某一种。现进行下列实验:
①各取少量三种盐,分别溶于盛有5 mL蒸馏水的三支试管中,只有X溶液呈蓝色。
②分别向三支试管中加入2 mL稀盐酸,发现Y溶液中产生白色沉淀,Z溶液无明显现象。回答下列问题:
(1)根据实验推测,X、Z的化学式依次为_______。
(2)盛有Y溶液试管中产生白色沉淀的离子方程式为_______。
Ⅱ.海水资源丰富,从海水中提取镁的简单步骤如下:
(3)“操作1”与“操作2”相同,下列选项中与“操作1”相同的操作是_______(填字母)。
A. B.
C. D.
(4)沉淀2主要成分的化学式为_______(不考虑)。
(5)工业上“沉镁”时加入试剂M的化学式为_______。
(6)最后一步由无水制取Mg的方法是电解,该反应的化学方程式为_______;若最终制得36t Mg,则理论上需消耗的质量为_______。
18. 亚氯酸钠()主要用作棉纺、造纸业的漂白剂。以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示:
已知:①亚氯酸钠受热易分解;②常温下为气体。
回答下列问题:
(1)“反应1”中发生反应□□□□,配平该方程式_______,该反应中氧化剂与还原剂的质量比为_______。
(2)从“母液”中可回收的主要物质是_______(填化学式)。
(3)“反应2”的化学方程式为_______,反应中作_______(填“氧化剂”或“还原剂”)。
(4)“操作X”宜采用_______(填“蒸发结晶”或“低温蒸发浓缩、冷却结晶”)。
(5)酸性条件下,吸收剂可有效氧化NO,该氧化吸收法是常见的消除氮氧化物尾气的方法之一,其他条件一定时,温度对NO去除率的影响如图所示,温度高于60℃后,NO去除率下降,其原因可能是_______。
2024~2025学年高一10月质量检测卷
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟,
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版必修第一册第一章。
5.可能用到的相对原子质量:H1 C12 O16 Na23 Mg24 S32 Cl35.5
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的)
【1题答案】
【答案】C
【2题答案】
【答案】D
【3题答案】
【答案】D
【4题答案】
【答案】B
【5题答案】
【答案】A
【6题答案】
【答案】C
【7题答案】
【答案】B
【8题答案】
【答案】A
【9题答案】
【答案】B
【10题答案】
【答案】C
【11题答案】
【答案】B
【12题答案】
【答案】A
【13题答案】
【答案】D
【14题答案】
【答案】D
二、非选择题(本题共4小题,共58分)
【15题答案】
【答案】(1)树状分类法
(2) ①. ①②⑤⑨ ②. ⑤⑨ ③. ③⑥
(3) ①. 属于 ②. KAl(SO4)2=K++Al3++2
(4)Ba2++CO=BaCO3↓
(5)CaO+2HCl=CaCl2+H2O
【16题答案】
【答案】(1)氧化还原
(2) ①. 蓝 ②. H2O
(3)
(4)干燥气体防止水蒸气进入硬质玻璃管
(5) ①. ②. CO2
(6)甲同学 (7)氢氧化钠
【17题答案】
【答案】(1)CuSO4、BaCl2
(2)Ag++Cl-=AgCl (3)A
(4)BaCO3、CaCO3
(5)Ca(OH)2 (6) ①. ②.
【18题答案】
【答案】(1) ①. 2NaClO3+SO2=2ClO2+Na2SO4 ②. 213:64
(2)Na2SO4 (3) ①. H2O2+2ClO2+2NaOH=2NaClO2+2H2O+O2 ②. 还原剂
(4)低温蒸发浓缩、冷却结晶
(5)NaClO2受热易分解
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟,
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版必修第一册第一章。
5.可能用到的相对原子质量:H1 C12 O16 Na23 Mg24 S32 Cl35.5
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1. 下列诗句中对所涉及物质的性质、现象或变化的描述错误的是
A. “钻石恒久远,一颗永流传”说明了常温下碳的化学性质稳定
B. “炉火照天地,红星乱紫烟”形象地描写了金属的冶炼过程
C. “掬月水在手,弄花香满衣”诗文中隐含着化学变化
D. “遥知不是雪,为有暗香来”说明了分子在不停地运动
2. 下列诺贝尔奖获奖原因中不属于化学研究范畴的是
A. 准晶体的发现 B. 核糖体结构和功能方面的研究
C. 量子点的发现和合成 D. 发现巨磁电阻效应
3. 图a~c分别为氯化钠在不同状态下的导电实验(X、Y均表示石墨电极,X与电源正极相连,Y与电源负极相连,Y极聚集大量电子)微观示意图。下列说法错误的是
A. 图示中●代表 B. 图a中氯化钠固体不能导电
C. 图b表示NaCl(熔融) D. 图c中水合氯离子应向Y极移动
4. 下列分散系能产生“丁达尔效应”的是
A. 葡萄糖溶液 B. 鸡蛋清溶液 C. 纳米级氯化钠 D. 油水混合物
5. 氢化钠(NaH)可在野外用作生氢剂,其中氢元素为-1价。NaH用作生氢剂时化学反应原理为:NaH + H2O = NaOH + H2↑。下列有关该反应的说法中,正确的是
A. H2O中的氢元素部分被还原 B. 该反应属于复分解反应
C. NaH是氧化剂 D. 该反应属于置换反应
6. 根据图示关系判断,下列化学反应中属于阴影区域的是
A. B.
C. D.
7. 构建知识网络是一种重要的学习方法。“—”表示相连的两种物质能发生反应,“→”表示一种物质能一步转化为另一种物质,x、y、z分别属于不同类别的化合物,则x、y、z可能是
A. NaOH,, B. KOH,,
C. ,,CuO D. NaOH,HCl,
8. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 的溶液中:,,,
B. 无色溶液中:,,,
C. 使紫色石蕊试液变红的溶液中:,,,
D. 苏打溶液中:,,,
9. 下列各物质的化学式、俗称(或名称)和物质类别均对应正确的一组是
选项 化学式 俗称(或名称) 物质类别
A 烧碱 盐
B 干冰 酸性氧化物
C 生石灰 酸
D 高锰酸钾 还原剂
A. A B. B C. C D. D
10. 关于反应,下列说法正确的是
A. 氧化性:
B. 每生成3个,转移6个电子
C. 氧化产物与还原产物的质量之比为5∶1
D. 该反应体现了HCl的酸性和强氧化性
11. 下列指定反应的离子方程式书写正确的是
A. 食醋去除水垢中的:
B. 氢氧化钠溶液中通入过量二氧化碳:
C 向足量盐酸中滴入氨水:
D. 向中加入少量稀盐酸:
12. 某混合溶液中所含离子个数如表,则可能为
所含离子
个数 4a a 2a 2a
A. B. C. D.
13. 城市污水中含有一定量的,,向污水中加入菌体和溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ.从而实现,的脱除,转化过程如图所示。下列说法正确的是
A. “过程Ⅰ”中为催化剂
B. 的氧化性强于
C. 高温条件更有利于该污水处理过程
D. “过程Ⅱ”中发生反应的离子方程式为
14. 向一定体积的溶液中逐滴加入溶液,测得混合溶液的导电能力随时间的变化曲线如下图所示。下列说法正确的是
A. AB段溶液的导电能力不断减弱,说明产物是非电解质
B. AB段反应的离子方程式为:
C. BC段溶液的导电能力不断增强,说明过量的发生电离
D. BC段溶液中:、、和可以大量共存
二、非选择题(本题共4小题,共58分)
15. 用分类思想研究一类物质的通性和特殊性是学习化学的一种重要方法。按一定方法对下列物质进行的分类如图所示,回答下列问题:
(1)上述分类方法的名称为_______。
(2)上述9种物质中属于电解质的有_______(填序号,下同),属于盐的是_______,属于Y处的物质有_______。
(3)②_______(填“属于”或“不属于”)碱性氧化物,⑨溶于水后的电离方程式为_______。
(4)①与⑤在水中反应的离子方程式为_______。
(5)②与⑦反应的化学方程式为_______。
16. 某校研究性学习小组设计实验,验证草酸()受热分解的产物。将草酸受热分解的产物(混合气)依次通过下列实验装置。
已知:草酸受热分解的化学方程式为。
回答下列问题:
(1)草酸受热分解反应属于_______(填“氧化还原”或“非氧化还原”)反应。
(2)装置A中无水硫酸铜变_______色,证明草酸分解产物之一为_______(填化学式)。
(3)装置B中发生反应的离子方程式为_______。
(4)装置C中浓硫酸的作用为_______。
(5)写出装置D中发生反应的化学方程式并用双线桥表示电子转移的方向和数目。_______,该反应中氧化产物为_______(填化学式)。
(6)甲、乙同学对上述实验判断草酸分解产物有CO依据,持有不同看法:
①甲同学认:装置D中黑色固体逐渐变为红色,即可以证明草酸分解有CO生成。
②乙同学认为:装置E中澄清石灰水变浑浊,就可以证明草酸分解有CO生成。
你认为以上分析正确的同学是_______(填“甲同学”或“乙同学”)。
(7)为排除未反应完全的的干扰,应在装置B后增加一个广口瓶,新增的广口瓶中所加入的试剂为_______(填名称)。
17. Ⅰ.X、Y、Z三种可溶性盐,其阳离子分别是、、中的某一种,阴离子分别是、、中的某一种。现进行下列实验:
①各取少量三种盐,分别溶于盛有5 mL蒸馏水的三支试管中,只有X溶液呈蓝色。
②分别向三支试管中加入2 mL稀盐酸,发现Y溶液中产生白色沉淀,Z溶液无明显现象。回答下列问题:
(1)根据实验推测,X、Z的化学式依次为_______。
(2)盛有Y溶液试管中产生白色沉淀的离子方程式为_______。
Ⅱ.海水资源丰富,从海水中提取镁的简单步骤如下:
(3)“操作1”与“操作2”相同,下列选项中与“操作1”相同的操作是_______(填字母)。
A. B.
C. D.
(4)沉淀2主要成分的化学式为_______(不考虑)。
(5)工业上“沉镁”时加入试剂M的化学式为_______。
(6)最后一步由无水制取Mg的方法是电解,该反应的化学方程式为_______;若最终制得36t Mg,则理论上需消耗的质量为_______。
18. 亚氯酸钠()主要用作棉纺、造纸业的漂白剂。以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示:
已知:①亚氯酸钠受热易分解;②常温下为气体。
回答下列问题:
(1)“反应1”中发生反应□□□□,配平该方程式_______,该反应中氧化剂与还原剂的质量比为_______。
(2)从“母液”中可回收的主要物质是_______(填化学式)。
(3)“反应2”的化学方程式为_______,反应中作_______(填“氧化剂”或“还原剂”)。
(4)“操作X”宜采用_______(填“蒸发结晶”或“低温蒸发浓缩、冷却结晶”)。
(5)酸性条件下,吸收剂可有效氧化NO,该氧化吸收法是常见的消除氮氧化物尾气的方法之一,其他条件一定时,温度对NO去除率的影响如图所示,温度高于60℃后,NO去除率下降,其原因可能是_______。
2024~2025学年高一10月质量检测卷
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟,
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版必修第一册第一章。
5.可能用到的相对原子质量:H1 C12 O16 Na23 Mg24 S32 Cl35.5
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的)
【1题答案】
【答案】C
【2题答案】
【答案】D
【3题答案】
【答案】D
【4题答案】
【答案】B
【5题答案】
【答案】A
【6题答案】
【答案】C
【7题答案】
【答案】B
【8题答案】
【答案】A
【9题答案】
【答案】B
【10题答案】
【答案】C
【11题答案】
【答案】B
【12题答案】
【答案】A
【13题答案】
【答案】D
【14题答案】
【答案】D
二、非选择题(本题共4小题,共58分)
【15题答案】
【答案】(1)树状分类法
(2) ①. ①②⑤⑨ ②. ⑤⑨ ③. ③⑥
(3) ①. 属于 ②. KAl(SO4)2=K++Al3++2
(4)Ba2++CO=BaCO3↓
(5)CaO+2HCl=CaCl2+H2O
【16题答案】
【答案】(1)氧化还原
(2) ①. 蓝 ②. H2O
(3)
(4)干燥气体防止水蒸气进入硬质玻璃管
(5) ①. ②. CO2
(6)甲同学 (7)氢氧化钠
【17题答案】
【答案】(1)CuSO4、BaCl2
(2)Ag++Cl-=AgCl (3)A
(4)BaCO3、CaCO3
(5)Ca(OH)2 (6) ①. ②.
【18题答案】
【答案】(1) ①. 2NaClO3+SO2=2ClO2+Na2SO4 ②. 213:64
(2)Na2SO4 (3) ①. H2O2+2ClO2+2NaOH=2NaClO2+2H2O+O2 ②. 还原剂
(4)低温蒸发浓缩、冷却结晶
(5)NaClO2受热易分解
同课章节目录
