4.1化合价与化学式的书写课件(共22张PPT)-九年级化学科粤版上册
文档属性
| 名称 | 4.1化合价与化学式的书写课件(共22张PPT)-九年级化学科粤版上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 6.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-30 00:00:00 | ||
图片预览








文档简介
(共22张PPT)
4.1 化学式
---- 化合价与化学式的书写
第四单元 化学式与化学方程式
化合物的化学式一定要死记硬背吗?可真烦人!
不一定!有巧方法哟!
一氧化氮:NO
二氧化氮:NO2
我们可以利用化合价书写化学式,那怎样利用化合价来推求化学式呢?
添加相关标题
添加相关标题
H
Cl
H
H
O
H
H
H
N
①氯化氢HCl
②水H2O
③氨气NH3
原子的个数比:
1:1
2:1
3:1
在不同元素间形成的化合物中,它们的原子个数比是不相同的,显示了这些元素某种特性,即元素的化合价。
1、元素的化合价
【观察】下列化学式在组成上有何特点?
四、 化合价
2、化合价的标法:
(2)“+”、“-“号在前,数字在后,若数字为1不能省
(1)标在元素符号或原子团的正上方
3、化合价的实质:
微观
失去2个电子
宏观
钙元素化合价为+2价
得到2个电子
氧元素化合价为-2价
R
+n
R
-n
四、 化合价
氧化镁中镁元素显+2价
MgO
+2
符号与数字的位置 符号与数字的顺序 “1” 例子
离子
化合价
联系与区别
元素符号或原子团的右上角
先数值后正负号
省略
元素符号或原子团的正上方
先正负号再数值
不能省略
通常数值相等,正、负号相同,只是位置不同
Na
+1
Na
+
+2
Mg
Mg
2+
4、与离子符号比较
四、 化合价
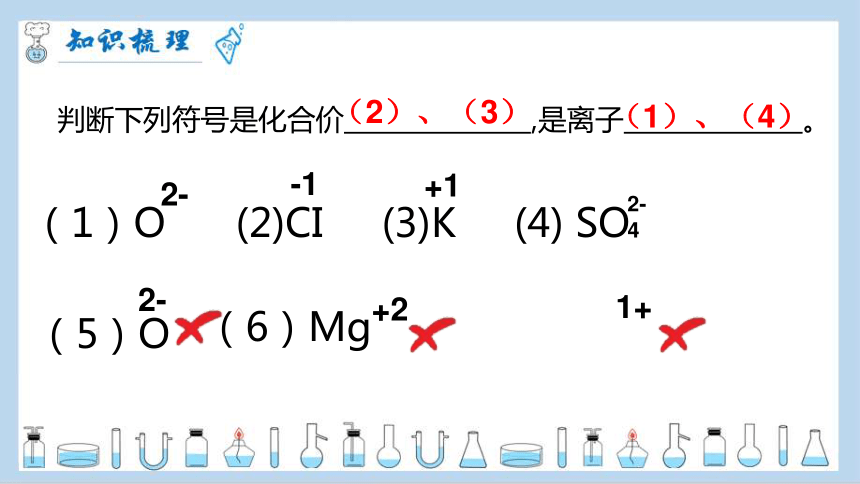
判断下列符号是化合价 ,是离子 。
2-
+1
-1
2-
4
(1)O (2)CI (3)K (4) SO
(5)O
2-
(6)Mg
+2
1+
(1)、(4)
(2)、(3)
2、在化合物里氢元素通常显___价、氧元素___价,许多非金属元素与氧元素形成化合物时,显____价。
1、金属与非金属形成化合物时,金属元素在化合物中通常显____价,非金属元素显_____价。
+1
-2
正
负
正
3、部分元素可以有不同的化合价。
同一元素在不同的物质中可显示不同的化合价,如 CO2、 CO。
同一元素在同种物质中可显不同的化合价,如NH4NO3。
+4
+2
-3
+5
特例:H2O2中氧元素的化合价为-1价
5.化合价的规律
四、 化合价
6、单质中元素的化合价为____.
C
Na
O2
O3
C60
0
0
0
0
0
0
4、某些原子团也表现出一定的化合价(整体参加反应)。
例如,氢氧根:________价;硫酸根:________价。
-1
-2
5、化合物中元素的正负化合价代数和为0。
Al2O3
则(+3)×2+(-2)×3=0
+3
-2
四、 化合价
元素名称 符号 化合价 元素名称 符号 化合价
氢 H +1 铁 Fe +2、+3
钠 Na +1 锰 Mn +2、+4、+6、+7
银 Ag +1 氯 Cl -1、+1、+5、+7
钾 K +1 溴 Br -1
钙 Ca +2 氧 O -2
镁 Mg +2 硫 S -2、+4、+6
钡 Ba +2 碳 C +2、+4
锌 Zn +2 硅 Si +4
铝 Al +3 氮 N -3、+2、+3、+4、+5
铁 Fe +2、+3 磷 P -3、+3、+5
一些常见元素的化合价
四、 化合价
钾钠银氢正一价,
钙镁钡锌正二价;
氟氯溴碘负一价,
氧负二,铁正二三;
铜汞二价最常见;
三铝四硅五氮磷,
硫有负二正四六,
单质零价永不变。
当铁元素在化合物中显+2价时,读作亚铁
当铁元素在化合物中显+3价时,读作铁
化合价口诀:
必须熟记
碳有正二和正四;
四、 化合价
负三记住磷酸根( PO43-)
负一硝酸根(NO3-)、氢氧根(OH-),
负二硫酸根( SO42- )、碳酸根( CO32-)
必须熟记
化合价口诀:
正一价是铵根( NH4+)
根的名称 根的符号 化合价
氢氧根 OH-
硝酸根 NO3-
硫酸根 SO42-
碳酸根 CO32-
铵根 NH4+
-1
-1
-2
+1
-2
常见的根及其化合价:
四、 化合价
1、下列化学符号中数字“2”表示的意义,正确的是( )
A.2O:2个氧元素
B.CO2:二氧化碳分子中含有2个氧分子
C. O:氧化钙中钙元素的化合价为+2价
D.Fe2+:1个铁离子带2个单位正电荷
C
1.根据化合价写化学式
方法:十字交叉法
排列元素
正价在前
负价在后
标出元素
的化合价
交叉价数
检查代数和是否为零
“排 标 叉 查”
五、 化合价和化学式
H O
+1 -2
H O
H2O
2 1
“1”省略不写
1:正确书写元素符号
3:若能化简则化简
水
注意
2:标价、交叉价数互为底
1.根据化合价写化学式
五、 化合价和化学式
Cu O
+2 -2
Cu O
CuO
1 1
氧化铜
常见原子团:NO3- OH- SO42- CO32- NH4+
Cu SO4
+2 -2
Cu SO4
Cu1(SO4)1
硫酸铜
注意:1省略不写。
CuSO4
五、 化合价和化学式
Mg OH
+2 -1
Mg OH
Mg(OH)2
氢氧化镁
注意:若原子团有角标,且化简后不为1,需要给原子团带括号,括号外右下角写数字
2.根据化学式求元素的化合价
计算依据:
【典例】求氧化铁(Fe2O3 )中,氧元素为-2价,求铁元素的化合价。
在化合物中,正负化合价的代数和为0。
解:根据化合物中正负化合价的代数和为0的原则,设铁元素的化合价为x,列式:
2 x+(-2)×3=0
解得x=+3
答:氧化铁(Fe2O3 )中铁元素的化合价为+3。
五、 化合价和化学式
CO2 C CH4 H2CO3 CO
总结:同种元素在不同的化学式中化合价不同
S H2S SO2 SO3 H2SO4
Cl2 HCl HClO HClO3 HClO4
+5
0
+4
0
+4
-4
+4
+2
0
-2
+6
+6
-1
+7
+1
2.根据化学式求元素的化合价
六、易错点辨析
标出K2Cr2O7中Cr元素的化合价
写出K2Cr2O7中Cr元素的化合价
总结
K2Cr2O7
+6
+6
①标:先写化学式,再在该元素的正上方标出化合价
②写:直接写化合价即可
2、高氯酸镁[化学式:Mg(ClO4)2]可以作火箭、导弹、焰火等的固体氧化剂。高氯酸镁中氯元素化合价为( )
A.+1 B.+3 C.+5 D.+7
D
1. (2022年广西北部湾)Na2FeO4是一种新型水处理剂,其中Fe元素的化合价为( )A. +6
B. +3
C. +2
D. 0
A
例如:MgO、CaO、CO 、 CO2 、Fe3O4
金属在左,非金属在右,如:CuCl2、NaCl
1、金属元素和非金属元素形成的化合物
2、氧化物:氧在后
某化某
氧化某
六、怎样读化合物的化学式
3、氢元素和其他非金属元素组成的化合物
① 一般规律: 氢在左
② 特殊: H2O(水)、CH4(甲烷)、NH3(氨气)
某化氢
例如: HF
氟化氢
氯化氢
HCl
溴化氢
HBr
六、怎样读化合物的化学式
4、含有原子团的化合物
①酸:“某酸”,如:H2SO4,H2CO3,HNO3,HCl
②碱:“氢氧化某”,如:NaOH,Ca(OH)2,Fe(OH)2,Fe(OH)3
③盐:“某酸某”,如Na2CO3,KNO3, Al2(SO4)3
CO2 P2O5 N2 Ar 。
氩气 氮气 铁 水 。
氧化钙 二氧化锰 五氧化二氮 ;
1、请你写出下列物质的化学式
2、请你读出下列物质的名称
CaO
MnO2
N2O5
Ar
N2
Fe
H2O
氯化钠
氧化镁
硫化钙
氟化氢
二氧化碳
五氧化二磷
氮气
氩气
NaCl MgO CaS HF ;
4.1 化学式
---- 化合价与化学式的书写
第四单元 化学式与化学方程式
化合物的化学式一定要死记硬背吗?可真烦人!
不一定!有巧方法哟!
一氧化氮:NO
二氧化氮:NO2
我们可以利用化合价书写化学式,那怎样利用化合价来推求化学式呢?
添加相关标题
添加相关标题
H
Cl
H
H
O
H
H
H
N
①氯化氢HCl
②水H2O
③氨气NH3
原子的个数比:
1:1
2:1
3:1
在不同元素间形成的化合物中,它们的原子个数比是不相同的,显示了这些元素某种特性,即元素的化合价。
1、元素的化合价
【观察】下列化学式在组成上有何特点?
四、 化合价
2、化合价的标法:
(2)“+”、“-“号在前,数字在后,若数字为1不能省
(1)标在元素符号或原子团的正上方
3、化合价的实质:
微观
失去2个电子
宏观
钙元素化合价为+2价
得到2个电子
氧元素化合价为-2价
R
+n
R
-n
四、 化合价
氧化镁中镁元素显+2价
MgO
+2
符号与数字的位置 符号与数字的顺序 “1” 例子
离子
化合价
联系与区别
元素符号或原子团的右上角
先数值后正负号
省略
元素符号或原子团的正上方
先正负号再数值
不能省略
通常数值相等,正、负号相同,只是位置不同
Na
+1
Na
+
+2
Mg
Mg
2+
4、与离子符号比较
四、 化合价
判断下列符号是化合价 ,是离子 。
2-
+1
-1
2-
4
(1)O (2)CI (3)K (4) SO
(5)O
2-
(6)Mg
+2
1+
(1)、(4)
(2)、(3)
2、在化合物里氢元素通常显___价、氧元素___价,许多非金属元素与氧元素形成化合物时,显____价。
1、金属与非金属形成化合物时,金属元素在化合物中通常显____价,非金属元素显_____价。
+1
-2
正
负
正
3、部分元素可以有不同的化合价。
同一元素在不同的物质中可显示不同的化合价,如 CO2、 CO。
同一元素在同种物质中可显不同的化合价,如NH4NO3。
+4
+2
-3
+5
特例:H2O2中氧元素的化合价为-1价
5.化合价的规律
四、 化合价
6、单质中元素的化合价为____.
C
Na
O2
O3
C60
0
0
0
0
0
0
4、某些原子团也表现出一定的化合价(整体参加反应)。
例如,氢氧根:________价;硫酸根:________价。
-1
-2
5、化合物中元素的正负化合价代数和为0。
Al2O3
则(+3)×2+(-2)×3=0
+3
-2
四、 化合价
元素名称 符号 化合价 元素名称 符号 化合价
氢 H +1 铁 Fe +2、+3
钠 Na +1 锰 Mn +2、+4、+6、+7
银 Ag +1 氯 Cl -1、+1、+5、+7
钾 K +1 溴 Br -1
钙 Ca +2 氧 O -2
镁 Mg +2 硫 S -2、+4、+6
钡 Ba +2 碳 C +2、+4
锌 Zn +2 硅 Si +4
铝 Al +3 氮 N -3、+2、+3、+4、+5
铁 Fe +2、+3 磷 P -3、+3、+5
一些常见元素的化合价
四、 化合价
钾钠银氢正一价,
钙镁钡锌正二价;
氟氯溴碘负一价,
氧负二,铁正二三;
铜汞二价最常见;
三铝四硅五氮磷,
硫有负二正四六,
单质零价永不变。
当铁元素在化合物中显+2价时,读作亚铁
当铁元素在化合物中显+3价时,读作铁
化合价口诀:
必须熟记
碳有正二和正四;
四、 化合价
负三记住磷酸根( PO43-)
负一硝酸根(NO3-)、氢氧根(OH-),
负二硫酸根( SO42- )、碳酸根( CO32-)
必须熟记
化合价口诀:
正一价是铵根( NH4+)
根的名称 根的符号 化合价
氢氧根 OH-
硝酸根 NO3-
硫酸根 SO42-
碳酸根 CO32-
铵根 NH4+
-1
-1
-2
+1
-2
常见的根及其化合价:
四、 化合价
1、下列化学符号中数字“2”表示的意义,正确的是( )
A.2O:2个氧元素
B.CO2:二氧化碳分子中含有2个氧分子
C. O:氧化钙中钙元素的化合价为+2价
D.Fe2+:1个铁离子带2个单位正电荷
C
1.根据化合价写化学式
方法:十字交叉法
排列元素
正价在前
负价在后
标出元素
的化合价
交叉价数
检查代数和是否为零
“排 标 叉 查”
五、 化合价和化学式
H O
+1 -2
H O
H2O
2 1
“1”省略不写
1:正确书写元素符号
3:若能化简则化简
水
注意
2:标价、交叉价数互为底
1.根据化合价写化学式
五、 化合价和化学式
Cu O
+2 -2
Cu O
CuO
1 1
氧化铜
常见原子团:NO3- OH- SO42- CO32- NH4+
Cu SO4
+2 -2
Cu SO4
Cu1(SO4)1
硫酸铜
注意:1省略不写。
CuSO4
五、 化合价和化学式
Mg OH
+2 -1
Mg OH
Mg(OH)2
氢氧化镁
注意:若原子团有角标,且化简后不为1,需要给原子团带括号,括号外右下角写数字
2.根据化学式求元素的化合价
计算依据:
【典例】求氧化铁(Fe2O3 )中,氧元素为-2价,求铁元素的化合价。
在化合物中,正负化合价的代数和为0。
解:根据化合物中正负化合价的代数和为0的原则,设铁元素的化合价为x,列式:
2 x+(-2)×3=0
解得x=+3
答:氧化铁(Fe2O3 )中铁元素的化合价为+3。
五、 化合价和化学式
CO2 C CH4 H2CO3 CO
总结:同种元素在不同的化学式中化合价不同
S H2S SO2 SO3 H2SO4
Cl2 HCl HClO HClO3 HClO4
+5
0
+4
0
+4
-4
+4
+2
0
-2
+6
+6
-1
+7
+1
2.根据化学式求元素的化合价
六、易错点辨析
标出K2Cr2O7中Cr元素的化合价
写出K2Cr2O7中Cr元素的化合价
总结
K2Cr2O7
+6
+6
①标:先写化学式,再在该元素的正上方标出化合价
②写:直接写化合价即可
2、高氯酸镁[化学式:Mg(ClO4)2]可以作火箭、导弹、焰火等的固体氧化剂。高氯酸镁中氯元素化合价为( )
A.+1 B.+3 C.+5 D.+7
D
1. (2022年广西北部湾)Na2FeO4是一种新型水处理剂,其中Fe元素的化合价为( )A. +6
B. +3
C. +2
D. 0
A
例如:MgO、CaO、CO 、 CO2 、Fe3O4
金属在左,非金属在右,如:CuCl2、NaCl
1、金属元素和非金属元素形成的化合物
2、氧化物:氧在后
某化某
氧化某
六、怎样读化合物的化学式
3、氢元素和其他非金属元素组成的化合物
① 一般规律: 氢在左
② 特殊: H2O(水)、CH4(甲烷)、NH3(氨气)
某化氢
例如: HF
氟化氢
氯化氢
HCl
溴化氢
HBr
六、怎样读化合物的化学式
4、含有原子团的化合物
①酸:“某酸”,如:H2SO4,H2CO3,HNO3,HCl
②碱:“氢氧化某”,如:NaOH,Ca(OH)2,Fe(OH)2,Fe(OH)3
③盐:“某酸某”,如Na2CO3,KNO3, Al2(SO4)3
CO2 P2O5 N2 Ar 。
氩气 氮气 铁 水 。
氧化钙 二氧化锰 五氧化二氮 ;
1、请你写出下列物质的化学式
2、请你读出下列物质的名称
CaO
MnO2
N2O5
Ar
N2
Fe
H2O
氯化钠
氧化镁
硫化钙
氟化氢
二氧化碳
五氧化二磷
氮气
氩气
NaCl MgO CaS HF ;
同课章节目录
