1.1.3 物质的转化 课件(共12张ppt)高中化学 人教版 必修一
文档属性
| 名称 | 1.1.3 物质的转化 课件(共12张ppt)高中化学 人教版 必修一 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-29 00:00:00 | ||
图片预览



文档简介
(共12张PPT)
第一节 物质的分类及转化
课时3 物质的转化
人教版2019必修第一册
新课导入
溶洞的形成是碳酸钙与二氧化碳、水同时反应生成碳酸氢钙,反应的化学方程式为:
钟乳石和石笋的形成是碳酸氢钙分解生成碳酸钙、水和二氧化碳,反应的化学方程式为:
CaCO3+CO2+H2O = Ca(HCO3)2
Ca(HCO3)2 = CaCO3↓+H2O+CO2↑
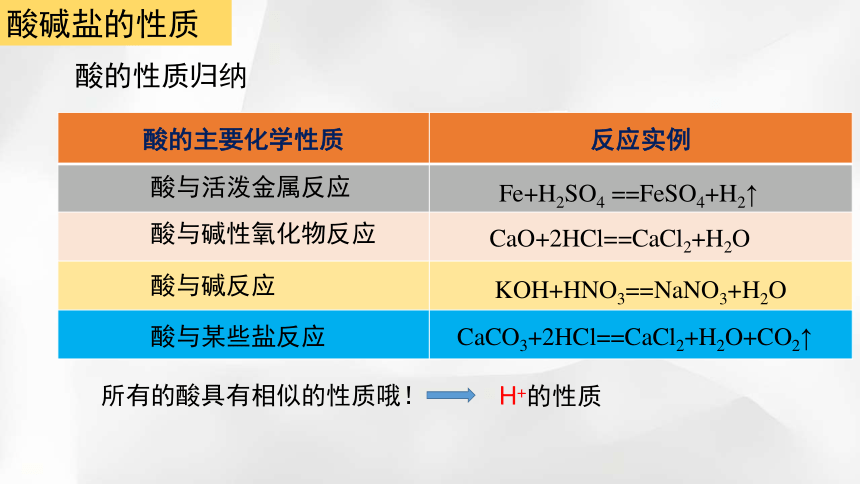
酸的性质归纳
酸的主要化学性质 反应实例
酸与活泼金属反应
酸与碱性氧化物反应
酸与碱反应
酸与某些盐反应
Fe+H2SO4 ==FeSO4+H2↑
CaO+2HCl==CaCl2+H2O
KOH+HNO3==NaNO3+H2O
CaCO3+2HCl==CaCl2+H2O+CO2↑
所有的酸具有相似的性质哦!
酸碱盐的性质
H+的性质
Fe2+溶液为浅绿色
Fe3+溶液为黄色
注意Fe元素的化合价!
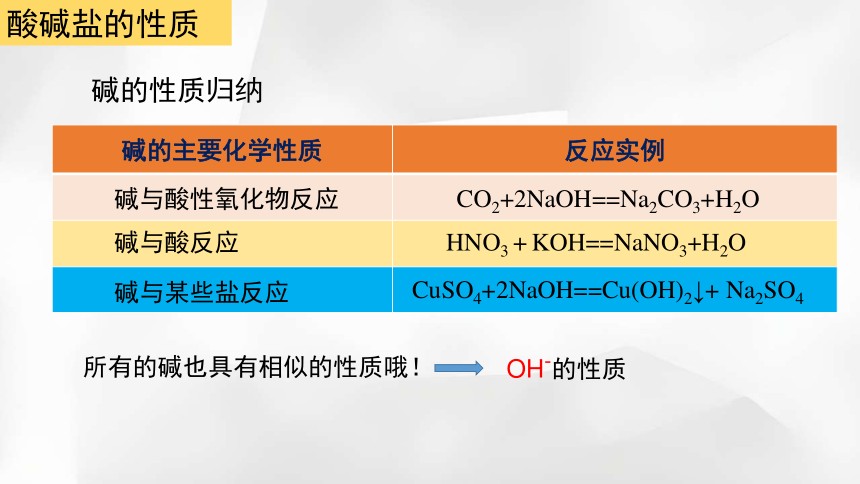
碱的性质归纳
碱的主要化学性质 反应实例
碱与酸性氧化物反应
碱与酸反应
碱与某些盐反应
CO2+2NaOH==Na2CO3+H2O
HNO3 + KOH==NaNO3+H2O
CuSO4+2NaOH==Cu(OH)2↓+ Na2SO4
所有的碱也具有相似的性质哦!
酸碱盐的性质
OH-的性质
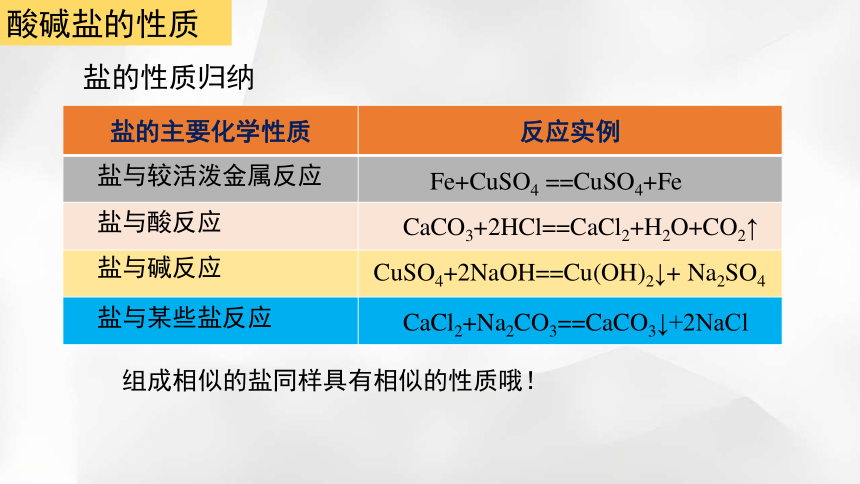
盐的性质归纳
盐的主要化学性质 反应实例
盐与较活泼金属反应
盐与酸反应
盐与碱反应
盐与某些盐反应
Fe+CuSO4 ==CuSO4+Fe
CaCO3+2HCl==CaCl2+H2O+CO2↑
CuSO4+2NaOH==Cu(OH)2↓+ Na2SO4
CaCl2+Na2CO3==CaCO3↓+2NaCl
组成相似的盐同样具有相似的性质哦!
酸碱盐的性质
化学反应的分类
反应通式 反应类型 实例(化学方程式)
A + B = C
C = A + B
AB + C = A + CB
AB + CD = AD + CB
化合反应
分解反应
置换反应
复分解反应
【思考与讨论】 P11
(1)写出下列物质之间转化的化学方程式,体会由金属单质到盐、非金属单质到盐的转化关系。
物质的转化
2Ca+O2 = 2CaO
CaO+H2O=Ca(OH)2
Ca(OH)2+H2SO4=CaSO4↓+2H2O
Ca(OH)2+SO3=CaSO4↓+H2O
O2
H2O
H2SO4、
SO3
O2
H2O
Ca(OH)2、
CaO
C+O2 == CO2
点燃
CO2+H2O == H2CO3
Ca(OH)2+H2CO3=CaCO3↓+2H2O
Ca(OH)2+CO2=CaCO3↓+H2O
思维发散
根据上述结论,请写出Na——Na2CO3、S——Na2SO3的转化关系?
Na——Na2CO3:
S——Na2SO3:
O2
H2O
H2CO3、CO2
O2
H2O
NaOH
小结
注意事项:
不是所有的酸和金属都能反应,且反应也不一定生成H2
酸性氧化物不一定与水反应生成酸。如SiO2(不溶于水)
碱性氧化物不一定与水反应生成碱。如CuO、Fe2O3(不溶于水)
物质转化的应用 P12
制备氢氧化钠的方法?
在制备时除要考虑反应进行的可能性外,还要考虑原料来源、成本高低和设备要求等因素。
1、碱性氧化物+水:Na2O + H2O = 2NaOH
2、碱+盐:Na2CO3 + Ca(OH)2 ═ CaCO3 ↓+ 2NaOH
来源少且成本高!
难以满足实际生产。
实际生产方法:电解饱和食盐水
2NaCl + 2H2O ══ 2NaOH + H2↑ + Cl2↑
电解
第一节 物质的分类及转化
课时3 物质的转化
人教版2019必修第一册
新课导入
溶洞的形成是碳酸钙与二氧化碳、水同时反应生成碳酸氢钙,反应的化学方程式为:
钟乳石和石笋的形成是碳酸氢钙分解生成碳酸钙、水和二氧化碳,反应的化学方程式为:
CaCO3+CO2+H2O = Ca(HCO3)2
Ca(HCO3)2 = CaCO3↓+H2O+CO2↑
酸的性质归纳
酸的主要化学性质 反应实例
酸与活泼金属反应
酸与碱性氧化物反应
酸与碱反应
酸与某些盐反应
Fe+H2SO4 ==FeSO4+H2↑
CaO+2HCl==CaCl2+H2O
KOH+HNO3==NaNO3+H2O
CaCO3+2HCl==CaCl2+H2O+CO2↑
所有的酸具有相似的性质哦!
酸碱盐的性质
H+的性质
Fe2+溶液为浅绿色
Fe3+溶液为黄色
注意Fe元素的化合价!
碱的性质归纳
碱的主要化学性质 反应实例
碱与酸性氧化物反应
碱与酸反应
碱与某些盐反应
CO2+2NaOH==Na2CO3+H2O
HNO3 + KOH==NaNO3+H2O
CuSO4+2NaOH==Cu(OH)2↓+ Na2SO4
所有的碱也具有相似的性质哦!
酸碱盐的性质
OH-的性质
盐的性质归纳
盐的主要化学性质 反应实例
盐与较活泼金属反应
盐与酸反应
盐与碱反应
盐与某些盐反应
Fe+CuSO4 ==CuSO4+Fe
CaCO3+2HCl==CaCl2+H2O+CO2↑
CuSO4+2NaOH==Cu(OH)2↓+ Na2SO4
CaCl2+Na2CO3==CaCO3↓+2NaCl
组成相似的盐同样具有相似的性质哦!
酸碱盐的性质
化学反应的分类
反应通式 反应类型 实例(化学方程式)
A + B = C
C = A + B
AB + C = A + CB
AB + CD = AD + CB
化合反应
分解反应
置换反应
复分解反应
【思考与讨论】 P11
(1)写出下列物质之间转化的化学方程式,体会由金属单质到盐、非金属单质到盐的转化关系。
物质的转化
2Ca+O2 = 2CaO
CaO+H2O=Ca(OH)2
Ca(OH)2+H2SO4=CaSO4↓+2H2O
Ca(OH)2+SO3=CaSO4↓+H2O
O2
H2O
H2SO4、
SO3
O2
H2O
Ca(OH)2、
CaO
C+O2 == CO2
点燃
CO2+H2O == H2CO3
Ca(OH)2+H2CO3=CaCO3↓+2H2O
Ca(OH)2+CO2=CaCO3↓+H2O
思维发散
根据上述结论,请写出Na——Na2CO3、S——Na2SO3的转化关系?
Na——Na2CO3:
S——Na2SO3:
O2
H2O
H2CO3、CO2
O2
H2O
NaOH
小结
注意事项:
不是所有的酸和金属都能反应,且反应也不一定生成H2
酸性氧化物不一定与水反应生成酸。如SiO2(不溶于水)
碱性氧化物不一定与水反应生成碱。如CuO、Fe2O3(不溶于水)
物质转化的应用 P12
制备氢氧化钠的方法?
在制备时除要考虑反应进行的可能性外,还要考虑原料来源、成本高低和设备要求等因素。
1、碱性氧化物+水:Na2O + H2O = 2NaOH
2、碱+盐:Na2CO3 + Ca(OH)2 ═ CaCO3 ↓+ 2NaOH
来源少且成本高!
难以满足实际生产。
实际生产方法:电解饱和食盐水
2NaCl + 2H2O ══ 2NaOH + H2↑ + Cl2↑
电解
