1.4物质性质的探究课件(共40张PPT内嵌视频)---九年级化学科粤版(2024)上册
文档属性
| 名称 | 1.4物质性质的探究课件(共40张PPT内嵌视频)---九年级化学科粤版(2024)上册 |  | |
| 格式 | pptx | ||
| 文件大小 | 16.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-10-31 22:11:06 | ||
图片预览











文档简介
(共40张PPT)
第一单元 大家都来学化学
科粤版 九年级上册
1.4 物质性质的探究
第1课时 物质的性质 物质性质的探究
第2课时 科学探究的一般过程
1、了解物质的物理性质和化学性质,并能识别。
2、能区分物质的物理变化与物理性质,化学变化与化学性质。
3、初步体验科学探究是研究物质的重要方法,逐步养成严谨的科学态度。
目标导航
第1课时 物质的性质 物质性质的探究
观察一瓶酒精,根据你的观察和生活经验,说出酒精有哪些性质?
颜色 状态 气味 密度 水溶性 挥发性
在化学变化中
表现出来的
没有经过化学
变化就表现出来
无色
液态
特殊气味
0.8g/mL
与水互溶
易挥发
能燃烧
在空气中点燃
新课导入
一、物质的性质
新课讲授
化学性质
物理性质
定义:物质在化学变化中才能表现出来的性质。
举例:可燃性、稳定性、氧化性、还原性、酸碱性
定义:不需要化学变化就能表现出来的性质 。
举例:物质的颜色、气味、状态、密度、熔点、沸点、硬度、挥发性、溶解性
可直接观察或用物理方法去测定。
要通过化学实验去观察和确定。
物质 颜色(常态) 气味 熔点/℃ 沸点/℃
水 无色(液态) 无气味 0 100
醋酸 无色(液态) 刺激性气味 17 118
铁 银白色(固态) 无气味 1 535 2 750
镁 银白色(固态) 无气味 649 1 107
氮气 无色(气态) 无气味 -210 -196
氧气 无色(气态) 无气味 -218 -183
几种常见物质的某些物理性质(标准大气压强下)
通常情况下,水是一种无色透明的液体,正常大气压下,0℃时水变成冰。
水
冰
检查站
请尝试描述水的物理性质。
描述性质时要注明条件!
下图哪些属于物理变化?哪些属于化学变化?为什么?
从这些变化中,你能推知相关物质各有哪些性质吗
问题探讨
化学变化
可燃性
化学变化
可燃性
物理变化
能蒸发
物理变化
易凝固
物理变化
易升华
化学变化
可燃性
物理变化
挥发性
性质和变化的区别和联系
物质的变化
物质的性质
酒精挥发(物理变化)
酒精能挥发(物理性质)
沥青凝固(物理变化)
沥青易凝固(物理性质)
纸片燃烧(化学变化)
纸片可燃烧(化学性质)
能、会、易、可
性质是物质的固有属性,是变化的内因。
变化是一个过程,是性质的具体表现。
助燃剂
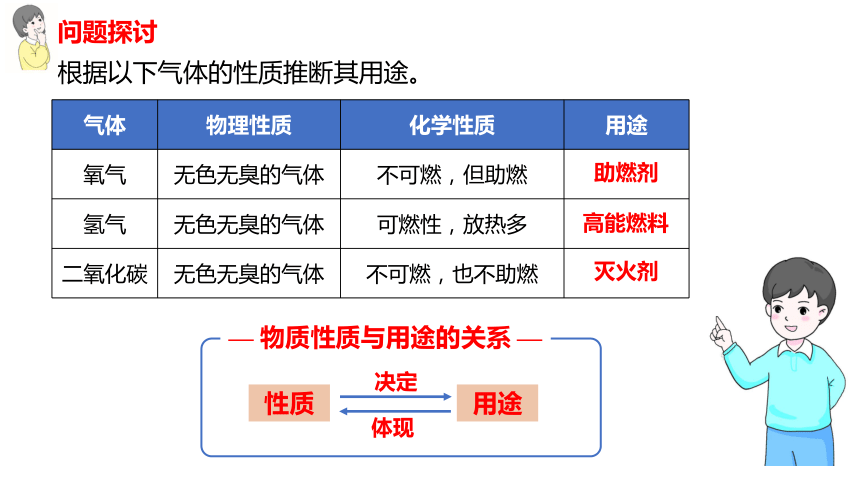
根据以下气体的性质推断其用途。
问题探讨
气体 物理性质 化学性质 用途
氧气 无色无臭的气体 不可燃,但助燃
氢气 无色无臭的气体 可燃性,放热多
二氧化碳 无色无臭的气体 不可燃,也不助燃
高能燃料
灭火剂
— 物质性质与用途的关系 —
性质
用途
决定
体现
二、性质的探究
科学探究是收集证据和作出解释,进行发现、创造与应用的科学实践活动,也是获取科学知识、理解科学本质、认识客观世界的重要途径。
我们可以通过铜受热变黑的化学实验来学习科学探究的方法。
探究实验
铜受热变黑原因的探究
铜片表面变黑的原因是什么?
提出问题:
形成假设:
假设一:铜片变黑,是因为火焰中的烟灰附着在铜片上。
如果铜片上附着的黑色物质是烟灰,则很容易抹去。
如果把铜片加热,而火焰没有与铜片接触,则铜片将不会变黑。
假设二:铜片变黑,是因为铜在空气中发生了化学反应。
若将铜片放在真空或隔绝空气的条件下加热,铜片的颜色将不变。
设计并实施实验 获取证据:
验证假设与预测一的实验。
用洁净的白色抹布轻轻擦一擦已冷却的铜片黑色部分。
将一段光亮铜片装在敞口的试管中,用酒精灯火焰加热试管。
验证假设与预测二的实验。
用银白色的金属铝箔将铜片严密包裹压紧,不留空隙,以保证隔绝空气,然后加热,再放冷,打开包裹的铝箔,观察铜片有无变色。
现象
判断 预测1______,预测2______。
错误
铜片上的黑色物质难擦掉;铜片在敞口试管中加热会变黑;用铝箔包裹加热,打开铝箔,铜片不变黑。
正确
获取证据 分析解释:
解释
【实验1】说明:铜片在空气中用酒精灯加热后变黑,黑色物质不是烟灰。
【实验2】说明:铜片在隔绝空气加热后不变色。据此可知:铜片在敞开的试管中加热后变黑,是因为铜片在空气中发生了化学反应,生成了黑色的新物质。
形成结论:
得出上述结论后,你可能还想问:
(1)生成的黑色物质是什么
(2)铜片和空气中的什么物质发生了反应
铜片在加热条件下,在空气中发生了化学反应,生成黑色物质。
反思评价:
(1)生成的黑色物质是什么?可设计以下实验。
【实验3】将铜片直接在酒精灯上多加热几分钟,冷却,用小刀将铜片表面生成的黑色物质刮落到干净的纸上,反复数次,使得到的黑色物质足够多,再移入试管中,滴加少量稀硫酸。
现象
判断 铜在空气或氧气中受热生成的黑色物质是_________,
所以上述“解释与结论”_______。
氧化铜
黑色物质溶于稀硫酸中,得到一种蓝色溶液。
正确
提出问题:铜片和空气中的什么物质发生了反应?
实验验证:使用氧气传感器定量测定反应过程中氧气含量的变化
得出结论:铜受热一段时间后,装置中的氧气含量不断减少,证明铜与氧气发生了反应。
利用手持技术数字化实验探究铜和氧气的反应
实验装置图
“氧气含量—时间”曲线图
表达交流:
1、以上铜片发生的化学反应可用文字表达:
(Cu)
(O2)
(CuO)
(括号里给出的是相应物质的化学符号)
加热
铜 + 氧气 氧化铜
— 化学反应的文字表达式—
化学反应的文字表达式是一种简化的化学反应表示方法。
反应物
生成物
反应条件
表达交流:
2、同学们就以上现象、解释和结论发表自己的意见,互相讨论交流,可提出其他预测和实验证实的思路。
课堂小结
铜的化学性质的探究
物质的性质
化学性质
提出问题、形成假设
物理性质
设计并实施实验、获取证据
1.4 物质性质的探究
分析解释 形成结论
反思评价
表达交流
1、物质的下列性质中,属于物理性质的是( )
A.氧化性 B.还原性 C.延展性 D.可燃性
C
随堂练习
这里的氧化性、还原性、可燃性均需要在化学变化中表现出来,属于化学性质,而延展性不需要发生化学变化就能表现出来,
属于物理性质。
2、下列属于氮气的化学性质的是( )
A.无色无臭 B.难溶于水
C.密度略小于空气 D.不支持燃烧
D
A、无色无臭描述的是物质的颜色、气味,不需要发生化学变化就能表现出来,属于物理性质;
B、难溶于水是指物质的水溶性,不需要发生化学变化就能表现出来,属于物理性质;
C、密度略小于空气,不需要发生化学变化就能表现出来,属于物理性质;
D、不支持燃烧,需要发生化学变化才能表现出来,属于化学性质。
.
3、下列物质的用途体现物质化学性质的是( )
A.金刚石的硬度大—刻划玻璃 B.氢气密度小—填充探空气球C.干冰有制冷作用—人工增雨 D.一氧化碳具有还原性—冶炼金属
D
A、金刚石的硬度大可以刻划玻璃,硬度不需要通过化学变化
表现出来,属于物理性质;
B、密度不需要通过化学变化表现出来,属于物理性质;
C、干冰有制冷作用,是利用干冰升华吸热,使周围温度降低,
水蒸气冷凝成水滴,属于物理性质;
D、冶炼金属是利用一氧化碳的还原性,用还原剂与含金属元素的化合物反应,利用了物质的化学性质。
4、某同学对一未知金属做了如下实验:取一块金属,用小刀切下一块,并将其投入水中,该金属漂浮于水面,并与水发生剧烈反应,在水面上急速转动,四处游动,同时发出嘶嘶的响声,立刻熔化成一个闪亮的、银白色的小球,并逐渐缩小,直至完全消失。
请分析以上实验现象,归纳出该金属四种性质:
(1)_________________,
(2)_________________,
(3)_________________,
(4)_________________。
硬度小
密度比水小
熔点低
银白色的固体
5、下面是某学习小组针对科学探究提出的几个问题,请将下列所述基本环节补充完整。
(1)“铜片在酒精灯上加热为什么会变黑?”属于科学探究中__________环节。
(2)“铜片变黑不是火焰中的烟灰附着在铜片上”属于科学探究中_________环节。
(3)“铜片变黑可能是火焰中的烟灰附着在铜片上”属于科学探究中___________环节。
(4)“将铜片放在敞口的试管中加热,铜片变黑”属于科学探究中 ____________环节。
(5)“这个实验既简单,现象又明显”,某同学的这句话属于科学探究中的___________
环节。
上述各环节的正确顺序是 ______________(填上述数字序号)。
提出问题
得出结论
假设与预测
实验与事实
反思与评价
(1) (3) (4) (2) (5)
1、初步学习科学探究的基本环节。
2、能结合具体探究活动说明科学探究的要素及各要素之间的关系。
3、感受合作与交流在科学探究中的重要作用。
目标导航
第2课时 科学探究的一般过程
新课导入
经过上节课的学习,我们知道了铜受热变黑的原因,经历了一个完整的科学探究过程。科学探究的一般过程包括了哪些环节呢
柯柯
提出问题
形成假设
设计并实施实验
获取证据
分析解释
形成结论,建构模型
反思评价
表达交流
在铜受热变黑原因的探究中,可以通过观察铜片受热的实验现象,收集证据进行定性探究。
在铜受热变黑原因的探究中,可以通过测定反应过程中氧气含量变化的数据证据进行定量探究。
实验原理
新课讲授
科学探究的一般过程包括了8个环节:
提出问题
形成假设
设计并实施实验
获取证据
分析解释
形成结论,建构模型
反思评价
表达交流
设计并实施实验
以现象证据为主的定性实验
以数据证据为主的定量实验
设计并实施调查方案
实践活动
目的:探究人体吸入和呼出气体成分含量的差异。
我们一生中不断吸入空气和呼出气体,吸入和呼出的气体成分含量有没有差别呢
提出问题
提示信息
空气
氮气
氧气
二氧化碳
水蒸气等
化学性质稳定
物质性质
氧气可以支持燃烧
二氧化碳可以使澄清石灰水变浑浊
可
探究成分
1、吸入空气中氧气的含量大于呼出气体中氧气的含量。
2、呼出气体中__________的含量大于吸入空气中__________的含量。
形成假设
提示信息
空气
氮气
氧气
二氧化碳
水蒸气等
化学性质稳定
物质性质
氧气可以支持燃烧
二氧化碳可以使澄清石灰水变浑浊
可
探究成分
二氧化碳
二氧化碳
呼出气体中________ 的含量大于吸入空气中_________的含量。
水蒸气
水蒸气
取两个空集气瓶,用玻璃片将瓶口盖好,作为空气样品;再用排水法收集两瓶呼出气体。比较呼出气体与新鲜空气中成分含量的差异。
设计并实施实验
(1)借助以下图示设计实验,验证假设1。
设计并实施实验
(2)设计实验,验证假设2。
设计并实施实验
(2)设计实验,验证假设2。
设计并实施实验
解释与结论
氧气 二氧化碳 水蒸气
吸入空气
呼出气体
较多 较少 较少
较少 较多 较多
除了以上实验方法,我们还可以运用手持技术数字化实验,通过氧气传感器和二氧化碳传感器定量测量吸入和呼出的气体中氧气、二氧化碳的含量。
表达交流
有人说:“人呼吸就是吸进氧气,呼出二氧化碳。”他的这种说法对吗?
从实验数据可以看出,人吸入的气体中很有二氧化碳,呼出的气体中仍然存在氧气,只是气体的含量发生了变化。
气体的体积分数 吸入气体(%) 呼出气体(%)
氧气 20.96 16.40
二氧化碳 0.04 4.10
其他气体 79.00 79.50
课堂小结
探究人体吸入和呼出气体成分含量的差异
科学探究的
一般过程
氧气含量减少
二氧化碳含量增多
水蒸气含量增多
1.4 物质性质的探究
1、科学探究的一个重要环节是“猜想”,猜想是依据已有知识、经验,对提出的问题进行合理的假设。下列对“影响食物腐败快慢的因素”的猜想不合理的是( )
A.环境温度 B.氧气浓度 C.食物品种 D.食物多少
D
随堂练习
根据影响食物腐败快慢的因素有内因和外因,内因是由物质本身的性质决定,而外因是指温度、浓度、压强、催化剂等因素,进行分析判断。D、取不同量的同种食物,在其它条件相同的情况下,食物腐败快慢相同,则食物的多少不是影响食物腐败快慢的因素,猜想不合理。
2、化学实验课上,吹灭燃烧的蜡烛时,有白烟产生。有同学说“白烟可能是石蜡蒸气凝结成的石蜡固体”,于是有同学用燃着的木条去点燃白烟。对于“用燃着的木条去点燃白烟”,属于科学探究中的( )
A.设计实验 B.提出问题 C.进行实验 D.得出结论
C
根据科学探究的主要环节有提出问题→猜想与假设→制定计划(或设计方案)→进行实验→收集证据→解释与结论→反思与评价→拓展与迁移。有同学用燃着的木条去点燃白烟,属于科学探究中的进行实验。
3、下面是一小组针对科学探究提出的几个问题,请将下列所述基本环节补充完整。
(1)“呼出的气体中一定有二氧化碳”属于科学探究的_________环节;
(2)“呼出的气体中可能有二氧化碳”属于科学探究的____________环节;
(3)“呼出的气体是什么?”属于科学探究的__________环节;
(4)“将呼出的气体吹入澄清石灰水中,发现石灰水变浑浊”属于科学探究的_________环节;
(5)“这个实验既操作简单,又现象明显”,某同学的这句话属于科学探究的
__________环节;
上述各环节的正确顺序是_____________________________。
提出问题
形成结论
形成假设
获取证据
反思评价
(3)(2)(4)(1)(5)
第一单元 大家都来学化学
科粤版 九年级上册
1.4 物质性质的探究
第1课时 物质的性质 物质性质的探究
第2课时 科学探究的一般过程
1、了解物质的物理性质和化学性质,并能识别。
2、能区分物质的物理变化与物理性质,化学变化与化学性质。
3、初步体验科学探究是研究物质的重要方法,逐步养成严谨的科学态度。
目标导航
第1课时 物质的性质 物质性质的探究
观察一瓶酒精,根据你的观察和生活经验,说出酒精有哪些性质?
颜色 状态 气味 密度 水溶性 挥发性
在化学变化中
表现出来的
没有经过化学
变化就表现出来
无色
液态
特殊气味
0.8g/mL
与水互溶
易挥发
能燃烧
在空气中点燃
新课导入
一、物质的性质
新课讲授
化学性质
物理性质
定义:物质在化学变化中才能表现出来的性质。
举例:可燃性、稳定性、氧化性、还原性、酸碱性
定义:不需要化学变化就能表现出来的性质 。
举例:物质的颜色、气味、状态、密度、熔点、沸点、硬度、挥发性、溶解性
可直接观察或用物理方法去测定。
要通过化学实验去观察和确定。
物质 颜色(常态) 气味 熔点/℃ 沸点/℃
水 无色(液态) 无气味 0 100
醋酸 无色(液态) 刺激性气味 17 118
铁 银白色(固态) 无气味 1 535 2 750
镁 银白色(固态) 无气味 649 1 107
氮气 无色(气态) 无气味 -210 -196
氧气 无色(气态) 无气味 -218 -183
几种常见物质的某些物理性质(标准大气压强下)
通常情况下,水是一种无色透明的液体,正常大气压下,0℃时水变成冰。
水
冰
检查站
请尝试描述水的物理性质。
描述性质时要注明条件!
下图哪些属于物理变化?哪些属于化学变化?为什么?
从这些变化中,你能推知相关物质各有哪些性质吗
问题探讨
化学变化
可燃性
化学变化
可燃性
物理变化
能蒸发
物理变化
易凝固
物理变化
易升华
化学变化
可燃性
物理变化
挥发性
性质和变化的区别和联系
物质的变化
物质的性质
酒精挥发(物理变化)
酒精能挥发(物理性质)
沥青凝固(物理变化)
沥青易凝固(物理性质)
纸片燃烧(化学变化)
纸片可燃烧(化学性质)
能、会、易、可
性质是物质的固有属性,是变化的内因。
变化是一个过程,是性质的具体表现。
助燃剂
根据以下气体的性质推断其用途。
问题探讨
气体 物理性质 化学性质 用途
氧气 无色无臭的气体 不可燃,但助燃
氢气 无色无臭的气体 可燃性,放热多
二氧化碳 无色无臭的气体 不可燃,也不助燃
高能燃料
灭火剂
— 物质性质与用途的关系 —
性质
用途
决定
体现
二、性质的探究
科学探究是收集证据和作出解释,进行发现、创造与应用的科学实践活动,也是获取科学知识、理解科学本质、认识客观世界的重要途径。
我们可以通过铜受热变黑的化学实验来学习科学探究的方法。
探究实验
铜受热变黑原因的探究
铜片表面变黑的原因是什么?
提出问题:
形成假设:
假设一:铜片变黑,是因为火焰中的烟灰附着在铜片上。
如果铜片上附着的黑色物质是烟灰,则很容易抹去。
如果把铜片加热,而火焰没有与铜片接触,则铜片将不会变黑。
假设二:铜片变黑,是因为铜在空气中发生了化学反应。
若将铜片放在真空或隔绝空气的条件下加热,铜片的颜色将不变。
设计并实施实验 获取证据:
验证假设与预测一的实验。
用洁净的白色抹布轻轻擦一擦已冷却的铜片黑色部分。
将一段光亮铜片装在敞口的试管中,用酒精灯火焰加热试管。
验证假设与预测二的实验。
用银白色的金属铝箔将铜片严密包裹压紧,不留空隙,以保证隔绝空气,然后加热,再放冷,打开包裹的铝箔,观察铜片有无变色。
现象
判断 预测1______,预测2______。
错误
铜片上的黑色物质难擦掉;铜片在敞口试管中加热会变黑;用铝箔包裹加热,打开铝箔,铜片不变黑。
正确
获取证据 分析解释:
解释
【实验1】说明:铜片在空气中用酒精灯加热后变黑,黑色物质不是烟灰。
【实验2】说明:铜片在隔绝空气加热后不变色。据此可知:铜片在敞开的试管中加热后变黑,是因为铜片在空气中发生了化学反应,生成了黑色的新物质。
形成结论:
得出上述结论后,你可能还想问:
(1)生成的黑色物质是什么
(2)铜片和空气中的什么物质发生了反应
铜片在加热条件下,在空气中发生了化学反应,生成黑色物质。
反思评价:
(1)生成的黑色物质是什么?可设计以下实验。
【实验3】将铜片直接在酒精灯上多加热几分钟,冷却,用小刀将铜片表面生成的黑色物质刮落到干净的纸上,反复数次,使得到的黑色物质足够多,再移入试管中,滴加少量稀硫酸。
现象
判断 铜在空气或氧气中受热生成的黑色物质是_________,
所以上述“解释与结论”_______。
氧化铜
黑色物质溶于稀硫酸中,得到一种蓝色溶液。
正确
提出问题:铜片和空气中的什么物质发生了反应?
实验验证:使用氧气传感器定量测定反应过程中氧气含量的变化
得出结论:铜受热一段时间后,装置中的氧气含量不断减少,证明铜与氧气发生了反应。
利用手持技术数字化实验探究铜和氧气的反应
实验装置图
“氧气含量—时间”曲线图
表达交流:
1、以上铜片发生的化学反应可用文字表达:
(Cu)
(O2)
(CuO)
(括号里给出的是相应物质的化学符号)
加热
铜 + 氧气 氧化铜
— 化学反应的文字表达式—
化学反应的文字表达式是一种简化的化学反应表示方法。
反应物
生成物
反应条件
表达交流:
2、同学们就以上现象、解释和结论发表自己的意见,互相讨论交流,可提出其他预测和实验证实的思路。
课堂小结
铜的化学性质的探究
物质的性质
化学性质
提出问题、形成假设
物理性质
设计并实施实验、获取证据
1.4 物质性质的探究
分析解释 形成结论
反思评价
表达交流
1、物质的下列性质中,属于物理性质的是( )
A.氧化性 B.还原性 C.延展性 D.可燃性
C
随堂练习
这里的氧化性、还原性、可燃性均需要在化学变化中表现出来,属于化学性质,而延展性不需要发生化学变化就能表现出来,
属于物理性质。
2、下列属于氮气的化学性质的是( )
A.无色无臭 B.难溶于水
C.密度略小于空气 D.不支持燃烧
D
A、无色无臭描述的是物质的颜色、气味,不需要发生化学变化就能表现出来,属于物理性质;
B、难溶于水是指物质的水溶性,不需要发生化学变化就能表现出来,属于物理性质;
C、密度略小于空气,不需要发生化学变化就能表现出来,属于物理性质;
D、不支持燃烧,需要发生化学变化才能表现出来,属于化学性质。
.
3、下列物质的用途体现物质化学性质的是( )
A.金刚石的硬度大—刻划玻璃 B.氢气密度小—填充探空气球C.干冰有制冷作用—人工增雨 D.一氧化碳具有还原性—冶炼金属
D
A、金刚石的硬度大可以刻划玻璃,硬度不需要通过化学变化
表现出来,属于物理性质;
B、密度不需要通过化学变化表现出来,属于物理性质;
C、干冰有制冷作用,是利用干冰升华吸热,使周围温度降低,
水蒸气冷凝成水滴,属于物理性质;
D、冶炼金属是利用一氧化碳的还原性,用还原剂与含金属元素的化合物反应,利用了物质的化学性质。
4、某同学对一未知金属做了如下实验:取一块金属,用小刀切下一块,并将其投入水中,该金属漂浮于水面,并与水发生剧烈反应,在水面上急速转动,四处游动,同时发出嘶嘶的响声,立刻熔化成一个闪亮的、银白色的小球,并逐渐缩小,直至完全消失。
请分析以上实验现象,归纳出该金属四种性质:
(1)_________________,
(2)_________________,
(3)_________________,
(4)_________________。
硬度小
密度比水小
熔点低
银白色的固体
5、下面是某学习小组针对科学探究提出的几个问题,请将下列所述基本环节补充完整。
(1)“铜片在酒精灯上加热为什么会变黑?”属于科学探究中__________环节。
(2)“铜片变黑不是火焰中的烟灰附着在铜片上”属于科学探究中_________环节。
(3)“铜片变黑可能是火焰中的烟灰附着在铜片上”属于科学探究中___________环节。
(4)“将铜片放在敞口的试管中加热,铜片变黑”属于科学探究中 ____________环节。
(5)“这个实验既简单,现象又明显”,某同学的这句话属于科学探究中的___________
环节。
上述各环节的正确顺序是 ______________(填上述数字序号)。
提出问题
得出结论
假设与预测
实验与事实
反思与评价
(1) (3) (4) (2) (5)
1、初步学习科学探究的基本环节。
2、能结合具体探究活动说明科学探究的要素及各要素之间的关系。
3、感受合作与交流在科学探究中的重要作用。
目标导航
第2课时 科学探究的一般过程
新课导入
经过上节课的学习,我们知道了铜受热变黑的原因,经历了一个完整的科学探究过程。科学探究的一般过程包括了哪些环节呢
柯柯
提出问题
形成假设
设计并实施实验
获取证据
分析解释
形成结论,建构模型
反思评价
表达交流
在铜受热变黑原因的探究中,可以通过观察铜片受热的实验现象,收集证据进行定性探究。
在铜受热变黑原因的探究中,可以通过测定反应过程中氧气含量变化的数据证据进行定量探究。
实验原理
新课讲授
科学探究的一般过程包括了8个环节:
提出问题
形成假设
设计并实施实验
获取证据
分析解释
形成结论,建构模型
反思评价
表达交流
设计并实施实验
以现象证据为主的定性实验
以数据证据为主的定量实验
设计并实施调查方案
实践活动
目的:探究人体吸入和呼出气体成分含量的差异。
我们一生中不断吸入空气和呼出气体,吸入和呼出的气体成分含量有没有差别呢
提出问题
提示信息
空气
氮气
氧气
二氧化碳
水蒸气等
化学性质稳定
物质性质
氧气可以支持燃烧
二氧化碳可以使澄清石灰水变浑浊
可
探究成分
1、吸入空气中氧气的含量大于呼出气体中氧气的含量。
2、呼出气体中__________的含量大于吸入空气中__________的含量。
形成假设
提示信息
空气
氮气
氧气
二氧化碳
水蒸气等
化学性质稳定
物质性质
氧气可以支持燃烧
二氧化碳可以使澄清石灰水变浑浊
可
探究成分
二氧化碳
二氧化碳
呼出气体中________ 的含量大于吸入空气中_________的含量。
水蒸气
水蒸气
取两个空集气瓶,用玻璃片将瓶口盖好,作为空气样品;再用排水法收集两瓶呼出气体。比较呼出气体与新鲜空气中成分含量的差异。
设计并实施实验
(1)借助以下图示设计实验,验证假设1。
设计并实施实验
(2)设计实验,验证假设2。
设计并实施实验
(2)设计实验,验证假设2。
设计并实施实验
解释与结论
氧气 二氧化碳 水蒸气
吸入空气
呼出气体
较多 较少 较少
较少 较多 较多
除了以上实验方法,我们还可以运用手持技术数字化实验,通过氧气传感器和二氧化碳传感器定量测量吸入和呼出的气体中氧气、二氧化碳的含量。
表达交流
有人说:“人呼吸就是吸进氧气,呼出二氧化碳。”他的这种说法对吗?
从实验数据可以看出,人吸入的气体中很有二氧化碳,呼出的气体中仍然存在氧气,只是气体的含量发生了变化。
气体的体积分数 吸入气体(%) 呼出气体(%)
氧气 20.96 16.40
二氧化碳 0.04 4.10
其他气体 79.00 79.50
课堂小结
探究人体吸入和呼出气体成分含量的差异
科学探究的
一般过程
氧气含量减少
二氧化碳含量增多
水蒸气含量增多
1.4 物质性质的探究
1、科学探究的一个重要环节是“猜想”,猜想是依据已有知识、经验,对提出的问题进行合理的假设。下列对“影响食物腐败快慢的因素”的猜想不合理的是( )
A.环境温度 B.氧气浓度 C.食物品种 D.食物多少
D
随堂练习
根据影响食物腐败快慢的因素有内因和外因,内因是由物质本身的性质决定,而外因是指温度、浓度、压强、催化剂等因素,进行分析判断。D、取不同量的同种食物,在其它条件相同的情况下,食物腐败快慢相同,则食物的多少不是影响食物腐败快慢的因素,猜想不合理。
2、化学实验课上,吹灭燃烧的蜡烛时,有白烟产生。有同学说“白烟可能是石蜡蒸气凝结成的石蜡固体”,于是有同学用燃着的木条去点燃白烟。对于“用燃着的木条去点燃白烟”,属于科学探究中的( )
A.设计实验 B.提出问题 C.进行实验 D.得出结论
C
根据科学探究的主要环节有提出问题→猜想与假设→制定计划(或设计方案)→进行实验→收集证据→解释与结论→反思与评价→拓展与迁移。有同学用燃着的木条去点燃白烟,属于科学探究中的进行实验。
3、下面是一小组针对科学探究提出的几个问题,请将下列所述基本环节补充完整。
(1)“呼出的气体中一定有二氧化碳”属于科学探究的_________环节;
(2)“呼出的气体中可能有二氧化碳”属于科学探究的____________环节;
(3)“呼出的气体是什么?”属于科学探究的__________环节;
(4)“将呼出的气体吹入澄清石灰水中,发现石灰水变浑浊”属于科学探究的_________环节;
(5)“这个实验既操作简单,又现象明显”,某同学的这句话属于科学探究的
__________环节;
上述各环节的正确顺序是_____________________________。
提出问题
形成结论
形成假设
获取证据
反思评价
(3)(2)(4)(1)(5)
同课章节目录
