3.2.1 金属材料 课件(共18张PPT)高中化学 人教版(2019)必修 第一册
文档属性
| 名称 | 3.2.1 金属材料 课件(共18张PPT)高中化学 人教版(2019)必修 第一册 |  | |
| 格式 | pptx | ||
| 文件大小 | 26.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-11-01 16:35:13 | ||
图片预览



文档简介
(共18张PPT)
第4课时
金属材料
第三章 第1节 铁及其化合物
合金
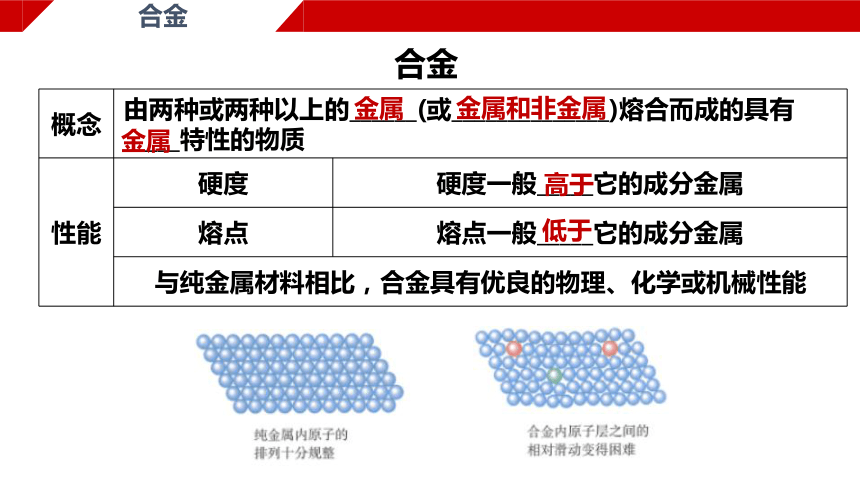
合金
概念 由两种或两种以上的______(或______________)熔合而成的具有_____特性的物质
性能 硬度 硬度一般_____它的成分金属
熔点 熔点一般_____它的成分金属
与纯金属材料相比,合金具有优良的物理、化学或机械性能
金属
金属和非金属
金属
高于
低于
不能。当铜开始熔化时,钠已经气化,所以二者不能形成合金。
1、改进合金性能的常用措施有哪些?
调节所添加的元素种类、含量和生成条件
2、合金比成分金属的硬度大,原因是什么?
纯金属所有原子的大小和形状相同,原子排列十分规整;
加入其他元素的原子后,改变了金属原子有规则的层状排列,
使原子层之间的相对滑动变得困难,导致合金硬度变大。
3、已知铜的熔点为1083℃,钠的沸点为883℃,试问铜与钠能否形成合金?
合金
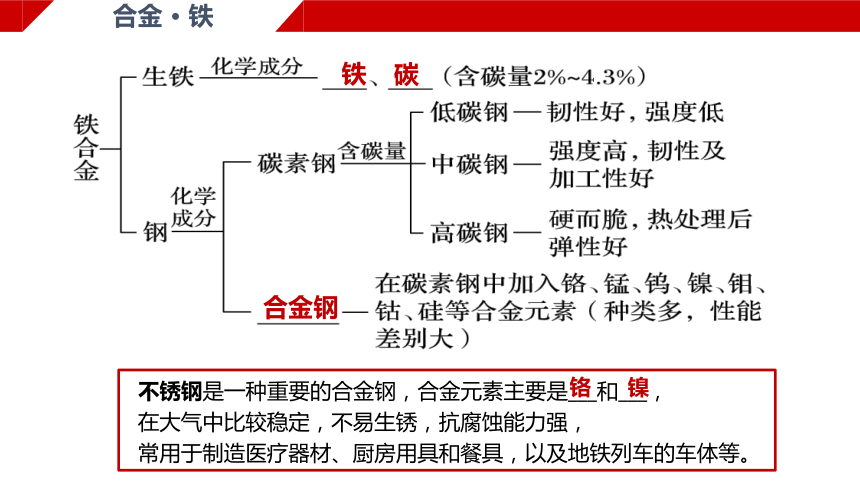
铁
碳
合金钢
不锈钢是一种重要的合金钢,合金元素主要是___和___,
在大气中比较稳定,不易生锈,抗腐蚀能力强,
常用于制造医疗器材、厨房用具和餐具,以及地铁列车的车体等。
铬
镍
合金 · 铁
2022年世界冬奥会和冬残奥会在北京举行,其中短道速滑项目队员所穿的速滑冰刀采用合金材料——不锈钢制成。
下列关于合金的叙述,错误的是( )
A.通过增加原子层之间的相对滑动难度,使合金的硬度变大
B.不锈钢中添加镍(Ni)和铬(Cr)等元素,因此不含非金属元素
C.储氢合金属于新型合金,可用于以氢气为燃料的汽车
D.硬铝具有强度高、密度小、抗腐蚀能力强等优点,常用于制造飞机外壳
B
合金 · 铁
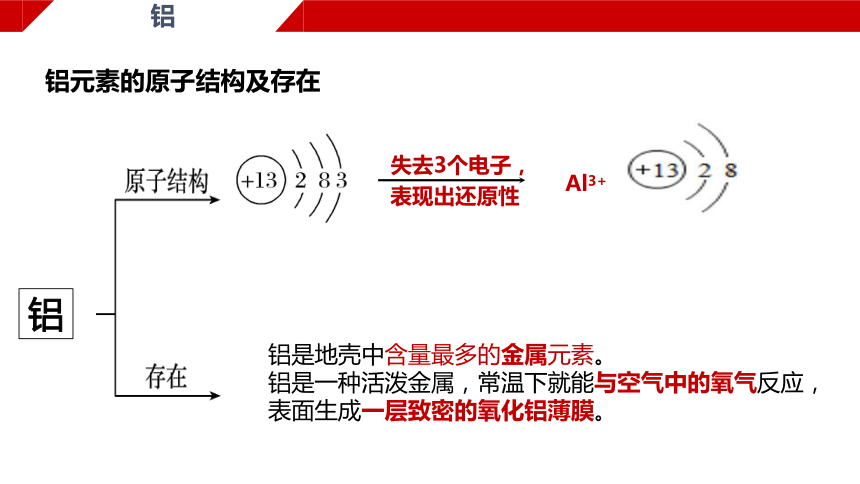
铝元素的原子结构及存在
铝
失去3个电子,
表现出还原性
Al3+
铝是地壳中含量最多的金属元素。
铝是一种活泼金属,常温下就能与空气中的氧气反应,
表面生成一层致密的氧化铝薄膜。
铝
铝
实验 操作
实验 现象 铝片_________,一段时间后有无色气泡冒出,将点燃的木条放在试管口有_______
逐渐溶解
爆鸣声
Al2O3+6HCl=2AlCl3+3H2O
2Al+6HCl=2AlCl3+3H2 ↑
铝
实验1:将未打磨的铝片放入盐酸中,
一段时间后将点燃的木条放在试管口
实验2:向两支装有NaOH的试管中,分别放入未打磨的铝片、打磨后的铝片;一段时间后将点燃的木条放在试管口
铝
实验操作
实验现象 试管①中一开始无气泡产生,一段时间后,铝片_____,有无色气泡冒出,
试管②中铝片溶解,立即产生无色气泡,将点燃的木条放在试管口,都有_______
化学方程式
溶解
爆鸣声
Al2O3+2NaOH +3H2O= 2Na[Al(OH)4]
2Al+2NaOH+6H2O = 2Na[Al(OH)4] +3H2↑
实验2:向两支装有NaOH的试管中,分别放入未打磨的铝片、打磨后的铝片;一段时间后将点燃的木条放在试管口
铝
【实验结论】
(1)Al 既能与稀HCl反应又能与NaOH溶液反应,都生成盐和氢气。
(2)Al2O3既能与稀HCl反应又能与NaOH溶液反应,都生成盐和水。
【两性氧化物、两性氢氧化物】
(1)两性氧化物:既能与酸反应生成盐和水,又能与碱反应生成盐和水的氧化物,如Al2O3。
(2)两性氢氧化物:既能与酸反应生成盐和水,又能与碱反应生成盐和水的氢氧化物,如Al(OH)3。
Al(OH)3溶于盐酸:_____________________________。
Al(OH)3溶于NaOH溶液:________________________________。
Al(OH)3+3HCl=AlCl3+3H2O
Al(OH)3+NaOH=Na[Al(OH)4]
Al
与酸反应
与碱反应
2Al+2NaOH+6H2O= 2Na[Al(OH)4] +3H2↑
2Al+6HCl=2AlCl3+3H2 ↑
Al2O3
与酸反应
与碱反应
Al2O3+2NaOH+3H2O= 2Na[Al(OH)4]
Al2O3+6HCl=2AlCl3+3H2 O
Al(OH)3
与酸反应
与碱反应
Al(OH)3+3HCl=AlCl3+3H2O
Al(OH)3+NaOH= Na[Al(OH)4]
两性氧化物
两性氢氧化物
铝
铝合金是目前用途广泛的合金之一,硬铝是在铝中添加了一定比例的Cu、Mg、Mn、Si,密度小,强度高,具有较强抗腐蚀能力,是制造飞机和宇宙飞船的理想材料。
铝合金
1.储氢合金:一类能够大量吸收H2,并与H2结合成金属氢化物的材料。如Ti-Fe合金、La-Ni合金,为氢气作为能源的实际应用起到重要的推动作用。
2.其他新型合金:钛合金、耐热合金和形状记忆合金等新型合金广泛应用于航空航天、生物工程和电子工业等领域。
新型合金
(1)镧系元素(57~71号元素)及钇和钪,共17种元素为稀土元素。
我国拥有丰富的稀土资源,现已查明的世界稀土资源中,80%分布在我国,并且品种齐全。
(2)稀土金属有着广泛的用途,它既可以单独使用,也可用于生产合金。在合金中加入适量稀土金属,能大大改善合金的性能。因而,稀土元素又被称为“冶金工业的维生素”。
稀土
1、我国“蛟龙”号载人潜水器已成功下潜至海中7 062.68米处。“蛟龙”号载人潜水器的外壳是耐超高压的钛合金,下面有关合金的说法正确的是( )
A.钛合金是一种新型金属单质 B.钛合金熔点比钛金属高
C.钛合金的硬度与钛单质相同 D.青铜、合金钢和硬铝都是合金
D
2、下列关于新型合金材料说法不正确的是( )
A.镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料
B.钛合金生物相容性好,强度大,可作人造骨骼
C.形状记忆合金可在使合金发生形变的作用力消失后恢复原状
D.利用合金的熔点低于成分金属这一特点可制得耐热合金
D
练习
3、镁铝合金质优体轻,又不易锈蚀,大量用于航空工业、造船工业、日用化工等领域。下列关于镁铝合金性质的叙述中,不正确的是( )
A.此合金的熔点比镁和铝的熔点都低
B.此合金能全部溶解于足量稀盐酸中
C.此合金能全部溶解于足量氢氧化钠溶液中
D.此合金的硬度比镁和铝的硬度都大
C
练习
4、某学习小组用如图所示装置测定铝镁合金中铝的质量分数
(1)A中试剂为 。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,
其目的是 。
(3)B中发生反应的化学方程式为___________
_____________________________________。
氢氧化钠溶液
除去铝镁合金表面的氧化膜
2Al+2NaOH+6H2O= 2Na[Al(OH)4] +3H2↑
练习
第4课时
金属材料
第三章 第1节 铁及其化合物
合金
合金
概念 由两种或两种以上的______(或______________)熔合而成的具有_____特性的物质
性能 硬度 硬度一般_____它的成分金属
熔点 熔点一般_____它的成分金属
与纯金属材料相比,合金具有优良的物理、化学或机械性能
金属
金属和非金属
金属
高于
低于
不能。当铜开始熔化时,钠已经气化,所以二者不能形成合金。
1、改进合金性能的常用措施有哪些?
调节所添加的元素种类、含量和生成条件
2、合金比成分金属的硬度大,原因是什么?
纯金属所有原子的大小和形状相同,原子排列十分规整;
加入其他元素的原子后,改变了金属原子有规则的层状排列,
使原子层之间的相对滑动变得困难,导致合金硬度变大。
3、已知铜的熔点为1083℃,钠的沸点为883℃,试问铜与钠能否形成合金?
合金
铁
碳
合金钢
不锈钢是一种重要的合金钢,合金元素主要是___和___,
在大气中比较稳定,不易生锈,抗腐蚀能力强,
常用于制造医疗器材、厨房用具和餐具,以及地铁列车的车体等。
铬
镍
合金 · 铁
2022年世界冬奥会和冬残奥会在北京举行,其中短道速滑项目队员所穿的速滑冰刀采用合金材料——不锈钢制成。
下列关于合金的叙述,错误的是( )
A.通过增加原子层之间的相对滑动难度,使合金的硬度变大
B.不锈钢中添加镍(Ni)和铬(Cr)等元素,因此不含非金属元素
C.储氢合金属于新型合金,可用于以氢气为燃料的汽车
D.硬铝具有强度高、密度小、抗腐蚀能力强等优点,常用于制造飞机外壳
B
合金 · 铁
铝元素的原子结构及存在
铝
失去3个电子,
表现出还原性
Al3+
铝是地壳中含量最多的金属元素。
铝是一种活泼金属,常温下就能与空气中的氧气反应,
表面生成一层致密的氧化铝薄膜。
铝
铝
实验 操作
实验 现象 铝片_________,一段时间后有无色气泡冒出,将点燃的木条放在试管口有_______
逐渐溶解
爆鸣声
Al2O3+6HCl=2AlCl3+3H2O
2Al+6HCl=2AlCl3+3H2 ↑
铝
实验1:将未打磨的铝片放入盐酸中,
一段时间后将点燃的木条放在试管口
实验2:向两支装有NaOH的试管中,分别放入未打磨的铝片、打磨后的铝片;一段时间后将点燃的木条放在试管口
铝
实验操作
实验现象 试管①中一开始无气泡产生,一段时间后,铝片_____,有无色气泡冒出,
试管②中铝片溶解,立即产生无色气泡,将点燃的木条放在试管口,都有_______
化学方程式
溶解
爆鸣声
Al2O3+2NaOH +3H2O= 2Na[Al(OH)4]
2Al+2NaOH+6H2O = 2Na[Al(OH)4] +3H2↑
实验2:向两支装有NaOH的试管中,分别放入未打磨的铝片、打磨后的铝片;一段时间后将点燃的木条放在试管口
铝
【实验结论】
(1)Al 既能与稀HCl反应又能与NaOH溶液反应,都生成盐和氢气。
(2)Al2O3既能与稀HCl反应又能与NaOH溶液反应,都生成盐和水。
【两性氧化物、两性氢氧化物】
(1)两性氧化物:既能与酸反应生成盐和水,又能与碱反应生成盐和水的氧化物,如Al2O3。
(2)两性氢氧化物:既能与酸反应生成盐和水,又能与碱反应生成盐和水的氢氧化物,如Al(OH)3。
Al(OH)3溶于盐酸:_____________________________。
Al(OH)3溶于NaOH溶液:________________________________。
Al(OH)3+3HCl=AlCl3+3H2O
Al(OH)3+NaOH=Na[Al(OH)4]
Al
与酸反应
与碱反应
2Al+2NaOH+6H2O= 2Na[Al(OH)4] +3H2↑
2Al+6HCl=2AlCl3+3H2 ↑
Al2O3
与酸反应
与碱反应
Al2O3+2NaOH+3H2O= 2Na[Al(OH)4]
Al2O3+6HCl=2AlCl3+3H2 O
Al(OH)3
与酸反应
与碱反应
Al(OH)3+3HCl=AlCl3+3H2O
Al(OH)3+NaOH= Na[Al(OH)4]
两性氧化物
两性氢氧化物
铝
铝合金是目前用途广泛的合金之一,硬铝是在铝中添加了一定比例的Cu、Mg、Mn、Si,密度小,强度高,具有较强抗腐蚀能力,是制造飞机和宇宙飞船的理想材料。
铝合金
1.储氢合金:一类能够大量吸收H2,并与H2结合成金属氢化物的材料。如Ti-Fe合金、La-Ni合金,为氢气作为能源的实际应用起到重要的推动作用。
2.其他新型合金:钛合金、耐热合金和形状记忆合金等新型合金广泛应用于航空航天、生物工程和电子工业等领域。
新型合金
(1)镧系元素(57~71号元素)及钇和钪,共17种元素为稀土元素。
我国拥有丰富的稀土资源,现已查明的世界稀土资源中,80%分布在我国,并且品种齐全。
(2)稀土金属有着广泛的用途,它既可以单独使用,也可用于生产合金。在合金中加入适量稀土金属,能大大改善合金的性能。因而,稀土元素又被称为“冶金工业的维生素”。
稀土
1、我国“蛟龙”号载人潜水器已成功下潜至海中7 062.68米处。“蛟龙”号载人潜水器的外壳是耐超高压的钛合金,下面有关合金的说法正确的是( )
A.钛合金是一种新型金属单质 B.钛合金熔点比钛金属高
C.钛合金的硬度与钛单质相同 D.青铜、合金钢和硬铝都是合金
D
2、下列关于新型合金材料说法不正确的是( )
A.镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料
B.钛合金生物相容性好,强度大,可作人造骨骼
C.形状记忆合金可在使合金发生形变的作用力消失后恢复原状
D.利用合金的熔点低于成分金属这一特点可制得耐热合金
D
练习
3、镁铝合金质优体轻,又不易锈蚀,大量用于航空工业、造船工业、日用化工等领域。下列关于镁铝合金性质的叙述中,不正确的是( )
A.此合金的熔点比镁和铝的熔点都低
B.此合金能全部溶解于足量稀盐酸中
C.此合金能全部溶解于足量氢氧化钠溶液中
D.此合金的硬度比镁和铝的硬度都大
C
练习
4、某学习小组用如图所示装置测定铝镁合金中铝的质量分数
(1)A中试剂为 。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,
其目的是 。
(3)B中发生反应的化学方程式为___________
_____________________________________。
氢氧化钠溶液
除去铝镁合金表面的氧化膜
2Al+2NaOH+6H2O= 2Na[Al(OH)4] +3H2↑
练习
