第二章 物质的量 第二节 物质的量浓度 2025年高考化学基础专项复习(共38张PPT)
文档属性
| 名称 | 第二章 物质的量 第二节 物质的量浓度 2025年高考化学基础专项复习(共38张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-11-06 18:38:51 | ||
图片预览











文档简介
(共38张PPT)
第二章 物质的量
2025年高考化学专项复习
第二节 物质的量浓度
目录
物质的量浓度的相关计算
一定物质的量浓度溶液的配制及误差分析
必做实验:配制一定物质的量浓度的溶液
壹
贰
叁
物质的量浓度的相关计算
第一章
教材知识萃取
教材素材变式
1.[人教版必修第一册P61第9题变式]有硫酸镁溶液,它的密度是,其中 的质量分数是
(不考虑 的水解)。下列有关该溶液的说法错误的是( )
D
A.溶质的质量分数是
B.溶液的物质的量浓度是
C.溶质和溶剂的物质的量之比约为
D.配制此溶液时,需用托盘天平称量 固体
【解析】由的质量分数可知的质量分数为 ,A项正确;溶液的物质的量浓度
,B项正确;溶质与溶剂的物质的量之比为 ,
C项正确;需要称量的质量 ,
计算固体质量时应把结晶水计算在内,托盘天平称量的质量应保留小数点后一位,D项错误。
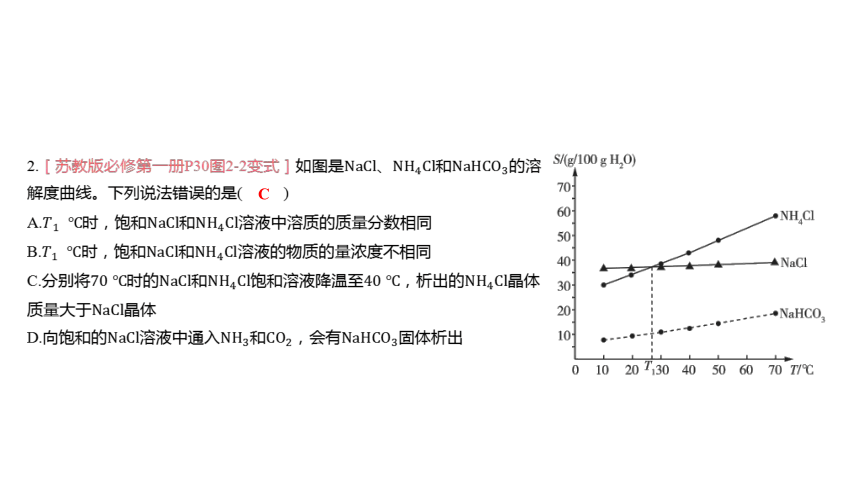
2.[苏教版必修第一册P30图2-2变式]如图是、和 的溶
解度曲线。下列说法错误的是( )
C
A.时,饱和和 溶液中溶质的质量分数相同
B.时,饱和和 溶液的物质的量浓度不相同
C.分别将时的和饱和溶液降温至,析出的 晶体
质量大于 晶体
D.向饱和的溶液中通入和,会有 固体析出
【解析】时,和的溶解度相同,饱和溶液中溶质的质量分数溶解度/(溶解度) ,
则饱和和溶液中溶质的质量分数相同,A项正确; 时,和的溶解度相同,则饱和 和
溶液中溶质的质量分数相同,但溶液的密度不同,溶液的体积不同,溶质的摩尔质量不同,故饱和 和
溶液的物质的量浓度不同,B项正确;两饱和溶液的质量不确定,无法确定析出晶体质量的大小关系,C项
错误;结合题图的溶解度曲线可知,在水中的溶解度不大,且溶解度比和 的溶解度小很
多,向饱和的溶液中通入和,会有 固体析出,D项正确。
3.[链接人教版必修第一册P57~58]在标准状况下,将气体溶于 水中,所得盐酸的密度为
,试计算:
(1)所得盐酸的质量分数和物质的量浓度分别是_______、_____________。
【解题思路】标准状况下,氯化氢气体的物质的量为 ,质量为
,溶于水中所得溶液的质量为 ,溶液的体积为
,则所得盐酸的质量分数为 ,物质的量浓度为
。
(2)取这种盐酸,稀释至 ,所得稀盐酸的物质的量浓度是___________。
【解题思路】设稀释后稀盐酸的物质的量浓度为 ,根据稀释前后溶质的物质的量不变可得:
,解得 。
(3)在溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生
气体,加入稀盐酸的体积最多不超过____ 。
2.6
【解题思路】稀盐酸逐滴加入碳酸钠溶液中,反应的化学方程式为 ,
,若使反应不产生 气体,则只发生反应①,碳酸钠的物质的量为
,加入稀盐酸的体积最多不超过 。
(4)将不纯的样品(样品含少量和水),放入 的盐酸中,充分反应后,溶液呈
酸性,中和多余的酸又用去的溶液。蒸发中和后的溶液,最终得到_____ 固体。
5.85
【解题思路】由题意可知,中和后的溶液为氯化钠溶液,由氯原子个数守恒可知,氯化钠的物质的量与盐酸中氯
化氢的物质的量相等,则最终得到氯化钠的质量为 。
一定物质的量浓度溶液的配制及误差分析
第二章
教材知识萃取
1.一定物质的量浓度溶液的配制
2.误差分析
1.实验步骤
①计算 根据
②称量或量取 用分析天平称量固体时,可精确到
时,可精确到
浓溶液的体积
③溶解 把称量好的
棒充分搅拌,冷却(恢复)至室温
④转移 将玻璃棒下端靠在容量瓶刻度线以下的内壁上,上端不与容量瓶瓶
口接触,将烧杯中的溶液沿
⑤洗涤 用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,每次的洗涤液都要注
入容量瓶内。轻轻摇动容量瓶,使溶液混合均匀
烧杯
玻璃棒
⑥定容 将蒸馏水注入容量瓶,当液面在容量瓶颈部的刻度线以下
___时,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切
⑦摇匀 盖好瓶塞,反复上下颠倒,摇匀
⑧装瓶 将配制好的溶液倒入试剂瓶中,并贴好标签
续表
1 2
cm
第一章
2.误差分析
步骤 误差分析依据:
称量固体 或量取浓 溶液 药品和砝码位置颠倒(使用了游 码) 偏小 不变 偏小
砝码生锈或沾有其他物质 偏大 不变 偏大
溶质已潮解或含有其他杂质 偏小 不变 偏小
称量带结晶水的固体时,部分失去 结晶水 偏大 不变 偏大
用量筒量取浓溶液时仰视读数 偏大 不变 偏大
步骤 误差分析依据:
溶解 有少量溶液溅出 偏小 不变 偏小
用蒸馏水洗涤量筒中残留的浓溶 液,将洗涤液也倒进烧杯里 偏大 不变 偏大
转移溶液 容量瓶中有少量水 不变 不变 不变
溶液未冷却就转入容量瓶进行定容 不变 偏小 偏大
转移时有少量液体洒在容量瓶外 偏小 不变 偏小
未洗涤烧杯和玻璃棒 偏小 不变 偏小
续表
步骤 误差分析依据:
定容 仰视容量瓶刻度线 不变 偏大 偏小
液面超过刻度线,用胶头滴管吸出 偏小 不变 偏小
摇匀后液面下降,又加入蒸馏水 不变 偏大 偏小
续表
教材素材变式
1.[链接人教版必修第一册P59【实验2-10】]配制
的 溶液,部分实验操作
示意图如下:
下列说法正确的是( )
B
A.需称量 固体
B.上述实验操作步骤的正确顺序为③①②④
C.将容量瓶洗涤干净,需干燥后才可使用
D.定容时仰视刻度线,使溶液浓度偏高
【解析】配制的溶液用容量瓶,需称量 固体,A错误;实验操作
步骤的正确顺序为③①②④,B正确;容量瓶洗涤干净,不用干燥,只要定容准确即可,C错误;定容时仰视刻度
线,会使溶液体积偏大,导致浓度偏低,D错误。
方法总结
定容时视线引起误差的分析方法
图1使所配溶液体积偏大,浓度偏低;图2使所配溶液体积偏小,浓度偏高。
2.[链接人教版必修第一册P65实验活动1]用质量分数为的浓硫酸 配制
稀硫酸。下列说法正确的是( )
C
A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B.需要的定量仪器有量筒、 容量瓶和托盘天平
C.量取浓硫酸的体积为
D.先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
【解析】稀释浓硫酸时,应将浓硫酸缓慢注入水中并不断搅拌,A项错误;没有固体需要称量,该实验不需要托盘
天平,B项错误;浓硫酸的物质的量浓度为 ,根据稀释前后溶质质量不变
可知,配制该稀硫酸需要浓硫酸的体积为 ,C项正确;不能在容量瓶中稀释浓硫酸,
应在烧杯中稀释并冷却后,再转移到容量瓶中,最后加水定容,D项错误。
3.[苏教版必修第一册P43第6题变式]用重铬酸钾法(一种氧化还原滴定法)可测定 中的二价铁含量。若需
配制浓度为的 标准溶液,回答下列问题。
(1)配制溶液时需要准确称量的质量是_______ [保留四位有效数字,
已知 。
0.7350
【解题思路】 ,
。
(2)配制该标准溶液时,下列仪器中不会用到的有______(填序号)。
①电子天平 托盘天平
③玻璃棒 量筒
容量瓶 胶头滴管
⑦滴定管 烧杯
②⑦
【解题思路】由于称量的 的质量要求保留四位有效数字,配制该标准溶液时,需要使用电子天平准确称量
其质量,用量筒盛装蒸馏水,然后在烧杯中溶解溶质,为加快物质溶解,要使用玻璃棒进行搅拌,待溶液冷却至
室温后通过玻璃棒引流,将溶液转移至容量瓶中,再洗涤烧杯和玻璃棒 次,洗涤液也转移至容量瓶中,
最后定容时要使用胶头滴管滴加蒸馏水至凹液面与刻度线相切,故配制该标准溶液需要使用的仪器是①③④⑤⑥
⑧,不需要使用的仪器是②⑦。
(3)配制溶液的操作步骤:计算 称量 ______ 移液 洗涤 ______ 摇匀等。
溶解
定容
【解题思路】根据(2)分析可知,配制溶液的操作步骤是:计算 称量 溶解 移液
洗涤 定容 摇匀等。
(4)配制 溶液过程中,若未洗涤烧杯和玻璃棒,则所配溶液浓度______(填“偏高”“偏
低”或“无影响”)。
偏低
【解题思路】配制过程中未洗涤烧杯和玻璃棒,导致所配溶液中溶质的物质的量减少,由于溶液的体积不变,则最终会使所配溶液的浓度偏低。
【解析】 知识总结
常见不当操作及造成的误差
引起误差的一些操作(以配制的 溶液为 例) 变量
砝码与药品颠倒(使用游码) 减小 — 偏低
用滤纸称 减小 — 向容量瓶转移溶液时少量溅出 减小 — 未洗涤烧杯和玻璃棒 减小 — 定容时,水加多了用滴管吸出 减小 — 定容摇匀后液面下降再加水 — 增大 砝码上有其他物质或砝码已生锈 增大 — 偏高
未冷却至室温就注入容量瓶定容 — 减小 容量瓶洗涤后未干燥 — — 不变
定容后经振荡、摇匀、静置,液面下降 — — 拓展必做实验:配制一定物质的量浓度的溶液
第三章
教材实验要点
溶液配制过程中的四个重要数据
数据 要求或解释
药品的质量 实验室中一般用托盘天平称量药品,而托盘天平只能精确到 ,所以记录数据时只能
保留小数点后一位数字
容量瓶的规格 ①选择容量瓶的规格时应该与所配溶液体积相等或稍大。如需要 某溶液,则应该
选择 容量瓶。
#b#
②回答补充仪器的问题时应该注明容量瓶的规格
洗涤烧杯 次 洗涤烧杯 次是为了确保溶质全部转移到容量瓶中,否则会导致溶液浓度偏低
液面离容量瓶颈刻度 线下 定容时,当液面离容量瓶颈刻度线下 时,应该改用胶头滴管滴加,否则容易使液
体体积超过刻度线,导致溶液浓度偏低
必做实验拓展
1.[链接人教版必修第一册P65实验活动1,2022广东卷节选]食醋是烹饪美食的调味品,有效成分主要为醋酸(用
表示)。
(1)配制的溶液,需溶液的体积为____ 。
5.0
【解题思路】根据配制前后溶质的物质的量不变,列式:, ,
得 。
(2)下列关于 容量瓶的操作,正确的是___。
C
A.&1& B.&2& C.&3& D.&4&
【解题思路】振荡时应用瓶塞塞住容量瓶口,不可用手指压住容量瓶口,A项错误;定容时眼睛应该平视刻度线且胶头滴管的尖嘴不能插入容量瓶内,B项错误;转移溶液时用玻璃棒引流,且玻璃棒下端紧靠在容量瓶刻度线以下的内壁上,C项正确;缺少另一只手托住瓶底,D项错误。
【解析】 知识总结
容量瓶使用中的“四个不能”
①固体或浓溶液不能直接在容量瓶中溶解或稀释;②不能作为反应容器或长期贮存溶液;③容量瓶的容积是在瓶身所标温度下确定的,因而不能将过冷或过热的溶液转移到容量瓶中;④只能配制容量瓶上规定容积的溶液,不能配制任意体积的溶液。
2.[人教版必修第一册P64第12题变式]草酸、 均是重要的化学分析试剂,某实验小组需用到
的草酸溶液,试回答下列问题。
(1)实验中需要称取_____草酸晶体 。称量后________(填“需要”或“不需要”)加热除去晶体中
的结晶水。配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及____________________。
12.6
不需要
容量瓶、烧杯
【解题思路】因没有的容量瓶,故实际配制的是 溶液,因此所需要溶质的质量为
。结晶水不需要加热除去,因为溶解后结晶水会转化为溶剂。配
制溶液时还需要使用的玻璃仪器有 容量瓶、烧杯。
(2)假设称取草酸时使用的是托盘天平,称量中试剂与砝码的位置放颠倒了,则所配溶液中 ___(填“
”“”或“ ”,下同)。若定容时俯视刻度线,则所配溶液中___ 。
【解题思路】试剂与砝码位置放颠倒时,称量的试剂的质量小于 ,故最后所配溶液浓度小于
。若定容时俯视刻度线,则实际液面在刻度线以下,故所配溶液浓度大于 。
(3)若配制溶液时所用草酸晶体不纯(杂质无还原性),为测定草酸晶体的纯度,某同学量取 上述所配
溶液放入锥形瓶中,然后用的酸性标准溶液进行滴定(氧化产物是 ),达到滴定终点
时消耗 标准溶液。
①标准溶液应使用____(填“酸”或“碱”)式滴定管量取, 值可能为___(填序号)。
A.15.8 B.16.20
C.15.82 D.16.18
酸
C
【解题思路】酸性高锰酸钾溶液具有强氧化性,会腐蚀碱式滴定管的橡胶管,故应使用酸式滴定管量取酸性
溶液。当样品为纯净物时,由关系式 可得,
, ,由于草酸晶体不纯(杂质无还原
性),故实际消耗酸性溶液的体积不可能大于 ,B、D项错误,用滴定管量取标准溶液,所得体积
以“ ”为单位时应保留两位小数,C项正确。
②达到滴定终点时溶液颜色的变化为_____________________________________,样品中草酸晶体的纯度为
________(用含 的式子表示)。
溶液由无色变为浅红色且在内不褪色
【解题思路】设所配溶液中 ,则有
, ,故样品中草酸晶体的纯度为
。
谢谢
第二章 物质的量
2025年高考化学专项复习
第二节 物质的量浓度
目录
物质的量浓度的相关计算
一定物质的量浓度溶液的配制及误差分析
必做实验:配制一定物质的量浓度的溶液
壹
贰
叁
物质的量浓度的相关计算
第一章
教材知识萃取
教材素材变式
1.[人教版必修第一册P61第9题变式]有硫酸镁溶液,它的密度是,其中 的质量分数是
(不考虑 的水解)。下列有关该溶液的说法错误的是( )
D
A.溶质的质量分数是
B.溶液的物质的量浓度是
C.溶质和溶剂的物质的量之比约为
D.配制此溶液时,需用托盘天平称量 固体
【解析】由的质量分数可知的质量分数为 ,A项正确;溶液的物质的量浓度
,B项正确;溶质与溶剂的物质的量之比为 ,
C项正确;需要称量的质量 ,
计算固体质量时应把结晶水计算在内,托盘天平称量的质量应保留小数点后一位,D项错误。
2.[苏教版必修第一册P30图2-2变式]如图是、和 的溶
解度曲线。下列说法错误的是( )
C
A.时,饱和和 溶液中溶质的质量分数相同
B.时,饱和和 溶液的物质的量浓度不相同
C.分别将时的和饱和溶液降温至,析出的 晶体
质量大于 晶体
D.向饱和的溶液中通入和,会有 固体析出
【解析】时,和的溶解度相同,饱和溶液中溶质的质量分数溶解度/(溶解度) ,
则饱和和溶液中溶质的质量分数相同,A项正确; 时,和的溶解度相同,则饱和 和
溶液中溶质的质量分数相同,但溶液的密度不同,溶液的体积不同,溶质的摩尔质量不同,故饱和 和
溶液的物质的量浓度不同,B项正确;两饱和溶液的质量不确定,无法确定析出晶体质量的大小关系,C项
错误;结合题图的溶解度曲线可知,在水中的溶解度不大,且溶解度比和 的溶解度小很
多,向饱和的溶液中通入和,会有 固体析出,D项正确。
3.[链接人教版必修第一册P57~58]在标准状况下,将气体溶于 水中,所得盐酸的密度为
,试计算:
(1)所得盐酸的质量分数和物质的量浓度分别是_______、_____________。
【解题思路】标准状况下,氯化氢气体的物质的量为 ,质量为
,溶于水中所得溶液的质量为 ,溶液的体积为
,则所得盐酸的质量分数为 ,物质的量浓度为
。
(2)取这种盐酸,稀释至 ,所得稀盐酸的物质的量浓度是___________。
【解题思路】设稀释后稀盐酸的物质的量浓度为 ,根据稀释前后溶质的物质的量不变可得:
,解得 。
(3)在溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生
气体,加入稀盐酸的体积最多不超过____ 。
2.6
【解题思路】稀盐酸逐滴加入碳酸钠溶液中,反应的化学方程式为 ,
,若使反应不产生 气体,则只发生反应①,碳酸钠的物质的量为
,加入稀盐酸的体积最多不超过 。
(4)将不纯的样品(样品含少量和水),放入 的盐酸中,充分反应后,溶液呈
酸性,中和多余的酸又用去的溶液。蒸发中和后的溶液,最终得到_____ 固体。
5.85
【解题思路】由题意可知,中和后的溶液为氯化钠溶液,由氯原子个数守恒可知,氯化钠的物质的量与盐酸中氯
化氢的物质的量相等,则最终得到氯化钠的质量为 。
一定物质的量浓度溶液的配制及误差分析
第二章
教材知识萃取
1.一定物质的量浓度溶液的配制
2.误差分析
1.实验步骤
①计算 根据
②称量或量取 用分析天平称量固体时,可精确到
时,可精确到
浓溶液的体积
③溶解 把称量好的
棒充分搅拌,冷却(恢复)至室温
④转移 将玻璃棒下端靠在容量瓶刻度线以下的内壁上,上端不与容量瓶瓶
口接触,将烧杯中的溶液沿
⑤洗涤 用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,每次的洗涤液都要注
入容量瓶内。轻轻摇动容量瓶,使溶液混合均匀
烧杯
玻璃棒
⑥定容 将蒸馏水注入容量瓶,当液面在容量瓶颈部的刻度线以下
___时,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切
⑦摇匀 盖好瓶塞,反复上下颠倒,摇匀
⑧装瓶 将配制好的溶液倒入试剂瓶中,并贴好标签
续表
cm
第一章
2.误差分析
步骤 误差分析依据:
称量固体 或量取浓 溶液 药品和砝码位置颠倒(使用了游 码) 偏小 不变 偏小
砝码生锈或沾有其他物质 偏大 不变 偏大
溶质已潮解或含有其他杂质 偏小 不变 偏小
称量带结晶水的固体时,部分失去 结晶水 偏大 不变 偏大
用量筒量取浓溶液时仰视读数 偏大 不变 偏大
步骤 误差分析依据:
溶解 有少量溶液溅出 偏小 不变 偏小
用蒸馏水洗涤量筒中残留的浓溶 液,将洗涤液也倒进烧杯里 偏大 不变 偏大
转移溶液 容量瓶中有少量水 不变 不变 不变
溶液未冷却就转入容量瓶进行定容 不变 偏小 偏大
转移时有少量液体洒在容量瓶外 偏小 不变 偏小
未洗涤烧杯和玻璃棒 偏小 不变 偏小
续表
步骤 误差分析依据:
定容 仰视容量瓶刻度线 不变 偏大 偏小
液面超过刻度线,用胶头滴管吸出 偏小 不变 偏小
摇匀后液面下降,又加入蒸馏水 不变 偏大 偏小
续表
教材素材变式
1.[链接人教版必修第一册P59【实验2-10】]配制
的 溶液,部分实验操作
示意图如下:
下列说法正确的是( )
B
A.需称量 固体
B.上述实验操作步骤的正确顺序为③①②④
C.将容量瓶洗涤干净,需干燥后才可使用
D.定容时仰视刻度线,使溶液浓度偏高
【解析】配制的溶液用容量瓶,需称量 固体,A错误;实验操作
步骤的正确顺序为③①②④,B正确;容量瓶洗涤干净,不用干燥,只要定容准确即可,C错误;定容时仰视刻度
线,会使溶液体积偏大,导致浓度偏低,D错误。
方法总结
定容时视线引起误差的分析方法
图1使所配溶液体积偏大,浓度偏低;图2使所配溶液体积偏小,浓度偏高。
2.[链接人教版必修第一册P65实验活动1]用质量分数为的浓硫酸 配制
稀硫酸。下列说法正确的是( )
C
A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B.需要的定量仪器有量筒、 容量瓶和托盘天平
C.量取浓硫酸的体积为
D.先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
【解析】稀释浓硫酸时,应将浓硫酸缓慢注入水中并不断搅拌,A项错误;没有固体需要称量,该实验不需要托盘
天平,B项错误;浓硫酸的物质的量浓度为 ,根据稀释前后溶质质量不变
可知,配制该稀硫酸需要浓硫酸的体积为 ,C项正确;不能在容量瓶中稀释浓硫酸,
应在烧杯中稀释并冷却后,再转移到容量瓶中,最后加水定容,D项错误。
3.[苏教版必修第一册P43第6题变式]用重铬酸钾法(一种氧化还原滴定法)可测定 中的二价铁含量。若需
配制浓度为的 标准溶液,回答下列问题。
(1)配制溶液时需要准确称量的质量是_______ [保留四位有效数字,
已知 。
0.7350
【解题思路】 ,
。
(2)配制该标准溶液时,下列仪器中不会用到的有______(填序号)。
①电子天平 托盘天平
③玻璃棒 量筒
容量瓶 胶头滴管
⑦滴定管 烧杯
②⑦
【解题思路】由于称量的 的质量要求保留四位有效数字,配制该标准溶液时,需要使用电子天平准确称量
其质量,用量筒盛装蒸馏水,然后在烧杯中溶解溶质,为加快物质溶解,要使用玻璃棒进行搅拌,待溶液冷却至
室温后通过玻璃棒引流,将溶液转移至容量瓶中,再洗涤烧杯和玻璃棒 次,洗涤液也转移至容量瓶中,
最后定容时要使用胶头滴管滴加蒸馏水至凹液面与刻度线相切,故配制该标准溶液需要使用的仪器是①③④⑤⑥
⑧,不需要使用的仪器是②⑦。
(3)配制溶液的操作步骤:计算 称量 ______ 移液 洗涤 ______ 摇匀等。
溶解
定容
【解题思路】根据(2)分析可知,配制溶液的操作步骤是:计算 称量 溶解 移液
洗涤 定容 摇匀等。
(4)配制 溶液过程中,若未洗涤烧杯和玻璃棒,则所配溶液浓度______(填“偏高”“偏
低”或“无影响”)。
偏低
【解题思路】配制过程中未洗涤烧杯和玻璃棒,导致所配溶液中溶质的物质的量减少,由于溶液的体积不变,则最终会使所配溶液的浓度偏低。
【解析】 知识总结
常见不当操作及造成的误差
引起误差的一些操作(以配制的 溶液为 例) 变量
砝码与药品颠倒(使用游码) 减小 — 偏低
用滤纸称 减小 — 向容量瓶转移溶液时少量溅出 减小 — 未洗涤烧杯和玻璃棒 减小 — 定容时,水加多了用滴管吸出 减小 — 定容摇匀后液面下降再加水 — 增大 砝码上有其他物质或砝码已生锈 增大 — 偏高
未冷却至室温就注入容量瓶定容 — 减小 容量瓶洗涤后未干燥 — — 不变
定容后经振荡、摇匀、静置,液面下降 — — 拓展必做实验:配制一定物质的量浓度的溶液
第三章
教材实验要点
溶液配制过程中的四个重要数据
数据 要求或解释
药品的质量 实验室中一般用托盘天平称量药品,而托盘天平只能精确到 ,所以记录数据时只能
保留小数点后一位数字
容量瓶的规格 ①选择容量瓶的规格时应该与所配溶液体积相等或稍大。如需要 某溶液,则应该
选择 容量瓶。
#b#
②回答补充仪器的问题时应该注明容量瓶的规格
洗涤烧杯 次 洗涤烧杯 次是为了确保溶质全部转移到容量瓶中,否则会导致溶液浓度偏低
液面离容量瓶颈刻度 线下 定容时,当液面离容量瓶颈刻度线下 时,应该改用胶头滴管滴加,否则容易使液
体体积超过刻度线,导致溶液浓度偏低
必做实验拓展
1.[链接人教版必修第一册P65实验活动1,2022广东卷节选]食醋是烹饪美食的调味品,有效成分主要为醋酸(用
表示)。
(1)配制的溶液,需溶液的体积为____ 。
5.0
【解题思路】根据配制前后溶质的物质的量不变,列式:, ,
得 。
(2)下列关于 容量瓶的操作,正确的是___。
C
A.&1& B.&2& C.&3& D.&4&
【解题思路】振荡时应用瓶塞塞住容量瓶口,不可用手指压住容量瓶口,A项错误;定容时眼睛应该平视刻度线且胶头滴管的尖嘴不能插入容量瓶内,B项错误;转移溶液时用玻璃棒引流,且玻璃棒下端紧靠在容量瓶刻度线以下的内壁上,C项正确;缺少另一只手托住瓶底,D项错误。
【解析】 知识总结
容量瓶使用中的“四个不能”
①固体或浓溶液不能直接在容量瓶中溶解或稀释;②不能作为反应容器或长期贮存溶液;③容量瓶的容积是在瓶身所标温度下确定的,因而不能将过冷或过热的溶液转移到容量瓶中;④只能配制容量瓶上规定容积的溶液,不能配制任意体积的溶液。
2.[人教版必修第一册P64第12题变式]草酸、 均是重要的化学分析试剂,某实验小组需用到
的草酸溶液,试回答下列问题。
(1)实验中需要称取_____草酸晶体 。称量后________(填“需要”或“不需要”)加热除去晶体中
的结晶水。配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及____________________。
12.6
不需要
容量瓶、烧杯
【解题思路】因没有的容量瓶,故实际配制的是 溶液,因此所需要溶质的质量为
。结晶水不需要加热除去,因为溶解后结晶水会转化为溶剂。配
制溶液时还需要使用的玻璃仪器有 容量瓶、烧杯。
(2)假设称取草酸时使用的是托盘天平,称量中试剂与砝码的位置放颠倒了,则所配溶液中 ___(填“
”“”或“ ”,下同)。若定容时俯视刻度线,则所配溶液中___ 。
【解题思路】试剂与砝码位置放颠倒时,称量的试剂的质量小于 ,故最后所配溶液浓度小于
。若定容时俯视刻度线,则实际液面在刻度线以下,故所配溶液浓度大于 。
(3)若配制溶液时所用草酸晶体不纯(杂质无还原性),为测定草酸晶体的纯度,某同学量取 上述所配
溶液放入锥形瓶中,然后用的酸性标准溶液进行滴定(氧化产物是 ),达到滴定终点
时消耗 标准溶液。
①标准溶液应使用____(填“酸”或“碱”)式滴定管量取, 值可能为___(填序号)。
A.15.8 B.16.20
C.15.82 D.16.18
酸
C
【解题思路】酸性高锰酸钾溶液具有强氧化性,会腐蚀碱式滴定管的橡胶管,故应使用酸式滴定管量取酸性
溶液。当样品为纯净物时,由关系式 可得,
, ,由于草酸晶体不纯(杂质无还原
性),故实际消耗酸性溶液的体积不可能大于 ,B、D项错误,用滴定管量取标准溶液,所得体积
以“ ”为单位时应保留两位小数,C项正确。
②达到滴定终点时溶液颜色的变化为_____________________________________,样品中草酸晶体的纯度为
________(用含 的式子表示)。
溶液由无色变为浅红色且在内不褪色
【解题思路】设所配溶液中 ,则有
, ,故样品中草酸晶体的纯度为
。
谢谢
同课章节目录
