第三章 金属及其化合物 第三节 镁、铝、铜及其化合物 金属矿物的开发利用(共84张PPT)
文档属性
| 名称 | 第三章 金属及其化合物 第三节 镁、铝、铜及其化合物 金属矿物的开发利用(共84张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 6.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-11-06 18:43:36 | ||
图片预览











文档简介
(共84张PPT)
第三章 金属及其化合物
2025年高考化学专项复习
第三节 镁、铝、铜及其化合物 金属矿物的开发利用
目录
镁及其化合物
壹
铝及其化合物
贰
铜及其化合物
叁
金属材料与金属矿物的开发利用
肆
必做实验:铁及其化合物的性质
伍
镁及其化合物
第一章
教材知识萃取
1.镁及其重要化合物的物理性质
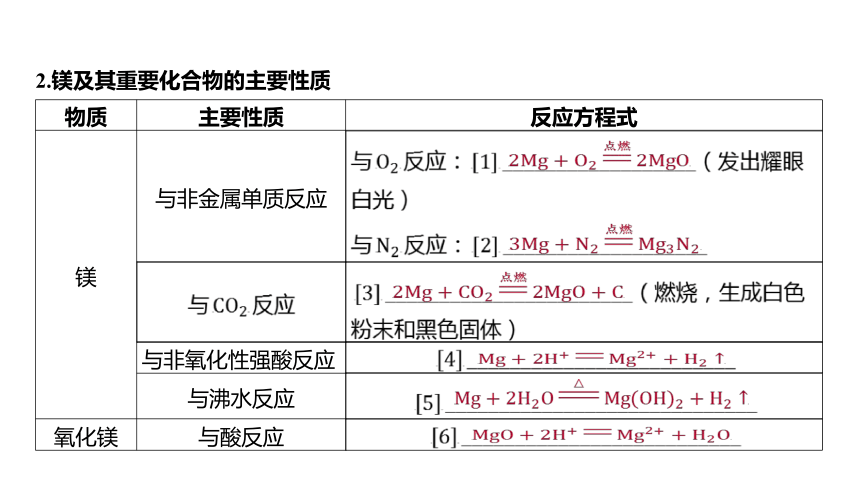
2.镁及其重要化合物的主要性质
物质 主要性质 反应方程式
镁 与非金属单质反应 与
白光)
与
与
粉末和黑色固体)
与非氧化性强酸反应
与沸水反应
氧化镁 与酸反应
物质 主要性质 反应方程式
氢氧化镁 与酸反应
热分解
氮化镁 发生水解反应
加热,
续表
物质 主要性质 反应方程式
电解制镁
&1& 氢氧化镁的溶解度小于碳酸镁,能发生反应
续表
3.从海水中提取镁的工艺流程
(1)流程
(2)主要化学反应
①制石灰乳:
②沉淀
③制备
④电解
教材素材变式
类型1 镁及其化合物的性质
1.[链接苏教版必修第一册P80~81]镁及其化合物在生产、生活中有广泛应用。下列物质的性质与用途不具有对应
关系的是( )
B
A. 具有碱性,可用于制胃酸中和剂
B. 具有很高的熔点,可制作焰火
C. 分解吸热且生成高熔点固体,可用作阻燃剂
D.镁合金的硬度和强度都较大,因此被大量用于制造火箭和飞机的部件
【解析】具有弱碱性,能与反应生成和,且无毒,可用于制胃酸中和剂,A项正确; 具有
很高的熔点,可作为耐高温材料,但不能制作焰火,B项错误;分解为吸热反应,且生成高熔点的 ,可
用作阻燃剂(【提示】和受热分解均会产生耐高温的 ,因此二者均能用作阻燃剂。),C项正
确;制作火箭和飞机的部件材料要求具有耐高温、耐腐蚀、密度低、硬度大等特性,镁合金具有这些特性,D项正
确。
2.[链接苏教版必修第一册P81等,2022上海卷]将加入稀 溶液中,发生反应
,下列说法正确的是( )
B
A.用湿润的蓝色石蕊试纸检验 B.经过一段时间之后可能生成 沉淀
C.和均为还原产物 D.充分反应生成 气体(标准状况下)
【解析】氨气可使湿润的红色石蕊试纸变蓝,因此检验氨气需用湿润的红色石蕊试纸,A错误;该反应经过一段时
间之后,溶液中有和生成,和可以发生反应生成,B正确;该反应中
中的部分氢元素由价变为0价,化合价降低,被还原,是还原产物,而生成的过程中 元素的化合
价没有变化,不是还原产物,C错误;由该反应的化学方程式可知,充分反应生成氨气和
氢气,其在标准状况下的体积为 ,D错误。
类型2 镁及其化合物的转化
3.[人教版必修第二册P106第6题变式,2021湖南卷]一种工业制备无水氯化镁的工艺流程如下:
下列说法错误的是( )
D
A.物质 常选用生石灰
B.工业上常用电解熔融 制备金属镁
C.“氯化”过程中发生的反应为
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水
【解析】
D项,,加热溶液会促进水解生成,且 逸出,最终得不到
无水 ,错误。
4.[链接苏教版必修第一册P80~81]以菱镁矿(主要成分为 ,含少量
、和 )为原料制备高纯镁砂的工艺流程如下:
已知浸出时产生的废渣中有、和 。下列说法错误的是
( )
B
A.浸出镁的反应为
B.浸出和沉镁的操作均应在较高温度下进行
C.流程中可循环使用的物质有、
D.分离与、是利用了它们氢氧化物 的不同
【解析】信息转换
结合工艺流程可知煅烧后得到的轻烧粉的成分为和少量、、, 溶液呈酸性,浸出时使
及、溶解,浸出后得到的废渣中含有、和,所得浸出液中含有 及过量的
,加入氨水时转化为,经煅烧得到高纯镁砂 。
结合流程图和上述分析可知浸出镁的反应为 ,A项正确;浸出可以在较高
温度下进行,促进水解和 的逸出,但沉镁时应在低温下进行,以减弱氨水分解,B项错误;结合流程图
可知浸出得到的可转化为氨水,用于沉镁,滤液中含有过量的 ,可用于浸出时的反应液,故该流程中
和可循环使用,C项正确;本流程中分离时,、 转化为沉淀,是利用了它们氢氧化物的
不同,D项正确。
铝及其化合物
第二章
教材知识萃取
1.铝的性质及用途
(1)铝的物理性质及用途
银白色固体,具有良好的导热性、导电性和延展性,熔点为
铝合金用于制造汽车、飞机、生活用品等。
(2)从原子结构角度认识铝的化学性质
铝在元素周期表中处于第
层有3个电子,在反应中易失去电子,表现出还原性。
三
与非金属单 质反应
与酸反应 遇冷的浓硫酸或浓硝酸
与非氧化性强酸(如稀盐酸、稀硫酸)反应:
__________(填离子方程式)
与强碱溶液 反应
铝热反应
钝化
2.
(1)
类别 两性氧化物 两性氢氧化物
物理 性质 高熔点,高沸点,高硬度,不溶 于水的白色固体 不溶于水的白色胶状固体,具有吸附性
化学 性质 ①与强酸反应:
(填离子方程式)
化学 性质 ②与强碱反应:
(填离子方程式)
③灼烧:
子方程式)
用途 作耐火材料;炼铝原料 可用作吸附剂、媒染剂和净水剂;治疗
胃酸过多;可作制造瓷釉、耐火材料、
防水织物的原料
续表
&4& 铝是活泼金属,但抗腐蚀性能强,原因是常温下
氧化物薄膜而防止内部金属进一步被氧化。
(2)
①向可溶性铝盐中加入足量氨水:
(填离子方程式)。
②向
(填离子方程式)。
3.
4.从铝土矿中提取
从铝土矿(主要成分是
大工艺流程:
教材素材变式
类型1 铝及其化合物的性质
1.[链接人教版必修第一册P82]下列物质的性质和用途具有对应关系的是( )
C
A.熔点高,可用于电解制铝 B. 不稳定,可用于治疗胃酸过多
C.明矾水解生成胶体,可用作混凝剂 D.铝具有导热性,可用于制备铝热剂
【解析】A项,(熔融)具有导电性,故可以电解生成(【易错辨析】电解 (熔融)冶炼金属铝,而
不用电解,因为为共价化合物,熔融态不导电。),错误;B项,可以与 反应,且碱性较弱,
可用于治疗胃酸过多,错误;C项,明矾水解生成的 胶体具有净水作用,可用作混凝剂,正确;D项,铝
具有强还原性,可以置换出部分金属氧化物中的金属,可用于制备铝热剂,错误。
拓展设问 判正误:铝的金属活泼性强,可用于制作铝金属制品( )
×
【解析】 铝可用于制作铝金属制品,是因为其表面有一层致密的氧化膜,不易被腐蚀,与活泼性无关。
类型2 铝及其化合物的转化
2.[链接苏教版必修第二册P97~98拓展视野]工业上用铝土矿(主要成分为,含 杂质)为原料冶炼铝
的工艺流程如下,下列叙述错误的是( )
C
A.步骤①中,试剂一般使用的是 溶液
B.步骤②中,主要的离子反应可能是:
C.实验室条件下,步骤③中的加热操作常在蒸发皿中完成
D.步骤④中,在电解装置的阴极得到液态金属铝
【解析】通过步骤①得到沉淀和滤液,根据和的性质差异及后续流程知,A项正确;步骤①中 转
化为,步骤②中转化为,要使完全转化为,可通入过量 ,
B项正确;加热 固体应在坩埚中完成,C项错误;电解熔融态的氧化铝制备铝时,由于氧化铝熔点高于铝,
在电解装置的阴极得到液态金属铝,D项正确。
拓展设问 判正误:步骤①中,主要反应的离子方程式为 ( )
√
【解析】 步骤①中,氧化铝与强碱溶液发生反应生成 ,离子方程式正确。
3.[人教版必修第一册P89第14题变式]某铝热剂由铝粉和铁的某种氧化物组成,二者恰好完全反应生成铁单质和
氧化铝。将该铝热剂分成两等份,同温同压下,一份直接与足量的溶液反应,放出的体积为 ;另一份
在完全发生铝热反应后与足量的盐酸反应,放出的体积为 。下列说法错误的是( )
C
A.两份铝热剂分别生成氢气的质量之比一定为
B.两份铝热剂消耗和的物质的量之比一定为
C.铝热剂中铝元素和铁元素的物质的量之比一定为
D.铝热剂中氧元素和铁元素的物质的量之比一定为
【解析】综合分析
设铁的氧化物为,则铝热反应为,将含和 的铝热剂分
成两等份进行实验,则每份中铝的物质的量为,其中一份铝热剂发生铝热反应生成铁的物质的量为 。
设该条件下气体摩尔体积为,铝与足量氢氧化钠溶液反应的关系式为 ,由生成氢气
的体积可以计算出消耗的物质的量为,由,可以计算出 ;铁与盐酸反应的
关系式为,由生成氢气的体积可以计算出消耗的物质的量为,由 ,可计
算出 。
同温同压下,气体的体积之比等于气体的物质的量之比,对于同一种物质,质量之比等于其物质的量之比,故同
温同压下两份铝热剂分别生成氢气的质量之比一定为,A项正确;也与反应,两份铝热剂消耗
和的物质的量之比为 ,B项正确;铝热剂中铝元素和铁元素的物质的量之比
为,C项错误;铝热剂中氧元素和铁元素的物质的量之比 ,
D项正确。
铜及其化合物
第三章
教材知识萃取
1.铜的性质
2.铜的氧化物和氢氧化物的性质
等具有还原性的物质反应生成
_________________
__________________________
3.铜盐的性质
分解为氧化铜可溶性铜盐能与
铜盐
4.铜的冶炼方法
传统湿法炼铜
用碱式碳酸铜制备 方案一,干法:
,
方案二,湿法:
__________,
高温炼铜 工业上用高温冶炼黄铜矿的方法获得铜(粗铜)。
续表
教材素材变式
类型1 铜及其化合物的性质
1.[链接人教版必修第二册P7资料卡片,2023浙江卷1月]硫酸铜应用广泛,下列说法不正确的是( )
A
A.元素位于周期表 区 B.硫酸铜属于强电解质 C.硫酸铜溶液呈酸性 D.硫酸铜能使蛋白质变性
【解析】的价电子排布式为,位于周期表 区,A项错误;硫酸铜属于盐,溶于水或熔融状态下完全电
离,属于强电解质,B项正确;硫酸铜为强酸弱碱盐,由于 水解溶液呈酸性,C项正确;硫酸铜属于重金属盐,
能使蛋白质变性,D项正确。
2.[链接苏教版必修第二册P111第6题等]中国古代涉及的“铜”文化丰富多彩。下列说法错误的是( )
B
A.“石胆化铁为铜”中涉及金属键的断裂
B.铸造铜钱用的材料黄铜是单质铜
C.诗句“庐山山南刷铜绿”中的“铜绿”借指的是 的颜色
D.“青铜器时期”早于“铁器时期”的原因之一是铜比铁稳定
【解析】该反应为, 中的金属键断裂,A项正确;黄铜是铜锌合金,B项错误;碱式碳酸
铜俗称铜绿,C项正确;铜的性质比铁稳定,较易以单质的形式存在,是青铜器时期早于铁器时期的原因之一,D
项正确。
类型2 铜及其化合物的转化
3.[链接苏教版必修第二册P102实验探究等]部分含铜物质的价类关系
如图所示。下列说法正确的是( )
B
A.能与溶液反应:
B.在酸性环境中可以转化为和
C.经一步反应可转化为
D.若为,则其水溶液中可能大量存在、、
【解析】解题关键
根据图示可知,为,为,为,为,为价铜的盐(如 )。
未配平,正确的反应为。为 ,在酸性溶液中发生歧化反应,即
。为,为,不能直接转化为。若 为
,在酸性条件下具有氧化性, 具有还原性,会发生反应
,所以溶液中不能大量存在、 。
4.[链接人教版必修第二册P6资料卡片] 样
品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如
图所示:
下列判断不正确的是( )
D
A.时固体物质的化学式为
B.胆矾晶体存在的最高温度为
C.实验室灼烧固体所需器材除热源外,还需要坩埚、泥三角、
三脚架、坩埚钳等
D.继续升高温度,当固体残留率(剩余固体质量/原始固体质量)
为 时,所得固体产物为黑色
【解析】初始时,样品的物质的量为 ,样品中
,。 时减少的水
的总质量为,则所得固体中 ,此时固体组
成表示为,A项正确; 时固体质量开始减小,即胆矾晶体开始脱水,说明胆矾晶体存在的最高温
度为 ,B项正确;实验室灼烧固体所需器材除热源外,还需坩埚、泥三角、三脚架、坩埚钳等,C项正确;
固体残留率为时,剩余固体的质量为,说明此时 开始分解,生成
铜的氧化物,铜元素质量不变,则氧元素的质量为 ,其物质的
量为,由此可确定固体的组成为, 是一种砖红色固体,D项错误。
金属材料与金属矿物的开发利用
第四章
教材知识萃取
金属材料 包括金属和合金。合金具有金属特性,熔点低于成分金属、硬度高于成分金属
金属冶炼的方法
1.金属的冶炼
(1)实质:使金属离子得到电子,被还原成金属单质的过程。
(2)金属冶炼的一般步骤
2.常见金属的冶炼方法
3.金属冶炼方法的选择
利用金属活泼性的差异,可以采取不同的冶炼方法冶炼金属,常见金属的冶炼方法如表所示:
金属的活动 性顺序
自然界中存 在形式 化合态(陨铁中有单质铁) 少量游离态,主要 化合态 游离态
冶炼方法 电解法 热还原法 热分解法 富集法
教材素材变式
类型1 金属材料
1.[链接人教版必修第一册P78~80,2021河北卷]“灌钢法”是我国古代劳动人民对钢铁冶炼技术的重大贡献,陶弘景
在其《本草经集注》中提到“钢铁是杂炼生 作刀镰者”。“灌钢法”主要是将生铁和熟铁(含碳量约 )混合加
热,生铁熔化灌入熟铁,再锻打成钢。下列说法错误的是( )
C
A.钢是以铁为主的含碳合金 B.钢的含碳量越高,硬度和脆性越大
C.生铁由于含碳量高,熔点比熟铁高 D.冶炼铁的原料之一赤铁矿的主要成分为
【解析】钢是以铁为主的含碳合金,A项正确;纯铁硬度小,质地较软,随着含碳量的升高,钢的硬度和脆性增大,
B项正确;熟铁含碳量比生铁的含碳量低,结合题目信息“生铁熔化灌入熟铁”可知生铁的熔点比熟铁低,C项错误;
赤铁矿为红色,主要成分是 ,D项正确。
类型2 金属的冶炼
2.[链接人教版必修第二册P106第8题等,2022山东卷]高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿
(含、元素的杂质)为主要原料制备 粉的工艺流程如下,可能用到的数据见下表。
开始沉淀 1.9 4.2 6.2
沉淀完全 3.2 6.7 8.2
下列说法错误的是( )
D
A.固体主要成分是和;金属为
B.浸取时,增大 压强可促进金属离子浸出
C.中和调的范围为
D.还原时,增大溶液酸度有利于 的生成
【解析】流程梳理
由上述分析知,A项正确;浸取时,增大 压强即增大反应物浓度,可加快反应速率,促进金属离子浸出,B项正
确;中和调是为了沉淀而不沉淀、,结合表中数据可知,调的范围为 ,C项正确;还
原时发生反应,故增大溶液酸度不利于 的生成,D项错误。
3.[链接苏教版必修第二册P94~98]金、银是贵金属,废旧中含单质、和。从废旧 中回收
单质、 的方法如图所示。
已知:①浓硝酸不能单独将 溶解;
②王水是浓硝酸与浓盐酸的混合物(体积比 );
。
下列说法错误的是( )
C
A.用浓盐酸与也可能使 溶解
B.试剂 可以是浓氨水
C.王水中浓盐酸的主要作用是增强溶液的酸性
D.恰好被完全还原,可消耗
(仅考虑 的反应)
【解析】从流程中可以看出,在、、同时存在时金可溶解,用浓盐酸和 可能使金溶解。
与过量浓氨水能生成,试剂可以是浓氨水。王水中浓盐酸的主要作用是提供 ,
可以得到溶液。仅考虑的反应,结合已知③可知,粉将还原为和 ,金元
素由价降至0价,氢元素由价降为0价,消耗的物质的量为 。
4.[链接鲁科版必修第一册P69化学与技术,2022湖南卷节选]钛 及其合金是理想的高强度、低密度结构材料。以
钛渣(主要成分为,含少量、和 的氧化物杂质)为原料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗 中含有的几种物质的沸点:
回答下列问题:
(1)与C、在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
①该温度下,与C、 反应的总化学方程式为_________________________________________;
【解题思路】 根据混合气体中、、的分压,可计算出三者的物质的量之比约为 ,结合得
失电子守恒和物料守恒可写出总反应的化学方程式为 。
②随着温度升高,尾气中 的含量升高,原因是_________________________。
温度升高,C主要转化为
(2)“除钒”过程中的化学方程式为____________________________;“除硅、铝”过程中,分离中含、 杂质
的方法是________。
蒸馏法
【解题思路】 结合图示流程可知“除钒”时与发生反应生成和。根据与、 沸点相
差较大,知可对混合物进行加热蒸馏,收集约的蒸馏产物,即可除去含、 杂质。
(3)“除钒”和“除硅、铝”的顺序______(填“能”或“不能”)交换,理由是___________________________________
_________________________________。
(4)下列金属冶炼方法与本工艺流程中加入冶炼 的方法相似的是_____。
不能
“除钒”后产生的可在“除硅、铝”时除去,若交换顺序,无法除去
AC
A.高炉炼铁 B.电解熔融氯化钠制钠 C.铝热反应制锰 D.氧化汞分解制汞
【解题思路】 该工艺流程中冶炼时发生反应: ,是利用热还原法,与A、C项原理
相同,而B项是电解法,D项是热分解法,均与该原理不相似。
类型3 金属矿物的开发利用
5.[链接苏教版必修第二册P97拓展视野,2023浙江卷6月]某研究小组用铝土矿为原料制备絮凝剂聚合氯化铝
, ,按如下流程开展实验。
已知:主要成分为,含少量和。用溶液溶解铝土矿过程中 转变为难溶性的铝硅酸
盐。
的絮凝效果可用盐基度衡量,盐基度。当盐基度为 时,絮凝效果较好。
请回答:
(1)步骤Ⅰ所得滤液中主要溶质的化学式是____________。
【解题思路】 步骤Ⅰ中主要发生铝土矿中、溶解于 溶液中的反应,结合已知①及各物质性质知,滤
液中的主要溶质为 。
(2)下列说法不正确的是_____。
BC
A.步骤Ⅰ,反应须在密闭耐高压容器中进行,以实现所需反应温度
B.步骤Ⅱ,滤液浓度较大时通入过量有利于减少 沉淀中的杂质
C.步骤Ⅲ,为减少 吸附的杂质,洗涤时需对漏斗中的沉淀充分搅拌
D.步骤Ⅳ,控制和 的投料比可控制产品盐基度
【解题思路】 步骤Ⅰ为铝土矿的高温碱液浸取过程,故反应须在密闭耐高压容器中进行,A项正确;步骤Ⅱ发生反
应:,当滤液中浓度较大时,通入过量,因 溶
解度较小,从而使含较多 杂质,B项错误;过滤时,漏斗中垫有滤纸,若搅拌则可能导致滤纸破损,
从而导致过滤失败,C项错误;由产品聚合氯化铝的化学式及已知②可知,步骤Ⅳ控制和 的投料比可
控制产品的盐基度,D项正确。
(3)步骤Ⅴ采用如图所示的蒸汽浴加热,仪器A的名称是________;步骤Ⅴ不宜用酒精灯直接加热
的原因是____________________________。
蒸发皿
温度升高,聚合氯化铝会分解
【解题思路】 由仪器A的构造可知其名称为蒸发皿。用酒精灯直接加热时,温度较高,聚合氯化铝会分解。
(4)测定产品的盐基度。
的定量测定:称取一定量样品,配成溶液,移取溶液于锥形瓶中,调,滴加指示剂 溶
液。在不断摇动下,用标准溶液滴定至浅红色(有 沉淀),30秒内不褪色。平行测
试3次,平均消耗标准溶液 。
另测得上述样品溶液中 。
①产品的盐基度为____。
0.7
【解题思路】测定过程中发生反应: ,则
, ,由化合物中各元素化合价代数
和为0知聚合氯化铝为,故产品的盐基度为 。
②测定过程中溶液 过低或过高均会影响测定结果,原因是_____________________________________________
_________________________________________________________________________。
过低,转为,浓度降低,不能形成沉淀显色以指示终点;过高,转为(或)沉淀,影响测定
【解题思路】 测定过程中,溶液中存在反应:,溶液 过低,即
浓度过大,平衡正向移动,从而影响的生成;过高,则易形成或 。
必做实验:铁及其化合物的性质
第五章
必做实验拓展
1.[链接人教版必修第一册P90实验活动2,2023浙江卷1月]探究铁及其化合物的性质,下列方案设计、现象和结论都正确的是 ( )
实验 方案 现象 结论
A 往溶液中加入 片 短时间内无明显现象 的氧化能力比 弱
B 往溶液中滴加 溶液,再加入少 量 固体 溶液先变成血红色后 无明显变化 与 的反应不可逆
C 将食品脱氧剂样品中的还原铁粉溶于盐酸, 滴加 溶液 溶液呈浅绿色 食品脱氧剂样品中没有 价铁
D 向沸水中逐滴加滴饱和 溶液,持续 煮沸 溶液先变成红褐色再 析出沉淀 先水解得 再聚集成
沉淀
D
【解析】 往溶液中加入片,发生反应,的氧化能力比 的强,A项错误;
往溶液中滴加溶液,发生反应,溶液变血红色,再加入少量 固体,
对平衡无影响,故不能说明与的反应不可逆,B项错误;若食品脱氧剂样品中有价铁,铁粉与 价铁
发生反应,滴加溶液,溶液呈浅绿色,C项错误;向沸水中逐滴加滴饱和 溶液,
继续煮沸至溶液呈红褐色,得到胶体,持续煮沸, 胶体发生聚沉,析出红褐色沉淀,D项正确。
2.[链接人教版必修第一册P90实验活动2]在工业上用途非常广泛,通过下列实验探究 溶液的性质。
实验1:将浓 溶液滴入沸水中,分散系呈现红褐色;
实验2:在装有少量 溶液的试管中加入铜粉充分振荡,溶液由黄色变成蓝色;
实验3:在装有少量溶液的试管中加入过量溶液,充分振荡后,分成两份:一份加入有机溶剂 ,振荡后
层显紫红色;另一份加入 溶液,溶液显红色;
实验4:在装有少量溶液的试管中加入少量 溶液,充分振荡后产生白色沉淀。下列说法正确的是( )
C
A.实验1中的铁元素形成的粒子大小没有改变
B.实验2中发生反应的离子方程式为
C.实验3中与 发生氧化还原反应,但该反应存在限度
D.实验4静置后溶液中大量存在的离子有、、、
【解析】实验1中得到的红褐色分散系为 胶体,其胶体粒子直径大于溶液中铁元素形成的分子、离子的直
径,A项错误;实验2中发生的反应为,B项错误;实验3中一份振荡后 层呈紫红色,
说明过量溶液和少量溶液发生氧化还原反应生成了,另一份反应液能使 溶液呈红色,说明溶液中仍
含,即和的反应是可逆的,该反应存在限度,C项正确;与反应生成沉淀,即溶液中 、
不能大量存在,D项错误。
3.[链接人教版必修第一册P76研究与实践等,2023海南卷]某小组开展“木耳中铁元素的检测”活动。检测方案的主要步骤有:粉碎、称量、灰化、氧化、稀释、过滤、滴定等。回答问题:
(1)实验方案中出现的图标 和 ,前者提示实验中会用到温度较高的设备,后者要求实验者____________
(填防护措施)。
佩戴护目镜
【解题思路】实验中的&4& 标识要求实验者佩戴护目镜,以保护眼睛。
(2)灰化:干燥样品应装入__中(填标号),置高温炉内,控制炉温 ,在充足空气气氛中燃烧成灰渣。
.不锈钢培养皿 .玻璃烧杯
.石英坩埚
【解题思路】高温灼烧固体物质需在坩埚中进行。
(3)向灰渣中滴加 的硝酸,直至没有气泡产生。灰化容器中出现的红棕色气体主要成分是_____
(填化学式),因而本实验应在实验室的________中进行(填设施名称)。若将漏斗直接置于容量瓶上
过滤收集滤液(如图所示),存在安全风险,原因是______________________。
通风橱
装置重心不稳,易倾倒
【解题思路】向灰渣中滴加的硝酸,灰化容器中出现的红棕色气体主要成分是,由于 有毒,
所以需在通风橱中进行;将漏斗直接置于容量瓶上过滤收集滤液,装置较高,易重心不稳,存在安全风
险。
(4)测定铁含量基本流程:将滤液在容量瓶中定容,移取,驱尽并将全部还原为 。
用微量滴定管盛装 标准溶液进行滴定。
①选用微量滴定管的原因是________________________________。
减小误差,滴定更准确,节约试剂
【解题思路】木耳中铁含量较少,选用微量滴定管可减小实验误差,使滴定更准确,并且节约试剂。
②三次平行测定的数据如下表。针对该滴定数据,应采取的措施是________________。
序号 1 2 3
标准溶液用量/ 2.715 2.905 2.725
舍去第二次数据
【解题思路】三次平行滴定中,第二组数据偏差较大,可能为错误操作得到的数据,应舍去。
③本实验中,使测定结果偏小的是__(填标号)。
.样品未完全干燥
.微量滴定管未用标准溶液润洗
.灰渣中有少量炭黑
【解题思路】铁元素的含量,样品未完全干燥,会造成样品质量偏大,使测定结果偏小,
正确;微量滴定管未用标准溶液润洗,会使标准溶液被稀释,消耗的标准溶液体积偏大,测定结果偏大, 错误;
灰渣中有少量炭黑,对测定结果无影响, 错误。
命题动向
立足教材,强化对教材内容的深度思考,强化教学导向
以实验为基础是化学学科的重要特征之一,化学实验对于全面发展考生的化学学科核心素养有极为关键的作用。选择教材实验作为命题素材,有利于落实基础性的考查,有利于检测各学校贯彻新课程标准关于培养考生实验能力的要求,有利于了解和掌握教师对教科书的使用水平。本题实验源自人教版必修第一册第三章第一节的研究与实践“检验食品中的铁元素”,其中(1)中图标源自人教版必修第一册第一章第一节中的提示栏目。
4.[链接鲁科版必修第一册P88活动·探究]柠檬酸亚铁是一种补血铁制剂,可以用于药物开发及饲料添加剂。以硫酸亚铁和柠檬酸为主要原料的制备程序及有关装置如下:
(1)制备
①该制备实验所用的溶液、 溶液需临时配制,配制这些溶液的蒸馏水必须煮沸冷却,目的是_______
_______________。
除去蒸馏水中溶解的氧
【解题思路】为防止被溶液中溶解的 氧化,配制溶液的蒸馏水必须煮沸冷却。
【解题思路】反应Ⅰ生成和,则操作Ⅰ中将沉淀洗涤后,可以通过检验最后一次洗涤液中是否含有
来检验是否洗涤干净,故所选试剂为 溶液。
②操作Ⅰ中将沉淀洗涤后,检验是否洗涤干净的试剂为______(填化学式)。
(2)制备柠檬酸亚铁
①反应Ⅱ中 与柠檬酸反应制备柠檬酸亚铁时需加入抗氧化剂,该抗氧化剂是___(填标号)。
粉粉 粉
【解题思路】为不引入新的杂质离子,选择的抗氧化剂应为铁粉。
②操作Ⅱ应先加入无水乙醇,再静置、抽滤、洗涤、干燥。加入无水乙醇的目的是________________________。
减小柠檬酸亚铁的溶解度
【解题思路】操作Ⅱ先加入无水乙醇,再静置、抽滤、洗涤、干燥,获得柠檬酸亚铁,则加入无水乙醇可减小柠檬酸亚铁的溶解度。
(3)实验测得产品柠檬酸亚铁的产率和产品中的铁含量随着溶液 、温度的变
化曲线如图所示。则该方法制备柠檬酸亚铁的最佳条件是__________________。
较高时,产品产率降低的原因是_______________________________________
________________________________。
左右,
大于7时,水解程度增大,转化为,导致柠檬酸亚铁的产率降低
【解题思路】根据图示,左右、 时柠檬酸亚铁的产率大、产品中铁
的含量高,为制备柠檬酸亚铁的最佳条件。大于7时, 水解程度增大,转
化为 ,导致柠檬酸亚铁的产率降低。
(4)称取上述方法制备的柠檬酸亚铁样品,配制成一定物质的量浓度的溶液,量取 溶液转
移至锥形瓶中,加酸性溶液,至溶液恰好出现粉红色,且 内不褪色,再向溶液中加入适量还原剂将
完全还原为,加入酸化后,用溶液滴定四次,消耗的 溶液体积如下
表:
测定组次 1 2 3 4
消耗溶液体积/ 17.09 20.3 16.97 16.94
该柠檬酸亚铁样品中铁含量为______%。
19.04
【解题思路】根据得失电子守恒,可得关系式 ,四次实验中第二次实验数据误差较大,舍去,取其
余三次实验的数据平均值,消耗溶液,则 样品中
,该柠檬酸亚铁样品中铁含量为
。
谢谢
第三章 金属及其化合物
2025年高考化学专项复习
第三节 镁、铝、铜及其化合物 金属矿物的开发利用
目录
镁及其化合物
壹
铝及其化合物
贰
铜及其化合物
叁
金属材料与金属矿物的开发利用
肆
必做实验:铁及其化合物的性质
伍
镁及其化合物
第一章
教材知识萃取
1.镁及其重要化合物的物理性质
2.镁及其重要化合物的主要性质
物质 主要性质 反应方程式
镁 与非金属单质反应 与
白光)
与
与
粉末和黑色固体)
与非氧化性强酸反应
与沸水反应
氧化镁 与酸反应
物质 主要性质 反应方程式
氢氧化镁 与酸反应
热分解
氮化镁 发生水解反应
加热,
续表
物质 主要性质 反应方程式
电解制镁
&1& 氢氧化镁的溶解度小于碳酸镁,能发生反应
续表
3.从海水中提取镁的工艺流程
(1)流程
(2)主要化学反应
①制石灰乳:
②沉淀
③制备
④电解
教材素材变式
类型1 镁及其化合物的性质
1.[链接苏教版必修第一册P80~81]镁及其化合物在生产、生活中有广泛应用。下列物质的性质与用途不具有对应
关系的是( )
B
A. 具有碱性,可用于制胃酸中和剂
B. 具有很高的熔点,可制作焰火
C. 分解吸热且生成高熔点固体,可用作阻燃剂
D.镁合金的硬度和强度都较大,因此被大量用于制造火箭和飞机的部件
【解析】具有弱碱性,能与反应生成和,且无毒,可用于制胃酸中和剂,A项正确; 具有
很高的熔点,可作为耐高温材料,但不能制作焰火,B项错误;分解为吸热反应,且生成高熔点的 ,可
用作阻燃剂(【提示】和受热分解均会产生耐高温的 ,因此二者均能用作阻燃剂。),C项正
确;制作火箭和飞机的部件材料要求具有耐高温、耐腐蚀、密度低、硬度大等特性,镁合金具有这些特性,D项正
确。
2.[链接苏教版必修第一册P81等,2022上海卷]将加入稀 溶液中,发生反应
,下列说法正确的是( )
B
A.用湿润的蓝色石蕊试纸检验 B.经过一段时间之后可能生成 沉淀
C.和均为还原产物 D.充分反应生成 气体(标准状况下)
【解析】氨气可使湿润的红色石蕊试纸变蓝,因此检验氨气需用湿润的红色石蕊试纸,A错误;该反应经过一段时
间之后,溶液中有和生成,和可以发生反应生成,B正确;该反应中
中的部分氢元素由价变为0价,化合价降低,被还原,是还原产物,而生成的过程中 元素的化合
价没有变化,不是还原产物,C错误;由该反应的化学方程式可知,充分反应生成氨气和
氢气,其在标准状况下的体积为 ,D错误。
类型2 镁及其化合物的转化
3.[人教版必修第二册P106第6题变式,2021湖南卷]一种工业制备无水氯化镁的工艺流程如下:
下列说法错误的是( )
D
A.物质 常选用生石灰
B.工业上常用电解熔融 制备金属镁
C.“氯化”过程中发生的反应为
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水
【解析】
D项,,加热溶液会促进水解生成,且 逸出,最终得不到
无水 ,错误。
4.[链接苏教版必修第一册P80~81]以菱镁矿(主要成分为 ,含少量
、和 )为原料制备高纯镁砂的工艺流程如下:
已知浸出时产生的废渣中有、和 。下列说法错误的是
( )
B
A.浸出镁的反应为
B.浸出和沉镁的操作均应在较高温度下进行
C.流程中可循环使用的物质有、
D.分离与、是利用了它们氢氧化物 的不同
【解析】信息转换
结合工艺流程可知煅烧后得到的轻烧粉的成分为和少量、、, 溶液呈酸性,浸出时使
及、溶解,浸出后得到的废渣中含有、和,所得浸出液中含有 及过量的
,加入氨水时转化为,经煅烧得到高纯镁砂 。
结合流程图和上述分析可知浸出镁的反应为 ,A项正确;浸出可以在较高
温度下进行,促进水解和 的逸出,但沉镁时应在低温下进行,以减弱氨水分解,B项错误;结合流程图
可知浸出得到的可转化为氨水,用于沉镁,滤液中含有过量的 ,可用于浸出时的反应液,故该流程中
和可循环使用,C项正确;本流程中分离时,、 转化为沉淀,是利用了它们氢氧化物的
不同,D项正确。
铝及其化合物
第二章
教材知识萃取
1.铝的性质及用途
(1)铝的物理性质及用途
银白色固体,具有良好的导热性、导电性和延展性,熔点为
铝合金用于制造汽车、飞机、生活用品等。
(2)从原子结构角度认识铝的化学性质
铝在元素周期表中处于第
层有3个电子,在反应中易失去电子,表现出还原性。
三
与非金属单 质反应
与酸反应 遇冷的浓硫酸或浓硝酸
与非氧化性强酸(如稀盐酸、稀硫酸)反应:
__________(填离子方程式)
与强碱溶液 反应
铝热反应
钝化
2.
(1)
类别 两性氧化物 两性氢氧化物
物理 性质 高熔点,高沸点,高硬度,不溶 于水的白色固体 不溶于水的白色胶状固体,具有吸附性
化学 性质 ①与强酸反应:
(填离子方程式)
化学 性质 ②与强碱反应:
(填离子方程式)
③灼烧:
子方程式)
用途 作耐火材料;炼铝原料 可用作吸附剂、媒染剂和净水剂;治疗
胃酸过多;可作制造瓷釉、耐火材料、
防水织物的原料
续表
&4& 铝是活泼金属,但抗腐蚀性能强,原因是常温下
氧化物薄膜而防止内部金属进一步被氧化。
(2)
①向可溶性铝盐中加入足量氨水:
(填离子方程式)。
②向
(填离子方程式)。
3.
4.从铝土矿中提取
从铝土矿(主要成分是
大工艺流程:
教材素材变式
类型1 铝及其化合物的性质
1.[链接人教版必修第一册P82]下列物质的性质和用途具有对应关系的是( )
C
A.熔点高,可用于电解制铝 B. 不稳定,可用于治疗胃酸过多
C.明矾水解生成胶体,可用作混凝剂 D.铝具有导热性,可用于制备铝热剂
【解析】A项,(熔融)具有导电性,故可以电解生成(【易错辨析】电解 (熔融)冶炼金属铝,而
不用电解,因为为共价化合物,熔融态不导电。),错误;B项,可以与 反应,且碱性较弱,
可用于治疗胃酸过多,错误;C项,明矾水解生成的 胶体具有净水作用,可用作混凝剂,正确;D项,铝
具有强还原性,可以置换出部分金属氧化物中的金属,可用于制备铝热剂,错误。
拓展设问 判正误:铝的金属活泼性强,可用于制作铝金属制品( )
×
【解析】 铝可用于制作铝金属制品,是因为其表面有一层致密的氧化膜,不易被腐蚀,与活泼性无关。
类型2 铝及其化合物的转化
2.[链接苏教版必修第二册P97~98拓展视野]工业上用铝土矿(主要成分为,含 杂质)为原料冶炼铝
的工艺流程如下,下列叙述错误的是( )
C
A.步骤①中,试剂一般使用的是 溶液
B.步骤②中,主要的离子反应可能是:
C.实验室条件下,步骤③中的加热操作常在蒸发皿中完成
D.步骤④中,在电解装置的阴极得到液态金属铝
【解析】通过步骤①得到沉淀和滤液,根据和的性质差异及后续流程知,A项正确;步骤①中 转
化为,步骤②中转化为,要使完全转化为,可通入过量 ,
B项正确;加热 固体应在坩埚中完成,C项错误;电解熔融态的氧化铝制备铝时,由于氧化铝熔点高于铝,
在电解装置的阴极得到液态金属铝,D项正确。
拓展设问 判正误:步骤①中,主要反应的离子方程式为 ( )
√
【解析】 步骤①中,氧化铝与强碱溶液发生反应生成 ,离子方程式正确。
3.[人教版必修第一册P89第14题变式]某铝热剂由铝粉和铁的某种氧化物组成,二者恰好完全反应生成铁单质和
氧化铝。将该铝热剂分成两等份,同温同压下,一份直接与足量的溶液反应,放出的体积为 ;另一份
在完全发生铝热反应后与足量的盐酸反应,放出的体积为 。下列说法错误的是( )
C
A.两份铝热剂分别生成氢气的质量之比一定为
B.两份铝热剂消耗和的物质的量之比一定为
C.铝热剂中铝元素和铁元素的物质的量之比一定为
D.铝热剂中氧元素和铁元素的物质的量之比一定为
【解析】综合分析
设铁的氧化物为,则铝热反应为,将含和 的铝热剂分
成两等份进行实验,则每份中铝的物质的量为,其中一份铝热剂发生铝热反应生成铁的物质的量为 。
设该条件下气体摩尔体积为,铝与足量氢氧化钠溶液反应的关系式为 ,由生成氢气
的体积可以计算出消耗的物质的量为,由,可以计算出 ;铁与盐酸反应的
关系式为,由生成氢气的体积可以计算出消耗的物质的量为,由 ,可计
算出 。
同温同压下,气体的体积之比等于气体的物质的量之比,对于同一种物质,质量之比等于其物质的量之比,故同
温同压下两份铝热剂分别生成氢气的质量之比一定为,A项正确;也与反应,两份铝热剂消耗
和的物质的量之比为 ,B项正确;铝热剂中铝元素和铁元素的物质的量之比
为,C项错误;铝热剂中氧元素和铁元素的物质的量之比 ,
D项正确。
铜及其化合物
第三章
教材知识萃取
1.铜的性质
2.铜的氧化物和氢氧化物的性质
等具有还原性的物质反应生成
_________________
__________________________
3.铜盐的性质
分解为氧化铜可溶性铜盐能与
铜盐
4.铜的冶炼方法
传统湿法炼铜
用碱式碳酸铜制备 方案一,干法:
,
方案二,湿法:
__________,
高温炼铜 工业上用高温冶炼黄铜矿的方法获得铜(粗铜)。
续表
教材素材变式
类型1 铜及其化合物的性质
1.[链接人教版必修第二册P7资料卡片,2023浙江卷1月]硫酸铜应用广泛,下列说法不正确的是( )
A
A.元素位于周期表 区 B.硫酸铜属于强电解质 C.硫酸铜溶液呈酸性 D.硫酸铜能使蛋白质变性
【解析】的价电子排布式为,位于周期表 区,A项错误;硫酸铜属于盐,溶于水或熔融状态下完全电
离,属于强电解质,B项正确;硫酸铜为强酸弱碱盐,由于 水解溶液呈酸性,C项正确;硫酸铜属于重金属盐,
能使蛋白质变性,D项正确。
2.[链接苏教版必修第二册P111第6题等]中国古代涉及的“铜”文化丰富多彩。下列说法错误的是( )
B
A.“石胆化铁为铜”中涉及金属键的断裂
B.铸造铜钱用的材料黄铜是单质铜
C.诗句“庐山山南刷铜绿”中的“铜绿”借指的是 的颜色
D.“青铜器时期”早于“铁器时期”的原因之一是铜比铁稳定
【解析】该反应为, 中的金属键断裂,A项正确;黄铜是铜锌合金,B项错误;碱式碳酸
铜俗称铜绿,C项正确;铜的性质比铁稳定,较易以单质的形式存在,是青铜器时期早于铁器时期的原因之一,D
项正确。
类型2 铜及其化合物的转化
3.[链接苏教版必修第二册P102实验探究等]部分含铜物质的价类关系
如图所示。下列说法正确的是( )
B
A.能与溶液反应:
B.在酸性环境中可以转化为和
C.经一步反应可转化为
D.若为,则其水溶液中可能大量存在、、
【解析】解题关键
根据图示可知,为,为,为,为,为价铜的盐(如 )。
未配平,正确的反应为。为 ,在酸性溶液中发生歧化反应,即
。为,为,不能直接转化为。若 为
,在酸性条件下具有氧化性, 具有还原性,会发生反应
,所以溶液中不能大量存在、 。
4.[链接人教版必修第二册P6资料卡片] 样
品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如
图所示:
下列判断不正确的是( )
D
A.时固体物质的化学式为
B.胆矾晶体存在的最高温度为
C.实验室灼烧固体所需器材除热源外,还需要坩埚、泥三角、
三脚架、坩埚钳等
D.继续升高温度,当固体残留率(剩余固体质量/原始固体质量)
为 时,所得固体产物为黑色
【解析】初始时,样品的物质的量为 ,样品中
,。 时减少的水
的总质量为,则所得固体中 ,此时固体组
成表示为,A项正确; 时固体质量开始减小,即胆矾晶体开始脱水,说明胆矾晶体存在的最高温
度为 ,B项正确;实验室灼烧固体所需器材除热源外,还需坩埚、泥三角、三脚架、坩埚钳等,C项正确;
固体残留率为时,剩余固体的质量为,说明此时 开始分解,生成
铜的氧化物,铜元素质量不变,则氧元素的质量为 ,其物质的
量为,由此可确定固体的组成为, 是一种砖红色固体,D项错误。
金属材料与金属矿物的开发利用
第四章
教材知识萃取
金属材料 包括金属和合金。合金具有金属特性,熔点低于成分金属、硬度高于成分金属
金属冶炼的方法
1.金属的冶炼
(1)实质:使金属离子得到电子,被还原成金属单质的过程。
(2)金属冶炼的一般步骤
2.常见金属的冶炼方法
3.金属冶炼方法的选择
利用金属活泼性的差异,可以采取不同的冶炼方法冶炼金属,常见金属的冶炼方法如表所示:
金属的活动 性顺序
自然界中存 在形式 化合态(陨铁中有单质铁) 少量游离态,主要 化合态 游离态
冶炼方法 电解法 热还原法 热分解法 富集法
教材素材变式
类型1 金属材料
1.[链接人教版必修第一册P78~80,2021河北卷]“灌钢法”是我国古代劳动人民对钢铁冶炼技术的重大贡献,陶弘景
在其《本草经集注》中提到“钢铁是杂炼生 作刀镰者”。“灌钢法”主要是将生铁和熟铁(含碳量约 )混合加
热,生铁熔化灌入熟铁,再锻打成钢。下列说法错误的是( )
C
A.钢是以铁为主的含碳合金 B.钢的含碳量越高,硬度和脆性越大
C.生铁由于含碳量高,熔点比熟铁高 D.冶炼铁的原料之一赤铁矿的主要成分为
【解析】钢是以铁为主的含碳合金,A项正确;纯铁硬度小,质地较软,随着含碳量的升高,钢的硬度和脆性增大,
B项正确;熟铁含碳量比生铁的含碳量低,结合题目信息“生铁熔化灌入熟铁”可知生铁的熔点比熟铁低,C项错误;
赤铁矿为红色,主要成分是 ,D项正确。
类型2 金属的冶炼
2.[链接人教版必修第二册P106第8题等,2022山东卷]高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿
(含、元素的杂质)为主要原料制备 粉的工艺流程如下,可能用到的数据见下表。
开始沉淀 1.9 4.2 6.2
沉淀完全 3.2 6.7 8.2
下列说法错误的是( )
D
A.固体主要成分是和;金属为
B.浸取时,增大 压强可促进金属离子浸出
C.中和调的范围为
D.还原时,增大溶液酸度有利于 的生成
【解析】流程梳理
由上述分析知,A项正确;浸取时,增大 压强即增大反应物浓度,可加快反应速率,促进金属离子浸出,B项正
确;中和调是为了沉淀而不沉淀、,结合表中数据可知,调的范围为 ,C项正确;还
原时发生反应,故增大溶液酸度不利于 的生成,D项错误。
3.[链接苏教版必修第二册P94~98]金、银是贵金属,废旧中含单质、和。从废旧 中回收
单质、 的方法如图所示。
已知:①浓硝酸不能单独将 溶解;
②王水是浓硝酸与浓盐酸的混合物(体积比 );
。
下列说法错误的是( )
C
A.用浓盐酸与也可能使 溶解
B.试剂 可以是浓氨水
C.王水中浓盐酸的主要作用是增强溶液的酸性
D.恰好被完全还原,可消耗
(仅考虑 的反应)
【解析】从流程中可以看出,在、、同时存在时金可溶解,用浓盐酸和 可能使金溶解。
与过量浓氨水能生成,试剂可以是浓氨水。王水中浓盐酸的主要作用是提供 ,
可以得到溶液。仅考虑的反应,结合已知③可知,粉将还原为和 ,金元
素由价降至0价,氢元素由价降为0价,消耗的物质的量为 。
4.[链接鲁科版必修第一册P69化学与技术,2022湖南卷节选]钛 及其合金是理想的高强度、低密度结构材料。以
钛渣(主要成分为,含少量、和 的氧化物杂质)为原料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗 中含有的几种物质的沸点:
回答下列问题:
(1)与C、在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
①该温度下,与C、 反应的总化学方程式为_________________________________________;
【解题思路】 根据混合气体中、、的分压,可计算出三者的物质的量之比约为 ,结合得
失电子守恒和物料守恒可写出总反应的化学方程式为 。
②随着温度升高,尾气中 的含量升高,原因是_________________________。
温度升高,C主要转化为
(2)“除钒”过程中的化学方程式为____________________________;“除硅、铝”过程中,分离中含、 杂质
的方法是________。
蒸馏法
【解题思路】 结合图示流程可知“除钒”时与发生反应生成和。根据与、 沸点相
差较大,知可对混合物进行加热蒸馏,收集约的蒸馏产物,即可除去含、 杂质。
(3)“除钒”和“除硅、铝”的顺序______(填“能”或“不能”)交换,理由是___________________________________
_________________________________。
(4)下列金属冶炼方法与本工艺流程中加入冶炼 的方法相似的是_____。
不能
“除钒”后产生的可在“除硅、铝”时除去,若交换顺序,无法除去
AC
A.高炉炼铁 B.电解熔融氯化钠制钠 C.铝热反应制锰 D.氧化汞分解制汞
【解题思路】 该工艺流程中冶炼时发生反应: ,是利用热还原法,与A、C项原理
相同,而B项是电解法,D项是热分解法,均与该原理不相似。
类型3 金属矿物的开发利用
5.[链接苏教版必修第二册P97拓展视野,2023浙江卷6月]某研究小组用铝土矿为原料制备絮凝剂聚合氯化铝
, ,按如下流程开展实验。
已知:主要成分为,含少量和。用溶液溶解铝土矿过程中 转变为难溶性的铝硅酸
盐。
的絮凝效果可用盐基度衡量,盐基度。当盐基度为 时,絮凝效果较好。
请回答:
(1)步骤Ⅰ所得滤液中主要溶质的化学式是____________。
【解题思路】 步骤Ⅰ中主要发生铝土矿中、溶解于 溶液中的反应,结合已知①及各物质性质知,滤
液中的主要溶质为 。
(2)下列说法不正确的是_____。
BC
A.步骤Ⅰ,反应须在密闭耐高压容器中进行,以实现所需反应温度
B.步骤Ⅱ,滤液浓度较大时通入过量有利于减少 沉淀中的杂质
C.步骤Ⅲ,为减少 吸附的杂质,洗涤时需对漏斗中的沉淀充分搅拌
D.步骤Ⅳ,控制和 的投料比可控制产品盐基度
【解题思路】 步骤Ⅰ为铝土矿的高温碱液浸取过程,故反应须在密闭耐高压容器中进行,A项正确;步骤Ⅱ发生反
应:,当滤液中浓度较大时,通入过量,因 溶
解度较小,从而使含较多 杂质,B项错误;过滤时,漏斗中垫有滤纸,若搅拌则可能导致滤纸破损,
从而导致过滤失败,C项错误;由产品聚合氯化铝的化学式及已知②可知,步骤Ⅳ控制和 的投料比可
控制产品的盐基度,D项正确。
(3)步骤Ⅴ采用如图所示的蒸汽浴加热,仪器A的名称是________;步骤Ⅴ不宜用酒精灯直接加热
的原因是____________________________。
蒸发皿
温度升高,聚合氯化铝会分解
【解题思路】 由仪器A的构造可知其名称为蒸发皿。用酒精灯直接加热时,温度较高,聚合氯化铝会分解。
(4)测定产品的盐基度。
的定量测定:称取一定量样品,配成溶液,移取溶液于锥形瓶中,调,滴加指示剂 溶
液。在不断摇动下,用标准溶液滴定至浅红色(有 沉淀),30秒内不褪色。平行测
试3次,平均消耗标准溶液 。
另测得上述样品溶液中 。
①产品的盐基度为____。
0.7
【解题思路】测定过程中发生反应: ,则
, ,由化合物中各元素化合价代数
和为0知聚合氯化铝为,故产品的盐基度为 。
②测定过程中溶液 过低或过高均会影响测定结果,原因是_____________________________________________
_________________________________________________________________________。
过低,转为,浓度降低,不能形成沉淀显色以指示终点;过高,转为(或)沉淀,影响测定
【解题思路】 测定过程中,溶液中存在反应:,溶液 过低,即
浓度过大,平衡正向移动,从而影响的生成;过高,则易形成或 。
必做实验:铁及其化合物的性质
第五章
必做实验拓展
1.[链接人教版必修第一册P90实验活动2,2023浙江卷1月]探究铁及其化合物的性质,下列方案设计、现象和结论都正确的是 ( )
实验 方案 现象 结论
A 往溶液中加入 片 短时间内无明显现象 的氧化能力比 弱
B 往溶液中滴加 溶液,再加入少 量 固体 溶液先变成血红色后 无明显变化 与 的反应不可逆
C 将食品脱氧剂样品中的还原铁粉溶于盐酸, 滴加 溶液 溶液呈浅绿色 食品脱氧剂样品中没有 价铁
D 向沸水中逐滴加滴饱和 溶液,持续 煮沸 溶液先变成红褐色再 析出沉淀 先水解得 再聚集成
沉淀
D
【解析】 往溶液中加入片,发生反应,的氧化能力比 的强,A项错误;
往溶液中滴加溶液,发生反应,溶液变血红色,再加入少量 固体,
对平衡无影响,故不能说明与的反应不可逆,B项错误;若食品脱氧剂样品中有价铁,铁粉与 价铁
发生反应,滴加溶液,溶液呈浅绿色,C项错误;向沸水中逐滴加滴饱和 溶液,
继续煮沸至溶液呈红褐色,得到胶体,持续煮沸, 胶体发生聚沉,析出红褐色沉淀,D项正确。
2.[链接人教版必修第一册P90实验活动2]在工业上用途非常广泛,通过下列实验探究 溶液的性质。
实验1:将浓 溶液滴入沸水中,分散系呈现红褐色;
实验2:在装有少量 溶液的试管中加入铜粉充分振荡,溶液由黄色变成蓝色;
实验3:在装有少量溶液的试管中加入过量溶液,充分振荡后,分成两份:一份加入有机溶剂 ,振荡后
层显紫红色;另一份加入 溶液,溶液显红色;
实验4:在装有少量溶液的试管中加入少量 溶液,充分振荡后产生白色沉淀。下列说法正确的是( )
C
A.实验1中的铁元素形成的粒子大小没有改变
B.实验2中发生反应的离子方程式为
C.实验3中与 发生氧化还原反应,但该反应存在限度
D.实验4静置后溶液中大量存在的离子有、、、
【解析】实验1中得到的红褐色分散系为 胶体,其胶体粒子直径大于溶液中铁元素形成的分子、离子的直
径,A项错误;实验2中发生的反应为,B项错误;实验3中一份振荡后 层呈紫红色,
说明过量溶液和少量溶液发生氧化还原反应生成了,另一份反应液能使 溶液呈红色,说明溶液中仍
含,即和的反应是可逆的,该反应存在限度,C项正确;与反应生成沉淀,即溶液中 、
不能大量存在,D项错误。
3.[链接人教版必修第一册P76研究与实践等,2023海南卷]某小组开展“木耳中铁元素的检测”活动。检测方案的主要步骤有:粉碎、称量、灰化、氧化、稀释、过滤、滴定等。回答问题:
(1)实验方案中出现的图标 和 ,前者提示实验中会用到温度较高的设备,后者要求实验者____________
(填防护措施)。
佩戴护目镜
【解题思路】实验中的&4& 标识要求实验者佩戴护目镜,以保护眼睛。
(2)灰化:干燥样品应装入__中(填标号),置高温炉内,控制炉温 ,在充足空气气氛中燃烧成灰渣。
.不锈钢培养皿 .玻璃烧杯
.石英坩埚
【解题思路】高温灼烧固体物质需在坩埚中进行。
(3)向灰渣中滴加 的硝酸,直至没有气泡产生。灰化容器中出现的红棕色气体主要成分是_____
(填化学式),因而本实验应在实验室的________中进行(填设施名称)。若将漏斗直接置于容量瓶上
过滤收集滤液(如图所示),存在安全风险,原因是______________________。
通风橱
装置重心不稳,易倾倒
【解题思路】向灰渣中滴加的硝酸,灰化容器中出现的红棕色气体主要成分是,由于 有毒,
所以需在通风橱中进行;将漏斗直接置于容量瓶上过滤收集滤液,装置较高,易重心不稳,存在安全风
险。
(4)测定铁含量基本流程:将滤液在容量瓶中定容,移取,驱尽并将全部还原为 。
用微量滴定管盛装 标准溶液进行滴定。
①选用微量滴定管的原因是________________________________。
减小误差,滴定更准确,节约试剂
【解题思路】木耳中铁含量较少,选用微量滴定管可减小实验误差,使滴定更准确,并且节约试剂。
②三次平行测定的数据如下表。针对该滴定数据,应采取的措施是________________。
序号 1 2 3
标准溶液用量/ 2.715 2.905 2.725
舍去第二次数据
【解题思路】三次平行滴定中,第二组数据偏差较大,可能为错误操作得到的数据,应舍去。
③本实验中,使测定结果偏小的是__(填标号)。
.样品未完全干燥
.微量滴定管未用标准溶液润洗
.灰渣中有少量炭黑
【解题思路】铁元素的含量,样品未完全干燥,会造成样品质量偏大,使测定结果偏小,
正确;微量滴定管未用标准溶液润洗,会使标准溶液被稀释,消耗的标准溶液体积偏大,测定结果偏大, 错误;
灰渣中有少量炭黑,对测定结果无影响, 错误。
命题动向
立足教材,强化对教材内容的深度思考,强化教学导向
以实验为基础是化学学科的重要特征之一,化学实验对于全面发展考生的化学学科核心素养有极为关键的作用。选择教材实验作为命题素材,有利于落实基础性的考查,有利于检测各学校贯彻新课程标准关于培养考生实验能力的要求,有利于了解和掌握教师对教科书的使用水平。本题实验源自人教版必修第一册第三章第一节的研究与实践“检验食品中的铁元素”,其中(1)中图标源自人教版必修第一册第一章第一节中的提示栏目。
4.[链接鲁科版必修第一册P88活动·探究]柠檬酸亚铁是一种补血铁制剂,可以用于药物开发及饲料添加剂。以硫酸亚铁和柠檬酸为主要原料的制备程序及有关装置如下:
(1)制备
①该制备实验所用的溶液、 溶液需临时配制,配制这些溶液的蒸馏水必须煮沸冷却,目的是_______
_______________。
除去蒸馏水中溶解的氧
【解题思路】为防止被溶液中溶解的 氧化,配制溶液的蒸馏水必须煮沸冷却。
【解题思路】反应Ⅰ生成和,则操作Ⅰ中将沉淀洗涤后,可以通过检验最后一次洗涤液中是否含有
来检验是否洗涤干净,故所选试剂为 溶液。
②操作Ⅰ中将沉淀洗涤后,检验是否洗涤干净的试剂为______(填化学式)。
(2)制备柠檬酸亚铁
①反应Ⅱ中 与柠檬酸反应制备柠檬酸亚铁时需加入抗氧化剂,该抗氧化剂是___(填标号)。
粉粉 粉
【解题思路】为不引入新的杂质离子,选择的抗氧化剂应为铁粉。
②操作Ⅱ应先加入无水乙醇,再静置、抽滤、洗涤、干燥。加入无水乙醇的目的是________________________。
减小柠檬酸亚铁的溶解度
【解题思路】操作Ⅱ先加入无水乙醇,再静置、抽滤、洗涤、干燥,获得柠檬酸亚铁,则加入无水乙醇可减小柠檬酸亚铁的溶解度。
(3)实验测得产品柠檬酸亚铁的产率和产品中的铁含量随着溶液 、温度的变
化曲线如图所示。则该方法制备柠檬酸亚铁的最佳条件是__________________。
较高时,产品产率降低的原因是_______________________________________
________________________________。
左右,
大于7时,水解程度增大,转化为,导致柠檬酸亚铁的产率降低
【解题思路】根据图示,左右、 时柠檬酸亚铁的产率大、产品中铁
的含量高,为制备柠檬酸亚铁的最佳条件。大于7时, 水解程度增大,转
化为 ,导致柠檬酸亚铁的产率降低。
(4)称取上述方法制备的柠檬酸亚铁样品,配制成一定物质的量浓度的溶液,量取 溶液转
移至锥形瓶中,加酸性溶液,至溶液恰好出现粉红色,且 内不褪色,再向溶液中加入适量还原剂将
完全还原为,加入酸化后,用溶液滴定四次,消耗的 溶液体积如下
表:
测定组次 1 2 3 4
消耗溶液体积/ 17.09 20.3 16.97 16.94
该柠檬酸亚铁样品中铁含量为______%。
19.04
【解题思路】根据得失电子守恒,可得关系式 ,四次实验中第二次实验数据误差较大,舍去,取其
余三次实验的数据平均值,消耗溶液,则 样品中
,该柠檬酸亚铁样品中铁含量为
。
谢谢
同课章节目录
