北京市重点中学2016届高三化学 元素化合物复习指导课件(2015年11月)
文档属性
| 名称 | 北京市重点中学2016届高三化学 元素化合物复习指导课件(2015年11月) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-03-11 00:00:00 | ||
图片预览









文档简介
课件48张PPT。2016元素化合物复习的思考 2015化学主观试题分数统计表
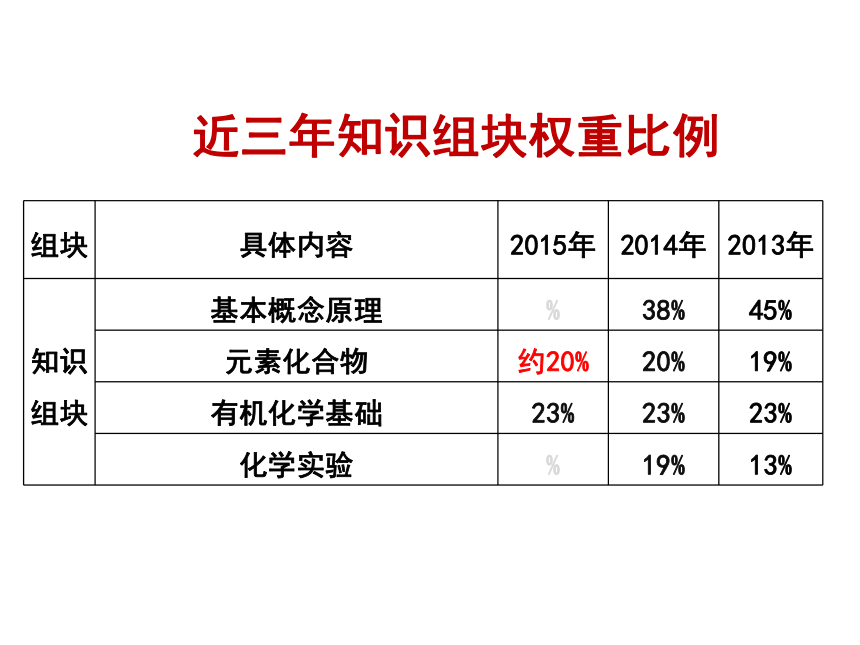
近三年元素化合物知识组块权重比例
一轮复习元素化合物知识组块的课例
元素化合物知识与理论、概念、实验的关联的课例
交流内容
化学学科特点是以元素为核心,从微观的角度研究物质的变化及其规律的科学。
元素化合物的总体认识1、元素有多种存在形式(物质的分类和元素价态)
2、不同形式物质之间可以相互转化
3、转化是有规律的(酸碱规律,氧还规律)
4、转化可以有多种途径
5、转化过程是有条件的(温度、浓度、压强、用量)
6、转化过程是可控制的(反应速率和反应限度)元素化合物的考查角度:
核心价值:新课程化学学科的核心价值是:化学学科思想、学科方法、应用。
核心知识:体现核心价值的是化学概念、化学原理、化学研究的基本方法等核心知识。
知识载体:知识支撑化学核心知识的载体是元素化合物知识,以元素化合物知识为载体进行知识应用和能力测试。
考题内容:用化工生产、能源、材料、环境等生产、生活方面的常见化学事物为背景,以元素化合物知识为载体重点考查考生的化学概念、化学原理等知识及化学实验方法与技能。 近三年知识组块权重比例体会元素化合物在高考的呈现2014年元素化合物知识点分布26(1)
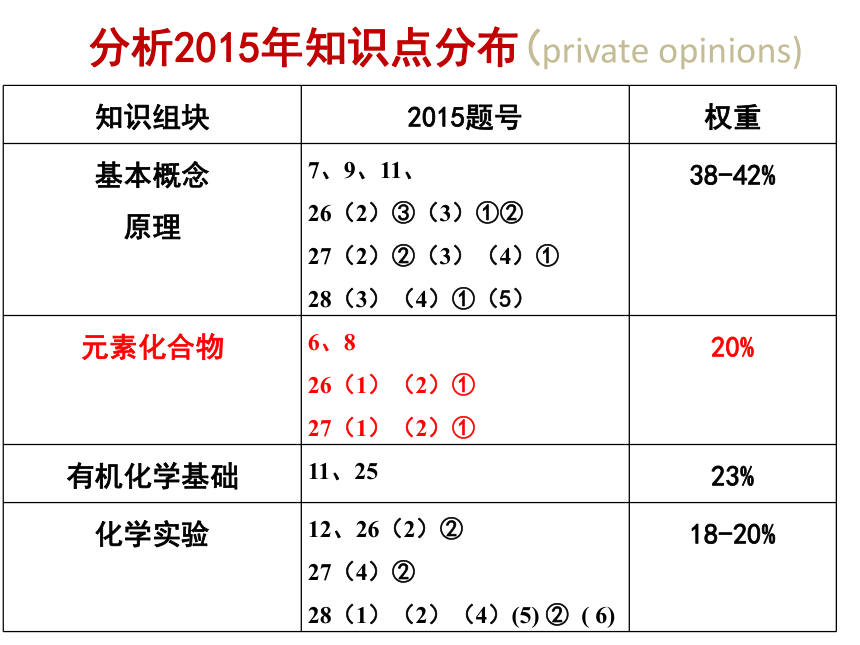
27(1)①(2)①分析2015年知识点分布(private opinions)2015年元素化合物知识点分布(学生)通过___了解___提高____
(学生)通过___掌握___反思____
对元素化合物复习的过程思考知识:回答“是什么”问题;
能力:回答“为什么”问题;
学科思想:回答“怎么办”问题高三复习:不是简单知识的重复,
是知识的整合、能力和思想的提升。学生自主做帮助学生做思考1:复习的有效性取决于什么?策略的科学性-------认真研读《考试说明》
目标的准确性-------考题的知识点与能力点
(指导如何选题)
设计的针对性-------学生实际知识 和能力结构
(内容安排的顺序)一 、学习《考试说明》----复习的定位 (内容)
二 、分析高考试题、北京模拟题------复习的资源(选题)
三 、建构知识网络-----复习的脉络(师生)
四 、培养能力与方法-----复习的技巧(师生)
五 、设计实施方案-----复习的计划 (落实)
六、关注每个学生-----复习的有效 (成绩)
思考2:复习的框架是什么? 一轮复习元素化合物知识组块的课例课例1-核心物质SO2的性质 元素的复习,采用“由个别到一般,再由一般到个别”
的复习方式 利用反应规律复习元素化合物知识。
抓住两条主线:
复分解反应原理主线
氧化还原反应原理主线
Fe3++SO2Fe2+ +SO42-Fe(SO2)63+ 红浅绿瞬间约15分钟第二天红浅绿红色逐渐褪去反应速率快反应程度大“竞争关系”A反应B反应结论:SO2与Fe3+的反应过程中,配合反应
和氧化还原反应同时存在,配合反应速率
更快,氧化还原反应限度更大。
Fe3++6SO2 Fe(SO2)63+ AB由现象说明A反应慢,但反应程度(限度)大
B反应快,但反应程度(限度)小如何选题落实知识B装置中现象微观成因
因素1酸雾H2SO4
因素2 O2
因素1酸雾、因素2 O2
控制酸雾
控制O2
找证据
下结论(例题2011年第27题)B实验过程:未知微粒的探究过程SO2
酸性
还原性 C装置中现象微观成因
H2SO3
NO3-
SO4
微粒反应
条件
找证据
下结论C实验过程:已知微粒的验证过程SO2
酸性
还原性 (例题2013年第28)i.液面上方出现白雾;
ii.稍后,出现浑浊,溶液变为黄绿色;
iii.稍后,产生大量白色沉淀,黄绿色褪去 。实验过程:课例2-核心元素 Fe3+与Fe2+相互转化 word设计实验探究Fe3+与Fe2+相互转化
实验探究Fe3+与Fe2+相互转化?(分别取1ml)
实验1:??0.1?mol/L?FeCl2溶液???????????????? 无明显现象??????????? 溶液变红?
实验2:??0.1?mol/L?FeCl3溶液???????????????? 溶液变红?????????????? 红色未褪去
滴加氯水滴加KSCN
溶液滴加0.1?mol/L?
KI溶液滴加KSCN
溶液实验2的现象与预测不同?
试题的改进和融合实验2的现象与预测不同,?为探究可能的原因,又进行了如下实验:????
步骤1:10?mL?0.1?mol/L?KI溶液?????????????????????? 溶液明显变黄
步骤2:将黄色溶液分为三份:???????????????
试管1?取2?mL黄色溶液????????????????? 溶液变红??????
试管2?取2?mL黄色溶液??????????????????? 溶液变蓝??????
得出的实验结论是____________________ 。??滴加KSCN溶液滴加6滴0.1?mol/L
?FeCl3溶液?滴加铁氰化钾溶液2Fe3++2I- 2Fe2++I2Fe2+被空气氧化成Fe3+?
如何证明某化学反应是可逆的?
方案1:检验产物,检验不足量的反应物有剩余
若是可逆反应,应当有平衡移动,又进行了如下实验设计:?
试管3?取2?mL黄色溶液???????? 取上层溶液???????????溶液变蓝
试管4?取2?mL黄色溶液???????? 溶液黄色褪去
?加入2mlCCl4?滴加铁氰
化钾溶液(比试管2中溶液颜色深)?已知:FeF63-是一种无色的稳定的络离子滴加NH4F溶液?得出的实验结论____________________ 。?2Fe3++2I- 2Fe2++I2如何证明某可逆反应存在?
方案2:存在动态平衡
如何证明某可逆反应存在?
方案3:原电池
设计如图原电池装置,接通灵敏
电流计,指针向右偏转(注:灵
敏电流计指针总是偏向电源正极)
,随着时间进行电流计读数逐渐变
小,最后读数变为零.当指针读数
变零后,在乙烧杯中加入1mol/L
FeCl2溶液,若观察到灵敏电流计
的指针向左方向偏转。即可判断该反应为可逆反应。
为探讨化学平衡移动原理与氧化还原反应规律的联系,某同学
通过改变浓度研究“2 Fe + 2 I ≒ 2 Fe + I2”反应中Fe 和Fe 的
相互转化。实验如下:以核心元素性质及其转化为基础载体
猜想
方案
现象
结论结构分离
提纯
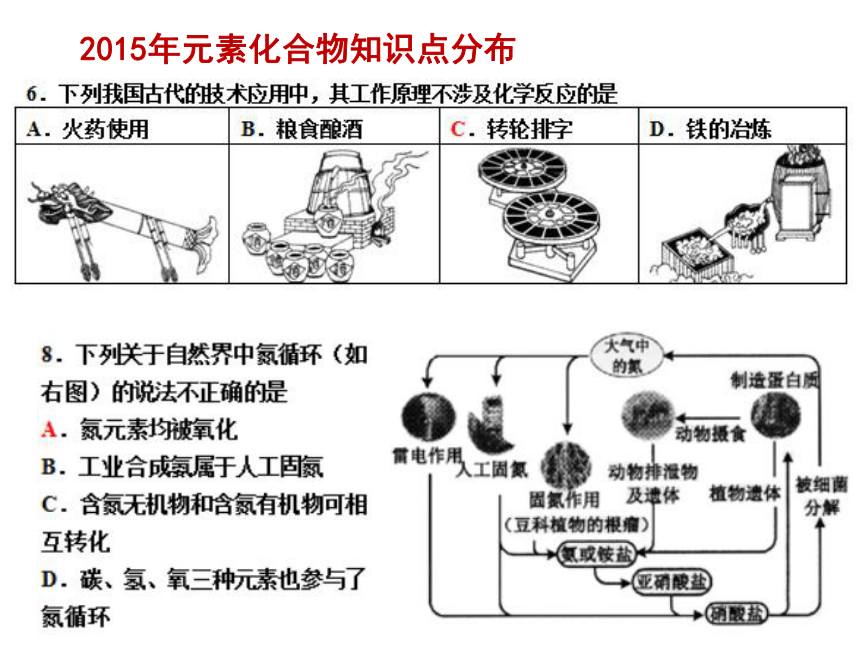
元素化合物知识与理论、概念、实验的关联性课例3-核心元素N的转化 -3 0 +1 +2 +3 +4 +5 物质分类、酸碱规律、氧化还原性规律Ⅴ基础概念和理论化学实验工业生产环境问题制备:实验室制
NH3, NO2, NO
性质:NH4+检验;
HNO3性质NH3、HNO3、
有机含氮化合物NOx、酸雨、水富营养化氧还、热反应、结构、
平衡、电解质、电化学2015-8-N元素及其化合物的性质2014-26-热能2014-26-热能、平衡常数2013-26-原电池 ①还原 ②NO+O2--2e-=NO22014-26(4)-电解池
IV中,电解NO制备
NH4NO3,其工作原理如右
图所示,为使电解产物全
部转化为NH4NO3,需补充
物质A,A是________,
说明理由:_______________________________
NH32014-6(1)(2)-化学平衡
2013-西城-实验探究 化学高考命题,信息素养考察非常明确,采用多种
形式呈现试题内容,为考生提供图表、模型、流程图、
数据、实验现象等丰富的信息,创设真实的、有价值的、
有较强思维力度的问题情境,考查学生收集信息、捕捉
有用信息、分析处理材料和解决问题的能力。试题的呈现特点2016年的化学复习建议:
复习夯实基础、不做偏难怪题、注意方法总结、
注意高考题和模拟题的有效利用。
近三年元素化合物知识组块权重比例
一轮复习元素化合物知识组块的课例
元素化合物知识与理论、概念、实验的关联的课例
交流内容
化学学科特点是以元素为核心,从微观的角度研究物质的变化及其规律的科学。
元素化合物的总体认识1、元素有多种存在形式(物质的分类和元素价态)
2、不同形式物质之间可以相互转化
3、转化是有规律的(酸碱规律,氧还规律)
4、转化可以有多种途径
5、转化过程是有条件的(温度、浓度、压强、用量)
6、转化过程是可控制的(反应速率和反应限度)元素化合物的考查角度:
核心价值:新课程化学学科的核心价值是:化学学科思想、学科方法、应用。
核心知识:体现核心价值的是化学概念、化学原理、化学研究的基本方法等核心知识。
知识载体:知识支撑化学核心知识的载体是元素化合物知识,以元素化合物知识为载体进行知识应用和能力测试。
考题内容:用化工生产、能源、材料、环境等生产、生活方面的常见化学事物为背景,以元素化合物知识为载体重点考查考生的化学概念、化学原理等知识及化学实验方法与技能。 近三年知识组块权重比例体会元素化合物在高考的呈现2014年元素化合物知识点分布26(1)
27(1)①(2)①分析2015年知识点分布(private opinions)2015年元素化合物知识点分布(学生)通过___了解___提高____
(学生)通过___掌握___反思____
对元素化合物复习的过程思考知识:回答“是什么”问题;
能力:回答“为什么”问题;
学科思想:回答“怎么办”问题高三复习:不是简单知识的重复,
是知识的整合、能力和思想的提升。学生自主做帮助学生做思考1:复习的有效性取决于什么?策略的科学性-------认真研读《考试说明》
目标的准确性-------考题的知识点与能力点
(指导如何选题)
设计的针对性-------学生实际知识 和能力结构
(内容安排的顺序)一 、学习《考试说明》----复习的定位 (内容)
二 、分析高考试题、北京模拟题------复习的资源(选题)
三 、建构知识网络-----复习的脉络(师生)
四 、培养能力与方法-----复习的技巧(师生)
五 、设计实施方案-----复习的计划 (落实)
六、关注每个学生-----复习的有效 (成绩)
思考2:复习的框架是什么? 一轮复习元素化合物知识组块的课例课例1-核心物质SO2的性质 元素的复习,采用“由个别到一般,再由一般到个别”
的复习方式 利用反应规律复习元素化合物知识。
抓住两条主线:
复分解反应原理主线
氧化还原反应原理主线
Fe3++SO2Fe2+ +SO42-Fe(SO2)63+ 红浅绿瞬间约15分钟第二天红浅绿红色逐渐褪去反应速率快反应程度大“竞争关系”A反应B反应结论:SO2与Fe3+的反应过程中,配合反应
和氧化还原反应同时存在,配合反应速率
更快,氧化还原反应限度更大。
Fe3++6SO2 Fe(SO2)63+ AB由现象说明A反应慢,但反应程度(限度)大
B反应快,但反应程度(限度)小如何选题落实知识B装置中现象微观成因
因素1酸雾H2SO4
因素2 O2
因素1酸雾、因素2 O2
控制酸雾
控制O2
找证据
下结论(例题2011年第27题)B实验过程:未知微粒的探究过程SO2
酸性
还原性 C装置中现象微观成因
H2SO3
NO3-
SO4
微粒反应
条件
找证据
下结论C实验过程:已知微粒的验证过程SO2
酸性
还原性 (例题2013年第28)i.液面上方出现白雾;
ii.稍后,出现浑浊,溶液变为黄绿色;
iii.稍后,产生大量白色沉淀,黄绿色褪去 。实验过程:课例2-核心元素 Fe3+与Fe2+相互转化 word设计实验探究Fe3+与Fe2+相互转化
实验探究Fe3+与Fe2+相互转化?(分别取1ml)
实验1:??0.1?mol/L?FeCl2溶液???????????????? 无明显现象??????????? 溶液变红?
实验2:??0.1?mol/L?FeCl3溶液???????????????? 溶液变红?????????????? 红色未褪去
滴加氯水滴加KSCN
溶液滴加0.1?mol/L?
KI溶液滴加KSCN
溶液实验2的现象与预测不同?
试题的改进和融合实验2的现象与预测不同,?为探究可能的原因,又进行了如下实验:????
步骤1:10?mL?0.1?mol/L?KI溶液?????????????????????? 溶液明显变黄
步骤2:将黄色溶液分为三份:???????????????
试管1?取2?mL黄色溶液????????????????? 溶液变红??????
试管2?取2?mL黄色溶液??????????????????? 溶液变蓝??????
得出的实验结论是____________________ 。??滴加KSCN溶液滴加6滴0.1?mol/L
?FeCl3溶液?滴加铁氰化钾溶液2Fe3++2I- 2Fe2++I2Fe2+被空气氧化成Fe3+?
如何证明某化学反应是可逆的?
方案1:检验产物,检验不足量的反应物有剩余
若是可逆反应,应当有平衡移动,又进行了如下实验设计:?
试管3?取2?mL黄色溶液???????? 取上层溶液???????????溶液变蓝
试管4?取2?mL黄色溶液???????? 溶液黄色褪去
?加入2mlCCl4?滴加铁氰
化钾溶液(比试管2中溶液颜色深)?已知:FeF63-是一种无色的稳定的络离子滴加NH4F溶液?得出的实验结论____________________ 。?2Fe3++2I- 2Fe2++I2如何证明某可逆反应存在?
方案2:存在动态平衡
如何证明某可逆反应存在?
方案3:原电池
设计如图原电池装置,接通灵敏
电流计,指针向右偏转(注:灵
敏电流计指针总是偏向电源正极)
,随着时间进行电流计读数逐渐变
小,最后读数变为零.当指针读数
变零后,在乙烧杯中加入1mol/L
FeCl2溶液,若观察到灵敏电流计
的指针向左方向偏转。即可判断该反应为可逆反应。
为探讨化学平衡移动原理与氧化还原反应规律的联系,某同学
通过改变浓度研究“2 Fe + 2 I ≒ 2 Fe + I2”反应中Fe 和Fe 的
相互转化。实验如下:以核心元素性质及其转化为基础载体
猜想
方案
现象
结论结构分离
提纯
元素化合物知识与理论、概念、实验的关联性课例3-核心元素N的转化 -3 0 +1 +2 +3 +4 +5 物质分类、酸碱规律、氧化还原性规律Ⅴ基础概念和理论化学实验工业生产环境问题制备:实验室制
NH3, NO2, NO
性质:NH4+检验;
HNO3性质NH3、HNO3、
有机含氮化合物NOx、酸雨、水富营养化氧还、热反应、结构、
平衡、电解质、电化学2015-8-N元素及其化合物的性质2014-26-热能2014-26-热能、平衡常数2013-26-原电池 ①还原 ②NO+O2--2e-=NO22014-26(4)-电解池
IV中,电解NO制备
NH4NO3,其工作原理如右
图所示,为使电解产物全
部转化为NH4NO3,需补充
物质A,A是________,
说明理由:_______________________________
NH32014-6(1)(2)-化学平衡
2013-西城-实验探究 化学高考命题,信息素养考察非常明确,采用多种
形式呈现试题内容,为考生提供图表、模型、流程图、
数据、实验现象等丰富的信息,创设真实的、有价值的、
有较强思维力度的问题情境,考查学生收集信息、捕捉
有用信息、分析处理材料和解决问题的能力。试题的呈现特点2016年的化学复习建议:
复习夯实基础、不做偏难怪题、注意方法总结、
注意高考题和模拟题的有效利用。
同课章节目录
