6.3.2 实验室制取二氧化碳 课件(共29张PPT) 2024-2025学年化学鲁教版九年级上册
文档属性
| 名称 | 6.3.2 实验室制取二氧化碳 课件(共29张PPT) 2024-2025学年化学鲁教版九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 52.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-11-09 00:00:00 | ||
图片预览






文档简介
(共29张PPT)
6.3.2 实验室制取二氧化碳
“双碳目标”
1.探究实验室中制取二氧化碳的装置。
2.初步学习在实验室制取二氧化碳。
3.了解碳达峰和碳中和的意义以及实现“双碳目标”的路径。
在生活中,只要稍加留意,我们不难发现二氧化碳的身影,它与人类的生产、生活密不可分。
思考
实验室里如何制取二氧化碳呢?
一、实验室制取二氧化碳
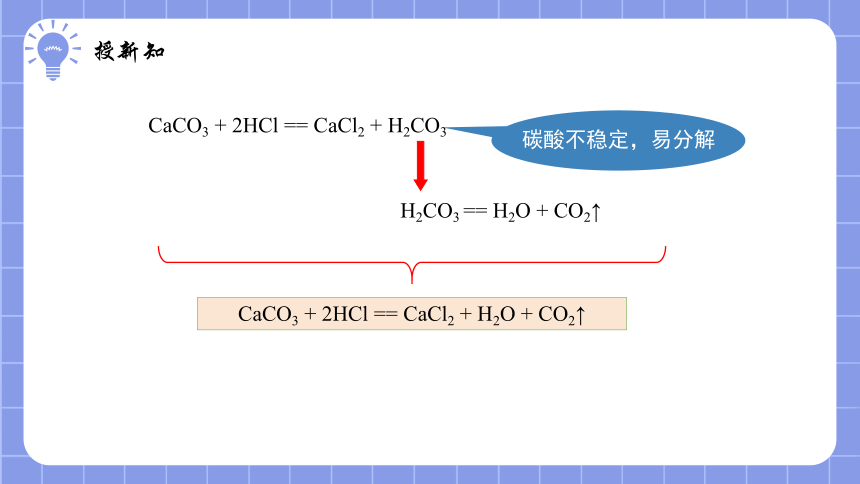
1.反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑
实验室常用大理石(或石灰石)与稀盐酸反应制取二氧化碳。
CaCO3 + 2HCl == CaCl2 + H2CO3
H2CO3 == H2O + CO2↑
碳酸不稳定,易分解
CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
为什么不用稀硫酸与石灰石反应制取二氧化碳呢?
虽然该反应能生成二氧化碳:
CaCO3+H2SO4===CaSO4 +H2O+CO2↑
但生成的CaSO4微溶于水,覆盖在大理石表面,形成一层薄膜,使石灰石与酸不能接触,反应难以进行。
实验室制取二氧化碳不能用稀硫酸代替稀盐酸
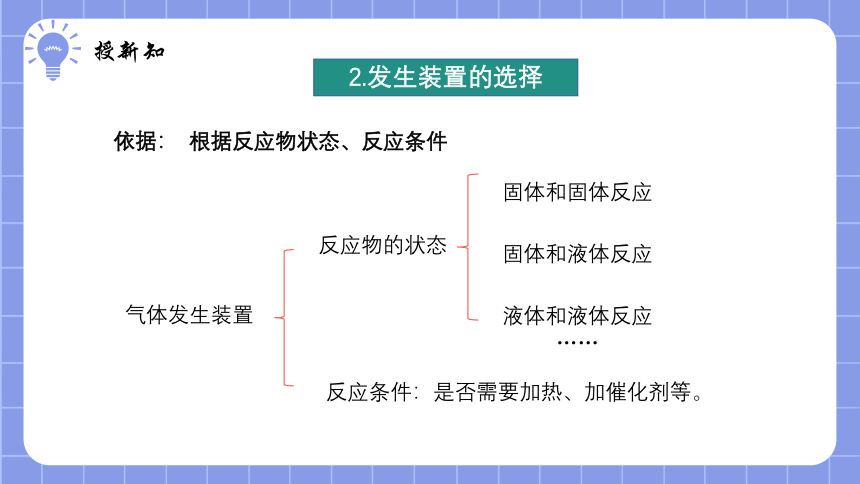
依据: 根据反应物状态、反应条件
气体发生装置
反应物的状态
固体和固体反应
固体和液体反应
液体和液体反应
……
反应条件:是否需要加热、加催化剂等。
2.发生装置的选择
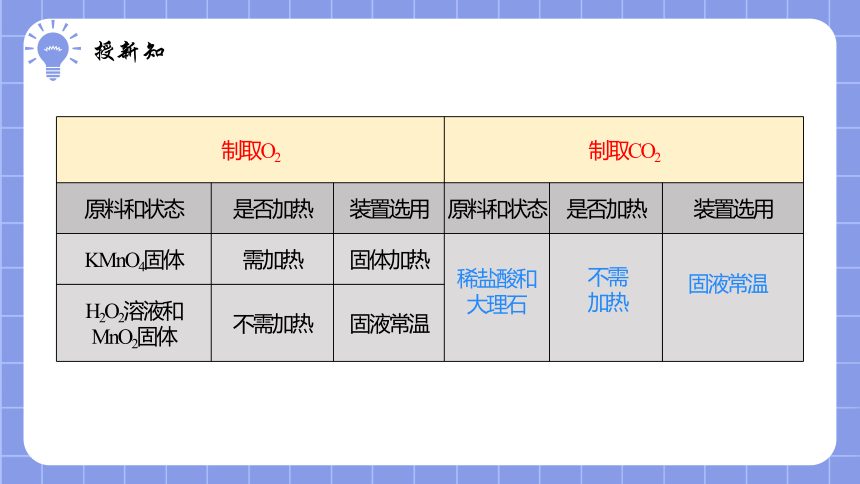
制取O2 制取CO2 原料和状态 是否加热 装置选用 原料和状态 是否加热 装置选用
KMnO4固体 需加热 固体加热
H2O2溶液和MnO2固体 不需加热 固液常温 稀盐酸和大理石
不需加热
固液常温
排水法:不易溶于水,不与水发生反应。
气体收集装置
排空气法
密度比空气大的——向上排空气法
密度比空气小的——向下排空气法
气体收集装置取决于气体的密度和溶解性。
3.收集装置的选择
制取O2 制取CO2 密度与空气比较 是否溶于水 装置选用 密度与空气比较 是否溶于水 装置选用
大于空气 不易溶于水 向上排空气或排水法
大于空气
易溶于水
向上排空气法
实验装置
CaCO3+2HCl=CaCl2+H2O+CO2↑
1
2
实验步骤
①检验气密性——②加入药品——③收集气体——④进行验满——⑤检验气体
1.如何检验该发生装置的气密性?
发生装置
收集装置
2.如何检验二氧化碳是否收集满?
微热法
方法:
用手握住试管,导管末端产生气泡。松开手一段时间后,导管末端上升一段水柱,一段时间不下降说明气密性良好。
方法:
将燃着的木条放在集气瓶口,若木条熄灭,则CO2已满。
验满
注意事项:
长颈漏斗下端应浸入液面以下
导管应刚露出橡皮塞即可
以利于气体的导出
导管应伸入集气瓶底部
防止气体从长颈漏斗逸出
有利于排尽集气瓶内的空气
距今10000 年到270年间,大气中的二氧化碳浓度维持在相对稳定的水平。18 世纪工业革命之后,随着大规模砍伐森林、化石燃料的燃烧量急剧增加,海洋和陆地生物圈不能完全吸收排放出的二氧化碳,导致大气中二氧化碳浓度不断增加,自然界中碳循环的平衡被打破,对人类生存环境产生了不利影响。
为加强对气候变化威胁的应对,《联合国气候变化框架公约》近200个缔约方于2015年12 月达成《巴黎协定》,提出把全球平均气温较工业化前水平升高制在 2℃之内,并为把升温控制在1.5℃之内而努力。
二、实现“双碳”目标的路径
通过植树造林、节能减排等形式,抵消自身产生的二氧化碳或温室气体排放量,实现正负抵消,达到相对“零排放”。
某一个时刻,二氧化碳排放量达到历史最高值,之后逐步回落。
碳达峰
碳中和
为体现中国在应对气候变化问题上的大国担当,我国宣布提高国家自主贡献力度,二氧化碳排放力争于2030年前达到峰值,努力争取 2060 年前实现碳中和。
近 年 来
积极布局碳中和
积极参与国际社会碳减排
顺应绿色低碳发展潮流
中国共产党第二十次全国代表大会报告中指出:“实现碳达峰碳中和是一场广泛而深刻的经济社会系统性变革,立足我国能源资源禀赋,坚持先立后破,有计划分步骤实施碳达峰行动。完善能源消耗总量和强度调控,重点控制化石能源消费,逐步转向碳排放总量和强度‘双控’制度。推动能源清洁低碳高效利用,推进工业、建筑、交通等领域清洁低碳转型。”
发展数字产业
高新技术产业
控制化石能源
现代服务业
植 树 造 林
循 环 利 用
碳中和目标的实现和我们每个个体都息息相关。每个人都应该为碳中和、碳减排贡献自己的力量。
步 行
节 水
节 电
减 少 浪 费
拼 车 出 行
公 共 交 通
种 一 棵 树
随手关闭电脑
自备购物袋
实现“双碳”目标中化学科学的新使命
全世界科学家高度关注二氧化碳的转化和综合利用,尝试运用化学原理和方法,积极研究如何使二氧化碳资源化,以促进自然界中碳的循环;寻求低成本的捕集方法,把二氧化碳转变为燃料,从而使二氧化碳在促进人类可持续发展中发挥更大的作用。
CO2 + 3H2
CH3OH + H2O
催化剂
1.鉴别空气、氧气和二氧化碳三种气体,简便可行的方法是
A.观察气体的颜色、气味
B.将气体分别通入澄清石灰水中
C.将燃着的小木条分别插入气体中
D.通过实验比较三种气体的溶解性
C
2.制备二氧化碳的下列装置图中哪个装置中既有错误,也不能“即开即用,随关随停” ( )
A. B. C. D.
A
3.碳中和的实现途径不包括( )
A.加大可再生能源的开发和利用
B.增加森林砍伐以扩大城市建设用地
C.改进生产工艺,提高能源利用效率
D.推广新能源汽车,减少燃油消耗
B
二氧化碳制取的研究
药品:石灰石(大理石)和稀盐酸
反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑
检验:通入澄清石灰水,石灰水变浑浊。
发生装置:固液不加热型
收集装置:向上排空气法
装置的确定
验满:将燃着的木条放在瓶口,熄灭则已满。
“双碳目标”
碳达峰——碳排放的最高点
碳中和——碳排放与吸收达到平衡
从源头控制碳排放
措施
加大力度促进二氧化碳的吸收和转化
6.3.2 实验室制取二氧化碳
“双碳目标”
1.探究实验室中制取二氧化碳的装置。
2.初步学习在实验室制取二氧化碳。
3.了解碳达峰和碳中和的意义以及实现“双碳目标”的路径。
在生活中,只要稍加留意,我们不难发现二氧化碳的身影,它与人类的生产、生活密不可分。
思考
实验室里如何制取二氧化碳呢?
一、实验室制取二氧化碳
1.反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑
实验室常用大理石(或石灰石)与稀盐酸反应制取二氧化碳。
CaCO3 + 2HCl == CaCl2 + H2CO3
H2CO3 == H2O + CO2↑
碳酸不稳定,易分解
CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
为什么不用稀硫酸与石灰石反应制取二氧化碳呢?
虽然该反应能生成二氧化碳:
CaCO3+H2SO4===CaSO4 +H2O+CO2↑
但生成的CaSO4微溶于水,覆盖在大理石表面,形成一层薄膜,使石灰石与酸不能接触,反应难以进行。
实验室制取二氧化碳不能用稀硫酸代替稀盐酸
依据: 根据反应物状态、反应条件
气体发生装置
反应物的状态
固体和固体反应
固体和液体反应
液体和液体反应
……
反应条件:是否需要加热、加催化剂等。
2.发生装置的选择
制取O2 制取CO2 原料和状态 是否加热 装置选用 原料和状态 是否加热 装置选用
KMnO4固体 需加热 固体加热
H2O2溶液和MnO2固体 不需加热 固液常温 稀盐酸和大理石
不需加热
固液常温
排水法:不易溶于水,不与水发生反应。
气体收集装置
排空气法
密度比空气大的——向上排空气法
密度比空气小的——向下排空气法
气体收集装置取决于气体的密度和溶解性。
3.收集装置的选择
制取O2 制取CO2 密度与空气比较 是否溶于水 装置选用 密度与空气比较 是否溶于水 装置选用
大于空气 不易溶于水 向上排空气或排水法
大于空气
易溶于水
向上排空气法
实验装置
CaCO3+2HCl=CaCl2+H2O+CO2↑
1
2
实验步骤
①检验气密性——②加入药品——③收集气体——④进行验满——⑤检验气体
1.如何检验该发生装置的气密性?
发生装置
收集装置
2.如何检验二氧化碳是否收集满?
微热法
方法:
用手握住试管,导管末端产生气泡。松开手一段时间后,导管末端上升一段水柱,一段时间不下降说明气密性良好。
方法:
将燃着的木条放在集气瓶口,若木条熄灭,则CO2已满。
验满
注意事项:
长颈漏斗下端应浸入液面以下
导管应刚露出橡皮塞即可
以利于气体的导出
导管应伸入集气瓶底部
防止气体从长颈漏斗逸出
有利于排尽集气瓶内的空气
距今10000 年到270年间,大气中的二氧化碳浓度维持在相对稳定的水平。18 世纪工业革命之后,随着大规模砍伐森林、化石燃料的燃烧量急剧增加,海洋和陆地生物圈不能完全吸收排放出的二氧化碳,导致大气中二氧化碳浓度不断增加,自然界中碳循环的平衡被打破,对人类生存环境产生了不利影响。
为加强对气候变化威胁的应对,《联合国气候变化框架公约》近200个缔约方于2015年12 月达成《巴黎协定》,提出把全球平均气温较工业化前水平升高制在 2℃之内,并为把升温控制在1.5℃之内而努力。
二、实现“双碳”目标的路径
通过植树造林、节能减排等形式,抵消自身产生的二氧化碳或温室气体排放量,实现正负抵消,达到相对“零排放”。
某一个时刻,二氧化碳排放量达到历史最高值,之后逐步回落。
碳达峰
碳中和
为体现中国在应对气候变化问题上的大国担当,我国宣布提高国家自主贡献力度,二氧化碳排放力争于2030年前达到峰值,努力争取 2060 年前实现碳中和。
近 年 来
积极布局碳中和
积极参与国际社会碳减排
顺应绿色低碳发展潮流
中国共产党第二十次全国代表大会报告中指出:“实现碳达峰碳中和是一场广泛而深刻的经济社会系统性变革,立足我国能源资源禀赋,坚持先立后破,有计划分步骤实施碳达峰行动。完善能源消耗总量和强度调控,重点控制化石能源消费,逐步转向碳排放总量和强度‘双控’制度。推动能源清洁低碳高效利用,推进工业、建筑、交通等领域清洁低碳转型。”
发展数字产业
高新技术产业
控制化石能源
现代服务业
植 树 造 林
循 环 利 用
碳中和目标的实现和我们每个个体都息息相关。每个人都应该为碳中和、碳减排贡献自己的力量。
步 行
节 水
节 电
减 少 浪 费
拼 车 出 行
公 共 交 通
种 一 棵 树
随手关闭电脑
自备购物袋
实现“双碳”目标中化学科学的新使命
全世界科学家高度关注二氧化碳的转化和综合利用,尝试运用化学原理和方法,积极研究如何使二氧化碳资源化,以促进自然界中碳的循环;寻求低成本的捕集方法,把二氧化碳转变为燃料,从而使二氧化碳在促进人类可持续发展中发挥更大的作用。
CO2 + 3H2
CH3OH + H2O
催化剂
1.鉴别空气、氧气和二氧化碳三种气体,简便可行的方法是
A.观察气体的颜色、气味
B.将气体分别通入澄清石灰水中
C.将燃着的小木条分别插入气体中
D.通过实验比较三种气体的溶解性
C
2.制备二氧化碳的下列装置图中哪个装置中既有错误,也不能“即开即用,随关随停” ( )
A. B. C. D.
A
3.碳中和的实现途径不包括( )
A.加大可再生能源的开发和利用
B.增加森林砍伐以扩大城市建设用地
C.改进生产工艺,提高能源利用效率
D.推广新能源汽车,减少燃油消耗
B
二氧化碳制取的研究
药品:石灰石(大理石)和稀盐酸
反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑
检验:通入澄清石灰水,石灰水变浑浊。
发生装置:固液不加热型
收集装置:向上排空气法
装置的确定
验满:将燃着的木条放在瓶口,熄灭则已满。
“双碳目标”
碳达峰——碳排放的最高点
碳中和——碳排放与吸收达到平衡
从源头控制碳排放
措施
加大力度促进二氧化碳的吸收和转化
同课章节目录
