陕西省咸阳市武功县2024-2025学年高一上学期期中考试化学试题(无答案)
文档属性
| 名称 | 陕西省咸阳市武功县2024-2025学年高一上学期期中考试化学试题(无答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 402.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-11-13 14:07:53 | ||
图片预览

文档简介
2024 2025学年度期中考试卷
高一化学
考试模块:必修第一册
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版必修第一册第一章~第二章。
5.可能用到的相对原子质量:H1 C12 N14 O16 Na23 Cl35.5
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.生活处处充满化学,下列过程属于化学变化的是( )
A.乒乓球球拍被踩断 B.神舟十八点火升空
C.安装太阳能电池板 D.清晨升旗献唱国歌
2.胶体区别于其他分散系的本质特征是( )
A.分散质粒子直径为 B.胶体能产生丁达尔效应
C.胶体的分散质能通过滤纸空隙 D.胶体在一定条件下能稳定存在
3.下列说法正确的是( )
A.物质的量就是一定体积的物质的质量
B.阿伏加德罗常数就是
C.钠的摩尔质量等于它的相对原子质量
D.在标准状况下,任何气体的体积都约为
4.有关物质之间的部分转化关系如图所示(物质中不含钙元素),其中“—”表示物质之间能发生化学反应,“→”表示物质之间的转化关系。下列说法中正确的是( )
A.物质是一种常见的酸性氧化物
B.反应①~⑥中涉及氧化还原反应
C.图中涉及的物质均为电解质
D.的电离方程式:
5.在汽车尾气处理装置中发生反应:。下列有关该反应的说法中正确的是( )
A.是氧化剂 B.被还原
C.发生还原反应 D.是氧化产物
6.在、、形成的混合溶液中,,,,则为( )
A. B. C. D.
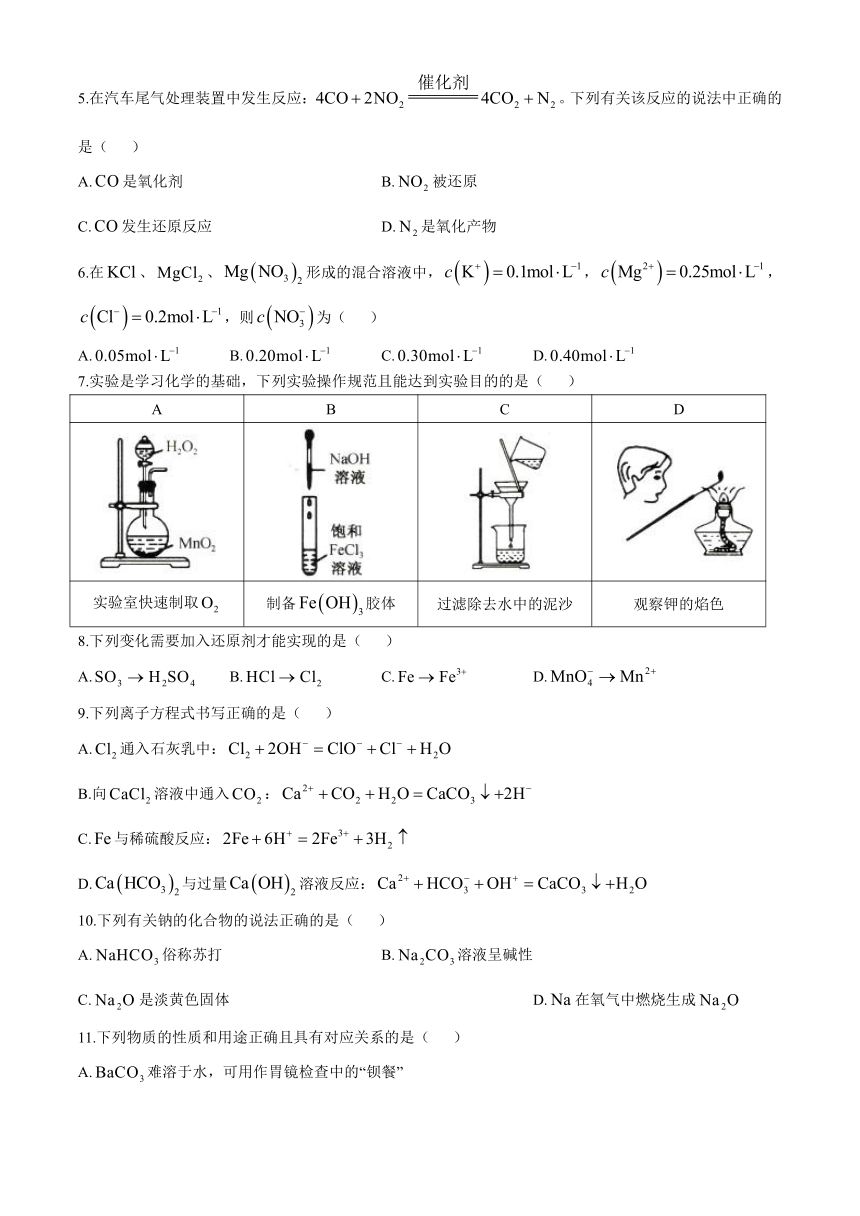
7.实验是学习化学的基础,下列实验操作规范且能达到实验目的的是( )
A B C D
实验室快速制取 制备胶体 过滤除去水中的泥沙 观察钾的焰色
8.下列变化需要加入还原剂才能实现的是( )
A. B. C. D.
9.下列离子方程式书写正确的是( )
A.通入石灰乳中:
B.向溶液中通入:
C.与稀硫酸反应:
D.与过量溶液反应:
10.下列有关钠的化合物的说法正确的是( )
A.俗称苏打 B.溶液呈碱性
C.是淡黄色固体 D.在氧气中燃烧生成
11.下列物质的性质和用途正确且具有对应关系的是( )
A.难溶于水,可用作胃镜检查中的“钡餐”
B.金属具有良好的导热性,可用作高压钠灯
C.能与盐酸反应,可用于治疗胃酸过多症
D.氩气常温下为无色气体,可用作冶炼金属保护气
12.下列物质提纯(括号内的物质是杂质),所选用的除杂试剂或方法正确的是( )
选项 物质 除杂试剂或方法
A () 、点燃
B 铁粉(铜粉) 溶液
C () 饱和溶液
D () 加热
13.配制一定物质的量浓度的溶液,下列操作正确的是( )
A.称量时,应将固体放在称量纸上称量
B.将称量的固体置于小烧杯中溶解,待溶液恢复至室温再转移
C.定容时若加水超过了刻度线,可用胶头滴管直接将多余溶液吸出
D.为减小误差,必须使用更精确的容量瓶配制
14.侯氏制碱法的第一步反应为。用表示阿伏加德罗常数的值,下列说法正确的是( )
A.含有的分子数为
B.中含有的氢原子数为
C.固体中含有的数目为
D.标准状况下,含有的分子数为
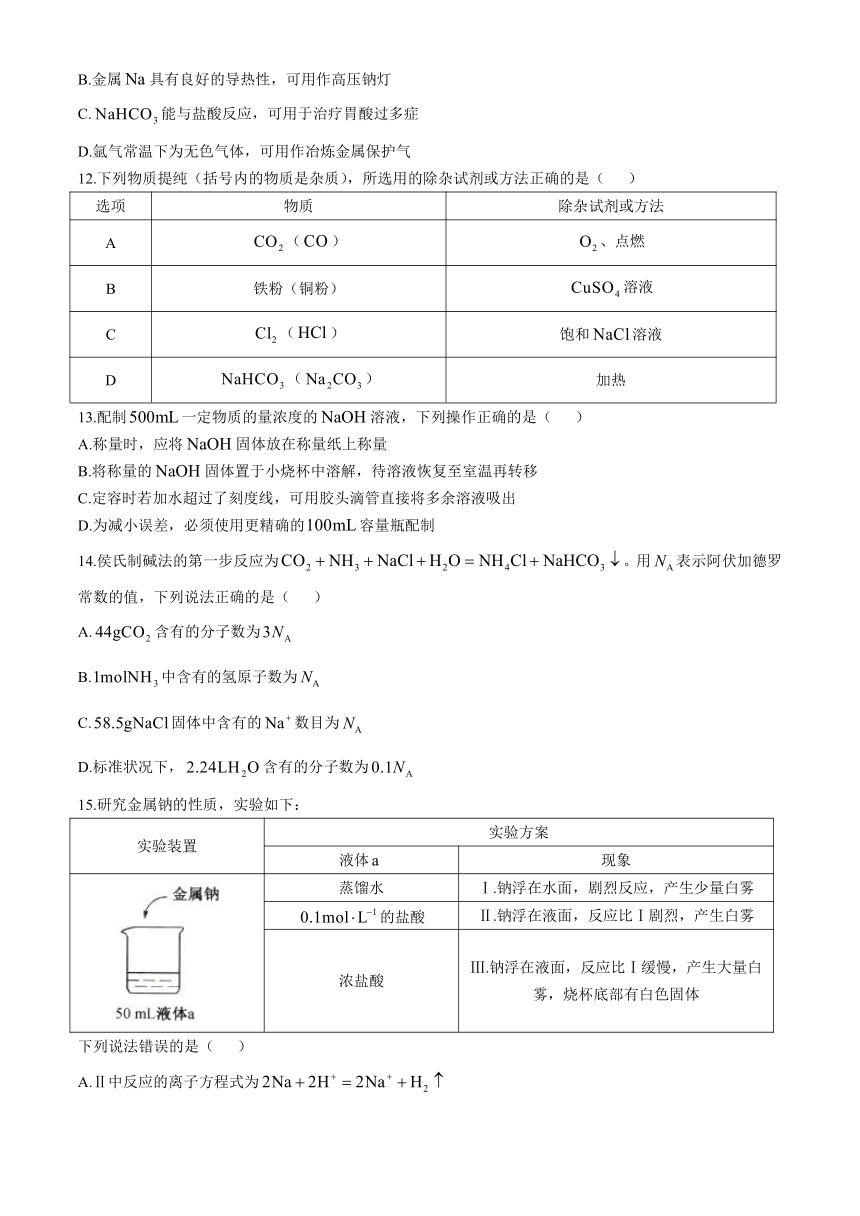
15.研究金属钠的性质,实验如下:
实验装置 实验方案
液体 现象
蒸馏水 Ⅰ.钠浮在水面,剧烈反应,产生少量白雾
的盐酸 Ⅱ.钠浮在液面,反应比Ⅰ剧烈,产生白雾
浓盐酸 Ⅲ.钠浮在液面,反应比Ⅰ缓慢,产生大量白雾,烧杯底部有白色固体
下列说法错误的是( )
A.Ⅱ中反应的离子方程式为
B.对比Ⅰ、Ⅱ、Ⅲ可知,随着增大,反应的剧烈程度增大
C.实验Ⅰ、Ⅱ、Ⅲ均有白雾产生,说明与水或酸反应均放出大量热
D.推测Ⅲ中白色固体为,白雾为盐酸小液滴
二、非选择题:本题共4小题,共55分。
16.(14分)①硫酸钠是一种无机化合物,难溶于②乙醇,能溶于③水,用途非常广泛。硫酸钠的制备方法很多,例如可由④或⑤与⑥在溶液中反应制得,也可由⑦溶液与⑧溶液反应制得,除了生成外,还生成⑨、⑩。回答下列问题:
(1)上述标有序号的物质中属于电解质的是______(填序号,下同),属于盐的是______。
(2)①在水中的电离方程式为________________________。
(3)将少量⑩通入④的溶液中反应的化学方程式为______________________________;向⑨中滴加少量⑥的稀溶液,发生反应的离子方程式为______________________________。
(4)将少量④加入⑧中,产生的实验现象为______________________________。
(5)中学学过的电解水实验中,通常会在水中加入少量①,目的是______________________________,写出该反应的化学方程式并用双线桥标出电子转移的方向和数目:______________________________。
17.(14分)工业上氯及其化合物的用途非常广泛。回答下列问题:
(1)实验室利用与浓盐酸制取氯气的化学方程式为________________________。
(2)下表是研究氯水性质实验的部分活动记录。
实验内容 实验现象 解释原因(文字或反应)
观察氯水颜色 ①______ 氯水中含有氯气分子
向氯水中滴入溶液 有无色气体生成 ②______(写离子方程式)
用玻璃棒蘸取氯水,点在品红试纸上 红色褪去 ③______
(3)“价-类”二维图是研究元素的重要方法,如图为氯及其化合物的“价-类”二维图。
①二维图缺失的类别是______;的化学式为______;的焰色试验呈紫色,则为______(填化学式)。②是______(填“酸性”或“碱性”)氧化物。
③“84”消毒液露置于空气中,其有效成分在空气中的作用下生成两种物质,其中一种是,另一种是酸式盐,写出该反应的化学方程式:________________________。
(4)如图是用强光照射密闭广口瓶中新制氯水时,用数字化传感器采集的图像,下列纵坐标()代表的物理量与图像相符的是______(填字母)。
a.溶液颜色的变化 b.瓶中氧气的体积分数
c.溶液的导电能力 d.溶液的漂白能力
18.(14分)某溶液可能大量含有、、、、、、中的若干种,取适量溶液进行实验。回答下列问题:
(1)气体1的化学式为______。经过第一步操作推断原溶液中一定含有的离子为______。
(2)生成白色沉淀1的离子方程式为__________________________________________。
(3)某同学根据生成白色沉淀2推断原溶液中一定含有,该同学的结论______(填“正确”或“错误”),判断的理由:________________________。
(4)实验中使用的盐酸是的溶液,该溶液是利用浓盐酸稀释而成,浓盐酸的标签如图所示。
盐酸 分子式: 相对分子质量: 密度: 的质量分数:
①若要配制溶液,需用量筒量取______浓盐酸。
②下列操作的正确顺序是______(用字母与箭头表示)。
A.上下颠倒摇匀;B.量取;C.洗涤;D.定容;E.稀释;F.移液;G.装瓶
③进行配制操作时,下列仪器中不需要用到的是______(填字母,下同)。
④下列操作会使所配溶液浓度偏低的是______。
a.配制前,容量瓶中有少量蒸馏水
b.量取盐酸读数时,仰视刻度线
c.量取盐酸后,洗涤量筒倒入烧杯中
d.向容量瓶中转移溶液时,不慎有液滴洒在容量瓶外面
19.(13分)置于空气中容易变质,某化学兴趣小组设计如图所示实验装置计算已变质的(含)纯度(为弹性良好的气囊,夹持装置已省略)。回答下列问题:
(1)仪器的名称为______,橡胶管的作用为______________________________。
(2)在气囊中,与稀反应的化学方程式为____________________________________。
(3)称取样品进行实验,实验前关闭,打开,打开仪器的旋塞,气囊膨胀,用排水量气法测定反应生成的气体体积(已转化为标准状况下,下同);再次称取样品进行实验。关闭,缓缓打开、及仪器的旋塞,量筒Ⅱ中收集的气体为____________(填化学式),读取量筒Ⅱ中体积。样品中的质量分数为______(用含、的式子表示)。
(4)广口瓶中煤油的作用为_______________________。
(5)若只进行第一次实验,只读取量筒Ⅰ中体积,______(填“能”或“不能”)计算出的质量分数。
高一化学
考试模块:必修第一册
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版必修第一册第一章~第二章。
5.可能用到的相对原子质量:H1 C12 N14 O16 Na23 Cl35.5
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.生活处处充满化学,下列过程属于化学变化的是( )
A.乒乓球球拍被踩断 B.神舟十八点火升空
C.安装太阳能电池板 D.清晨升旗献唱国歌
2.胶体区别于其他分散系的本质特征是( )
A.分散质粒子直径为 B.胶体能产生丁达尔效应
C.胶体的分散质能通过滤纸空隙 D.胶体在一定条件下能稳定存在
3.下列说法正确的是( )
A.物质的量就是一定体积的物质的质量
B.阿伏加德罗常数就是
C.钠的摩尔质量等于它的相对原子质量
D.在标准状况下,任何气体的体积都约为
4.有关物质之间的部分转化关系如图所示(物质中不含钙元素),其中“—”表示物质之间能发生化学反应,“→”表示物质之间的转化关系。下列说法中正确的是( )
A.物质是一种常见的酸性氧化物
B.反应①~⑥中涉及氧化还原反应
C.图中涉及的物质均为电解质
D.的电离方程式:
5.在汽车尾气处理装置中发生反应:。下列有关该反应的说法中正确的是( )
A.是氧化剂 B.被还原
C.发生还原反应 D.是氧化产物
6.在、、形成的混合溶液中,,,,则为( )
A. B. C. D.
7.实验是学习化学的基础,下列实验操作规范且能达到实验目的的是( )
A B C D
实验室快速制取 制备胶体 过滤除去水中的泥沙 观察钾的焰色
8.下列变化需要加入还原剂才能实现的是( )
A. B. C. D.
9.下列离子方程式书写正确的是( )
A.通入石灰乳中:
B.向溶液中通入:
C.与稀硫酸反应:
D.与过量溶液反应:
10.下列有关钠的化合物的说法正确的是( )
A.俗称苏打 B.溶液呈碱性
C.是淡黄色固体 D.在氧气中燃烧生成
11.下列物质的性质和用途正确且具有对应关系的是( )
A.难溶于水,可用作胃镜检查中的“钡餐”
B.金属具有良好的导热性,可用作高压钠灯
C.能与盐酸反应,可用于治疗胃酸过多症
D.氩气常温下为无色气体,可用作冶炼金属保护气
12.下列物质提纯(括号内的物质是杂质),所选用的除杂试剂或方法正确的是( )
选项 物质 除杂试剂或方法
A () 、点燃
B 铁粉(铜粉) 溶液
C () 饱和溶液
D () 加热
13.配制一定物质的量浓度的溶液,下列操作正确的是( )
A.称量时,应将固体放在称量纸上称量
B.将称量的固体置于小烧杯中溶解,待溶液恢复至室温再转移
C.定容时若加水超过了刻度线,可用胶头滴管直接将多余溶液吸出
D.为减小误差,必须使用更精确的容量瓶配制
14.侯氏制碱法的第一步反应为。用表示阿伏加德罗常数的值,下列说法正确的是( )
A.含有的分子数为
B.中含有的氢原子数为
C.固体中含有的数目为
D.标准状况下,含有的分子数为
15.研究金属钠的性质,实验如下:
实验装置 实验方案
液体 现象
蒸馏水 Ⅰ.钠浮在水面,剧烈反应,产生少量白雾
的盐酸 Ⅱ.钠浮在液面,反应比Ⅰ剧烈,产生白雾
浓盐酸 Ⅲ.钠浮在液面,反应比Ⅰ缓慢,产生大量白雾,烧杯底部有白色固体
下列说法错误的是( )
A.Ⅱ中反应的离子方程式为
B.对比Ⅰ、Ⅱ、Ⅲ可知,随着增大,反应的剧烈程度增大
C.实验Ⅰ、Ⅱ、Ⅲ均有白雾产生,说明与水或酸反应均放出大量热
D.推测Ⅲ中白色固体为,白雾为盐酸小液滴
二、非选择题:本题共4小题,共55分。
16.(14分)①硫酸钠是一种无机化合物,难溶于②乙醇,能溶于③水,用途非常广泛。硫酸钠的制备方法很多,例如可由④或⑤与⑥在溶液中反应制得,也可由⑦溶液与⑧溶液反应制得,除了生成外,还生成⑨、⑩。回答下列问题:
(1)上述标有序号的物质中属于电解质的是______(填序号,下同),属于盐的是______。
(2)①在水中的电离方程式为________________________。
(3)将少量⑩通入④的溶液中反应的化学方程式为______________________________;向⑨中滴加少量⑥的稀溶液,发生反应的离子方程式为______________________________。
(4)将少量④加入⑧中,产生的实验现象为______________________________。
(5)中学学过的电解水实验中,通常会在水中加入少量①,目的是______________________________,写出该反应的化学方程式并用双线桥标出电子转移的方向和数目:______________________________。
17.(14分)工业上氯及其化合物的用途非常广泛。回答下列问题:
(1)实验室利用与浓盐酸制取氯气的化学方程式为________________________。
(2)下表是研究氯水性质实验的部分活动记录。
实验内容 实验现象 解释原因(文字或反应)
观察氯水颜色 ①______ 氯水中含有氯气分子
向氯水中滴入溶液 有无色气体生成 ②______(写离子方程式)
用玻璃棒蘸取氯水,点在品红试纸上 红色褪去 ③______
(3)“价-类”二维图是研究元素的重要方法,如图为氯及其化合物的“价-类”二维图。
①二维图缺失的类别是______;的化学式为______;的焰色试验呈紫色,则为______(填化学式)。②是______(填“酸性”或“碱性”)氧化物。
③“84”消毒液露置于空气中,其有效成分在空气中的作用下生成两种物质,其中一种是,另一种是酸式盐,写出该反应的化学方程式:________________________。
(4)如图是用强光照射密闭广口瓶中新制氯水时,用数字化传感器采集的图像,下列纵坐标()代表的物理量与图像相符的是______(填字母)。
a.溶液颜色的变化 b.瓶中氧气的体积分数
c.溶液的导电能力 d.溶液的漂白能力
18.(14分)某溶液可能大量含有、、、、、、中的若干种,取适量溶液进行实验。回答下列问题:
(1)气体1的化学式为______。经过第一步操作推断原溶液中一定含有的离子为______。
(2)生成白色沉淀1的离子方程式为__________________________________________。
(3)某同学根据生成白色沉淀2推断原溶液中一定含有,该同学的结论______(填“正确”或“错误”),判断的理由:________________________。
(4)实验中使用的盐酸是的溶液,该溶液是利用浓盐酸稀释而成,浓盐酸的标签如图所示。
盐酸 分子式: 相对分子质量: 密度: 的质量分数:
①若要配制溶液,需用量筒量取______浓盐酸。
②下列操作的正确顺序是______(用字母与箭头表示)。
A.上下颠倒摇匀;B.量取;C.洗涤;D.定容;E.稀释;F.移液;G.装瓶
③进行配制操作时,下列仪器中不需要用到的是______(填字母,下同)。
④下列操作会使所配溶液浓度偏低的是______。
a.配制前,容量瓶中有少量蒸馏水
b.量取盐酸读数时,仰视刻度线
c.量取盐酸后,洗涤量筒倒入烧杯中
d.向容量瓶中转移溶液时,不慎有液滴洒在容量瓶外面
19.(13分)置于空气中容易变质,某化学兴趣小组设计如图所示实验装置计算已变质的(含)纯度(为弹性良好的气囊,夹持装置已省略)。回答下列问题:
(1)仪器的名称为______,橡胶管的作用为______________________________。
(2)在气囊中,与稀反应的化学方程式为____________________________________。
(3)称取样品进行实验,实验前关闭,打开,打开仪器的旋塞,气囊膨胀,用排水量气法测定反应生成的气体体积(已转化为标准状况下,下同);再次称取样品进行实验。关闭,缓缓打开、及仪器的旋塞,量筒Ⅱ中收集的气体为____________(填化学式),读取量筒Ⅱ中体积。样品中的质量分数为______(用含、的式子表示)。
(4)广口瓶中煤油的作用为_______________________。
(5)若只进行第一次实验,只读取量筒Ⅰ中体积,______(填“能”或“不能”)计算出的质量分数。
同课章节目录
