辽宁省丹东市东港市2024-2025学年九年级上学期期中教学质量监测化学试卷(含解析)
文档属性
| 名称 | 辽宁省丹东市东港市2024-2025学年九年级上学期期中教学质量监测化学试卷(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-11-14 00:00:00 | ||
图片预览




文档简介
辽宁省丹东市东港市2024-2025学年九年级上学期期中教学质量监测化学试卷
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.《开学第一课》提到武夷山的生态茶园,创造性提出了“茶豆油菜套作”的绿色生态模式,以下关于绿茶制作中涉及化学变化的是( )
A.自然晾晒,去除露水 B.高温,破坏酶的活性
C.通过外力作用将叶片揉碎 D.蒸发水分并整理外形
2.空气是一种宝贵的资源,下列气体不是来自空气的是( )
A. B. C. D.
3.下列有关化学用语的书写,正确的是( )
①硅元素——Si
②氮原子——He
③——氧原子
④铜——
⑤水分子——
⑥——氯离子
A.①②⑥ B.①③④ C.②④⑧ D.①⑤⑥
4.春天走近花园,花香扑鼻而来,用分子的观点解释正确的是( )
A.分子很小 B.分子不断运动
C.不同分子,性质不同 D.分子间有间隔
5.习近平总书记提出:“人不负青山,青山定不负人”。下列做法中符合这一理念的是( )
A.开发和使用清洁能源 B.工业废水集中直接排入海洋
C.所有垃圾集中焚烧处理 D.大量施用农药和化肥
6.科学家发现在负压和超低温条件下,水会像棉花糖一样,以蓬松轻盈的形式稳定存在,被称为“气凝胶冰”。下列说法正确的是( )
A.“气凝胶冰”是混合物 B.“气凝胶冰”与水的化学性质相同
C.“气凝胶冰”与冰的密度相同 D.结成“气凝胶冰”后,分子停止运动
7.亚硫酸钠()在造纸行业中广泛应用,下列关于亚硫酸钠的说法正确的是( )
A.属于氧化物 B.由钠、硫、氧三种原子构成
C.硫元素的质量分数最小 D.钠元素与氧元素的质量比为2:3
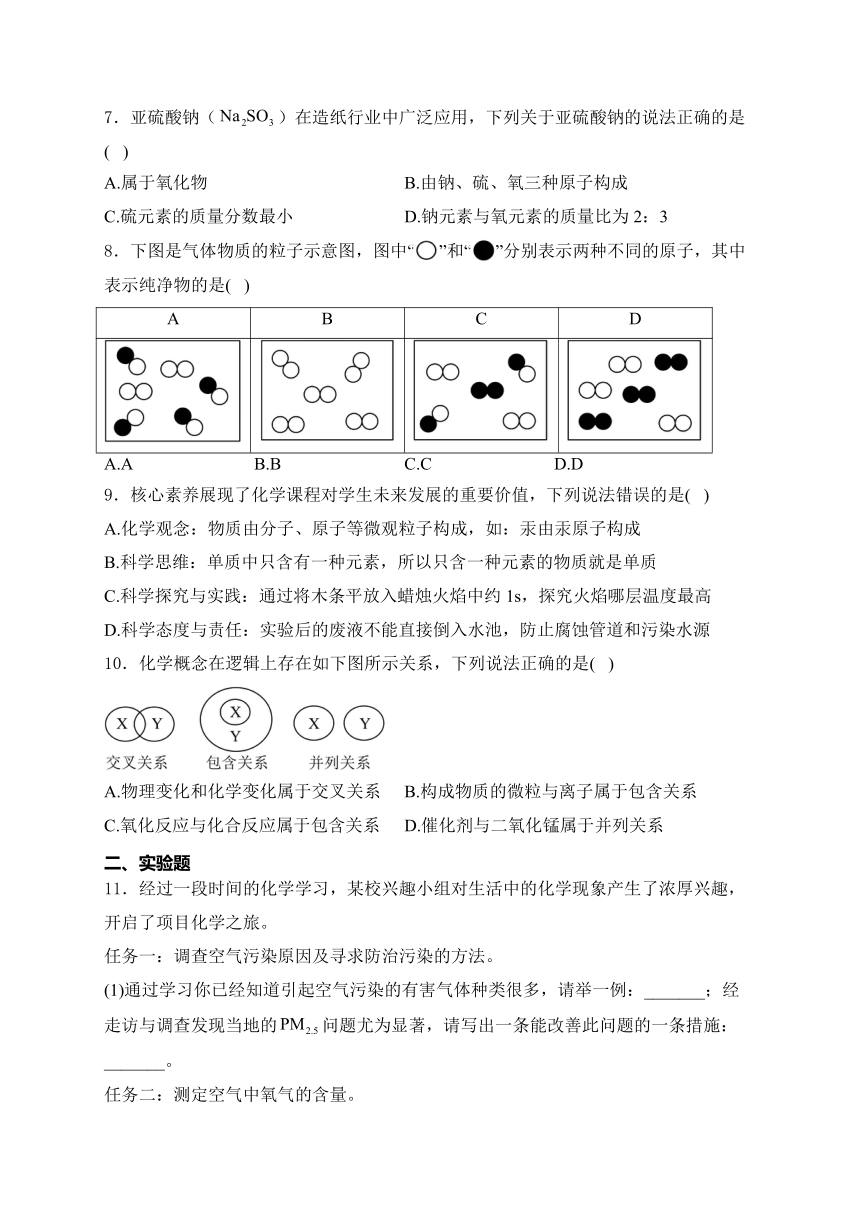
8.下图是气体物质的粒子示意图,图中“”和“”分别表示两种不同的原子,其中表示纯净物的是( )
A B C D
A.A B.B C.C D.D
9.核心素养展现了化学课程对学生未来发展的重要价值,下列说法错误的是( )
A.化学观念:物质由分子、原子等微观粒子构成,如:汞由汞原子构成
B.科学思维:单质中只含有一种元素,所以只含一种元素的物质就是单质
C.科学探究与实践:通过将木条平放入蜡烛火焰中约1s,探究火焰哪层温度最高
D.科学态度与责任:实验后的废液不能直接倒入水池,防止腐蚀管道和污染水源
10.化学概念在逻辑上存在如下图所示关系,下列说法正确的是( )
A.物理变化和化学变化属于交叉关系 B.构成物质的微粒与离子属于包含关系
C.氧化反应与化合反应属于包含关系 D.催化剂与二氧化锰属于并列关系
二、实验题
11.经过一段时间的化学学习,某校兴趣小组对生活中的化学现象产生了浓厚兴趣,开启了项目化学之旅。
任务一:调查空气污染原因及寻求防治污染的方法。
(1)通过学习你已经知道引起空气污染的有害气体种类很多,请举一例:_______;经走访与调查发现当地的问题尤为显著,请写出一条能改善此问题的一条措施:_______。
任务二:测定空气中氧气的含量。
(2)实验室常用红磷燃烧的方法测定空气中氧气的含量(如图甲所示),写出该反应的文字表达式_______。若用木炭代替红磷进行对比实验,集气瓶内压强变化趋势与图乙_______(填“一致”或“不一致”),D点后压强不再减少,说明氧气体积约占空气体积的_______。(写分数)
任务三:野外饮用水的获取
场景1:位于深山峡谷之中,只有浑浊的江水可用。
场景2:位于孤悬海岛之上,只有海水可用。
(3)在两种场景中,将这里水转换成饮用水主要方法是否相同_______(填“相同”、“不相同”),原因是_______。
任务四:比较不同水样的硬度
【进行实验】用四种水样完成实验,记录观察到泡沫产生时所需肥皂水的用量。
实验操作 水样 肥皂水用量/滴
市售纯净水 2
煮沸后的自来水 6
自来水 9
湖水 14
【解释与结论】
(4)硬度最大的水样是_______。
(5)继续实验,发现山泉水的硬度大于自来水的硬度,其实验方案为_______。
12.完成以下基础实验与学科实践内容
(1)性质检验
操作 现象 结论
铁丝燃烧时,观察到的现象是______ 能支持燃烧
集气瓶中水的作用是_______
(2)探究实验室制取氧气反应速率
Ⅰ.某化学兴趣小组进行不同催化剂对过氧化氢分解速率的影响,设计的方案和记录数据如下表所示:
实验序号 过氧化氢溶液体积、浓度 催化剂 收集50mL所用时间
① 30mL4% 无 ﹥200s
② 30mL4% 0.2g粉末 15s
③ 30mL4% ag粉末 34s
④ 30mL4% 0.2g粉末 27s
①表格中a的值为_______。
②实验②中制取氧气的符号表达式为_______。
③结论:通过上述实验对比,可得出的实验结论是_______。
Ⅱ.化学兴趣小组借助数字化实验手段用装置A探究其他条件对过氧化氢分解速率的影响,选用0.2g粉末作催化剂分组进行实验,通过压强传感器得到的数据如图所示。
分析图中实验1,溶液的浓度越大(即),反应速率_______(选填“越快”、“越慢”或“不影响”);分析图中实验2所示数据,你认为影响该反应速率的条件是_______。
(3)探究制氧机的原理
查阅资料:过氧化氢和过碳酸钠都可以产生氧气。
小组同学取上述两种药品分别加入0.2g二氧化锰进行对比实验,比较过氧化氢溶液和过碳酸钠制取氧气的效率。测得数据如图1(20min后几乎不产生氧气)请分析制氧剂选择过碳酸钠的依据是_______。
化学制氧机内缸如图2,为保证制氧的效果稳定,制氧机反应仓的加水量在夏季比冬季的高,原因是_______。
三、填空题
13.钛在航空航天,医疗器械等工业领域有着重要用途,生产钛的方法之一是利用四氯化钛与镁的反应。镁元素和钛元素在元素周期表中相关信息如图所示。
(1)镁元素的原子序数为_______,钛元素的相对原子质量为_______;
①镁元素和钛元素属于_______(填“金属”或“非金属”)元素。
②从物质的元素组成角度看,与镁、钛、氧气属于同一类别的是_______(填字母)。
A.空气 B.氧化镁 C.二氧化锰 D.铁
(2)下列原子结构示意图中,与镁原子的化学性质最相似的是______(填字母)。
A. B. C. D.
(3)钛元素能形成多种化合物,如、。请问
①钛有多种化合价,读作_______;
②中,钛元素的化合价是_______;
③从物质分类角度看,属于_______(填字母)。
A.混合物
B.氧化物
C.单质
D.化合物
E.纯净物
(4)一定条件下,四氯化钛与金属镁发生反应可获得金属钛,同时生成氯化镁。该反应的文字表达式为_______。
14.下面是实验室制取气体的几种发生装置和收集装置。请回答下列问题:
(1)仪器名称①_______。
(2)实验室用双氧水和二氧化锰制取并收集较纯净的氧气,应选装置_______(填字母)。
(3)实验室用装置A制取氧气的反应的文字表达式:_______,试管口放一团棉花的目的是_______。
(4)某同学设计图C装置,该装置与B相比优点是_______。
(5)利用G装置收集氧气,验满时将带火星的木条放在_______(填“a”或“b”)处。
(6)实验室常用醋酸钠固体和碱石灰固体混合加热制备甲烷气体,发生装置应选用_______,已知甲烷是一种密度比空气小、难溶于水的气体,这是甲烷的_______(选填“物理”或“化学”)性质,如从DEF装置中选择收集装置,可以选择_______。
参考答案
1.答案:B
解析:A、自然晾晒,去除露水,只是水的状态的改变,无新物质生成,属于物理变化;B、高温,破坏酶的活性,发生了蛋白质变性,有新物质生成,属于化学变化;C、通过外力作用将叶片揉碎,只是形状的改变,无新物质生成,属于物理变化;D、蒸发水分并整理外形,只是水的状态和形状的改变,无新物质生成,属于物理变化。故选B。
2.答案:A
解析:A、空气中不含氢气,氢气不是来自于空气。符合题意。B、氮气占空气体积的78%,氮气来自于空气。不符合题意。C、氧气占空气体积的21%,氧气来自于空气。不符合题意。D、氦气属于稀有气体,稀有气体占空气体积的0.94%,氦气来自于空气。不符合题意。故选A。
3.答案:D
解析:①硅元素的元素符号为Si,选项正确;②元素符号从微观上表示1个原子,则氮原子的符号为N,选项错误;③元素符号从微观上表示1个原子,则氧原子的符号为O,选项错误;④铜的符号为Cu,选项错误;⑤1个水分子由2个氢原子与1个氧原子构成,则水分子的符号为,选项正确;⑥数字而离子符号时,先写出相应的元素符号,然后在元素符号的右上角先写出离子所带电荷的数目,再写出电荷的电性,电荷数为1时省略不写,1个氯离子带1个单位的负电荷,则氯离子的符号为,选项正确,即正确选项为①⑤⑥,故选D。
4.答案:B
解析:花香的飘散微观上属于分子运动的现象,故选择B项。
5.答案:A
解析:A、开发和使用清洁能源可以减少有害气体和二氧化碳的排放,有利于环境保护,故A符合题意;B、工业废水集中直接排入海洋会对海洋的生态环境造成危害,不利于环境保护,故B不符合题意;C、所有垃圾集中焚烧处理会产生大量的有害气体污染空气,不利于环境保护,故C不符合题意;D、大量施用农药和化肥会造成土壤污染和水体污染,不利于环境保护,故D不符合题意。故选:A。
6.答案:B
解析:A、“气凝胶冰”中只含一种物质水,属于纯净物,故A错误;B、“气凝胶冰”与冰都是由水分子构成的,所以化学性质相同,故B正确;C、“气凝胶冰”是指水会像棉花糖一样,以蓬松轻盈的形式稳定存在,而冰是结构紧密的固体,二者密度不相同,故C错误;D、分子总是在不断运动的,故D错误。故选:B
7.答案:C
解析:A、氧化物是由两种元素组成的化合物,且一种元素为氧元素,亚硫酸钠是由钠、硫、氧三种元素组成,不属于氧化物,选项A错误;B、亚硫酸钠是由亚硫酸钠分子构成,亚硫酸钠分子由氢、硫、氧三种原子构成,选项B错误;C、亚硫酸钠中钠、硫、氧三种元素的质量比为(23×2):(32×1):(16×3)=23:16:24,所以硫元素的质量分数最小,选项C正确;D、亚硫酸钠中钠、氧两种元素的质量比为(23×2):(16×3)=23:24,选项D错误。故选:C。
8.答案:B
解析:A、图中由两种分子,表示混合物,选项错误;B、图中有一种分子,属于纯净物,选项正确;C、图中有三种分子,属于混合物,选项错误;D、图中有两种分子,属于混合物,选项错误,故选B。
9.答案:B
解析:A、物质是由分子、原子、离子构成,汞是由汞原子构成,该选项说法正确;B、单质是只有一种元素组成的纯净物,则只含一种元素的物质不一定为单质,还可能为混合物,该选项说法不正确;C、将木条平放入蜡烛火焰中约1s,根据木条的炭化情况,可探究火焰哪层温度最高,该选项说法正确;D、实验室的废液不能直接倾倒,否则会腐蚀管道和污染水源,该选项说法正确。故选B。
10.答案:B
解析:A、物理变化无新物质生成,化学变化有新物质生成,两者属于并列关系,故A说法错误;B、分子、原子和离子都是构成物质的微粒,构成物质的微粒与离子属于包含关系,故B说法正确;C、氧化反应是物质与氧的反应,化合反应指的是由两种或两种以上的物质反应生成一种新物质的反应,有的氧化反应是化合反应,如木炭燃烧生成二氧化碳,有的氧化反应不是化合反应,如蜡烛燃烧生成二氧化碳和水,两者属于交叉关系,故C说法错误;D、二氧化锰属于催化剂的一种,催化剂与二氧化锰属于包含关系,故D说法错误;故选:B。
11.答案:(1)二氧化氮(合理均可);开发利用新能源,减少化石燃料的使用,减少可吸入颗粒物的排放
(2)磷+氧气五氧化二磷;不一致;
(3)不相同;海水中有氯化钠、氯化镁等可溶性杂质,通过静置、过滤、吸附无法除去钠离子和氯离子(合理均可)
(4)湖水
(5)取相同量山泉水,滴加肥皂水记录产生泡沫所需肥皂水量,大于自来水所需肥皂水量,说明山泉水硬度大于自来水
解析:(1)引起空气污染的有害气体有二氧化硫、二氧化氮等,减少污染问题,可以开发利用新能源,减少化石燃料的使用,减少可吸入颗粒物的排放等,故填:二氧化氮、开发利用新能源,减少化石燃料的使用,减少可吸入颗粒物的排放;
(2)磷与氧气在点燃条件下反应生成五氧化二磷,该反应的文字表达式为:磷+氧气五氧化二磷,若用木炭代替红磷进行对比实验,木炭燃烧生成二氧化碳气体,在消耗氧气的同时会生成二氧化碳气体,故压强变化趋势与图乙不一致,D点后压强不再减小,这是说明剩余气体不和红磷反应,说明氧气体积约占空气体积的,故填:磷+氧气五氧化二磷、不一致、;
(3)江水为淡水,海水为咸水,通过静置、过滤、吸附可以除去江水中的难溶性杂质,但海水中有氯化钠、氯化镁等可溶性杂质,通过静置、过滤、吸附无法除去钠离子和氯离子,故填:不相同、海水中有氯化钠、氯化镁等可溶性杂质,通过静置、过滤、吸附无法除去钠离子和氯离子;
(4)本实验是记录的数据是观察到泡沫产生时所需肥皂水的用量,所以用到肥皂水滴数越多,说明水的硬度越大,所以硬度最大的水样是湖水,故填:湖水;
(5)硬度越大,观察到泡沫产生时所需肥皂水的用量越大,故验证山泉水的硬度大于自来水的硬度的方法:取相同量山泉水和自来水,滴加肥皂水,记录产生泡沫所需肥皂水量,山泉水大于自来水所需肥皂水量,说明山泉水硬度大于自来水,故填:取相同量山泉水,滴加肥皂水记录产生泡沫所需肥皂水量,大于自来水所需肥皂水量,说明山泉水硬度大于自来水。
12.答案:(1)剧烈燃烧,放出热量,火星四射,生成黑色固体;防止高温熔融物溅落,使瓶底炸裂
(2)0.2;;在过氧化氢溶液体积、浓度一定,催化剂质量一定时,二氧化锰的催化效果最好;越快;温度
(3)20分钟以内,过碳酸钠产生的氧气比过氧化氢产生的氧气多;夏天温度高,反应速率快,需要多加水,可以减慢氧气产生的速度
解析:(1)铁丝燃烧时,观察到的现象为:剧烈燃烧,放出热量,火星四射,生成黑色固体;集气瓶中水的作用是防止高温熔融物溅落,使瓶底炸裂;
(2)Ⅰ.①某化学兴趣小组研究的是不同催化剂对过氧化氢分解速率的影响,根据单一变量原则,催化剂可以改变,但质量不能改变,故a为0.2g;
②过氧化氢在二氧化锰的催化下生成水和氧气,故实验②中制取氧气的的符号表达式为:;
③根据表格中数据,收集50mL所用时间最少的是实验②,则在过氧化氢溶液体积、浓度一定,催化剂质量一定时,二氧化锰的催化效果最好;
Ⅱ.根据图中实验1,相同时间内,的浓度越大,产生的气体越多,锥形瓶内压强越大,反应速率越快;图中实验2所示数据,影响该反应速率的条件是温度;
(3)根据图1中测得数据(20min后几乎不产生氧气),制氧剂选择过碳酸钠的依据是:20min内,生成氧气的量比过氧化氢多;
为保证制氧的效果稳定,制氧机反应仓的加水量在夏季比冬季的高,是因为夏季温度高,反应速率快,多加水,可减缓生成氧气的速率。
13.答案:(1)12;47.87;金属;D
(2)D
(3)二氧化钛;+4/+4价;DE
(4)四氯化钛+镁钛+氯化镁
解析:(1)元素信息示意图左上角的数字表示原子序数,根据镁的元素信息示意图,镁元素的原子序数为12;元素信息示意图正下方的数字代表相对原子质量,根据钛的元素信息示意图,钛元素的相对原子质量为47.87;
①镁和钛都是“金字旁”的汉字,因此镁元素和钛元素属于金属元素;
②从物质的元素组成角度看,镁、钛、氧气都是由一种元素组成的纯净物,属于单质。
A、空气含有氮气、氧气、稀有气体等物质,不属于单质;
B、氧化镁是由两种元素组成的纯净物,不属于单质;
C、二氧化锰是由两种元素组成的纯净物,不属于单质;
D、铁是由一种元素组成的纯净物,属于单质。
故选:D。
(2)一般来说,原子的最外层电子数相等,化学性质相似。根据图像,镁原子的最外层电子数为2,没有排满,属于不稳定结构。A、B、C、D四种原子中,只有A和D的最外层电子数为2,其中A原子最外层排满电子,属于稳定结构,D原子最外层没有排满电子,属于不稳定结构,因此与镁原子的化学性质最相似的是D。
(3)①根据“顺写反读”的规则,读作二氧化钛;
②化合物中元素正负化合价之和为零,中,H显+1价,O显-2价,设钛元素的化合价为x,则,解得x=+4;
③混合物含有两种或两种以上物质;氧化物是由两种元素组成的含有氧元素的化合物;单质是由一种元素组成的纯净物;化合物是由两种或两种以上元素组成的纯净物;纯净物只含一种物质。从物质分类角度看,是由3种元素组成的纯净物,属于化合物,不属于混合物或单质或氧化物,故选:DE。
(4)一定条件下,四氯化钛与金属镁发生反应可获得金属钛,同时生成氯化镁,反应的文字表达式为:四氯化钛+镁钛+氯化镁。
14.答案:(1)长颈漏斗
(2)BF
(3)高锰酸钾锰酸钾+二氧化锰+氧气;防止加热时粉末状物质进入导管
(4)可以控制反应速率
(5)b
(6)A;物理;E/F
解析:(1)据图可知,仪器①的名称是长颈漏斗;
(2)用过氧化氢和二氧化锰制取氧气时不需要加热,应该用B装置作为发生装置;因为氧气的密度比空气大,可以用向上排空气法收集,即用E装置收集,氧气不易溶于水,可以用排水法收集,即用F装置收集,用排水法收集的氧气比用排空气法收集的氧气纯净;
(3)A装置为加热固体的装置,试管口有棉花,可选用高锰酸钾制取氧气,高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应的文字表达式为:高锰酸钾锰酸钾+二氧化锰+氧气,试管口还要放一团棉花,目的是:防止加热时粉末状物质进入导管;
(4)C装置中,小注射器能控制液体的滴加速度,从而控制反应速率;
(5)氧气的密度比空气大,用G装置收集氧气从a导管通入,空气从b导管逸出,当从b导管逸出的是氧气时,表示氧气已经收集满,所以验满时,带火星的木条放在b处;
(6)用醋酸钠固体和碱石灰固体混合加热制备甲烷是固体加热型反应,发生装置选择A;甲烷是一种密度比空气小、难溶于水的气体,不需要化学变化就可以表现出来,属于物理性质;甲烷密度比空气小,可选择E向下排空气法收集,难溶于水可使用F排水法收集,
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.《开学第一课》提到武夷山的生态茶园,创造性提出了“茶豆油菜套作”的绿色生态模式,以下关于绿茶制作中涉及化学变化的是( )
A.自然晾晒,去除露水 B.高温,破坏酶的活性
C.通过外力作用将叶片揉碎 D.蒸发水分并整理外形
2.空气是一种宝贵的资源,下列气体不是来自空气的是( )
A. B. C. D.
3.下列有关化学用语的书写,正确的是( )
①硅元素——Si
②氮原子——He
③——氧原子
④铜——
⑤水分子——
⑥——氯离子
A.①②⑥ B.①③④ C.②④⑧ D.①⑤⑥
4.春天走近花园,花香扑鼻而来,用分子的观点解释正确的是( )
A.分子很小 B.分子不断运动
C.不同分子,性质不同 D.分子间有间隔
5.习近平总书记提出:“人不负青山,青山定不负人”。下列做法中符合这一理念的是( )
A.开发和使用清洁能源 B.工业废水集中直接排入海洋
C.所有垃圾集中焚烧处理 D.大量施用农药和化肥
6.科学家发现在负压和超低温条件下,水会像棉花糖一样,以蓬松轻盈的形式稳定存在,被称为“气凝胶冰”。下列说法正确的是( )
A.“气凝胶冰”是混合物 B.“气凝胶冰”与水的化学性质相同
C.“气凝胶冰”与冰的密度相同 D.结成“气凝胶冰”后,分子停止运动
7.亚硫酸钠()在造纸行业中广泛应用,下列关于亚硫酸钠的说法正确的是( )
A.属于氧化物 B.由钠、硫、氧三种原子构成
C.硫元素的质量分数最小 D.钠元素与氧元素的质量比为2:3
8.下图是气体物质的粒子示意图,图中“”和“”分别表示两种不同的原子,其中表示纯净物的是( )
A B C D
A.A B.B C.C D.D
9.核心素养展现了化学课程对学生未来发展的重要价值,下列说法错误的是( )
A.化学观念:物质由分子、原子等微观粒子构成,如:汞由汞原子构成
B.科学思维:单质中只含有一种元素,所以只含一种元素的物质就是单质
C.科学探究与实践:通过将木条平放入蜡烛火焰中约1s,探究火焰哪层温度最高
D.科学态度与责任:实验后的废液不能直接倒入水池,防止腐蚀管道和污染水源
10.化学概念在逻辑上存在如下图所示关系,下列说法正确的是( )
A.物理变化和化学变化属于交叉关系 B.构成物质的微粒与离子属于包含关系
C.氧化反应与化合反应属于包含关系 D.催化剂与二氧化锰属于并列关系
二、实验题
11.经过一段时间的化学学习,某校兴趣小组对生活中的化学现象产生了浓厚兴趣,开启了项目化学之旅。
任务一:调查空气污染原因及寻求防治污染的方法。
(1)通过学习你已经知道引起空气污染的有害气体种类很多,请举一例:_______;经走访与调查发现当地的问题尤为显著,请写出一条能改善此问题的一条措施:_______。
任务二:测定空气中氧气的含量。
(2)实验室常用红磷燃烧的方法测定空气中氧气的含量(如图甲所示),写出该反应的文字表达式_______。若用木炭代替红磷进行对比实验,集气瓶内压强变化趋势与图乙_______(填“一致”或“不一致”),D点后压强不再减少,说明氧气体积约占空气体积的_______。(写分数)
任务三:野外饮用水的获取
场景1:位于深山峡谷之中,只有浑浊的江水可用。
场景2:位于孤悬海岛之上,只有海水可用。
(3)在两种场景中,将这里水转换成饮用水主要方法是否相同_______(填“相同”、“不相同”),原因是_______。
任务四:比较不同水样的硬度
【进行实验】用四种水样完成实验,记录观察到泡沫产生时所需肥皂水的用量。
实验操作 水样 肥皂水用量/滴
市售纯净水 2
煮沸后的自来水 6
自来水 9
湖水 14
【解释与结论】
(4)硬度最大的水样是_______。
(5)继续实验,发现山泉水的硬度大于自来水的硬度,其实验方案为_______。
12.完成以下基础实验与学科实践内容
(1)性质检验
操作 现象 结论
铁丝燃烧时,观察到的现象是______ 能支持燃烧
集气瓶中水的作用是_______
(2)探究实验室制取氧气反应速率
Ⅰ.某化学兴趣小组进行不同催化剂对过氧化氢分解速率的影响,设计的方案和记录数据如下表所示:
实验序号 过氧化氢溶液体积、浓度 催化剂 收集50mL所用时间
① 30mL4% 无 ﹥200s
② 30mL4% 0.2g粉末 15s
③ 30mL4% ag粉末 34s
④ 30mL4% 0.2g粉末 27s
①表格中a的值为_______。
②实验②中制取氧气的符号表达式为_______。
③结论:通过上述实验对比,可得出的实验结论是_______。
Ⅱ.化学兴趣小组借助数字化实验手段用装置A探究其他条件对过氧化氢分解速率的影响,选用0.2g粉末作催化剂分组进行实验,通过压强传感器得到的数据如图所示。
分析图中实验1,溶液的浓度越大(即),反应速率_______(选填“越快”、“越慢”或“不影响”);分析图中实验2所示数据,你认为影响该反应速率的条件是_______。
(3)探究制氧机的原理
查阅资料:过氧化氢和过碳酸钠都可以产生氧气。
小组同学取上述两种药品分别加入0.2g二氧化锰进行对比实验,比较过氧化氢溶液和过碳酸钠制取氧气的效率。测得数据如图1(20min后几乎不产生氧气)请分析制氧剂选择过碳酸钠的依据是_______。
化学制氧机内缸如图2,为保证制氧的效果稳定,制氧机反应仓的加水量在夏季比冬季的高,原因是_______。
三、填空题
13.钛在航空航天,医疗器械等工业领域有着重要用途,生产钛的方法之一是利用四氯化钛与镁的反应。镁元素和钛元素在元素周期表中相关信息如图所示。
(1)镁元素的原子序数为_______,钛元素的相对原子质量为_______;
①镁元素和钛元素属于_______(填“金属”或“非金属”)元素。
②从物质的元素组成角度看,与镁、钛、氧气属于同一类别的是_______(填字母)。
A.空气 B.氧化镁 C.二氧化锰 D.铁
(2)下列原子结构示意图中,与镁原子的化学性质最相似的是______(填字母)。
A. B. C. D.
(3)钛元素能形成多种化合物,如、。请问
①钛有多种化合价,读作_______;
②中,钛元素的化合价是_______;
③从物质分类角度看,属于_______(填字母)。
A.混合物
B.氧化物
C.单质
D.化合物
E.纯净物
(4)一定条件下,四氯化钛与金属镁发生反应可获得金属钛,同时生成氯化镁。该反应的文字表达式为_______。
14.下面是实验室制取气体的几种发生装置和收集装置。请回答下列问题:
(1)仪器名称①_______。
(2)实验室用双氧水和二氧化锰制取并收集较纯净的氧气,应选装置_______(填字母)。
(3)实验室用装置A制取氧气的反应的文字表达式:_______,试管口放一团棉花的目的是_______。
(4)某同学设计图C装置,该装置与B相比优点是_______。
(5)利用G装置收集氧气,验满时将带火星的木条放在_______(填“a”或“b”)处。
(6)实验室常用醋酸钠固体和碱石灰固体混合加热制备甲烷气体,发生装置应选用_______,已知甲烷是一种密度比空气小、难溶于水的气体,这是甲烷的_______(选填“物理”或“化学”)性质,如从DEF装置中选择收集装置,可以选择_______。
参考答案
1.答案:B
解析:A、自然晾晒,去除露水,只是水的状态的改变,无新物质生成,属于物理变化;B、高温,破坏酶的活性,发生了蛋白质变性,有新物质生成,属于化学变化;C、通过外力作用将叶片揉碎,只是形状的改变,无新物质生成,属于物理变化;D、蒸发水分并整理外形,只是水的状态和形状的改变,无新物质生成,属于物理变化。故选B。
2.答案:A
解析:A、空气中不含氢气,氢气不是来自于空气。符合题意。B、氮气占空气体积的78%,氮气来自于空气。不符合题意。C、氧气占空气体积的21%,氧气来自于空气。不符合题意。D、氦气属于稀有气体,稀有气体占空气体积的0.94%,氦气来自于空气。不符合题意。故选A。
3.答案:D
解析:①硅元素的元素符号为Si,选项正确;②元素符号从微观上表示1个原子,则氮原子的符号为N,选项错误;③元素符号从微观上表示1个原子,则氧原子的符号为O,选项错误;④铜的符号为Cu,选项错误;⑤1个水分子由2个氢原子与1个氧原子构成,则水分子的符号为,选项正确;⑥数字而离子符号时,先写出相应的元素符号,然后在元素符号的右上角先写出离子所带电荷的数目,再写出电荷的电性,电荷数为1时省略不写,1个氯离子带1个单位的负电荷,则氯离子的符号为,选项正确,即正确选项为①⑤⑥,故选D。
4.答案:B
解析:花香的飘散微观上属于分子运动的现象,故选择B项。
5.答案:A
解析:A、开发和使用清洁能源可以减少有害气体和二氧化碳的排放,有利于环境保护,故A符合题意;B、工业废水集中直接排入海洋会对海洋的生态环境造成危害,不利于环境保护,故B不符合题意;C、所有垃圾集中焚烧处理会产生大量的有害气体污染空气,不利于环境保护,故C不符合题意;D、大量施用农药和化肥会造成土壤污染和水体污染,不利于环境保护,故D不符合题意。故选:A。
6.答案:B
解析:A、“气凝胶冰”中只含一种物质水,属于纯净物,故A错误;B、“气凝胶冰”与冰都是由水分子构成的,所以化学性质相同,故B正确;C、“气凝胶冰”是指水会像棉花糖一样,以蓬松轻盈的形式稳定存在,而冰是结构紧密的固体,二者密度不相同,故C错误;D、分子总是在不断运动的,故D错误。故选:B
7.答案:C
解析:A、氧化物是由两种元素组成的化合物,且一种元素为氧元素,亚硫酸钠是由钠、硫、氧三种元素组成,不属于氧化物,选项A错误;B、亚硫酸钠是由亚硫酸钠分子构成,亚硫酸钠分子由氢、硫、氧三种原子构成,选项B错误;C、亚硫酸钠中钠、硫、氧三种元素的质量比为(23×2):(32×1):(16×3)=23:16:24,所以硫元素的质量分数最小,选项C正确;D、亚硫酸钠中钠、氧两种元素的质量比为(23×2):(16×3)=23:24,选项D错误。故选:C。
8.答案:B
解析:A、图中由两种分子,表示混合物,选项错误;B、图中有一种分子,属于纯净物,选项正确;C、图中有三种分子,属于混合物,选项错误;D、图中有两种分子,属于混合物,选项错误,故选B。
9.答案:B
解析:A、物质是由分子、原子、离子构成,汞是由汞原子构成,该选项说法正确;B、单质是只有一种元素组成的纯净物,则只含一种元素的物质不一定为单质,还可能为混合物,该选项说法不正确;C、将木条平放入蜡烛火焰中约1s,根据木条的炭化情况,可探究火焰哪层温度最高,该选项说法正确;D、实验室的废液不能直接倾倒,否则会腐蚀管道和污染水源,该选项说法正确。故选B。
10.答案:B
解析:A、物理变化无新物质生成,化学变化有新物质生成,两者属于并列关系,故A说法错误;B、分子、原子和离子都是构成物质的微粒,构成物质的微粒与离子属于包含关系,故B说法正确;C、氧化反应是物质与氧的反应,化合反应指的是由两种或两种以上的物质反应生成一种新物质的反应,有的氧化反应是化合反应,如木炭燃烧生成二氧化碳,有的氧化反应不是化合反应,如蜡烛燃烧生成二氧化碳和水,两者属于交叉关系,故C说法错误;D、二氧化锰属于催化剂的一种,催化剂与二氧化锰属于包含关系,故D说法错误;故选:B。
11.答案:(1)二氧化氮(合理均可);开发利用新能源,减少化石燃料的使用,减少可吸入颗粒物的排放
(2)磷+氧气五氧化二磷;不一致;
(3)不相同;海水中有氯化钠、氯化镁等可溶性杂质,通过静置、过滤、吸附无法除去钠离子和氯离子(合理均可)
(4)湖水
(5)取相同量山泉水,滴加肥皂水记录产生泡沫所需肥皂水量,大于自来水所需肥皂水量,说明山泉水硬度大于自来水
解析:(1)引起空气污染的有害气体有二氧化硫、二氧化氮等,减少污染问题,可以开发利用新能源,减少化石燃料的使用,减少可吸入颗粒物的排放等,故填:二氧化氮、开发利用新能源,减少化石燃料的使用,减少可吸入颗粒物的排放;
(2)磷与氧气在点燃条件下反应生成五氧化二磷,该反应的文字表达式为:磷+氧气五氧化二磷,若用木炭代替红磷进行对比实验,木炭燃烧生成二氧化碳气体,在消耗氧气的同时会生成二氧化碳气体,故压强变化趋势与图乙不一致,D点后压强不再减小,这是说明剩余气体不和红磷反应,说明氧气体积约占空气体积的,故填:磷+氧气五氧化二磷、不一致、;
(3)江水为淡水,海水为咸水,通过静置、过滤、吸附可以除去江水中的难溶性杂质,但海水中有氯化钠、氯化镁等可溶性杂质,通过静置、过滤、吸附无法除去钠离子和氯离子,故填:不相同、海水中有氯化钠、氯化镁等可溶性杂质,通过静置、过滤、吸附无法除去钠离子和氯离子;
(4)本实验是记录的数据是观察到泡沫产生时所需肥皂水的用量,所以用到肥皂水滴数越多,说明水的硬度越大,所以硬度最大的水样是湖水,故填:湖水;
(5)硬度越大,观察到泡沫产生时所需肥皂水的用量越大,故验证山泉水的硬度大于自来水的硬度的方法:取相同量山泉水和自来水,滴加肥皂水,记录产生泡沫所需肥皂水量,山泉水大于自来水所需肥皂水量,说明山泉水硬度大于自来水,故填:取相同量山泉水,滴加肥皂水记录产生泡沫所需肥皂水量,大于自来水所需肥皂水量,说明山泉水硬度大于自来水。
12.答案:(1)剧烈燃烧,放出热量,火星四射,生成黑色固体;防止高温熔融物溅落,使瓶底炸裂
(2)0.2;;在过氧化氢溶液体积、浓度一定,催化剂质量一定时,二氧化锰的催化效果最好;越快;温度
(3)20分钟以内,过碳酸钠产生的氧气比过氧化氢产生的氧气多;夏天温度高,反应速率快,需要多加水,可以减慢氧气产生的速度
解析:(1)铁丝燃烧时,观察到的现象为:剧烈燃烧,放出热量,火星四射,生成黑色固体;集气瓶中水的作用是防止高温熔融物溅落,使瓶底炸裂;
(2)Ⅰ.①某化学兴趣小组研究的是不同催化剂对过氧化氢分解速率的影响,根据单一变量原则,催化剂可以改变,但质量不能改变,故a为0.2g;
②过氧化氢在二氧化锰的催化下生成水和氧气,故实验②中制取氧气的的符号表达式为:;
③根据表格中数据,收集50mL所用时间最少的是实验②,则在过氧化氢溶液体积、浓度一定,催化剂质量一定时,二氧化锰的催化效果最好;
Ⅱ.根据图中实验1,相同时间内,的浓度越大,产生的气体越多,锥形瓶内压强越大,反应速率越快;图中实验2所示数据,影响该反应速率的条件是温度;
(3)根据图1中测得数据(20min后几乎不产生氧气),制氧剂选择过碳酸钠的依据是:20min内,生成氧气的量比过氧化氢多;
为保证制氧的效果稳定,制氧机反应仓的加水量在夏季比冬季的高,是因为夏季温度高,反应速率快,多加水,可减缓生成氧气的速率。
13.答案:(1)12;47.87;金属;D
(2)D
(3)二氧化钛;+4/+4价;DE
(4)四氯化钛+镁钛+氯化镁
解析:(1)元素信息示意图左上角的数字表示原子序数,根据镁的元素信息示意图,镁元素的原子序数为12;元素信息示意图正下方的数字代表相对原子质量,根据钛的元素信息示意图,钛元素的相对原子质量为47.87;
①镁和钛都是“金字旁”的汉字,因此镁元素和钛元素属于金属元素;
②从物质的元素组成角度看,镁、钛、氧气都是由一种元素组成的纯净物,属于单质。
A、空气含有氮气、氧气、稀有气体等物质,不属于单质;
B、氧化镁是由两种元素组成的纯净物,不属于单质;
C、二氧化锰是由两种元素组成的纯净物,不属于单质;
D、铁是由一种元素组成的纯净物,属于单质。
故选:D。
(2)一般来说,原子的最外层电子数相等,化学性质相似。根据图像,镁原子的最外层电子数为2,没有排满,属于不稳定结构。A、B、C、D四种原子中,只有A和D的最外层电子数为2,其中A原子最外层排满电子,属于稳定结构,D原子最外层没有排满电子,属于不稳定结构,因此与镁原子的化学性质最相似的是D。
(3)①根据“顺写反读”的规则,读作二氧化钛;
②化合物中元素正负化合价之和为零,中,H显+1价,O显-2价,设钛元素的化合价为x,则,解得x=+4;
③混合物含有两种或两种以上物质;氧化物是由两种元素组成的含有氧元素的化合物;单质是由一种元素组成的纯净物;化合物是由两种或两种以上元素组成的纯净物;纯净物只含一种物质。从物质分类角度看,是由3种元素组成的纯净物,属于化合物,不属于混合物或单质或氧化物,故选:DE。
(4)一定条件下,四氯化钛与金属镁发生反应可获得金属钛,同时生成氯化镁,反应的文字表达式为:四氯化钛+镁钛+氯化镁。
14.答案:(1)长颈漏斗
(2)BF
(3)高锰酸钾锰酸钾+二氧化锰+氧气;防止加热时粉末状物质进入导管
(4)可以控制反应速率
(5)b
(6)A;物理;E/F
解析:(1)据图可知,仪器①的名称是长颈漏斗;
(2)用过氧化氢和二氧化锰制取氧气时不需要加热,应该用B装置作为发生装置;因为氧气的密度比空气大,可以用向上排空气法收集,即用E装置收集,氧气不易溶于水,可以用排水法收集,即用F装置收集,用排水法收集的氧气比用排空气法收集的氧气纯净;
(3)A装置为加热固体的装置,试管口有棉花,可选用高锰酸钾制取氧气,高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应的文字表达式为:高锰酸钾锰酸钾+二氧化锰+氧气,试管口还要放一团棉花,目的是:防止加热时粉末状物质进入导管;
(4)C装置中,小注射器能控制液体的滴加速度,从而控制反应速率;
(5)氧气的密度比空气大,用G装置收集氧气从a导管通入,空气从b导管逸出,当从b导管逸出的是氧气时,表示氧气已经收集满,所以验满时,带火星的木条放在b处;
(6)用醋酸钠固体和碱石灰固体混合加热制备甲烷是固体加热型反应,发生装置选择A;甲烷是一种密度比空气小、难溶于水的气体,不需要化学变化就可以表现出来,属于物理性质;甲烷密度比空气小,可选择E向下排空气法收集,难溶于水可使用F排水法收集,
同课章节目录
