七下第一章第四节配制溶液
图片预览








文档简介
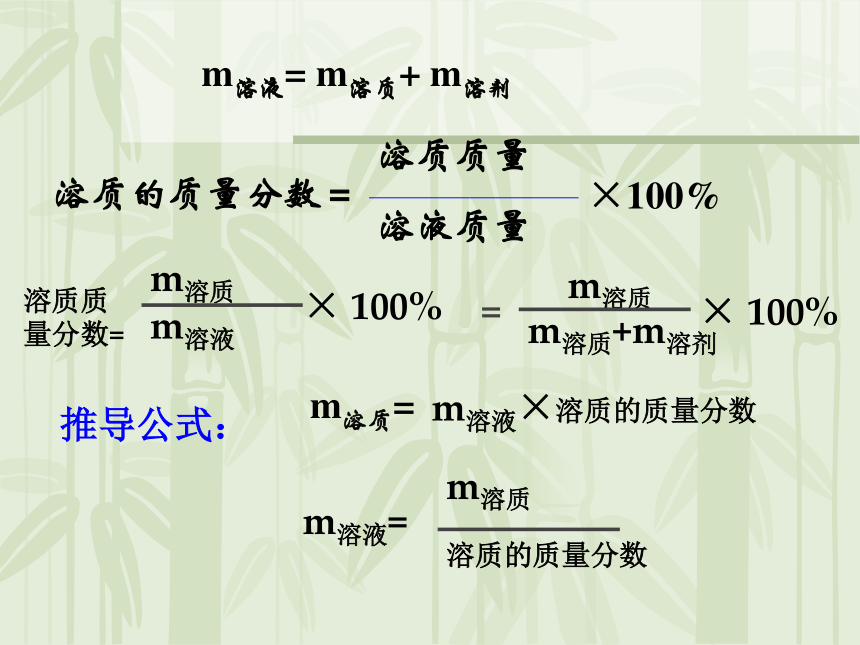
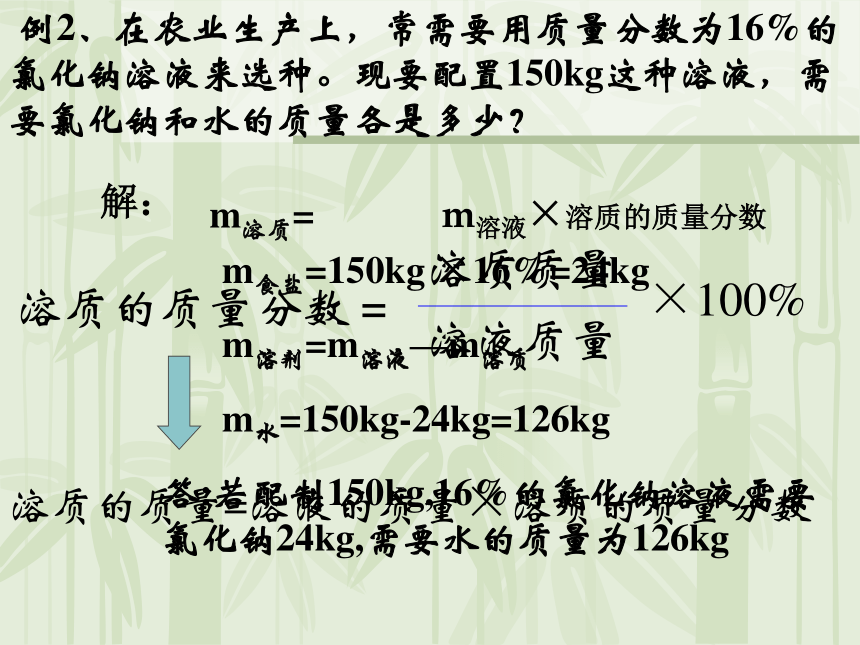
课件47张PPT。溶质的质量分数1,哪支试管中的溶液浓度更高?2,试管②颜色深是由什么原因造成的?②①3,试管②比试管①,浓度高多少?颜色的深浅(浓度的高低)是由溶质的质量和溶剂的质量共同造成的溶质的质量分数定义:溶液中,溶质的质量与溶液的质量之比。所以科学上用溶质的质量分数来定量的表示溶液的组成m溶质=推导公式:m溶液×溶质的质量分数m溶液= m溶质+ m溶剂二、溶液中溶质的质量分数计算 例1:从一瓶氯化钾溶液中取出20克溶液,蒸干后得到2.8克氯化钾固体。试确定这瓶溶液中溶质的质量分数。这瓶溶液中溶质的质量分数为:答:这瓶溶液中氯化钾的质量分数为14%。 例2、在农业生产上,常需要用质量分数为16%的氯化钠溶液来选种。现要配置150kg这种溶液,需要氯化钠和水的质量各是多少?溶质的质量=溶液的质量×溶质的质量分数m食盐=150kg ×16%=24kgm溶剂=m溶液—m溶质m水=150kg-24kg=126kg答:若配制150kg,16%的氯化钠溶液需要氯化钠24kg,需要水的质量为126kg解:你能求出溶液中溶质的质量吗 ?硫酸a%:98%M: 600g该瓶浓硫酸中含有溶质硫酸_____克m溶质=m溶液×a%=600g× 98%=588g588例3.现需要配制0.9%的生理盐水1000克,问需要9%
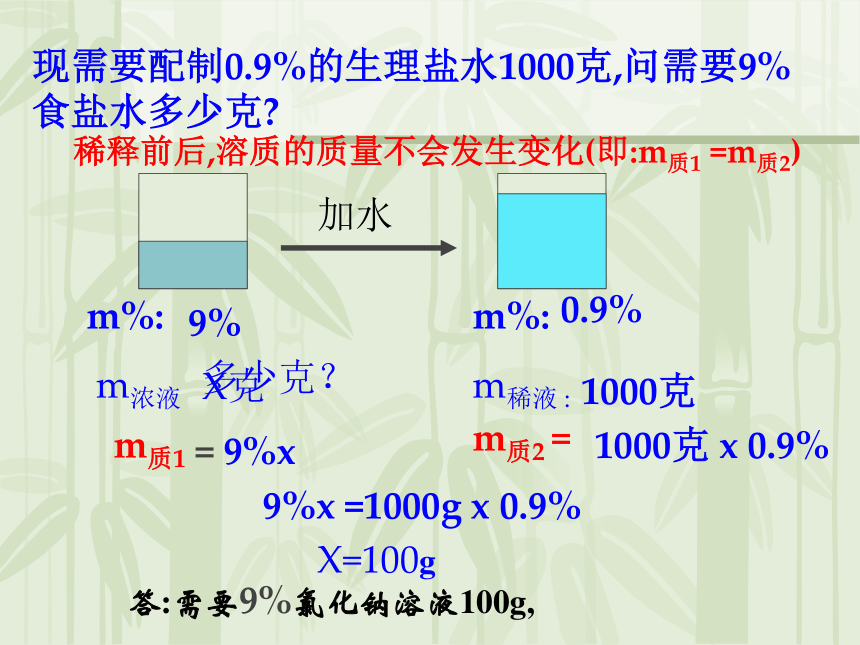
食盐水多少克?0.9%9%浓溶液稀溶液稀释思考:稀释后,哪些量发生了变化,哪些量没有发生变化?稀释前后,溶质的质量不会发生变化(即:m质1 =m质2)m质1 =m质2m浓×浓溶质的质量分数= m稀×稀溶质的质量分数现需要配制0.9%的生理盐水1000克,问需要9%
食盐水多少克?稀释前后,溶质的质量不会发生变化(即:m质1 =m质2)m%:
m稀液 :m%:
m浓液多少克?0.9%1000克9%加水X克= 9%xm质1m质2 =1000克 x 0.9%9%x =1000g x 0.9%X=100g答:需要9%氯化钠溶液100g,三、稀释问题的公式:
m浓×浓溶质的质量分数= m稀×稀溶质的质量分数
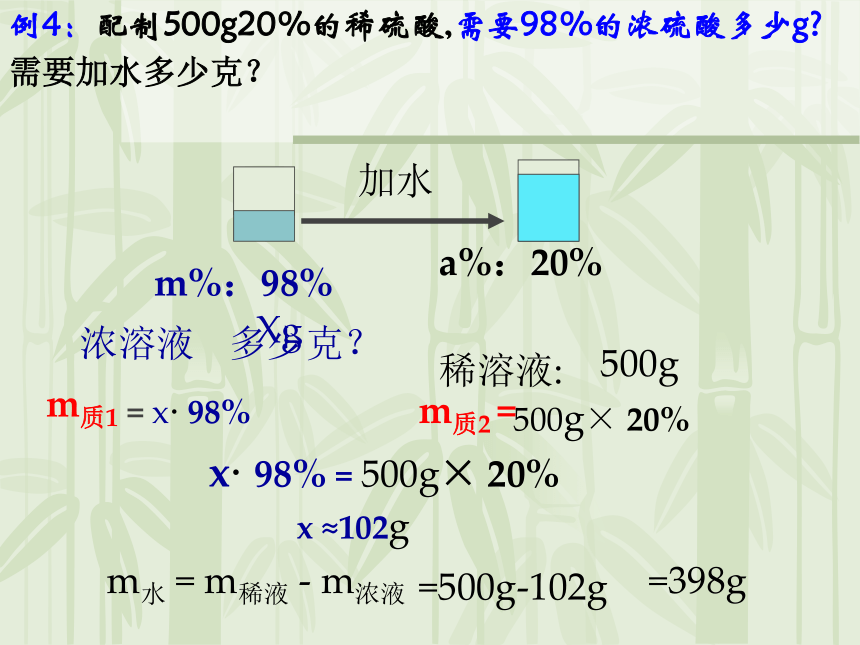
即:m质1 =m质21,设未知量 2, 列方程 、数据代入 3,解答例4:配制500g20%的稀硫酸,需要98%的浓硫酸多少g?需要加水多少克?多少克?加水Xg= x· 98% m质1m质2 =x· 98% = 500g× 20% m%:98%浓溶液 500g× 20% x ≈102g=398gm水 = m稀液 - m浓液=500g-102g练习:1、把200g 质量分数为98%的浓硫酸稀释成质量分数为10%的硫酸,需水多少g ?
2、将20g 15%的食盐水和20g5%的食盐水混合,所得溶液的质量为____g,其溶质的质量分数为___。
例5:20℃时,氯化钾的溶解度为40克,求:
(1)在20℃时,200克水最多能溶解多少克氯化钾?
(2)在20℃时,把50克氯化钾放入100克水中,充分溶解,得到溶液中溶质的质量分数是多少?分析:在20℃时,100克水最多能溶解40克氯化钾X=80g饱和溶液的溶质质量分数(S为溶解度) 例6、欲使100g 5%的硝酸钠溶液增大到20%,分别采用下列方法:(1) 需加入硝酸钠固体多少g ?(2) 需蒸发水多少g ?(3) 需加入50%的硝酸钠溶液多少g?四、浓缩问题的公式浓缩:①向原溶液中加溶质,设原溶液质量为A,溶质的质量分数为a%,加入溶质质量为x,所得浓溶液中溶质质量分数为b% ,
则有: m稀·a%+x=( m稀+x)·b%
浓缩:②将原溶液蒸发溶剂,设原溶液质量为A,溶质量分数为a%,蒸发溶剂质量为x,所得浓溶液中溶质质量分数为b%,
则有: m稀·a%=( m稀– x)·b% 课堂小结1,溶质质量分数的概念和作用2,有关溶质质量分数的计算①计算溶质的质量分数m水 = m稀液 - m浓液m质1 =m质2m浓×a%= m稀×b%②计算溶质和溶剂的质量③有关稀释问题的计算1、小李从100克10%的食盐溶液中取出30克溶液,则取出溶液的溶质的质量分数为( )A、10% B、1% C、33% D、3.3%2、将100克10%的氯化钠溶液进行如下操作后的溶质质量分数各为多少?A、蒸发掉一半的水 ; B、向原溶液中加入10克氯化钠 ; C、向原溶液中加入100克水 。做一做A18.2%18.2%5%`练习1:已知溶质和溶剂质量,求溶质的质量分数 上述实验配制的溶液中氯化钠的质量分数是多少?10%20%3、某同学把20克5%的硝酸钾溶液稀释至200克,则稀释后溶液中含硝酸钾的质量是( )A、10克 B、1克 C、0.1克 D、0.01克4、为了实验需要将20%的硫酸溶液100克与2%的硫酸溶液100克混合后,溶液的质量分数是( )A、20% B、22% C、2% D、11%BD5、为了实验需要将20%的硫酸溶液100克与2%的硫酸溶液200克混合后,溶液的质量分数是( )A、20% B、22% C、8% D、11%C6、某同学将5克某物质,加到95克水中,所得溶液溶质质量分数为( )A、小于5% B、等于5%C、大于 5% D、条件不全,以上答案都不对7、某同学在某温度下向一定量的水中不断地加入蔗糖,并搅拌。下列图中能正确反应所加入的蔗糖与所得溶液溶质质量分数之间关系的图象是( )DD50克4%的氯化钠溶液中,含有溶质氯化钠 克,水 克。 请 你完成:思考:需要配制50g 质量分数为4%的食盐溶液, 而实验室没有现成配制好的,要我们自己配制,该怎么做呢? 完成实验所需要的试剂:食盐蒸馏水完成实验所需要的仪器:烧杯玻璃棒天平、砝码量筒药匙滴管配制一定溶质质量分数的溶液的步骤:1、计算:2、称量:3、溶解:分度盘指针底座平衡螺母托盘砝码镊子托盘天平的构造横梁1标尺游码234567891011托盘支架托盘天平的使用口诀:
天平放平,游码归零,横梁调平,物左码右,重新平衡,物码复原。1、把天平放在 上,把游码移到横梁标尺 ,调节 ,使指针对准 ,这时横梁平衡。2、当天平调节平衡时,如图所示,物体的质量是 。
水平桌面左端零刻度线平衡螺母分度盘中央刻度线61.4克3、如果天平的游码未放到标尺零刻度线处就将横梁调节平衡,那么用这样的天平称物体质量所得的数值将比物体质量的真实值( )
A、大些 B、小些 C、相等 D、无法判断A6、量筒用途,量度液体体积。1、量筒没有0刻度、刻度上大下小。
2、量筒的规格是1、2、5。(最小的量筒是5ml,最大量程是1000毫升的)
3、量筒的分度值是量程除以50。
4、不能加热、不能作反应容器。注意事项:不能加热,不能做反应容器。如果视线没有与量筒内液体凹液面的最低处保持水平,而是采用仰视或俯视的方法,将会对读数产生什么影响?②、量取一定量的液体—用量筒和滴管。步骤:
1、倾倒液体。
2、滴管定容。
3、正确读数。仰视:读数小于真实值!俯视:读数大于真实值!(二)量筒的使用1、操作要领:
量筒平放实验桌,先倒后滴把量瞅;
平视凹液最低处,三线一齐为读数.
2、注意:
平视:读数=实际体积数
俯视:读数﹥实际体积数
仰视:读数﹤实际体积数1、有10ml、50ml、100ml三种规格的量筒,如果要量取8ml的水,选择哪种量筒较好?
2、某同学量8ml的水时,读数时仰视,则该同学实际量取的水是大于8ml还是小于8ml ?想一想大于8ml根据实验室有的浓盐酸,要求用2ml的浓盐酸配制1:4的稀盐酸,请同学们考虑需要哪些仪器和药品? 盐酸 化学纯
(500 mL)
品名盐酸
化学式 HCL 相对分子质量36.5
密度1.19g/cm3质量分数37%15%37%浓溶液稀溶液稀释思考:稀释后,哪些量发生了变化,哪些量没有发生变化?稀释前后,溶质的质量不会发生变化(即:m质1 =m质2)m质1 =m质2m浓×a%= m稀×b%完成实验所需要的试剂:浓盐酸蒸馏水完成实验所需要的仪器:烧杯玻璃棒量筒滴管配制一定溶质质量分数的溶液的步骤:1、计算:2、量取:3、溶解:1、用氯化钠固体配制一定质量分数的氯化钠溶液,必须使用的一组仪器是( )
A.天平、烧杯、量筒、玻璃棒、药匙 B.天平、烧杯、漏斗、蒸发皿、玻璃棒C.天平、烧杯、量筒、铁架台、药匙 D.天平、集气瓶、漏斗、蒸发皿、玻璃 棒
思考1:思考2:用98%的浓硫酸(密度1.84g/cm3 )和水配制100克10%的稀硫酸,下列仪器中一般必需要使用的是( )
A、100毫升的量筒 B、天平
C、10毫升量筒 D、250毫升的烧杯 思考3:3、用浓盐酸配制一定质量分数的稀盐酸,用量筒量取浓盐酸时,视线仰视读数;量水时,视线俯视,则所配的溶液的质量分数将( )
A、偏高 B、偏低
C、不变 D、无法判断
思考4:4、某同学在配制100克质量分数为5.1%的氯化钠溶液时,有以下操作:
①在天平的左边加5克砝码,移动游码到0.1克,右边加入氯化钠固体,直到天平平衡,将称好的氯化钠固体倒入烧杯
②用100毫升的量筒量取94.9毫升水时,仰读刻度。将水倒入装有氯化钠的烧杯中,搅拌,让氯化钠全部溶解即可。
指出上述操作过程中的错误及可能产生的后果。 11、胶头滴管 用于吸取和滴加少量液体药品,用过后应该立即洗干净,然后再去吸取其它药品。12、滴瓶 用于盛放液体药品,滴瓶上的滴管是专管专用,所以用过后没有必要清洗!3、胶头滴管的使用2、滴管不得伸入容器口、以免污染药品1、先排空橡胶帽里的空气,伸入液体里面,再松开手,以防空气与液体反应。3、用过后的滴管要清洗,不得平放或倒放。4、滴瓶上的胶头滴管不用清洗!很容易懂的,不必抄写。1、如图下列使用胶头滴管的方法中正确的是( )B2、以下存放和取用药品的方法不合理的是( )
A、锌粒存放于广口瓶中
B、盐酸存放于细口瓶中
C、用滴管取用大量液体
D、用药匙取用碳酸钠粉末D再见!
食盐水多少克?0.9%9%浓溶液稀溶液稀释思考:稀释后,哪些量发生了变化,哪些量没有发生变化?稀释前后,溶质的质量不会发生变化(即:m质1 =m质2)m质1 =m质2m浓×浓溶质的质量分数= m稀×稀溶质的质量分数现需要配制0.9%的生理盐水1000克,问需要9%
食盐水多少克?稀释前后,溶质的质量不会发生变化(即:m质1 =m质2)m%:
m稀液 :m%:
m浓液多少克?0.9%1000克9%加水X克= 9%xm质1m质2 =1000克 x 0.9%9%x =1000g x 0.9%X=100g答:需要9%氯化钠溶液100g,三、稀释问题的公式:
m浓×浓溶质的质量分数= m稀×稀溶质的质量分数
即:m质1 =m质21,设未知量 2, 列方程 、数据代入 3,解答例4:配制500g20%的稀硫酸,需要98%的浓硫酸多少g?需要加水多少克?多少克?加水Xg= x· 98% m质1m质2 =x· 98% = 500g× 20% m%:98%浓溶液 500g× 20% x ≈102g=398gm水 = m稀液 - m浓液=500g-102g练习:1、把200g 质量分数为98%的浓硫酸稀释成质量分数为10%的硫酸,需水多少g ?
2、将20g 15%的食盐水和20g5%的食盐水混合,所得溶液的质量为____g,其溶质的质量分数为___。
例5:20℃时,氯化钾的溶解度为40克,求:
(1)在20℃时,200克水最多能溶解多少克氯化钾?
(2)在20℃时,把50克氯化钾放入100克水中,充分溶解,得到溶液中溶质的质量分数是多少?分析:在20℃时,100克水最多能溶解40克氯化钾X=80g饱和溶液的溶质质量分数(S为溶解度) 例6、欲使100g 5%的硝酸钠溶液增大到20%,分别采用下列方法:(1) 需加入硝酸钠固体多少g ?(2) 需蒸发水多少g ?(3) 需加入50%的硝酸钠溶液多少g?四、浓缩问题的公式浓缩:①向原溶液中加溶质,设原溶液质量为A,溶质的质量分数为a%,加入溶质质量为x,所得浓溶液中溶质质量分数为b% ,
则有: m稀·a%+x=( m稀+x)·b%
浓缩:②将原溶液蒸发溶剂,设原溶液质量为A,溶质量分数为a%,蒸发溶剂质量为x,所得浓溶液中溶质质量分数为b%,
则有: m稀·a%=( m稀– x)·b% 课堂小结1,溶质质量分数的概念和作用2,有关溶质质量分数的计算①计算溶质的质量分数m水 = m稀液 - m浓液m质1 =m质2m浓×a%= m稀×b%②计算溶质和溶剂的质量③有关稀释问题的计算1、小李从100克10%的食盐溶液中取出30克溶液,则取出溶液的溶质的质量分数为( )A、10% B、1% C、33% D、3.3%2、将100克10%的氯化钠溶液进行如下操作后的溶质质量分数各为多少?A、蒸发掉一半的水 ; B、向原溶液中加入10克氯化钠 ; C、向原溶液中加入100克水 。做一做A18.2%18.2%5%`练习1:已知溶质和溶剂质量,求溶质的质量分数 上述实验配制的溶液中氯化钠的质量分数是多少?10%20%3、某同学把20克5%的硝酸钾溶液稀释至200克,则稀释后溶液中含硝酸钾的质量是( )A、10克 B、1克 C、0.1克 D、0.01克4、为了实验需要将20%的硫酸溶液100克与2%的硫酸溶液100克混合后,溶液的质量分数是( )A、20% B、22% C、2% D、11%BD5、为了实验需要将20%的硫酸溶液100克与2%的硫酸溶液200克混合后,溶液的质量分数是( )A、20% B、22% C、8% D、11%C6、某同学将5克某物质,加到95克水中,所得溶液溶质质量分数为( )A、小于5% B、等于5%C、大于 5% D、条件不全,以上答案都不对7、某同学在某温度下向一定量的水中不断地加入蔗糖,并搅拌。下列图中能正确反应所加入的蔗糖与所得溶液溶质质量分数之间关系的图象是( )DD50克4%的氯化钠溶液中,含有溶质氯化钠 克,水 克。 请 你完成:思考:需要配制50g 质量分数为4%的食盐溶液, 而实验室没有现成配制好的,要我们自己配制,该怎么做呢? 完成实验所需要的试剂:食盐蒸馏水完成实验所需要的仪器:烧杯玻璃棒天平、砝码量筒药匙滴管配制一定溶质质量分数的溶液的步骤:1、计算:2、称量:3、溶解:分度盘指针底座平衡螺母托盘砝码镊子托盘天平的构造横梁1标尺游码234567891011托盘支架托盘天平的使用口诀:
天平放平,游码归零,横梁调平,物左码右,重新平衡,物码复原。1、把天平放在 上,把游码移到横梁标尺 ,调节 ,使指针对准 ,这时横梁平衡。2、当天平调节平衡时,如图所示,物体的质量是 。
水平桌面左端零刻度线平衡螺母分度盘中央刻度线61.4克3、如果天平的游码未放到标尺零刻度线处就将横梁调节平衡,那么用这样的天平称物体质量所得的数值将比物体质量的真实值( )
A、大些 B、小些 C、相等 D、无法判断A6、量筒用途,量度液体体积。1、量筒没有0刻度、刻度上大下小。
2、量筒的规格是1、2、5。(最小的量筒是5ml,最大量程是1000毫升的)
3、量筒的分度值是量程除以50。
4、不能加热、不能作反应容器。注意事项:不能加热,不能做反应容器。如果视线没有与量筒内液体凹液面的最低处保持水平,而是采用仰视或俯视的方法,将会对读数产生什么影响?②、量取一定量的液体—用量筒和滴管。步骤:
1、倾倒液体。
2、滴管定容。
3、正确读数。仰视:读数小于真实值!俯视:读数大于真实值!(二)量筒的使用1、操作要领:
量筒平放实验桌,先倒后滴把量瞅;
平视凹液最低处,三线一齐为读数.
2、注意:
平视:读数=实际体积数
俯视:读数﹥实际体积数
仰视:读数﹤实际体积数1、有10ml、50ml、100ml三种规格的量筒,如果要量取8ml的水,选择哪种量筒较好?
2、某同学量8ml的水时,读数时仰视,则该同学实际量取的水是大于8ml还是小于8ml ?想一想大于8ml根据实验室有的浓盐酸,要求用2ml的浓盐酸配制1:4的稀盐酸,请同学们考虑需要哪些仪器和药品? 盐酸 化学纯
(500 mL)
品名盐酸
化学式 HCL 相对分子质量36.5
密度1.19g/cm3质量分数37%15%37%浓溶液稀溶液稀释思考:稀释后,哪些量发生了变化,哪些量没有发生变化?稀释前后,溶质的质量不会发生变化(即:m质1 =m质2)m质1 =m质2m浓×a%= m稀×b%完成实验所需要的试剂:浓盐酸蒸馏水完成实验所需要的仪器:烧杯玻璃棒量筒滴管配制一定溶质质量分数的溶液的步骤:1、计算:2、量取:3、溶解:1、用氯化钠固体配制一定质量分数的氯化钠溶液,必须使用的一组仪器是( )
A.天平、烧杯、量筒、玻璃棒、药匙 B.天平、烧杯、漏斗、蒸发皿、玻璃棒C.天平、烧杯、量筒、铁架台、药匙 D.天平、集气瓶、漏斗、蒸发皿、玻璃 棒
思考1:思考2:用98%的浓硫酸(密度1.84g/cm3 )和水配制100克10%的稀硫酸,下列仪器中一般必需要使用的是( )
A、100毫升的量筒 B、天平
C、10毫升量筒 D、250毫升的烧杯 思考3:3、用浓盐酸配制一定质量分数的稀盐酸,用量筒量取浓盐酸时,视线仰视读数;量水时,视线俯视,则所配的溶液的质量分数将( )
A、偏高 B、偏低
C、不变 D、无法判断
思考4:4、某同学在配制100克质量分数为5.1%的氯化钠溶液时,有以下操作:
①在天平的左边加5克砝码,移动游码到0.1克,右边加入氯化钠固体,直到天平平衡,将称好的氯化钠固体倒入烧杯
②用100毫升的量筒量取94.9毫升水时,仰读刻度。将水倒入装有氯化钠的烧杯中,搅拌,让氯化钠全部溶解即可。
指出上述操作过程中的错误及可能产生的后果。 11、胶头滴管 用于吸取和滴加少量液体药品,用过后应该立即洗干净,然后再去吸取其它药品。12、滴瓶 用于盛放液体药品,滴瓶上的滴管是专管专用,所以用过后没有必要清洗!3、胶头滴管的使用2、滴管不得伸入容器口、以免污染药品1、先排空橡胶帽里的空气,伸入液体里面,再松开手,以防空气与液体反应。3、用过后的滴管要清洗,不得平放或倒放。4、滴瓶上的胶头滴管不用清洗!很容易懂的,不必抄写。1、如图下列使用胶头滴管的方法中正确的是( )B2、以下存放和取用药品的方法不合理的是( )
A、锌粒存放于广口瓶中
B、盐酸存放于细口瓶中
C、用滴管取用大量液体
D、用药匙取用碳酸钠粉末D再见!
同课章节目录
- 第1章 水
- 1 地球上的水
- 2 水的三态变化
- 3 水是常用的溶剂
- 4 配制溶液
- 5 水的组成
- 6 水资源的利用和保护
- 第2章 空气
- 1 空气的存在
- 2 空气的成分
- 3 氧气
- 4 二氧化碳
- 5 保护大气圈
- 第3章 阳光
- 1 太阳辐射能
- 2 阳光的传播
- 3 阳光的组成
- 第4章 土壤
- 1 土壤的组成和性状
- 2 土壤与植物
- 3 人类活动与土壤
- 第5章 生态系统
- 1 种群和群落
- 2 生态系统
- 3 生物圈
- 第6章 动物和人的生殖与发育
- 1 动物的生殖与发育
- 2 人的生殖与发育
- 第7章 植物和微生物的生殖与发育
- 1 绿色开花植物的有性生殖和发育
- 2 种子的萌发和幼苗形成
- 3 植物的无性生殖
- 4 细菌和真菌的繁殖
