2025鲁教版高中化学必修第二册强化练习题--第3课时 化学电池(含答案)
文档属性
| 名称 | 2025鲁教版高中化学必修第二册强化练习题--第3课时 化学电池(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 537.1KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-11-19 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
2025鲁教版高中化学必修第二册
第3课时 化学电池
基础过关练
题组一 常见化学电池
1.(2024陕西西安交通大学附属中学期中)电池研发与生产生活领域的发展密切相关,下列有关电池的说法正确的是( )
A.燃料电池的能量转化率可以达到100%
B.手机、照相机和摄像机等电器所用的锂离子电池为二次电池
C.二氧化硅可以制成人造卫星的硅太阳能电池
D.原电池是一种将电能转化为化学能的装置
2.(经典题)(2024山东威海二中月考)微型银—锌电池可用作电子仪器的电源,其电极分别是Ag/Ag2O和Zn,电解质溶液为KOH溶液,电池总反应为Ag2O+Zn+H2O 2Ag+Zn(OH)2。下列说法正确的是( )
A.电池工作过程中,负极发生还原反应
B.电池工作过程中,电解液中OH-向正极移动
C.负极电极反应为Zn+2OH--2e- Zn(OH)2
D.正极电极反应为Ag2O+2H+-2e- 2Ag+H2O
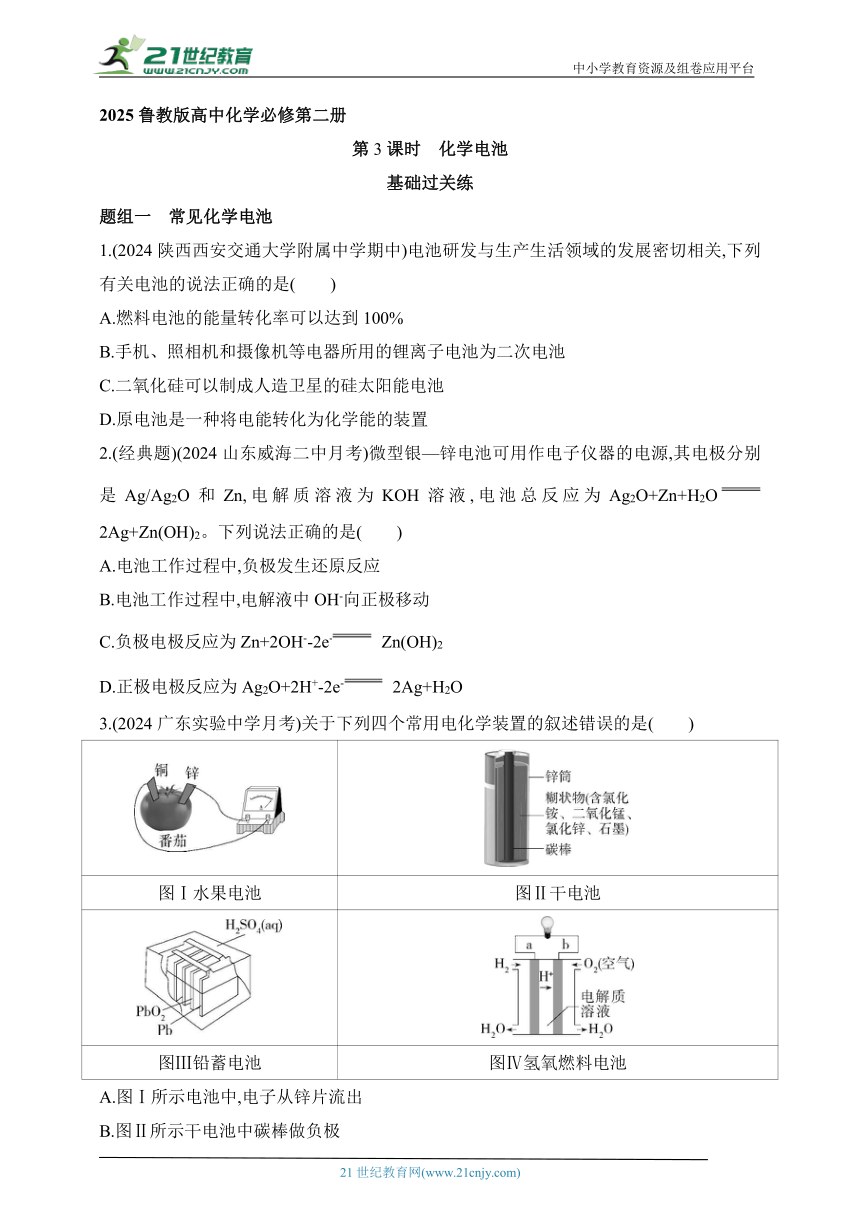
3.(2024广东实验中学月考)关于下列四个常用电化学装置的叙述错误的是( )
图Ⅰ水果电池 图Ⅱ干电池
图Ⅲ铅蓄电池 图Ⅳ氢氧燃料电池
A.图Ⅰ所示电池中,电子从锌片流出
B.图Ⅱ所示干电池中碳棒做负极
C.图Ⅲ所示电池为二次电池
D.图Ⅳ所示电池中正极反应为O2+4H++4e- 2H2O
题组二 燃料电池
4.(2024河南郑州期中)氢氧燃料电池已广泛应用于新能源公交汽车中,其反应原理如图所示。下列说法不正确的是( )
A.该电池工作时化学能转化为电能
B.该电池工作时阴离子向电极a移动
C.该电池工作时电子由电极a沿外电路流向电极b
D.若离子导体选择稀硫酸,则电池正极反应式为O2+4e-+2H2O 4OH-
5.(2024湖北武汉月考)H2S是一种剧毒气体,如图为质子膜H2S燃料电池的示意图,可对H2S废气资源化利用。下列叙述错误的是( )
A.电极a是负极,电池工作时,电子的流动方向是电极a→负载→电极b→质子固体电解质膜→电极a
B.电池工作时,化学能转化为电能和热能
C.电极b上发生的电极反应式为O2+4e-+4H+ 2H2O
D.当电路中通过4 mol电子时,有4 mol H+经质子固体电解质膜进入正极区
能力提升练
题组 化学电池的工作原理
1.(2024福建福州期中)科学家设计了一种新型全固态电池,巧妙利用火星大气中含有的大量CO2为火星探测器供电。该电池工作时的总反应为4Na+3CO2 2Na2CO3+C,下列说法不正确的是( )
A.负极上金属Na失电子发生氧化反应
B.正极电极反应式为3CO2+4e- C+2C
C.该电池中,阴离子由正极移向负极
D.若有0.3 mol CO2反应,流经固体电解质的电子数为0.4NA
2.(2024安徽蚌埠第二中学期中)锂—空气电池的装置示意图如图所示,下列说法不正确的是( )
A.金属锂为负极,发生氧化反应
B.Li+通过有机电解质向电解质水溶液移动
C.正极的电极反应:O2+4e- 2O2-
D.电池每消耗标准状况下56 L空气(O2约占),电路中通过的电子为2 mol
3.(2024山东师范大学附中月考)Hg-Hg2SO4标准电极在生活中常用于测定其他电极的电势,测知Hg-Hg2SO4电极的电势高于Cu电极的电势。以下说法正确的是( )
A.K2SO4溶液可用CCl4代替
B.Hg-Hg2SO4电极的电极反应式为Hg2SO4-2e- 2Hg+S
C.微孔瓷片起到阻隔离子通过的作用
D.若把Cu-CuSO4体系换作Zn-ZnSO4体系,电压表的示数变大
4.(经典题)(2023江西上饶阶段测试)金属(M)—空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为4M+nO2+2nH2O 4M(OH)n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是 ( )
A.采用多孔电极的目的是提高电极与电解质的接触面积,并有利于空气中氧气扩散至电极表面
B.比较M(Mg、Al、Zn)-空气电池,Al-空气电池的理论比能量最高
C.M-空气电池放电过程的正极电极反应式为4Mn++nO2+2nH2O+4ne- 4M(OH)n
D.在M-空气电池中,每转移4n mol电子,负极增重68n g
答案与分层梯度式解析
第3课时 化学电池
基础过关练
1.B 燃料电池的能量转化率虽然高,但仍有少量能量转化为热能而损耗,则能量转化率小于100%,故A错误;锂离子电池能反复充、放电,能循环使用,属于二次电池,故B正确;晶体硅为良好的半导体,可以制成硅太阳能电池,二氧化硅不具有此性质,故C错误;原电池是一种将化学能转化为电能的装置,故D错误。
2.C 电池工作过程中,Zn失电子做负极,发生氧化反应,电极反应为Zn+2OH--2e- Zn(OH)2,A错误、C正确;电池工作过程中,电解液中的OH-向负极移动,B错误;正极Ag2O得电子,发生还原反应,碱性环境下,电极反应为Ag2O+H2O+2e- 2Ag+2OH-,D错误。
3.B 图Ⅰ水果电池中,锌活动性比铜强,锌做负极,铜做正极,电子由负极流出,故A正确;图Ⅱ为酸性锌锰干电池,锌为金属,做负极,碳棒做正极,故B错误;图Ⅲ为铅蓄电池,铅做负极,二氧化铅做正极,是二次电池,即可充电的电池,故C正确;图Ⅳ为氢氧燃料电池,正极电极反应为O2+4H++4e- 2H2O,故D正确。
4.D 该电池工作时,化学能转化为电能,A正确;原电池工作时,阴离子向负极移动,则该电池工作时,阴离子向电极a移动,B正确;原电池工作时,电子由负极沿外电路流向正极,则该电池中的电子由电极a沿外电路流向电极b,C正确;若离子导体选择稀硫酸,则电池工作时,正极反应式为O2+4e-+4H+ 2H2O,D不正确。
5.A 该燃料电池中,电极a为负极,电极b为正极,电子由负极经过外电路流向正极,但不能经过质子固体电解质膜,故A错误;该装置为原电池,化学能主要转化为电能,少部分转化为热能,故B正确;电极b为正极,正极上O2发生得电子的还原反应生成水,电极反应式为O2+4e-+4H+ 2H2O,当电路中通过4 mol电子时,有4 mol H+经质子固体电解质膜进入正极区,故C、D正确。
能力提升练
1.D 根据电池总反应4Na+3CO2 2Na2CO3+C,可知负极上Na发生氧化反应失去电子生成Na+,故A正确;在正极CO2得到电子生成C,结合总反应,知正极电极反应式为3CO2+4e- C+2C,故B正确;放电时阴离子由正极移向负极,故C正确;每3 mol CO2反应,转移4 mol电子,所以0.3 mol CO2反应,转移的电子为0.4 mol,但电子不能流经固体电解质,故D错误。
2.C 在锂—空气电池中,金属锂失电子,发生氧化反应,为负极,A项正确;Li在负极失去电子变成Li+,Li+向电解质水溶液处移动,B项正确;正极的电极反应式为O2+4e-+2H2O 4OH-,C项错误;电池每消耗标准状况下56 L空气(O2约占),所含氧气的物质的量为0.5 mol,则电路中通过的电子的物质的量为2 mol,故D正确。
3.D
4.C 反应物接触面积越大,反应速率越快,所以采用多孔电极的目的是提高电极与电解质的接触面积,并有利于空气中氧气扩散至电极表面,从而提高反应速率,故A正确;单位质量的电极材料失去电子的物质的量越多则释放的电能越多,假设质量都是1 g时,Mg、Al、Zn这三种金属转移电子的物质的量分别为 mol、 mol、 mol,所以Al-空气电池的理论比能量最高,故B正确;正极上氧气得电子和水反应生成OH-,因为是阴离子交换膜,所以阳离子不能进入正极区,则正极电极反应式为O2+2H2O+4e- 4OH-,故C错误;在M-空气电池中,每转移4n mol电子生成4n mol OH-,原电池中阴离子向负极移动与负极生成的阳离子结合,负极增重4n mol×17 g/mol=68n g,故D正确。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2025鲁教版高中化学必修第二册
第3课时 化学电池
基础过关练
题组一 常见化学电池
1.(2024陕西西安交通大学附属中学期中)电池研发与生产生活领域的发展密切相关,下列有关电池的说法正确的是( )
A.燃料电池的能量转化率可以达到100%
B.手机、照相机和摄像机等电器所用的锂离子电池为二次电池
C.二氧化硅可以制成人造卫星的硅太阳能电池
D.原电池是一种将电能转化为化学能的装置
2.(经典题)(2024山东威海二中月考)微型银—锌电池可用作电子仪器的电源,其电极分别是Ag/Ag2O和Zn,电解质溶液为KOH溶液,电池总反应为Ag2O+Zn+H2O 2Ag+Zn(OH)2。下列说法正确的是( )
A.电池工作过程中,负极发生还原反应
B.电池工作过程中,电解液中OH-向正极移动
C.负极电极反应为Zn+2OH--2e- Zn(OH)2
D.正极电极反应为Ag2O+2H+-2e- 2Ag+H2O
3.(2024广东实验中学月考)关于下列四个常用电化学装置的叙述错误的是( )
图Ⅰ水果电池 图Ⅱ干电池
图Ⅲ铅蓄电池 图Ⅳ氢氧燃料电池
A.图Ⅰ所示电池中,电子从锌片流出
B.图Ⅱ所示干电池中碳棒做负极
C.图Ⅲ所示电池为二次电池
D.图Ⅳ所示电池中正极反应为O2+4H++4e- 2H2O
题组二 燃料电池
4.(2024河南郑州期中)氢氧燃料电池已广泛应用于新能源公交汽车中,其反应原理如图所示。下列说法不正确的是( )
A.该电池工作时化学能转化为电能
B.该电池工作时阴离子向电极a移动
C.该电池工作时电子由电极a沿外电路流向电极b
D.若离子导体选择稀硫酸,则电池正极反应式为O2+4e-+2H2O 4OH-
5.(2024湖北武汉月考)H2S是一种剧毒气体,如图为质子膜H2S燃料电池的示意图,可对H2S废气资源化利用。下列叙述错误的是( )
A.电极a是负极,电池工作时,电子的流动方向是电极a→负载→电极b→质子固体电解质膜→电极a
B.电池工作时,化学能转化为电能和热能
C.电极b上发生的电极反应式为O2+4e-+4H+ 2H2O
D.当电路中通过4 mol电子时,有4 mol H+经质子固体电解质膜进入正极区
能力提升练
题组 化学电池的工作原理
1.(2024福建福州期中)科学家设计了一种新型全固态电池,巧妙利用火星大气中含有的大量CO2为火星探测器供电。该电池工作时的总反应为4Na+3CO2 2Na2CO3+C,下列说法不正确的是( )
A.负极上金属Na失电子发生氧化反应
B.正极电极反应式为3CO2+4e- C+2C
C.该电池中,阴离子由正极移向负极
D.若有0.3 mol CO2反应,流经固体电解质的电子数为0.4NA
2.(2024安徽蚌埠第二中学期中)锂—空气电池的装置示意图如图所示,下列说法不正确的是( )
A.金属锂为负极,发生氧化反应
B.Li+通过有机电解质向电解质水溶液移动
C.正极的电极反应:O2+4e- 2O2-
D.电池每消耗标准状况下56 L空气(O2约占),电路中通过的电子为2 mol
3.(2024山东师范大学附中月考)Hg-Hg2SO4标准电极在生活中常用于测定其他电极的电势,测知Hg-Hg2SO4电极的电势高于Cu电极的电势。以下说法正确的是( )
A.K2SO4溶液可用CCl4代替
B.Hg-Hg2SO4电极的电极反应式为Hg2SO4-2e- 2Hg+S
C.微孔瓷片起到阻隔离子通过的作用
D.若把Cu-CuSO4体系换作Zn-ZnSO4体系,电压表的示数变大
4.(经典题)(2023江西上饶阶段测试)金属(M)—空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为4M+nO2+2nH2O 4M(OH)n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是 ( )
A.采用多孔电极的目的是提高电极与电解质的接触面积,并有利于空气中氧气扩散至电极表面
B.比较M(Mg、Al、Zn)-空气电池,Al-空气电池的理论比能量最高
C.M-空气电池放电过程的正极电极反应式为4Mn++nO2+2nH2O+4ne- 4M(OH)n
D.在M-空气电池中,每转移4n mol电子,负极增重68n g
答案与分层梯度式解析
第3课时 化学电池
基础过关练
1.B 燃料电池的能量转化率虽然高,但仍有少量能量转化为热能而损耗,则能量转化率小于100%,故A错误;锂离子电池能反复充、放电,能循环使用,属于二次电池,故B正确;晶体硅为良好的半导体,可以制成硅太阳能电池,二氧化硅不具有此性质,故C错误;原电池是一种将化学能转化为电能的装置,故D错误。
2.C 电池工作过程中,Zn失电子做负极,发生氧化反应,电极反应为Zn+2OH--2e- Zn(OH)2,A错误、C正确;电池工作过程中,电解液中的OH-向负极移动,B错误;正极Ag2O得电子,发生还原反应,碱性环境下,电极反应为Ag2O+H2O+2e- 2Ag+2OH-,D错误。
3.B 图Ⅰ水果电池中,锌活动性比铜强,锌做负极,铜做正极,电子由负极流出,故A正确;图Ⅱ为酸性锌锰干电池,锌为金属,做负极,碳棒做正极,故B错误;图Ⅲ为铅蓄电池,铅做负极,二氧化铅做正极,是二次电池,即可充电的电池,故C正确;图Ⅳ为氢氧燃料电池,正极电极反应为O2+4H++4e- 2H2O,故D正确。
4.D 该电池工作时,化学能转化为电能,A正确;原电池工作时,阴离子向负极移动,则该电池工作时,阴离子向电极a移动,B正确;原电池工作时,电子由负极沿外电路流向正极,则该电池中的电子由电极a沿外电路流向电极b,C正确;若离子导体选择稀硫酸,则电池工作时,正极反应式为O2+4e-+4H+ 2H2O,D不正确。
5.A 该燃料电池中,电极a为负极,电极b为正极,电子由负极经过外电路流向正极,但不能经过质子固体电解质膜,故A错误;该装置为原电池,化学能主要转化为电能,少部分转化为热能,故B正确;电极b为正极,正极上O2发生得电子的还原反应生成水,电极反应式为O2+4e-+4H+ 2H2O,当电路中通过4 mol电子时,有4 mol H+经质子固体电解质膜进入正极区,故C、D正确。
能力提升练
1.D 根据电池总反应4Na+3CO2 2Na2CO3+C,可知负极上Na发生氧化反应失去电子生成Na+,故A正确;在正极CO2得到电子生成C,结合总反应,知正极电极反应式为3CO2+4e- C+2C,故B正确;放电时阴离子由正极移向负极,故C正确;每3 mol CO2反应,转移4 mol电子,所以0.3 mol CO2反应,转移的电子为0.4 mol,但电子不能流经固体电解质,故D错误。
2.C 在锂—空气电池中,金属锂失电子,发生氧化反应,为负极,A项正确;Li在负极失去电子变成Li+,Li+向电解质水溶液处移动,B项正确;正极的电极反应式为O2+4e-+2H2O 4OH-,C项错误;电池每消耗标准状况下56 L空气(O2约占),所含氧气的物质的量为0.5 mol,则电路中通过的电子的物质的量为2 mol,故D正确。
3.D
4.C 反应物接触面积越大,反应速率越快,所以采用多孔电极的目的是提高电极与电解质的接触面积,并有利于空气中氧气扩散至电极表面,从而提高反应速率,故A正确;单位质量的电极材料失去电子的物质的量越多则释放的电能越多,假设质量都是1 g时,Mg、Al、Zn这三种金属转移电子的物质的量分别为 mol、 mol、 mol,所以Al-空气电池的理论比能量最高,故B正确;正极上氧气得电子和水反应生成OH-,因为是阴离子交换膜,所以阳离子不能进入正极区,则正极电极反应式为O2+2H2O+4e- 4OH-,故C错误;在M-空气电池中,每转移4n mol电子生成4n mol OH-,原电池中阴离子向负极移动与负极生成的阳离子结合,负极增重4n mol×17 g/mol=68n g,故D正确。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
