江西省南昌市2024-2025学年高一上学期11月期中考试化学试题(含答案)
文档属性
| 名称 | 江西省南昌市2024-2025学年高一上学期11月期中考试化学试题(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 496.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-11-23 14:08:59 | ||
图片预览


文档简介
南昌2024-2025学年度上学期期中考试
高一化学试卷
第Ⅰ卷 选择题(42分)
可能用到的元素相对原子质量H 1 C 12 N 14 O 16 Na 23
一、单选题(各小题只有一个选项,本题共14小题,42分)
1.我国古代文化博大精深,下列与化学有关的描述不涉及氧化还原反应的是( )
A.《寒食》中“烧的情况
B.《荀子·劝学》述人类对结冰的认识
C.《抱朴子》中(HgS)烧之成水银,积变又还化过程
D.《天工开物》中“述黑火药的爆炸场景
2.下列分类或归类正确的是( )
液氯、氨水、干冰、 10H2O均为纯净物
、、、均为化合物
明矾、水银、烧碱、硫酸溶液均为电解质
碘酒、淀粉溶液、水雾、纳米材料均为胶体
、、金刚石、石墨均为碳的同素异形体
A. B.
C. D.
3.下列有关说法正确的是( )
A.碳酸钠可称为碳酸盐、钠盐或者碱式盐
B.鸡蛋清、浑浊的河水不可能属于同一类别
C.直径为的粒子不一定是胶体
D.强光通过胶体发生了显著的化学变化
4.设为阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,
B.7.8g Na2O2中含离子总数0.4NA
C.标准状况下,11.2L H2O中含有的分子数为0.5NA
D.粉在标准状况中完全燃烧转移电子数为
5.84消毒环境消毒,其有效成分为( )
A. B. C. D.
6.下列有关氯气及氯水的说法正确的是( )
A.久置氯水酸性比新制氯水强
B.新制的氯水保存在无色玻璃瓶中
C.氯气、次氯酸、次氯酸盐均具有漂白性,可以用于漂白各种产品
D.工业上将氯气通入饱和石灰水中制取漂白粉
7.下列关于钠及其化合物的性质说法错误的是( )
A.为鉴别和两种白色固体,可分别配成溶液做焰色试验实验,观察火焰的颜色
B.热稳定性、水中的溶解性以及与酸反应产生CO2的速率都是:
C.钠不可以从硫酸铜溶液中置换出铜
D.与的阴、阳离子个数比相同
8.下列离子方程式书写正确的是( )
A.过氧化钠与水的反应:Na2O2+2H2O═2Na++2OH-+O2↑
B.向Ca(ClO)2溶液中通入少量CO2的离子方程式:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO
C.水垢可用醋酸溶解:CaCO3+2H+═Ca2++H2O+CO2↑
D.向溶液中滴加少量氯水,反应的离子方程式为:
9.下列实验装置能达到实验目的的是( )
①验证Na和水反应是否为放热反应
②检验Na2O2与H2O反应有O2生成
③观察K2CO3的焰色试验
④比较Na2CO3、NaHCO3的稳定性
A.①② B.①③ C.②④ D.
10.某无色溶液中只含有中的几种,向溶液中滴加酚酞,溶液变红,下列说法正确的是( )
A.一定存在
B.可能存在
C.一定存在,可能存在
D.一定不存在
11.下列实验操作,现象及结论都正确的是( )
选项 实验操作和现象 结论
A 向某溶液中加入稀盐酸至溶液呈酸性,产生使澄清石灰水变浑浊的气体 该溶液中含有
B 对某碱性溶液进行焰色试验,火焰颜色为黄色 该溶液为溶液
C 向某溶液中加入氯化钡溶液有白色沉淀产生,再加过量稀盐酸,沉淀不消失 该溶液中含有
D 向某溶液中加入过量硝酸酸化的溶液,有白色沉淀生成 该溶液中含有
A.A B.B C.C D.D
12.下列各组物质中,因为反应物的用量或反应条件不同而发生不同化学反应的是( )
与与与溶液与溶液与盐酸
溶液与盐酸溶液与溶液
A.除外 B.除外 C.除外 D.除外
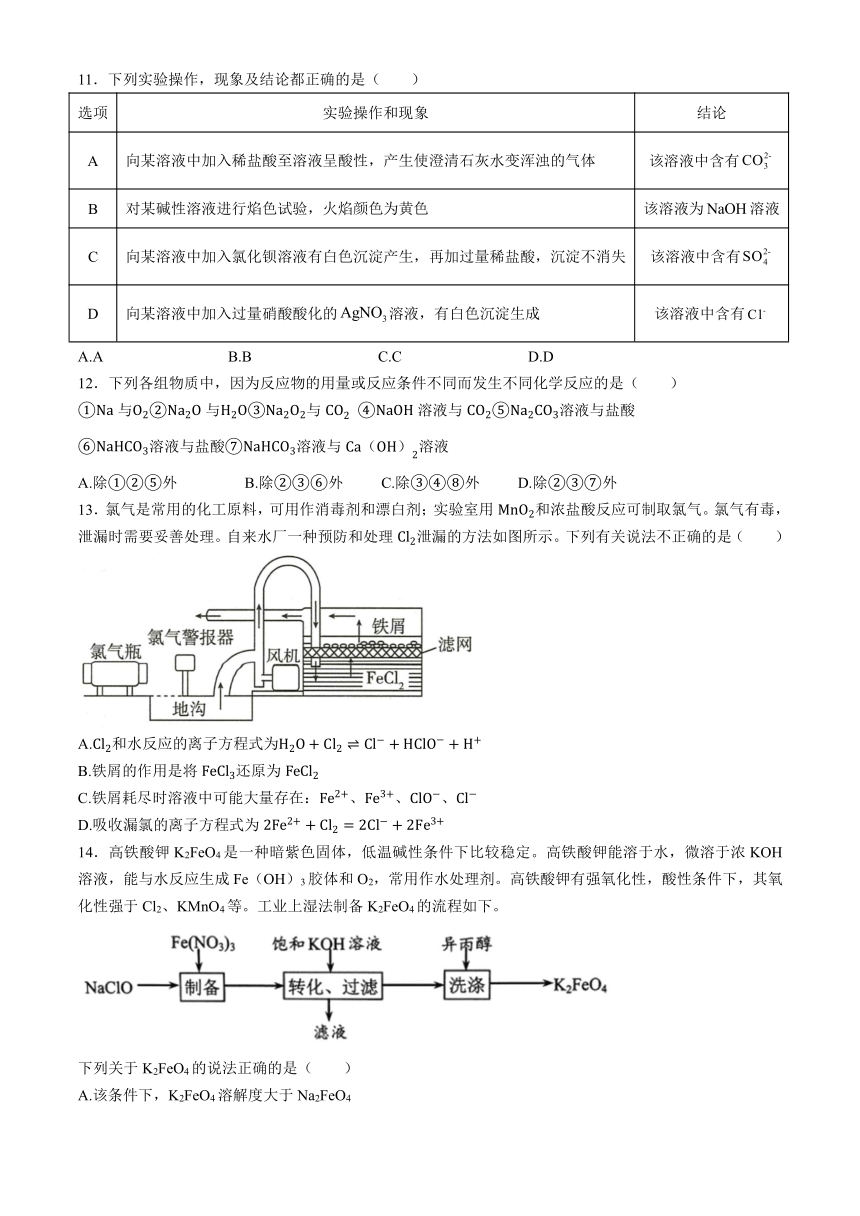
13.氯气是常用的化工原料,可用作消毒剂和漂白剂;实验室用和浓盐酸反应可制取氯气。氯气有毒,泄漏时需要妥善处理。自来水厂一种预防和处理泄漏的方法如图所示。下列有关说法不正确的是( )
A.和水反应的离子方程式为
B.铁屑的作用是将还原为
C.铁屑耗尽时溶液中可能大量存在:、、、
D.吸收漏氯的离子方程式为
14.高铁酸钾K2FeO4是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,微溶于浓KOH溶液,能与水反应生成Fe(OH)3胶体和O2,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下,其氧化性强于Cl2、KMnO4等。工业上湿法制备K2FeO4的流程如下。
下列关于K2FeO4的说法正确的是( )
A.该条件下,K2FeO4溶解度大于Na2FeO4
B.与水反应,每消耗1molK2FeO4转移6mol电子
C.将K2FeO4与盐酸混合使用,可增强其杀菌消毒效果
D.可用丁达尔效应鉴别K2FeO4和KMnO4两种紫红色溶液
第Ⅱ卷 非选择题(58分)
填空题(共4小题,58分)
15.(12分)计算填空:
相同条件下,某容器共收集到体积、体积,该容器中、的物质的量之比是_____;若该容器收集的、两种气体所含分子数相等,则、的质量之比是____________。
和恰好完全反应生成和一定量的气体。若的相对分子质量为,则标准状况下的体积为________。
已知是一种金属,中含有个硝酸根离子,则该硝酸盐的摩尔质量为________。
现有、两种气态化合物,其摩尔质量之比为,相同温度下,在两个相同容积的密闭容器中分别充入、,若两个容器中气体的密度相等,则充有、两种气体的两个容器中的压强之比为______。
标准状况下,将4.6g钠投入足量的水中,充分反应后,生成气体的体积为________。
16.(14分)碳酸钠俗称纯碱,用途非常广泛,我国化学家侯德榜发明了“侯氏制碱法”。某中学化学兴趣小组在实验室中模制备,进一步处理得到产品和,实验流程如图所示。
请回答下列问题:
上述流程中,所涉及的操作方法,包含过滤的是________填序号。
向装置Ⅰ的饱和溶液中通入足量的和,应先通入足量______填。装置Ⅰ中发生反应的化学方程式为________________________________。
检验装置Ⅱ中制备的纯碱含有的方法:取少量该纯碱样品溶于水,________________。
向母液中加入一定量粉末,存在。为使晶体充分析出并分离,根据如图中和溶解度曲线,需采用的操作为、______________、过滤、洗涤、干燥。
整个实验流程中,可循环利用的物质的化学式是_______、_______。
17.(14分)二氧化铈是一种重要的稀土化合物。提纯二氧化铈一种工艺流程如图所示:
稀土化合物中的化合价为_________。
在反应中体现_________填写出稀硫酸、与反应的化学方程式______________________________________。
由反应可知氧化性:填“”或“”或“”,反应中的氧化剂与还原剂的物质的量之比为_________,当消耗转移电子的物质的量为___________。
是汽车尾气净化催化剂中最重要的助剂,工作原理如图所示。
写出过程发生反应的化学方程式_______________________________________________。
18.(18分)氯水是实验室常需临时配制的一种试剂。图甲所示的是实验室配制氯水时的一种常用装置,图乙是某化学实验小组自行设计的一种配制氯水的装置图中的鼓气球是一种具有气体单向阀,可用于向瓶中鼓入空气的仪器。资料:已知常温下固体与浓盐酸反应产生氯气。
实验室还可以用二氧化锰和浓盐酸制取氯气,化学方程式为:________________________;氯水中含有多种粒子,其中除水分子以外的分子为________________________填化学式;需临时配制的原因是____________________用化学方程式表示。
图甲所示装置中,烧杯内的液体是________,烧杯中发生反应的离子方程式是__________________________。
用图乙所示装置配制氯水时,操作步骤如下:
关闭活塞,打开分液漏斗上口的玻璃塞,再打开活塞,将少量浓盐酸注入大试管内。
关闭活塞,盖上分液漏斗上口玻璃塞。浓盐酸和大试管内的高锰酸钾粉末反应产生氯气。
轻轻摇动瓶,使氯气不断溶入水中。
用图乙装置能在较短时间内得到饱和氯水。除了在摇动过程中增大了气体和水的接触面以外,另一个重要原因是_____________________________________。分液漏斗中的浓盐酸应分数次加入试管内。若一次加入太多的浓盐酸,可能引起的后果是__________________________。
配制氯水完成后,不必拆卸装置即可从瓶中取用少量氯水,方法是_________________。
如图向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图所示。下列说法正确的是__________填选项标号。
A.阶段说明氯气溶于水,溶于水的氯气全部与水反应
B.阶段的压强变小,该过程发生了氧化还原反应
C.阶段发生反应的离子方程式为
D.若将换成,所得的压强变化趋势与图相似
高一化学答案
1.B 2.A 3.C 4.D 5.B 6.A 7.B 8.B
9.A 10.C 11.D 12.B 13.C 14.D
15.(每空两分)(1)1:3;22:1 (2)11.2L (3)164 (4)1:2 (5)2.24L
16.(每空两分)
(1)①③
(2)
(3)加入硝酸酸化的硝酸银溶液,若有白色沉淀生成,说明含有氯离子
(4)冷却结晶
(5)、NaCl
17.(每空两分)(1)+4
(2)还原性
(3)> 1:2 4
(4)
18.(每空两分)
(1)
、HClO;
(2)NaOH溶液;
(3)氯气在瓶内产生较大压强,增大了氯气的溶解度;
瓶内产生过多的氯气,瓶内压强过大会使瓶A的橡胶塞弹开
(4)打开活塞2,关闭活塞1,用鼓气球向瓶A中鼓入空气
(5)BCD
高一化学试卷
第Ⅰ卷 选择题(42分)
可能用到的元素相对原子质量H 1 C 12 N 14 O 16 Na 23
一、单选题(各小题只有一个选项,本题共14小题,42分)
1.我国古代文化博大精深,下列与化学有关的描述不涉及氧化还原反应的是( )
A.《寒食》中“烧的情况
B.《荀子·劝学》述人类对结冰的认识
C.《抱朴子》中(HgS)烧之成水银,积变又还化过程
D.《天工开物》中“述黑火药的爆炸场景
2.下列分类或归类正确的是( )
液氯、氨水、干冰、 10H2O均为纯净物
、、、均为化合物
明矾、水银、烧碱、硫酸溶液均为电解质
碘酒、淀粉溶液、水雾、纳米材料均为胶体
、、金刚石、石墨均为碳的同素异形体
A. B.
C. D.
3.下列有关说法正确的是( )
A.碳酸钠可称为碳酸盐、钠盐或者碱式盐
B.鸡蛋清、浑浊的河水不可能属于同一类别
C.直径为的粒子不一定是胶体
D.强光通过胶体发生了显著的化学变化
4.设为阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,
B.7.8g Na2O2中含离子总数0.4NA
C.标准状况下,11.2L H2O中含有的分子数为0.5NA
D.粉在标准状况中完全燃烧转移电子数为
5.84消毒环境消毒,其有效成分为( )
A. B. C. D.
6.下列有关氯气及氯水的说法正确的是( )
A.久置氯水酸性比新制氯水强
B.新制的氯水保存在无色玻璃瓶中
C.氯气、次氯酸、次氯酸盐均具有漂白性,可以用于漂白各种产品
D.工业上将氯气通入饱和石灰水中制取漂白粉
7.下列关于钠及其化合物的性质说法错误的是( )
A.为鉴别和两种白色固体,可分别配成溶液做焰色试验实验,观察火焰的颜色
B.热稳定性、水中的溶解性以及与酸反应产生CO2的速率都是:
C.钠不可以从硫酸铜溶液中置换出铜
D.与的阴、阳离子个数比相同
8.下列离子方程式书写正确的是( )
A.过氧化钠与水的反应:Na2O2+2H2O═2Na++2OH-+O2↑
B.向Ca(ClO)2溶液中通入少量CO2的离子方程式:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO
C.水垢可用醋酸溶解:CaCO3+2H+═Ca2++H2O+CO2↑
D.向溶液中滴加少量氯水,反应的离子方程式为:
9.下列实验装置能达到实验目的的是( )
①验证Na和水反应是否为放热反应
②检验Na2O2与H2O反应有O2生成
③观察K2CO3的焰色试验
④比较Na2CO3、NaHCO3的稳定性
A.①② B.①③ C.②④ D.
10.某无色溶液中只含有中的几种,向溶液中滴加酚酞,溶液变红,下列说法正确的是( )
A.一定存在
B.可能存在
C.一定存在,可能存在
D.一定不存在
11.下列实验操作,现象及结论都正确的是( )
选项 实验操作和现象 结论
A 向某溶液中加入稀盐酸至溶液呈酸性,产生使澄清石灰水变浑浊的气体 该溶液中含有
B 对某碱性溶液进行焰色试验,火焰颜色为黄色 该溶液为溶液
C 向某溶液中加入氯化钡溶液有白色沉淀产生,再加过量稀盐酸,沉淀不消失 该溶液中含有
D 向某溶液中加入过量硝酸酸化的溶液,有白色沉淀生成 该溶液中含有
A.A B.B C.C D.D
12.下列各组物质中,因为反应物的用量或反应条件不同而发生不同化学反应的是( )
与与与溶液与溶液与盐酸
溶液与盐酸溶液与溶液
A.除外 B.除外 C.除外 D.除外
13.氯气是常用的化工原料,可用作消毒剂和漂白剂;实验室用和浓盐酸反应可制取氯气。氯气有毒,泄漏时需要妥善处理。自来水厂一种预防和处理泄漏的方法如图所示。下列有关说法不正确的是( )
A.和水反应的离子方程式为
B.铁屑的作用是将还原为
C.铁屑耗尽时溶液中可能大量存在:、、、
D.吸收漏氯的离子方程式为
14.高铁酸钾K2FeO4是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,微溶于浓KOH溶液,能与水反应生成Fe(OH)3胶体和O2,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下,其氧化性强于Cl2、KMnO4等。工业上湿法制备K2FeO4的流程如下。
下列关于K2FeO4的说法正确的是( )
A.该条件下,K2FeO4溶解度大于Na2FeO4
B.与水反应,每消耗1molK2FeO4转移6mol电子
C.将K2FeO4与盐酸混合使用,可增强其杀菌消毒效果
D.可用丁达尔效应鉴别K2FeO4和KMnO4两种紫红色溶液
第Ⅱ卷 非选择题(58分)
填空题(共4小题,58分)
15.(12分)计算填空:
相同条件下,某容器共收集到体积、体积,该容器中、的物质的量之比是_____;若该容器收集的、两种气体所含分子数相等,则、的质量之比是____________。
和恰好完全反应生成和一定量的气体。若的相对分子质量为,则标准状况下的体积为________。
已知是一种金属,中含有个硝酸根离子,则该硝酸盐的摩尔质量为________。
现有、两种气态化合物,其摩尔质量之比为,相同温度下,在两个相同容积的密闭容器中分别充入、,若两个容器中气体的密度相等,则充有、两种气体的两个容器中的压强之比为______。
标准状况下,将4.6g钠投入足量的水中,充分反应后,生成气体的体积为________。
16.(14分)碳酸钠俗称纯碱,用途非常广泛,我国化学家侯德榜发明了“侯氏制碱法”。某中学化学兴趣小组在实验室中模制备,进一步处理得到产品和,实验流程如图所示。
请回答下列问题:
上述流程中,所涉及的操作方法,包含过滤的是________填序号。
向装置Ⅰ的饱和溶液中通入足量的和,应先通入足量______填。装置Ⅰ中发生反应的化学方程式为________________________________。
检验装置Ⅱ中制备的纯碱含有的方法:取少量该纯碱样品溶于水,________________。
向母液中加入一定量粉末,存在。为使晶体充分析出并分离,根据如图中和溶解度曲线,需采用的操作为、______________、过滤、洗涤、干燥。
整个实验流程中,可循环利用的物质的化学式是_______、_______。
17.(14分)二氧化铈是一种重要的稀土化合物。提纯二氧化铈一种工艺流程如图所示:
稀土化合物中的化合价为_________。
在反应中体现_________填写出稀硫酸、与反应的化学方程式______________________________________。
由反应可知氧化性:填“”或“”或“”,反应中的氧化剂与还原剂的物质的量之比为_________,当消耗转移电子的物质的量为___________。
是汽车尾气净化催化剂中最重要的助剂,工作原理如图所示。
写出过程发生反应的化学方程式_______________________________________________。
18.(18分)氯水是实验室常需临时配制的一种试剂。图甲所示的是实验室配制氯水时的一种常用装置,图乙是某化学实验小组自行设计的一种配制氯水的装置图中的鼓气球是一种具有气体单向阀,可用于向瓶中鼓入空气的仪器。资料:已知常温下固体与浓盐酸反应产生氯气。
实验室还可以用二氧化锰和浓盐酸制取氯气,化学方程式为:________________________;氯水中含有多种粒子,其中除水分子以外的分子为________________________填化学式;需临时配制的原因是____________________用化学方程式表示。
图甲所示装置中,烧杯内的液体是________,烧杯中发生反应的离子方程式是__________________________。
用图乙所示装置配制氯水时,操作步骤如下:
关闭活塞,打开分液漏斗上口的玻璃塞,再打开活塞,将少量浓盐酸注入大试管内。
关闭活塞,盖上分液漏斗上口玻璃塞。浓盐酸和大试管内的高锰酸钾粉末反应产生氯气。
轻轻摇动瓶,使氯气不断溶入水中。
用图乙装置能在较短时间内得到饱和氯水。除了在摇动过程中增大了气体和水的接触面以外,另一个重要原因是_____________________________________。分液漏斗中的浓盐酸应分数次加入试管内。若一次加入太多的浓盐酸,可能引起的后果是__________________________。
配制氯水完成后,不必拆卸装置即可从瓶中取用少量氯水,方法是_________________。
如图向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图所示。下列说法正确的是__________填选项标号。
A.阶段说明氯气溶于水,溶于水的氯气全部与水反应
B.阶段的压强变小,该过程发生了氧化还原反应
C.阶段发生反应的离子方程式为
D.若将换成,所得的压强变化趋势与图相似
高一化学答案
1.B 2.A 3.C 4.D 5.B 6.A 7.B 8.B
9.A 10.C 11.D 12.B 13.C 14.D
15.(每空两分)(1)1:3;22:1 (2)11.2L (3)164 (4)1:2 (5)2.24L
16.(每空两分)
(1)①③
(2)
(3)加入硝酸酸化的硝酸银溶液,若有白色沉淀生成,说明含有氯离子
(4)冷却结晶
(5)、NaCl
17.(每空两分)(1)+4
(2)还原性
(3)> 1:2 4
(4)
18.(每空两分)
(1)
、HClO;
(2)NaOH溶液;
(3)氯气在瓶内产生较大压强,增大了氯气的溶解度;
瓶内产生过多的氯气,瓶内压强过大会使瓶A的橡胶塞弹开
(4)打开活塞2,关闭活塞1,用鼓气球向瓶A中鼓入空气
(5)BCD
同课章节目录
