3.2 课时1 铁合金和铝合金(共29张PPT)课件 2024-2025学年高一化学人教版(2019)必修一
文档属性
| 名称 | 3.2 课时1 铁合金和铝合金(共29张PPT)课件 2024-2025学年高一化学人教版(2019)必修一 |  | |
| 格式 | pptx | ||
| 文件大小 | 19.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-11-27 17:59:44 | ||
图片预览







文档简介
(共29张PPT)
铁合金 铝合金
第三章 铁 金属材料
宏观辨识与微观探析:
以铁合金、铝合金为例,能从元素组成上对合金进行分类,并认识不同类型金属材料组成、性能与应用的联系,强化性能决定用途的观念。
证据推理与模型认知:
通过对化学实验现象的观察进行适度的推理,建立证据意识,能基于证据对物质组成、结构及其变化提出可能的假设,通过分析推理加以证实。
科学探究与创新意识:
通过完成铝及其化合物的实验,初步体验有序地、全面地、敏锐地观察实验现象,并能准确地用语言描述,尝试对现象进行分析、归纳,了解科学探究的基本方法,培养初步的科学探究能力。
金属材料的发展历史
商朝
后母戊鼎
东汉
马踏飞燕
鸟巢体育馆
和谐号动车
春秋
铜柄铁剑
神州飞船
一、认识合金
资料卡
青铜是合金冶炼史上最早的合金,通过往纯铜中加入锡或铅的合金炼成。相较于紫铜(及纯铜),青铜硬度高且熔点低,铸造性好,更适合制作刀剑及工具
一、认识合金
资料卡
青铜是合金冶炼史上最早的合金,通过往纯铜中加入锡或铅的合金炼成。相较于紫铜(及纯铜),青铜硬度高且熔点低,铸造性好,更适合制作刀剑及工具
商朝
后母戊鼎
春秋
铜柄铁剑
东汉
马踏飞燕
什么是合金?
合金的性质与其成分金属有何差异?
一、认识合金
【定义】由两种或两种以上的金属与金属(非金属)熔合而成的具有金属特性的物质。
【性质】
1.硬度:合金的硬度一般大于其成分金属。
2.熔点:合金的熔点多数低于其成分金属。
3.化学性质:合金中各成分金属的化学性质不变。
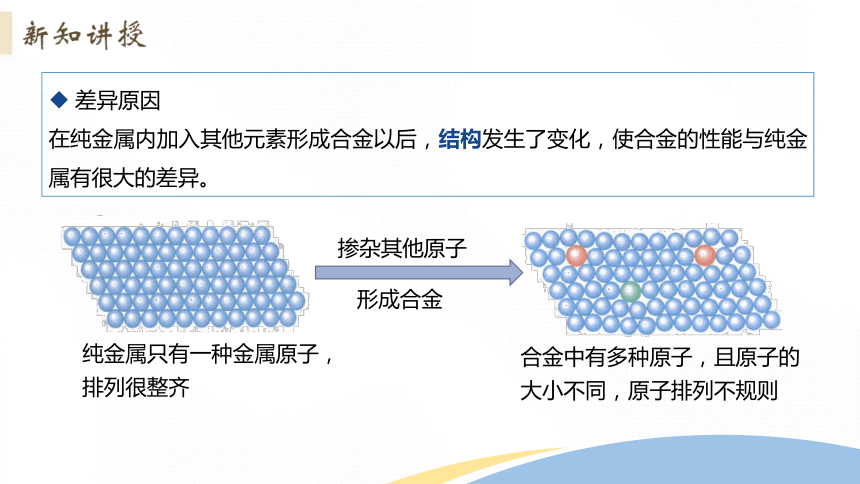
合金的硬度为什么比纯金属大?
纯金属只有一种金属原子,排列很整齐
合金中有多种原子,且原子的大小不同,原子排列不规则
掺杂其他原子
形成合金
差异原因
在纯金属内加入其他元素形成合金以后,结构发生了变化,使合金的性能与纯金属有很大的差异。
铁的储量远大于铜,为什么青铜器会优先于铁器出现?
春秋后期,人们依然能应用生铁冶铸技术冶炼出质硬脆而脆的生铁。生铁冶铸是指在高温下将铁矿石还原成铁,得到的铁会吸收碳,其熔点随之降低,渗碳2%—4.3%称为生铁。生铁可铸不可锻,古代冶金师们不断改进炼铁工艺,发明了“百炼钢技术”和“灌钢技术”,降低含碳量,提高韧性,降低脆性,含碳量将至0.03%—2%即为钢。
资料卡片
二、铁合金
生铁和钢
生铁 钢
含碳量 2%~4.3% 0.03%~2%
性能 生铁硬度大,抗压、性脆,可铸不可锻 强度大,韧性好,有良好的延展性,机械性能好,
可铸可锻
钢是用量最大、用途最广的合金
二、铁合金
钢
碳素钢 合金钢(特种钢)
相同点 都是合金 不同点 含碳量较低的碳合金 在碳素钢中加入了合金元素(不锈钢主要加入镍和铬)
性能 含碳量高的碳素钢,硬度大;含碳量低的碳素钢,韧性强 不锈钢在空气中比较稳定,不易生锈,具有很强的抗腐蚀能力
二、铁合金
铁合金
生铁
钢
碳素钢
合金钢
低碳钢
中碳钢
高碳钢
(2%—4.3%)
(0.03%—2%)
根据含碳量不同
(低于0.3%)
(0.3%—0.6%)
(高于0.6%)
韧性、焊接性好,但强度低,用于制造钢板、钢丝和钢管等
强度高,韧性及加工性好,用于 制造钢轨、车轮和建材等
硬而脆,热处理后弹性好,用于 制造器械、弹簧和刀具等
根据化学成分
根据含碳量不同
含碳量不同的铁合金微观结构不同,铁、碳原子的排列方式不同,决定了其不同的性能和用途
调节合金性能的基本措施
1.改变合金元素的种类
2.改变合金元素的含量
3.改变生成合金的条件
铝制易拉罐——碳酸饮料的不二选择
思考:
碳酸饮料易拉罐为何选择了铝质材料?
三、铝合金
问题1.铝作为较活泼金属,其制品的耐腐蚀性从何而来?
铝制餐具
铝合金门窗
失去3个电子
铝的化学性质活泼,具有较强的还原性。
K Ca Na Mg Zn Fe Sn Pb H Cu Hg …
Al
3+
铝是一种活泼的金属,为什么却能在空气中稳定的存在?
铝表面会与空气中氧气生成一层致密的氧化铝薄膜,保护内部金属。
4Al+3O2 = 2Al2O3
在一支试管中加入5 mL盐酸,再向其中放入一小块铝片,观察现象。一段时间后,将点燃的木条放在试管口,你观察到什么现象
在两支试管中分别加入少量NaOH溶液,然后向其中一支试管中放入一小块铝片,向另一支试管中放入用砂纸仔细打磨过(除去表面的氧化膜)的一小块铝片。观察现象。一段时间后,将点燃的木条分别放在两支试管口,你观察到什么现象
实验操作
实验现象
实验原理
铝片逐渐溶解,一段时间后产生气泡,试管壁有发热现象;将点燃的木条放在试管口,观察到淡蓝色火焰,爆鸣声。
Al2O3+6H+===2Al3++3H2O,
2Al+6H+ ===2Al3++3H2↑
实验操作
实验现象
实验原理 开始没有气泡,一段时间后才产生气泡,铝片逐渐溶解,将点燃的木条放在试管口有爆鸣声。
Al2O3+2OH- + 3H2O ===2Al(OH)4-
立即产生大量气泡,铝片逐渐溶解,将点燃的木条放在试管口有爆鸣声。
两支试管均放出H2,铝、氧化铝均能与NaOH溶液反应。
6H2O +2Al+ 2OH- === 2Al(OH)4- +3H2↑
2Al + 2NaOH +6H2O = 2Na[ Al(OH)4]+ 3H2↑
Al2O3 + 2NaOH + 3H2O = 2Na[ Al(OH)4]
铝制餐具为何不易用来蒸煮或长时间存放酸性或碱性食品?
由于Al和Al2O3均能与酸、碱反应,因此铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物。
为什么生活中很少见到以纯铝为材料的制品?
纯铝的硬度和强度都比较小,不适合作为生产生活中的材料使用,使用较多的是具有不同组成和性质的铝合金。
铝合金:铝合金是目前用途广泛的合金之一
主要组成元素 主要特性 主要用途
铝合金 硬铝 Al、Mg、Cu、Si、Mn等(Mg 0.5%、Cu 4%、Si 0.7%、Mn 0.5%) 密度小,强度和硬度都比纯铝的大,具有较强的抗腐蚀能力 用于汽车、飞机、火箭、船舶等制造业
镁铝合金 Mg、Al 强度和硬度都比纯铝和纯镁的大 用于火箭、飞机、轮船等制造业
铝
存在
物理性质
化学性质
硬铝
铝、氧化铝的性质——与酸反应
铝、氧化铝的性质——与碱反应
金属材料
合金
铁合金
铝合金
生铁
钢
碳素钢
合金钢
铝和氧化铝
1.下列关于合金的叙述中正确的是( )
A.合金是由两种或多种金属熔合而成的
B.日常生活中用到的五角硬币属于铜合金
C.合金在任何情况下都比单一金属性能优良
D.钢不属于合金
B
2.下列叙述正确的是( )
A.通过物理变化使铁制品表面生成致密的氧化膜,可以防止生锈
B.常见的合金钢主要有硅钢、锰钢、钨钢和不锈钢
C.氧化物只能作氧化剂,不能作还原剂
D.生铁中的球墨铸铁,没有机械强度,所以在任何场合都不可以代替钢
B
铁合金 铝合金
第三章 铁 金属材料
宏观辨识与微观探析:
以铁合金、铝合金为例,能从元素组成上对合金进行分类,并认识不同类型金属材料组成、性能与应用的联系,强化性能决定用途的观念。
证据推理与模型认知:
通过对化学实验现象的观察进行适度的推理,建立证据意识,能基于证据对物质组成、结构及其变化提出可能的假设,通过分析推理加以证实。
科学探究与创新意识:
通过完成铝及其化合物的实验,初步体验有序地、全面地、敏锐地观察实验现象,并能准确地用语言描述,尝试对现象进行分析、归纳,了解科学探究的基本方法,培养初步的科学探究能力。
金属材料的发展历史
商朝
后母戊鼎
东汉
马踏飞燕
鸟巢体育馆
和谐号动车
春秋
铜柄铁剑
神州飞船
一、认识合金
资料卡
青铜是合金冶炼史上最早的合金,通过往纯铜中加入锡或铅的合金炼成。相较于紫铜(及纯铜),青铜硬度高且熔点低,铸造性好,更适合制作刀剑及工具
一、认识合金
资料卡
青铜是合金冶炼史上最早的合金,通过往纯铜中加入锡或铅的合金炼成。相较于紫铜(及纯铜),青铜硬度高且熔点低,铸造性好,更适合制作刀剑及工具
商朝
后母戊鼎
春秋
铜柄铁剑
东汉
马踏飞燕
什么是合金?
合金的性质与其成分金属有何差异?
一、认识合金
【定义】由两种或两种以上的金属与金属(非金属)熔合而成的具有金属特性的物质。
【性质】
1.硬度:合金的硬度一般大于其成分金属。
2.熔点:合金的熔点多数低于其成分金属。
3.化学性质:合金中各成分金属的化学性质不变。
合金的硬度为什么比纯金属大?
纯金属只有一种金属原子,排列很整齐
合金中有多种原子,且原子的大小不同,原子排列不规则
掺杂其他原子
形成合金
差异原因
在纯金属内加入其他元素形成合金以后,结构发生了变化,使合金的性能与纯金属有很大的差异。
铁的储量远大于铜,为什么青铜器会优先于铁器出现?
春秋后期,人们依然能应用生铁冶铸技术冶炼出质硬脆而脆的生铁。生铁冶铸是指在高温下将铁矿石还原成铁,得到的铁会吸收碳,其熔点随之降低,渗碳2%—4.3%称为生铁。生铁可铸不可锻,古代冶金师们不断改进炼铁工艺,发明了“百炼钢技术”和“灌钢技术”,降低含碳量,提高韧性,降低脆性,含碳量将至0.03%—2%即为钢。
资料卡片
二、铁合金
生铁和钢
生铁 钢
含碳量 2%~4.3% 0.03%~2%
性能 生铁硬度大,抗压、性脆,可铸不可锻 强度大,韧性好,有良好的延展性,机械性能好,
可铸可锻
钢是用量最大、用途最广的合金
二、铁合金
钢
碳素钢 合金钢(特种钢)
相同点 都是合金 不同点 含碳量较低的碳合金 在碳素钢中加入了合金元素(不锈钢主要加入镍和铬)
性能 含碳量高的碳素钢,硬度大;含碳量低的碳素钢,韧性强 不锈钢在空气中比较稳定,不易生锈,具有很强的抗腐蚀能力
二、铁合金
铁合金
生铁
钢
碳素钢
合金钢
低碳钢
中碳钢
高碳钢
(2%—4.3%)
(0.03%—2%)
根据含碳量不同
(低于0.3%)
(0.3%—0.6%)
(高于0.6%)
韧性、焊接性好,但强度低,用于制造钢板、钢丝和钢管等
强度高,韧性及加工性好,用于 制造钢轨、车轮和建材等
硬而脆,热处理后弹性好,用于 制造器械、弹簧和刀具等
根据化学成分
根据含碳量不同
含碳量不同的铁合金微观结构不同,铁、碳原子的排列方式不同,决定了其不同的性能和用途
调节合金性能的基本措施
1.改变合金元素的种类
2.改变合金元素的含量
3.改变生成合金的条件
铝制易拉罐——碳酸饮料的不二选择
思考:
碳酸饮料易拉罐为何选择了铝质材料?
三、铝合金
问题1.铝作为较活泼金属,其制品的耐腐蚀性从何而来?
铝制餐具
铝合金门窗
失去3个电子
铝的化学性质活泼,具有较强的还原性。
K Ca Na Mg Zn Fe Sn Pb H Cu Hg …
Al
3+
铝是一种活泼的金属,为什么却能在空气中稳定的存在?
铝表面会与空气中氧气生成一层致密的氧化铝薄膜,保护内部金属。
4Al+3O2 = 2Al2O3
在一支试管中加入5 mL盐酸,再向其中放入一小块铝片,观察现象。一段时间后,将点燃的木条放在试管口,你观察到什么现象
在两支试管中分别加入少量NaOH溶液,然后向其中一支试管中放入一小块铝片,向另一支试管中放入用砂纸仔细打磨过(除去表面的氧化膜)的一小块铝片。观察现象。一段时间后,将点燃的木条分别放在两支试管口,你观察到什么现象
实验操作
实验现象
实验原理
铝片逐渐溶解,一段时间后产生气泡,试管壁有发热现象;将点燃的木条放在试管口,观察到淡蓝色火焰,爆鸣声。
Al2O3+6H+===2Al3++3H2O,
2Al+6H+ ===2Al3++3H2↑
实验操作
实验现象
实验原理 开始没有气泡,一段时间后才产生气泡,铝片逐渐溶解,将点燃的木条放在试管口有爆鸣声。
Al2O3+2OH- + 3H2O ===2Al(OH)4-
立即产生大量气泡,铝片逐渐溶解,将点燃的木条放在试管口有爆鸣声。
两支试管均放出H2,铝、氧化铝均能与NaOH溶液反应。
6H2O +2Al+ 2OH- === 2Al(OH)4- +3H2↑
2Al + 2NaOH +6H2O = 2Na[ Al(OH)4]+ 3H2↑
Al2O3 + 2NaOH + 3H2O = 2Na[ Al(OH)4]
铝制餐具为何不易用来蒸煮或长时间存放酸性或碱性食品?
由于Al和Al2O3均能与酸、碱反应,因此铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物。
为什么生活中很少见到以纯铝为材料的制品?
纯铝的硬度和强度都比较小,不适合作为生产生活中的材料使用,使用较多的是具有不同组成和性质的铝合金。
铝合金:铝合金是目前用途广泛的合金之一
主要组成元素 主要特性 主要用途
铝合金 硬铝 Al、Mg、Cu、Si、Mn等(Mg 0.5%、Cu 4%、Si 0.7%、Mn 0.5%) 密度小,强度和硬度都比纯铝的大,具有较强的抗腐蚀能力 用于汽车、飞机、火箭、船舶等制造业
镁铝合金 Mg、Al 强度和硬度都比纯铝和纯镁的大 用于火箭、飞机、轮船等制造业
铝
存在
物理性质
化学性质
硬铝
铝、氧化铝的性质——与酸反应
铝、氧化铝的性质——与碱反应
金属材料
合金
铁合金
铝合金
生铁
钢
碳素钢
合金钢
铝和氧化铝
1.下列关于合金的叙述中正确的是( )
A.合金是由两种或多种金属熔合而成的
B.日常生活中用到的五角硬币属于铜合金
C.合金在任何情况下都比单一金属性能优良
D.钢不属于合金
B
2.下列叙述正确的是( )
A.通过物理变化使铁制品表面生成致密的氧化膜,可以防止生锈
B.常见的合金钢主要有硅钢、锰钢、钨钢和不锈钢
C.氧化物只能作氧化剂,不能作还原剂
D.生铁中的球墨铸铁,没有机械强度,所以在任何场合都不可以代替钢
B
