天津市滨海新区塘沽紫云中学2024-2025学年高二上期中——化学试卷(含答案)
文档属性
| 名称 | 天津市滨海新区塘沽紫云中学2024-2025学年高二上期中——化学试卷(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-03 06:57:04 | ||
图片预览



文档简介
天津市滨海新区塘沽紫云中学教育集团校
2024—2025学年度第一学期高二年级期中检测化学学科试题
本试卷分为第Ⅰ卷(选择题) 和第Ⅱ卷(非选择题) 两部分,共100分,考试用时60分钟。第Ⅰ卷1到6页, 第Ⅱ卷7到10页。
答卷前,考生务必将自己的姓名、班号、考场号和座位号填写在答题卡上,将考号填、涂准确; 答卷时,考生务必将选择题答案涂在答题卡上,非选择题答在答题纸上、答在试卷上无效。
祝各位考生考试顺利!
第Ⅰ卷 选择题 (共40分)
单项选择题(每小题2分,共40分。每小题给出的四个选项中,只有一个选项是正确的。)
1. 下列说法错误的是 ( )
A. 泡沫灭火器中常使用的原料是碳酸氢钠和硫酸铝
B. 加热纯碱溶液可以增强清洗油污效果
C. 血浆的pH降到7.2以下会引起酸中毒,升到7.5以上会引起碱中毒,可以通过口服少量氢氧化钠稀溶液或稀盐酸进行治疗
D. 明矾能够净水,是因为Al 水解生成 Al(OH) 胶体可使水中细小的悬浮颗粒聚集成较大颗粒而沉降
2. 下列溶液因溶质的水解而呈酸性的是 ( )
A. K CO 溶液 B. NH Cl溶液 C. NaHSO 溶液 溶液
3. 依据下列反应(), 推论正确的是 ( )
A. 已知: 则稀盐酸与稀氨水完全反应生成
1mol H O(l), 放出的热量小于57.3 kJ
H的燃烧热为:
则
则该反应在任何温度下都能自发进行
高二化学 第 1 页 共10页
4. 已知: 不同条件下反应过程能量变化如图所示。下列说法中错误的是 20( )
A. 反应的
B. 过程b使用了催化剂
C. 使用催化剂,可以改变反应历程,从而提高 的平衡转化率
D. 活化分子具有的平均能量与反应物分子具有的平均能量之差,为反应的活化能
5.已知: 下列关于稀硫酸和稀NaOH溶液中和反应反应热的测定的表述,正确的是 ( )
A. 将量筒中的NaOH 溶液沿玻璃棒缓慢倒入量热计的内筒
B. 用如图所示装置可完成本实验
C. 取一次测量所得温度差作为该反应热的计算依据
高二化学 第 2 页 共10页
6. 下列有关化学反应速率的说法,错误的是 ( )
A. 用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率
B. Al在O 中燃烧生成Al O ,用铝粉代替铝片,可加快反应速率
C. 二氧化硫的催化氧化是一个放热反应,升高温度,反应速率加快
恒容下充入 He,化学反应速率不变
7. 对于一定条件下进行的化学反应: 改变下列条件,可以提高反应物中活化分子百分数的是 ( )
①增大反应物浓度 ②升高温度 ③加入催化剂 ④增大压强
A. ①② B. ①④ C. ①②③ D. ②③
8. 下列有关化学平衡的描述,错误的是 ( )
恒温恒容条件下,加入HI,容器内气体颜色变深
,恒容条件下,升高温度,容器内气体颜色变深
恒温恒容条件下,通入 平衡不移动
加入少量NaOH 固体,溶液颜色变浅
9. 研究NO 、SO 等气体的无害化处理对治理大气污染、建设生态文明具有重要意义。将 与
SO 以体积比1:3置于恒温恒容容器中,发生反应:
下列能说明该反应达到平衡状态的是 ( )
A. 混合气体的颜色保持不变 B. SO 和NO的体积比保持不变
C. 每生成 消耗 D. 容器内气体的平均摩尔质量保持不变
10. 在一定温度下的密闭容器中发生反应: 平衡时测得A的浓度为
0.80mol/L。保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得A的浓度为
0.50mol/L。下列判断正确的是 ( )
A. B. B的转化率减小 C. 平衡向正反应方向移动 D. C的体积分数增大
高二化学 第 3 页 共10页
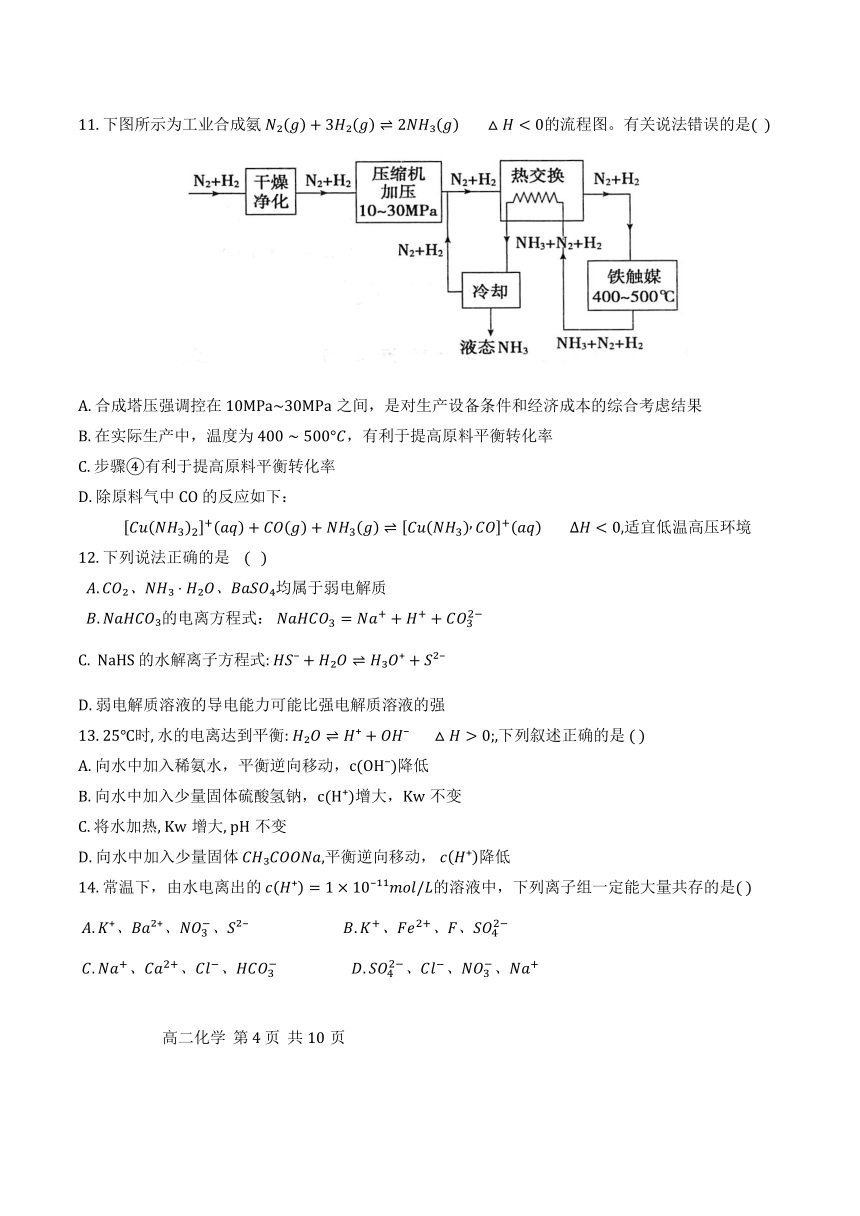
11. 下图所示为工业合成氨 的流程图。有关说法错误的是( )
A. 合成塔压强调控在 10MPa~30MPa之间,是对生产设备条件和经济成本的综合考虑结果
B. 在实际生产中,温度为 ,有利于提高原料平衡转化率
C. 步骤④有利于提高原料平衡转化率
D. 除原料气中CO 的反应如下:
适宜低温高压环境
12. 下列说法正确的是 ( )
均属于弱电解质
的电离方程式:
C. NaHS 的水解离子方程式:
D. 弱电解质溶液的导电能力可能比强电解质溶液的强
13. 25℃时, 水的电离达到平衡: 下列叙述正确的是 ( )
A. 向水中加入稀氨水,平衡逆向移动,c(OH )降低
B. 向水中加入少量固体硫酸氢钠,c(H )增大,Kw不变
C. 将水加热, Kw增大, pH不变
D. 向水中加入少量固体 平衡逆向移动, 降低
14. 常温下,由水电离出的 的溶液中,下列离子组一定能大量共存的是( )
高二化学 第 4 页 共10页
15. 下列说法正确的是 ( )
A. pH均为3 的醋酸和盐酸两种溶液,温度都升高20℃后,盐酸的pH大
B. 氨水、NaOH 溶液中分别加入适量氯化铵晶体后,前者pH增大,后者pH减小
C. 等浓度的下列溶液中, ①NH Al(SO ) 、②NH Cl、③CH COONH 、④NH ·H O; c(NH )
由大到小的顺序是: ③②①④
D. 常温下, pH=2的某酸HA与pH=12 的某碱BOH等体积混合溶液呈酸性, 则HA 为弱酸, BOH 为强碱
16. 下列说法错误的是 ( )
A. 实验室制备 Cl 时,用饱和食盐水溶液除去Cl 中的HCl气体,运用了平衡移动原理
B. 用 AICl 溶液和 Na S 溶液能制得硫化铝
C. 配制 FeSO 溶液时常加入稀硫酸和铁屑
D. 用饱和氯化铵溶液可以清洗钢铁表面的锈迹
17. 将6molA 和2molB 充入2L 的恒容密闭容器中, 发生的反应: 3A(s)+B(g) C(g)+2D(g),
5min后反应达到平衡, 测得C 的平均反应速率为0.1mol/(L· min), 下列结论正确的是( )
A. A 的平均反应速率为0.3mol/(L· min) B. 平衡时, C 的浓度为0.5mol/L
C. 平衡时, B的转化率为20% D. 平衡时,容器内压强为原来的7/8
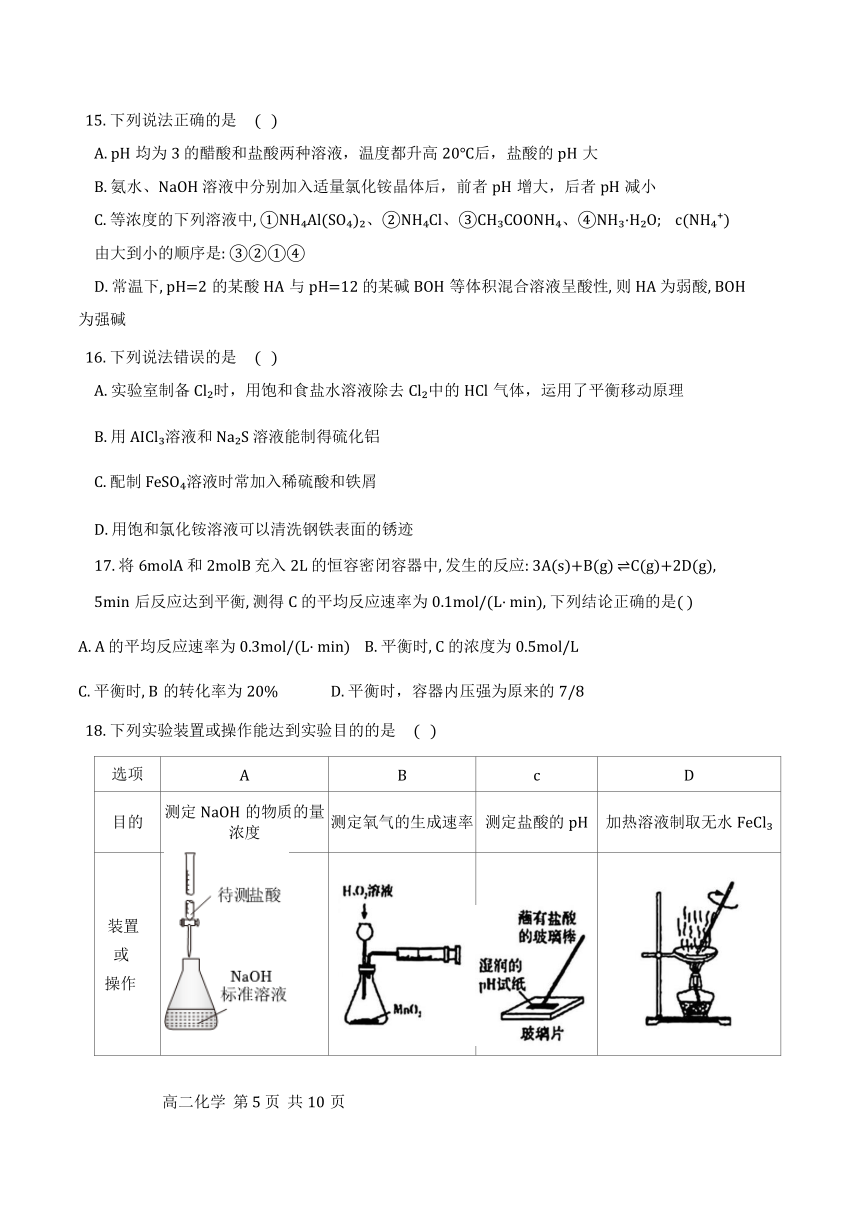
18. 下列实验装置或操作能达到实验目的的是 ( )
选项 A B c D
目的 测定NaOH的物质的量浓度 测定氧气的生成速率 测定盐酸的pH 加热溶液制取无水FeCl
装置 或 操作
高二化学 第 5 页 共10页
19. 下列叙述与图对应的是 ( )
A. 对于可逆反应: 图①表示在t 时刻充入了一定量的 平衡逆向移动
B. 由图②可知, 满足反应:
C. 图③表示的反应方程式为:
D. 对于反应 图④y轴可以表示Y的百分含量
20. 叠氮酸(HN )是一种弱酸。常温下, 向20mL 0.1m ol/L 的 溶液中逐滴加入0.1m ol/L NaOH 溶液。测得滴定过程中溶液的pH 随V(NaOH)变化如图所示,下列说法正确的( )
A. 该滴定过程应该选择甲基橙作为指示剂
B. 点②溶液中:
C. 常温下, 的数量级为
D. 点③溶液中,水电离出的
高二化学 第 6 页 共10页
第II卷 非选择题 (共60分)
21.(26分) 已知在 时,醋酸、次氯酸、碳酸和亚硫酸的电离平衡常数如下表所示:
电解质 电离平衡常数
CH COOH K =1.75×10
HClO K =4.0×10
H CO K =4.5×10 Ka =4.7×10 11
H SO K =1.4×10 K =6.0×10
在水溶液中的电离方程式为 。
的电离平衡常数表达式 Ka= 。
(2)根据上表可知, 酸性CH COOH HClO(填“>”“<”或“=”, 下同), 在相同条件下,试比较同浓度CH COONa、NaClO溶液的pH: CH COONa NaClO。
在溶液中的水解离子方程式为 向0.1mol/L 的 溶液中加入少量下列物质,其水解程度增大的是 。
固体 B. NH Cl固体 C. NaCl溶液 D. NaClO固体 E. HCl气体
(4)0.1mol/L 的NaHSO 溶液显 (填“中性”“酸性”或“碱性”), 该溶液中
(填), = mol/L.
(5)物质的量浓度均为0.1mol/L的下列四种溶液:pH 由大到小排列的顺序是 。
①NaClO ②NaHCO ③Na CO ④CH COONa
(6)25℃时,用pH 试纸测得NH Cl溶液的pH=5,则此溶液中水电离出来的氢离子浓度为 mol/L, pH=10的 Na CO 溶液中水电离出来的氢离子浓度为 mol/L
(7)将少量CO 气体通入NaClO溶液中,写出该反应离子方程式 。
22.(16分) I: 用0.1000 mol/L NaOH溶液分别滴定体积均为25.00mL浓度均为0.1000 mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
高二化学 第 7 页 共10页
(1) 滴定醋酸的曲线是 (填“图1”或“图2”)。
(2)滴定开始前, ①0.1000 mol/L NaOH ②0.1000 mol/L 的盐酸 ③0.1000 mol/L 醋酸三种溶液中由水电离出的c(H )最大的是 溶液。
(3) 用0.1m ol/L NaOH 溶液滴定盐酸可用 为指示剂。
判断达到滴定终点的现象为 .
(4) 用0.1000 mol/L NaOH 溶液滴定25.00mL 未知浓度的盐酸溶液。
I:下列操作会使测定结果偏低的 .
A. 量取盐酸溶液的酸式滴定管未用待测盐酸润洗
B. 碱式滴定管在滴定前有气泡,滴定后气泡消失
C. 滴定过程中滴定管内不慎有标准NaOH 溶液滴到锥形瓶外面
D. 读取NaOH 溶液体积时,开始仰视读数,滴定结束时平视
Ⅱ:实验时记录的实验数据如下:
滴定次数 待测液体积(mL) 标准 NaOH 溶液体积(mL)
滴定前读数(mL) 滴定后读数(mL)
第一次 25.00 0.50 26.40
第二次 25.00 0.00 V
第三次 25.00 1.20 27.30
高二化学 第 8 页 共10页
①第二次实验时,碱式滴定管的始、终液面如图所示,则
②根据上列数据:计算待测盐酸溶液的浓度为 mol/L。
(5) 氧化还原滴定实验与酸碱中和滴定类似,实验室可以用KMnO 酸性标准溶液滴定未知浓度的草酸:
滴定实验中,下列有关说法正确的是 .
A. 用蒸馏水洗净酸式滴定管、锥形瓶后可分别直接注入标准溶液和待测液
B. 滴定时左手旋转滴定管的玻璃活塞,右手不停地摇动锥形瓶,
两眼注视滴定管液面变化
C. 此滴定实验的滴定终点现象为:溶液由无色变为紫红色,且30s内颜色不变
D. 实验中盛装酸性KMnO 应选择图中的滴定管甲
23.(18分)将CO 作为资源进行再利用是重要的研究课题。工业上用 生产燃料甲醇的化学方程式: 回答下列问题:
(1)由CO 制备甲醇过程涉及反应如下:
反应I:
反应Ⅱ:
反应Ⅲ:
则△H = (用 表示),已知反应I、II、III的化学平衡常数分别为
K 、K , 则 (用 表示)。
(2)一定条件下,向1L的恒容密闭容器中按物质的量之比1∶3充入一定量 和 发生反应I,测得平衡时混合物中 的体积分数在不同压强下随温度的变化如图所示。(已知 时最初充入
高二化学 第 9 页 共10页
条件下,10min后达到平衡,则从反应开始到平衡,用 浓度变化表示化学反应速率为 , 的平衡转化率为 (用分数表示)
E点速率 (填)。
②若反应在恒温恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是 .
A. 容器中混合气体的密度保持不变 B. 容器内混合气体的压强保持不变
C. 反应速率: D. 同时断裂2mol C-H键和1mol H-H键
③由图可知,压强. (填下同);, A、B、C的平衡常数大小关系
为 (用表示)
④若恒温恒压条件下,在上述C点平衡后,向容器中充入
和 ,则平衡向 (填“正向移动”、“逆向移动”或“不移动”)。
⑤已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
则 C点对应温度下的 (用含 的代数式表示)。
高二化学 第 10 页 共10页
天津市滨海新区塘沽紫云中学教育集团校
2024—2025学年度第一学期 高二年级期中检测 化学学科试题解析
第Ⅰ卷 单项选择题(每题2分,共40分)
1 2 3 4 5 6 7 8 9 10
C B A C D A D C A B
11 12 13 14 15 16 17 18 19 20
B D B D A B B A B D
第II卷 非选择题
21.(每空2分, 共26分)
(2)>; <
CE
(4) 酸性; >; 0.1
(5) ③①②④
22.(每空2分, 共16分)
(1) 图1
(2)③
(3)酚酞(甲基橙); 滴入半滴氢氧化钠溶液后,溶液颜色由无色刚好变为粉红色(溶液颜色由橙色刚好变为黄色),且半分钟不变色,表示已经到达滴定终点。
(4) I: AD Ⅱ: ①26.00 ②0.1040
(5) CD
23.(每空2分, 共18分)
(1) △H -△H (1分) ; K /K (1分)
(2) ①9/40 或 0.225mol/(L· min) ; 75% 或 0.75 或 3/4 ; >
②B
③>; >=
④不移动
或 1 00/(3P )
2024—2025学年度第一学期高二年级期中检测化学学科试题
本试卷分为第Ⅰ卷(选择题) 和第Ⅱ卷(非选择题) 两部分,共100分,考试用时60分钟。第Ⅰ卷1到6页, 第Ⅱ卷7到10页。
答卷前,考生务必将自己的姓名、班号、考场号和座位号填写在答题卡上,将考号填、涂准确; 答卷时,考生务必将选择题答案涂在答题卡上,非选择题答在答题纸上、答在试卷上无效。
祝各位考生考试顺利!
第Ⅰ卷 选择题 (共40分)
单项选择题(每小题2分,共40分。每小题给出的四个选项中,只有一个选项是正确的。)
1. 下列说法错误的是 ( )
A. 泡沫灭火器中常使用的原料是碳酸氢钠和硫酸铝
B. 加热纯碱溶液可以增强清洗油污效果
C. 血浆的pH降到7.2以下会引起酸中毒,升到7.5以上会引起碱中毒,可以通过口服少量氢氧化钠稀溶液或稀盐酸进行治疗
D. 明矾能够净水,是因为Al 水解生成 Al(OH) 胶体可使水中细小的悬浮颗粒聚集成较大颗粒而沉降
2. 下列溶液因溶质的水解而呈酸性的是 ( )
A. K CO 溶液 B. NH Cl溶液 C. NaHSO 溶液 溶液
3. 依据下列反应(), 推论正确的是 ( )
A. 已知: 则稀盐酸与稀氨水完全反应生成
1mol H O(l), 放出的热量小于57.3 kJ
H的燃烧热为:
则
则该反应在任何温度下都能自发进行
高二化学 第 1 页 共10页
4. 已知: 不同条件下反应过程能量变化如图所示。下列说法中错误的是 20( )
A. 反应的
B. 过程b使用了催化剂
C. 使用催化剂,可以改变反应历程,从而提高 的平衡转化率
D. 活化分子具有的平均能量与反应物分子具有的平均能量之差,为反应的活化能
5.已知: 下列关于稀硫酸和稀NaOH溶液中和反应反应热的测定的表述,正确的是 ( )
A. 将量筒中的NaOH 溶液沿玻璃棒缓慢倒入量热计的内筒
B. 用如图所示装置可完成本实验
C. 取一次测量所得温度差作为该反应热的计算依据
高二化学 第 2 页 共10页
6. 下列有关化学反应速率的说法,错误的是 ( )
A. 用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率
B. Al在O 中燃烧生成Al O ,用铝粉代替铝片,可加快反应速率
C. 二氧化硫的催化氧化是一个放热反应,升高温度,反应速率加快
恒容下充入 He,化学反应速率不变
7. 对于一定条件下进行的化学反应: 改变下列条件,可以提高反应物中活化分子百分数的是 ( )
①增大反应物浓度 ②升高温度 ③加入催化剂 ④增大压强
A. ①② B. ①④ C. ①②③ D. ②③
8. 下列有关化学平衡的描述,错误的是 ( )
恒温恒容条件下,加入HI,容器内气体颜色变深
,恒容条件下,升高温度,容器内气体颜色变深
恒温恒容条件下,通入 平衡不移动
加入少量NaOH 固体,溶液颜色变浅
9. 研究NO 、SO 等气体的无害化处理对治理大气污染、建设生态文明具有重要意义。将 与
SO 以体积比1:3置于恒温恒容容器中,发生反应:
下列能说明该反应达到平衡状态的是 ( )
A. 混合气体的颜色保持不变 B. SO 和NO的体积比保持不变
C. 每生成 消耗 D. 容器内气体的平均摩尔质量保持不变
10. 在一定温度下的密闭容器中发生反应: 平衡时测得A的浓度为
0.80mol/L。保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得A的浓度为
0.50mol/L。下列判断正确的是 ( )
A. B. B的转化率减小 C. 平衡向正反应方向移动 D. C的体积分数增大
高二化学 第 3 页 共10页
11. 下图所示为工业合成氨 的流程图。有关说法错误的是( )
A. 合成塔压强调控在 10MPa~30MPa之间,是对生产设备条件和经济成本的综合考虑结果
B. 在实际生产中,温度为 ,有利于提高原料平衡转化率
C. 步骤④有利于提高原料平衡转化率
D. 除原料气中CO 的反应如下:
适宜低温高压环境
12. 下列说法正确的是 ( )
均属于弱电解质
的电离方程式:
C. NaHS 的水解离子方程式:
D. 弱电解质溶液的导电能力可能比强电解质溶液的强
13. 25℃时, 水的电离达到平衡: 下列叙述正确的是 ( )
A. 向水中加入稀氨水,平衡逆向移动,c(OH )降低
B. 向水中加入少量固体硫酸氢钠,c(H )增大,Kw不变
C. 将水加热, Kw增大, pH不变
D. 向水中加入少量固体 平衡逆向移动, 降低
14. 常温下,由水电离出的 的溶液中,下列离子组一定能大量共存的是( )
高二化学 第 4 页 共10页
15. 下列说法正确的是 ( )
A. pH均为3 的醋酸和盐酸两种溶液,温度都升高20℃后,盐酸的pH大
B. 氨水、NaOH 溶液中分别加入适量氯化铵晶体后,前者pH增大,后者pH减小
C. 等浓度的下列溶液中, ①NH Al(SO ) 、②NH Cl、③CH COONH 、④NH ·H O; c(NH )
由大到小的顺序是: ③②①④
D. 常温下, pH=2的某酸HA与pH=12 的某碱BOH等体积混合溶液呈酸性, 则HA 为弱酸, BOH 为强碱
16. 下列说法错误的是 ( )
A. 实验室制备 Cl 时,用饱和食盐水溶液除去Cl 中的HCl气体,运用了平衡移动原理
B. 用 AICl 溶液和 Na S 溶液能制得硫化铝
C. 配制 FeSO 溶液时常加入稀硫酸和铁屑
D. 用饱和氯化铵溶液可以清洗钢铁表面的锈迹
17. 将6molA 和2molB 充入2L 的恒容密闭容器中, 发生的反应: 3A(s)+B(g) C(g)+2D(g),
5min后反应达到平衡, 测得C 的平均反应速率为0.1mol/(L· min), 下列结论正确的是( )
A. A 的平均反应速率为0.3mol/(L· min) B. 平衡时, C 的浓度为0.5mol/L
C. 平衡时, B的转化率为20% D. 平衡时,容器内压强为原来的7/8
18. 下列实验装置或操作能达到实验目的的是 ( )
选项 A B c D
目的 测定NaOH的物质的量浓度 测定氧气的生成速率 测定盐酸的pH 加热溶液制取无水FeCl
装置 或 操作
高二化学 第 5 页 共10页
19. 下列叙述与图对应的是 ( )
A. 对于可逆反应: 图①表示在t 时刻充入了一定量的 平衡逆向移动
B. 由图②可知, 满足反应:
C. 图③表示的反应方程式为:
D. 对于反应 图④y轴可以表示Y的百分含量
20. 叠氮酸(HN )是一种弱酸。常温下, 向20mL 0.1m ol/L 的 溶液中逐滴加入0.1m ol/L NaOH 溶液。测得滴定过程中溶液的pH 随V(NaOH)变化如图所示,下列说法正确的( )
A. 该滴定过程应该选择甲基橙作为指示剂
B. 点②溶液中:
C. 常温下, 的数量级为
D. 点③溶液中,水电离出的
高二化学 第 6 页 共10页
第II卷 非选择题 (共60分)
21.(26分) 已知在 时,醋酸、次氯酸、碳酸和亚硫酸的电离平衡常数如下表所示:
电解质 电离平衡常数
CH COOH K =1.75×10
HClO K =4.0×10
H CO K =4.5×10 Ka =4.7×10 11
H SO K =1.4×10 K =6.0×10
在水溶液中的电离方程式为 。
的电离平衡常数表达式 Ka= 。
(2)根据上表可知, 酸性CH COOH HClO(填“>”“<”或“=”, 下同), 在相同条件下,试比较同浓度CH COONa、NaClO溶液的pH: CH COONa NaClO。
在溶液中的水解离子方程式为 向0.1mol/L 的 溶液中加入少量下列物质,其水解程度增大的是 。
固体 B. NH Cl固体 C. NaCl溶液 D. NaClO固体 E. HCl气体
(4)0.1mol/L 的NaHSO 溶液显 (填“中性”“酸性”或“碱性”), 该溶液中
(填), = mol/L.
(5)物质的量浓度均为0.1mol/L的下列四种溶液:pH 由大到小排列的顺序是 。
①NaClO ②NaHCO ③Na CO ④CH COONa
(6)25℃时,用pH 试纸测得NH Cl溶液的pH=5,则此溶液中水电离出来的氢离子浓度为 mol/L, pH=10的 Na CO 溶液中水电离出来的氢离子浓度为 mol/L
(7)将少量CO 气体通入NaClO溶液中,写出该反应离子方程式 。
22.(16分) I: 用0.1000 mol/L NaOH溶液分别滴定体积均为25.00mL浓度均为0.1000 mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
高二化学 第 7 页 共10页
(1) 滴定醋酸的曲线是 (填“图1”或“图2”)。
(2)滴定开始前, ①0.1000 mol/L NaOH ②0.1000 mol/L 的盐酸 ③0.1000 mol/L 醋酸三种溶液中由水电离出的c(H )最大的是 溶液。
(3) 用0.1m ol/L NaOH 溶液滴定盐酸可用 为指示剂。
判断达到滴定终点的现象为 .
(4) 用0.1000 mol/L NaOH 溶液滴定25.00mL 未知浓度的盐酸溶液。
I:下列操作会使测定结果偏低的 .
A. 量取盐酸溶液的酸式滴定管未用待测盐酸润洗
B. 碱式滴定管在滴定前有气泡,滴定后气泡消失
C. 滴定过程中滴定管内不慎有标准NaOH 溶液滴到锥形瓶外面
D. 读取NaOH 溶液体积时,开始仰视读数,滴定结束时平视
Ⅱ:实验时记录的实验数据如下:
滴定次数 待测液体积(mL) 标准 NaOH 溶液体积(mL)
滴定前读数(mL) 滴定后读数(mL)
第一次 25.00 0.50 26.40
第二次 25.00 0.00 V
第三次 25.00 1.20 27.30
高二化学 第 8 页 共10页
①第二次实验时,碱式滴定管的始、终液面如图所示,则
②根据上列数据:计算待测盐酸溶液的浓度为 mol/L。
(5) 氧化还原滴定实验与酸碱中和滴定类似,实验室可以用KMnO 酸性标准溶液滴定未知浓度的草酸:
滴定实验中,下列有关说法正确的是 .
A. 用蒸馏水洗净酸式滴定管、锥形瓶后可分别直接注入标准溶液和待测液
B. 滴定时左手旋转滴定管的玻璃活塞,右手不停地摇动锥形瓶,
两眼注视滴定管液面变化
C. 此滴定实验的滴定终点现象为:溶液由无色变为紫红色,且30s内颜色不变
D. 实验中盛装酸性KMnO 应选择图中的滴定管甲
23.(18分)将CO 作为资源进行再利用是重要的研究课题。工业上用 生产燃料甲醇的化学方程式: 回答下列问题:
(1)由CO 制备甲醇过程涉及反应如下:
反应I:
反应Ⅱ:
反应Ⅲ:
则△H = (用 表示),已知反应I、II、III的化学平衡常数分别为
K 、K , 则 (用 表示)。
(2)一定条件下,向1L的恒容密闭容器中按物质的量之比1∶3充入一定量 和 发生反应I,测得平衡时混合物中 的体积分数在不同压强下随温度的变化如图所示。(已知 时最初充入
高二化学 第 9 页 共10页
条件下,10min后达到平衡,则从反应开始到平衡,用 浓度变化表示化学反应速率为 , 的平衡转化率为 (用分数表示)
E点速率 (填)。
②若反应在恒温恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是 .
A. 容器中混合气体的密度保持不变 B. 容器内混合气体的压强保持不变
C. 反应速率: D. 同时断裂2mol C-H键和1mol H-H键
③由图可知,压强. (填下同);, A、B、C的平衡常数大小关系
为 (用表示)
④若恒温恒压条件下,在上述C点平衡后,向容器中充入
和 ,则平衡向 (填“正向移动”、“逆向移动”或“不移动”)。
⑤已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
则 C点对应温度下的 (用含 的代数式表示)。
高二化学 第 10 页 共10页
天津市滨海新区塘沽紫云中学教育集团校
2024—2025学年度第一学期 高二年级期中检测 化学学科试题解析
第Ⅰ卷 单项选择题(每题2分,共40分)
1 2 3 4 5 6 7 8 9 10
C B A C D A D C A B
11 12 13 14 15 16 17 18 19 20
B D B D A B B A B D
第II卷 非选择题
21.(每空2分, 共26分)
(2)>; <
CE
(4) 酸性; >; 0.1
(5) ③①②④
22.(每空2分, 共16分)
(1) 图1
(2)③
(3)酚酞(甲基橙); 滴入半滴氢氧化钠溶液后,溶液颜色由无色刚好变为粉红色(溶液颜色由橙色刚好变为黄色),且半分钟不变色,表示已经到达滴定终点。
(4) I: AD Ⅱ: ①26.00 ②0.1040
(5) CD
23.(每空2分, 共18分)
(1) △H -△H (1分) ; K /K (1分)
(2) ①9/40 或 0.225mol/(L· min) ; 75% 或 0.75 或 3/4 ; >
②B
③>; >=
④不移动
或 1 00/(3P )
同课章节目录
