2025届高考化学基础练作业课件 专题九 化学反应与电能 课件(102张)
文档属性
| 名称 | 2025届高考化学基础练作业课件 专题九 化学反应与电能 课件(102张) |

|
|
| 格式 | pptx | ||
| 文件大小 | 21.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-03 10:29:35 | ||
图片预览






文档简介
(共102张PPT)
考点26 原电池
考点27 电解池
考点28 金属的腐蚀与防护
专题综合训练
热考题型13 新型电化学装置分析
【考情分析】在高考中,每卷必考。常以新型电化学装置为载体,考查原电池和电解池原理,考查点涉及电极类
型的判断、离子移动方向、电子流向、电极反应式的书写、有关计算等。
考点26 原电池
01
经典3+2
1.[2023辽宁沈阳考试]将反应 设计成如图所示的原电池。开始
时向甲烧杯中加入少量浓硫酸,电流表指针发生偏转,一段时间后,电流表指针回到零,再
向甲烧杯中滴入几滴浓 溶液,电流表指针再次发生偏转。下列判断不正确的是( )
B
A.开始加入少量浓硫酸时,乙中石墨电极上发生氧化反应
B.开始加入少量浓硫酸时,同时在甲、乙烧杯中都加入淀粉溶液,只有乙烧杯中溶液变蓝
C.电流表读数为零时,反应达到化学平衡状态
D.两次电流表指针偏转方向相反
【解析】原理分析
将反应 设计成原电池,当加入少量浓硫酸时,负极的电极反应式为
,正极的电极 反应式为;当加入几滴浓 溶液时,正极
的电极反应式为,负极的电极反应式为 。
开始加入少量浓硫酸时,乙中石墨电极作负极, 发生氧化反应,A项正确;由电极反应式可以看出,开始加入少
量浓硫酸时,甲、乙烧杯中均有 生成,所以加入淀粉溶液,甲、乙烧杯中溶液均变蓝,B项错误;当电流表读数
为零时,反应达到化学平衡状态,C项正确;滴入浓硫酸时与滴入浓 溶液时,电池中两极的电极反应式不同,
总反应进行的方向不同,故两次电流表指针偏转方向相反,D项正确。
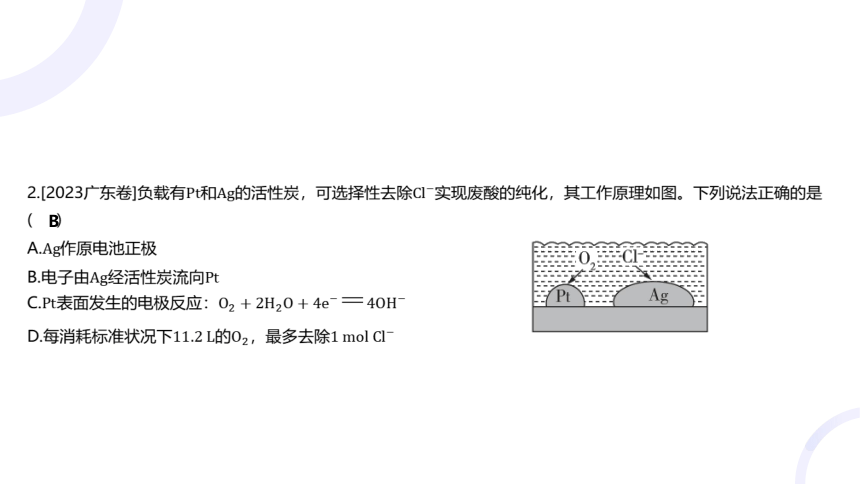
2.[2023广东卷]负载有和的活性炭,可选择性去除 实现废酸的纯化,其工作原理如图。下列说法正确的是
( )
B
A. 作原电池正极
B.电子由经活性炭流向
C.表面发生的电极反应:
D.每消耗标准状况下的,最多去除
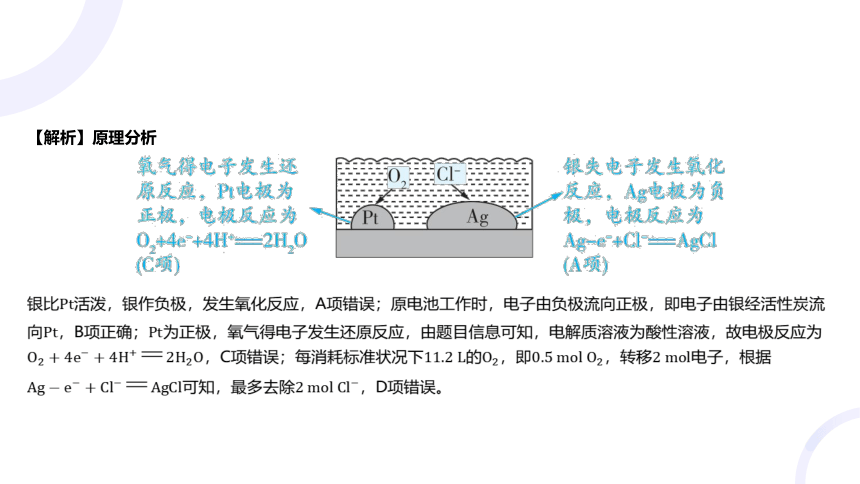
【解析】原理分析
银比 活泼,银作负极,发生氧化反应,A项错误;原电池工作时,电子由负极流向正极,即电子由银经活性炭流
向,B项正确; 为正极,氧气得电子发生还原反应,由题目信息可知,电解质溶液为酸性溶液,故电极反应为
,C项错误;每消耗标准状况下的,即,转移 电子,根据
可知,最多去除 ,D项错误。
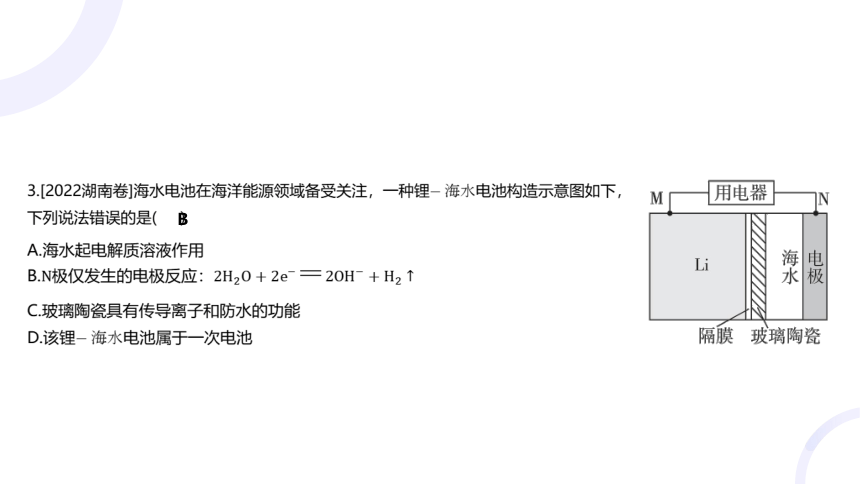
3.[2022湖南卷]海水电池在海洋能源领域备受关注,一种锂 电池构造示意图如下,
下列说法错误的是( )
B
A.海水起电解质溶液作用
B.极仅发生的电极反应:
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂 电池属于一次电池
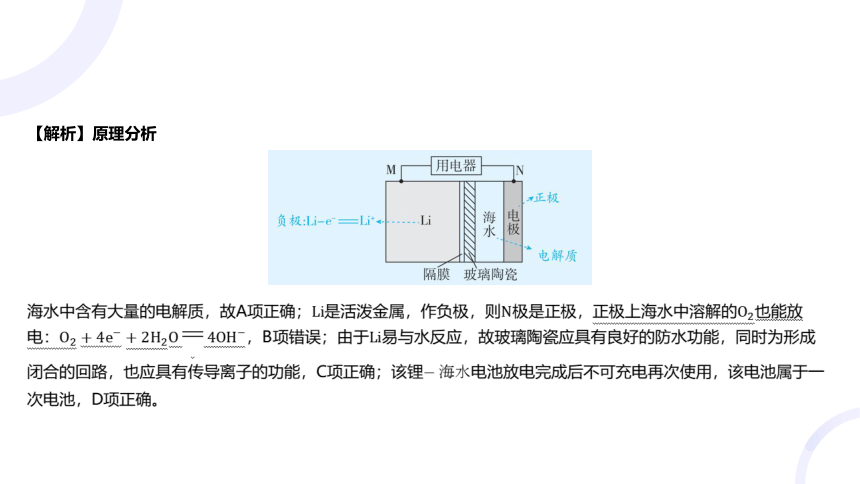
【解析】原理分析
海水中含有大量的电解质,故A项正确;是活泼金属,作负极,则极是正极,正极上海水中溶解的 也能放
电:,B项错误;由于 易与水反应,故玻璃陶瓷应具有良好的防水功能,同时为形成
闭合的回路,也应具有传导离子的功能,C项正确;该锂 电池放电完成后不可充电再次使用,该电池属于一
次电池,D项正确。
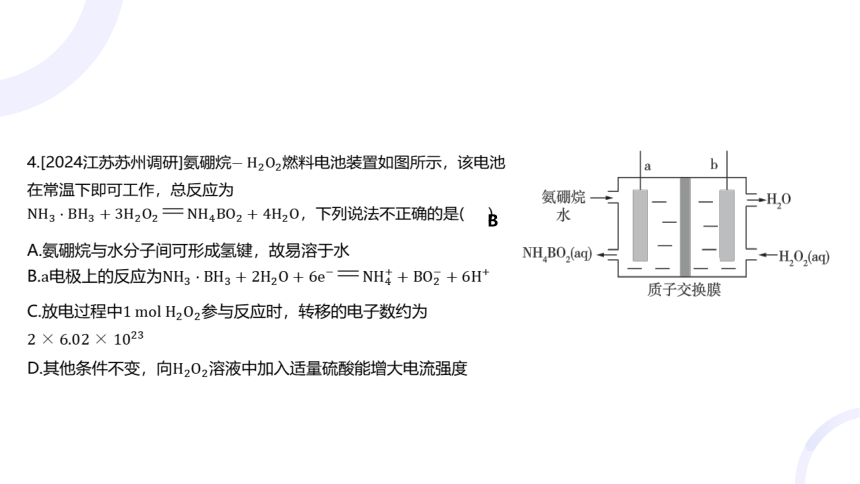
4.[2024江苏苏州调研]氨硼烷 燃料电池装置如图所示,该电池
在常温下即可工作,总反应为
,下列说法不正确的是( )
B
A.氨硼烷与水分子间可形成氢键,故易溶于水
B.电极上的反应为
C.放电过程中 参与反应时,转移的电子数约为
D.其他条件不变,向 溶液中加入适量硫酸能增大电流强度
【解析】原理分析
由总反应方程式可知,电极为负极,电极反应式为, 电极为正极,
电极反应式为 。
氨硼烷分子中含有氮氢键,能与水分子形成分子间氢键,所以氨硼烷易溶于水,A项正确;由上述分析可知,B项
错误;电极的反应式为,参与反应时,转移的电子数约为 ,
C项正确;硫酸为强电解质,加入适量的硫酸,可以增大溶液中离子浓度,增强导电能力,增大电流强度,D项正
确。
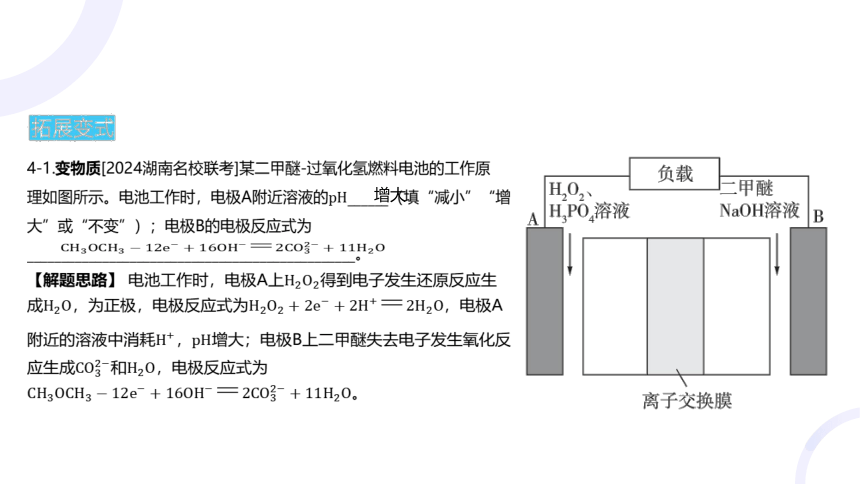
4-1.变物质[2024湖南名校联考]某二甲醚-过氧化氢燃料电池的工作原
理如图所示。电池工作时,电极A附近溶液的 ______(填“减小”“增
大”或“不变”);电极B的电极反应式为
________________________________________________。
增大
【解题思路】 电池工作时,电极A上 得到电子发生还原反应生
成,为正极,电极反应式为 ,电极A
附近的溶液中消耗, 增大;电极B上二甲醚失去电子发生氧化反
应生成和 ,电极反应式为
。
5.[2024湖北武汉部分学校调研]我国科技工作者设计了一种转化的多功能光电化学平台,实现了 生产与塑料
到化学品的协同转化,其原理如图所示。下列说法错误的是( )
D
A.光催化电极的电势:
B.电池工作时,负极区溶液的 减小
C.正极区的电极反应为
D.当电路中通过电子时,正极区溶液质量增大
【解析】根据光催化电极上转化为,发生还原反应,知为正极,则为负极,光催化电极的电势: ,
A项正确;负极上 降解为 和,
发生氧化反应转化为,电极反应式为 ,负极区
消耗,溶液的减小,B项正确;正极区转化为 ,电极反应为
,C项正确;由正、负极的电极反应及电解液保持电中性知,当电路中
通过电子时,正极区溶液增加“”,同时 通过阳离子交换膜进入正极区,溶液质量增大
,D项错误。
6.[2023全国乙卷]室温钠-硫电池被认为是一种成本低、比能量高的能源存储系
统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一
个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。 工作时,在硫
电极发生反应:
下列叙述错误的是( )
A
A.充电时从钠电极向硫电极迁移 B.放电时外电路电子流动的方向是
C.放电时正极反应为: D.炭化纤维素纸的作用是增强硫电极导电性能
, ,
【解析】原理分析
充电时,阳离子应向阴极钠电极迁移,A错误;放电时, 失去的电子经外电路流向正极,即电子流向是
,B正确;将题给硫电极发生的反应依次标号为,由 可得正极总反应,C正确;炭化
纤维素纸具有良好的导电性,D正确。
6-1.变载体[2023江西南昌模拟]一种新型的 电池原理如图所示。其电解质溶
液为溶液,正极采用含有、 的水溶液,负极采用固体有机聚合物,
聚合物离子交换膜将正负极分隔开。已知: (棕黄色),下列说
法不正确的是( )
A
A.图甲是原电池工作原理图,图乙是电池充电原理图
B.放电时,正极液态电解质溶液的颜色变浅
C.充电时, 从左向右通过聚合物离子交换膜
D.放电时,负极反应式为&3&
【解析】由题意可知,电池的正极采用含有、 的水溶液且正极发生得电子的还原反应,正极反应式为
;负极固体有机聚合物发生失电子的氧化反应,负极反应式
为 ,再结合题图中电子移动方向可知,图乙是原电池工作原理图,图
甲是电池充电原理图,A错误,D正确。由上述分析可知,放电时,正极反应式为,含 的溶液呈
棕黄色, 减小,则正极液态电解质溶液的颜色变浅,B正确。由上述分析可知,图甲为电解池,根据电子移
动方向可知,左侧电极为阳极,则充电时,由阳极移向阴极,即 从左向右通过聚合物离子交换膜,C正确。
(【必记结论】原电池中,阳离子向正极移动,阴离子向负极移动;电解池中,阳离子向阴极移动,阴离子向阳
极移动。)
创新1+1
1.新角度·双阴极微生物燃料电池处理废水[2024安徽部分学校考试]双阴极微生物燃料电池处理含 的废水的工作
原理如图a所示,双阴极通过的电流相等,废水在电池中的运行模式如图b所示。
下列说法正确的是( )
C
A.Ⅰ室为负极区
B. 离子交换膜为阴离子交换膜
C.Ⅲ室中除了,主要发生的反应为
D.生成,理论上需要消耗
【解析】&6& .
Ⅰ室发生反应,生成,左侧阴极(正极区)转移
电子,消耗,根据题中信息“双阴极通过的电流相等”可知,右侧阴极(正极区)也转移 电子,
右侧阴极(正极区)反应消耗的物质的量为 ,Ⅲ室还发生反应
,Ⅰ室消耗,则Ⅲ室需要生成,消耗 ,理论
上共需要消耗 ,D项错误。
2.新考法·模块融合(结构 电化学)[2023湖南长沙联考]水溶液锌电池(图1)的电极材料是研究热点之一。一种
在晶体中嵌入 的电极材料充放电过程的原理如图2所示。下列叙述正确的是( )
C
A.过程①为活化过程,其中 的化合价不变
B.在晶体中嵌入 的电极材料在锌电池中作为负极材料
C.过程②代表电池放电过程
D.晶体发生过程③时转移电子的物质的量为
【解析】题图2中过程①为晶胞中失去体心的,是产生空穴的过程,该过程为 活化过程,由化合物
中元素化合价的代数和为0可知,的化合价一定发生变化,A错误。由题图1可知, 电极发生失电子的氧化反
应,生成,则为负极材料,故在晶体中嵌入 的电极材料为正极材料,B错误。过程②表示向含有
空穴的氧化锰中嵌入,说明体系中有生成,发生反应, 移向正极补充空穴,因此为
放电过程,C正确。根据“均摊法”可知,晶胞中的个数为,和
晶胞中的个数均为3(脱去晶胞体心的),晶胞中的个数为,因此 与
的个数比为,则中为(【易错警示】容易直接按照个数比进行计算而忽略 的值,
从而计算错误。),过程③为的脱嵌过程,是充电过程,根据得失电子守恒可得, 晶
体发生过程③时转移电子的物质的量为 ,D错误。
3.新装置·协同转化装置[2024江西九校联考]我国科研人员设计的将脱除
的反应与制备 相结合的协同转化装置如图。在电场作用下,双
极膜中间层的解离为和 ,并向两极迁移。已知:
①单独制备 ,不能自发进行;
②单独脱除 ,能自发进行。
下列说法正确的是( )
A
A.正极的电极反应式:
B.单独脱除 的反应为吸热反应
C.反应过程中需补加稀
D.协同转化总反应:
【解析】原理分析
左侧:与反应生成,光催化下失去电子,发生氧化反应生成 ,左侧电极为负极,电极反应
式为 。
右侧:得到电子,发生还原反应生成,右侧电极为正极,电极反应式为 。
右侧电极为正极,正极反应为,A项正确;单独脱除 的反应是一个熵减反应,此反应
可自发进行,根据时反应自发进行,知该反应的 ,为放热反应,B项错误;反应过程中不需
要补加稀硫酸,因为右侧消耗的氢离子可由双极膜中迁移补充,C项错误;根据正负极反应可知,协同转化总反应
为 ,D项错误。
4.新角度·光催化电极产生电子和空穴[2022全国乙卷]
电池比能量高,在汽车、航天等领域具有良好应用前景。近
年来,科学家研究了一种光照充电 电池(如图所示)。
光照时,光催化电极产生电子和空穴 ,驱动阴极反
应和阳极反应
对电池进行充电。下列叙述错误的是( )
C
A.充电时,电池的总反应 B.充电效率与光照产生的电子和空穴量有关
C.放电时,从正极穿过离子交换膜向负极迁移 D.放电时,正极发生反应
【解析】原理分析
由图可知该装置为二次电池,放电时,;充电时, ,由此写出的电极反应
式如下:
电极 电极反应式
电解池 阳极(光催化电极)
阴极(金属锂)
原电池 正极(光催化电极)
负极(金属锂)
充电时为电解池,由题目信息知,光照时,光催化电极产生电子和空穴 ,电子通过外电路转移到锂电极发
生反应,光催化电极上发生反应,总反应为 ,因此充电
效率与光照产生的电子和空穴量有关,A、B项正确;放电时,阳离子移向正极,因此放电时, 从负极穿过离子
交换膜向正极迁移,C项错误;放电时,正极发生还原反应,其电极反应式为 ,D项正确。
考点27 电解池
02
经典3+2
1.[2024贵州贵阳摸底]电解催化 还原为乙烯能缓解碳排放引发的温室效应,
还将成为获得重要化工原料的补充形式,原理如图所示(、 均为惰性电
极)。下列说法正确的是( )
D
A.B为电源负极
B. 从左边透过阳离子交换膜到右边
C.电解一段时间后,阳极区溶液的 增大
D.阴极反应为
【解析】二氧化碳得电子生成乙烯,发生还原反应,所以为阴极, 为阳极,则B为电源正极,A错误;电解池中
阳离子从阳极向阴极移动,故 从右边向左边移动,B错误;由题图知,阳极发生反应:
,故阳极区溶液中 减小,C错误;阴极二氧化碳得电子生成乙烯,发生还原反
应,电极反应式为 ,D正确。
2.[2023广东卷]利用活性石墨电极电解饱和食盐水,进行如图所示实验。
闭合 ,一段时间后,( )
D
A.形管两侧均有气泡冒出,分别是和
B.处布条褪色,说明 具有漂白性
C.处出现蓝色,说明还原性:
D.断开,立刻闭合 ,电流表发生偏转
【解析】闭合,与电源正极相连的一极为阳极,发生反应 ,与电源负极相连的一极为阴极,
发生反应,故形管两侧均有气泡冒出,分别是和,A项错误; 处湿润的红色布
条褪色,是因为氯气与水反应生成的次氯酸具有强氧化性,氯气没有漂白性,B项错误; 处出现蓝色,说明生成
了,即发生反应:,可说明还原性,C项错误;断开,立刻闭合 ,会形成氢
氯燃料电池,电流表发生偏转,D项正确。
命题动向
综合性命题,关注问题的内涵和外延
本题以电解饱和食盐水为载体,综合考查了实验现象分析、物质性质及电化学知识,试题在突出对化学基本概念、
基本原理等内容考查的同时,强化对基础知识深入理解上的综合运用,引导中学教学注重培养考生的综合能力。
多模块知识综合命题不但有利于构建知识体系,更能让考生抓住问题本源、深度理解知识内核。
3.[2024福建漳州考试]是生产航空航天润滑剂的原料。清华大学首创三室膜电解法制备 ,其模拟装置如图
所示。下列有关说法正确的是( )
A
A.极的电极反应式为
B.极为电源的负极, 极上发生氧化反应
C.膜1为阳离子交换膜,膜2为阴离子交换膜
D.每转移电子,理论上生成
【解析】
多解
根据“离子迁移方向”速判电极:极区稀硫酸变为浓硫酸,增大,则通过膜1向 极移动,则膜1为阴离
子交换膜,根据电解池中阴离子移向阳极可知,极为阳极,连接电源正极(极);极区稀 溶液变为浓
溶液,增大,则通过膜2向极移动,则膜2为阳离子交换膜,根据电解池中阳离子移向阴极可知,
极为阴极,发生还原反应,B、C错误。
4.[2022重庆卷]硝酮是重要的有机合成中间体,可采用“成对间接电氧化”法合成。电解槽中水溶液的主要成分及反应过程如图所示。
下列说法错误的是( )
C
A.惰性电极2为阳极 B.反应前后 数量不变
C.消耗氧气,可得到硝酮 D.外电路通过电子,可得到 水
【解析】原理分析
阳极区反应为、 ;阴极区反应为 、
, ;制备硝酮的总反应
为 。
惰性电极2上转化为,发生氧化反应,为阳极,A项正确;由总反应可知,反应前后 数量不变,
B项正确;根据总反应知,消耗氧气,可得到硝酮,C项错误;根据阴极区反应知,外电路通过 电
子,可得到 水,D项正确。
4-1.变物质[2023辽宁沈阳模拟]利用间接成对
电化学法,以间硝基甲苯为原料合成间氨基苯
甲酸的工作原理如图所示。下列说法错误的是
( )
D
A.物质 为间硝基苯甲酸
B.右侧电极电势高于左侧电极电势
C.阳极的电极反应式:
D.当电路中转移 电子时,理论上可得到
间氨基苯甲酸
【解析】由题图可知,被还原为间氨基苯甲酸,则物质 为间硝基苯甲酸,A正确。右侧电极连接电源正极,
为阳极,左侧电极连接电源负极,为阴极,则右侧电极电势高于左侧电极电势(【结论速记】电解池中,阳极电
势高于阴极电势。),B正确。右侧电极为阳极,阳极上失去电子发生氧化反应生成 ,电极反应式为
,C正确。左侧电极为阴极,电极反应式为 ,阴极槽外反
应为间硝基苯甲酸和反应生成间氨基苯甲酸和,即 ,
则当电路中转移电子时,理论上可得到 间氨基苯甲酸(【多解】根据关系式: ,并
结合得失电子守恒可知,电路中每转移电子,生成 间氨基苯甲酸。),D错误。
5.[2024浙江名校协作体考试]以某锂离
子电池、丙烯腈电合成己二腈
的装置如图所示(电极
均为石墨)。该锂离子电池的总反应
是
。下列说法不正确的是( )
B
A.B为正极,电极反应式为
B.阴极区的电极反应为,一段时间后,阴极室的 增大
C.石墨电极C产生 ,稀硫酸的作用为增强溶液导电性
D.当电路中通过时,阳极室溶液质量减少 (不考虑氧气溶解)
【解析】根据装置图及该锂离子电池的总反应知,放电时 向B极移动,则B为正极,电极反应为
,A项正确;A极为负极,则D极为阴极,电极反应为
,阳极区透过质子交换膜进入阴极区,因此阴极室的 不变,B
项错误;C极为阳极,电极反应为 ,稀硫酸的作用为增强溶液导电性,C项正确;根据
阳极反应知,当电路中通过时,阳极室析出,同时有 进入
阴极室,相当于减少,因此阳极室溶液质量减少 ,D项正确。
命题动向
将电化学与实际相联系,从“解题”向“解决问题”转变
本题以锂离子电池和电合成己二腈为载体,考查串联电池分析、电极反应、电解液作用等,引导考生多关注创新
科技,有利于培养考生的证据推理和分析推测能力。电化学知识是高考中的热点和难点,常结合前沿科技、实际
生产生活进行考查,拓展考生视野,提升考生利用所学知识解决实际问题的能力。
6.[2022山东卷](双选)设计如图装置回收金属钴。保持细菌所在环
境稳定,借助其降解乙酸盐生成 ,将废旧锂离子电池的正极
材料转化为 ,工作时保持厌氧环境,并定时将乙
室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电
池。下列说法正确的是( )
BD
A.装置工作时,甲室溶液 逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为
D.若甲室减少,乙室增加 ,则此时已进行过
溶液转移
【解析】原理分析
根据右侧装置为原电池,乙酸盐降解为二氧化碳,发生氧化反应,转化为 ,发生还原反应,知右侧装
置左电极为负极,右电极为正极;左侧装置为电解池,左电极为阳极,乙酸盐转化为 气体,右电极为阴极,
转化为 单质。
装置工作时,甲室为阴极室,阳极发生反应 ,结合阴极反应及电解液呈
电中性知,阳极生成的通过阳膜进入阴极室,故甲室溶液 减小,A项错误;乙室为正极室,正极反应为
,消耗生成 ,电解质溶液酸性减弱,需要补充盐酸,B项正确,C
项错误;根据甲室中电极反应和乙室中电极反应可知,甲室中减少的 的质量为乙室中增加的
的质量的一半,则甲室减少,乙室增加 时已进行过溶液转移,D项正确。
7.[2023北京卷节选]尿素 合成的发展体现了化学科学与技术的不断进步。近
年研究发现,电催化和含氮物质( 等)在常温常压下合成尿素,有助于实现碳
中和及解决含氮废水污染问题。向一定浓度的溶液通 至饱和,在电极上反应生
成 ,电解原理如图所示。
①电极 是电解池的____极。
阳
【解题思路】 电极上失电子发生氧化反应生成 ,是电解池的阳极。
②电解过程中生成尿素的电极反应式是______________________________________________。
【解题思路】 电极 上硝酸根离子得电子发生还原反应生成尿素,再结合电解液环境(酸性)、电荷守恒、原子
守恒可写出电极反应式。
7-1.变物质[2024江苏南京六校调研]隔膜电解法同时脱硫脱硝的装置如图
所示,其中电极A、B均为惰性电极,电解液为稀硫酸。为提高脱除效率,
将阴极室的溶液调至 ,则阴极上的电极反应为________________
___________________。
【解题思路】 惰性电极A侧转变为,元素由价变为 价,
则电极A为电解池的阴极,结合电解液为稀硫酸可得阴极的电极反应式
为 。
创新1+1
1.新角度·与速率图像结合[2024江苏南通如皋考试]科研人员
发现利用低温固体质子导体作电解质,催化合成 ,与
传统的热催化合成氨相比,催化效率较高。其合成原理如
图1所示,电源电压改变与生成 速率的关系如图2所示,
下列说法不正确的是( )
C
A. 是该合成氨装置的阳极
B.电极上发生的反应为
C.若的进出口流量差为,则固体质子导体中的流速为
D.当电压高于时,混合气体中和的体积分数之和小于
【解析】原理分析
由题图1可知,电极上,是电解池的阳极,电极反应式为, 电极为阴极,
电极反应式为 。
由上述分析可知,A、B项正确;未给出气体所处状态,无法计算内氢气的物质的量和反应生成 的物
质的量,所以无法计算固体质子导体中的流速,C项错误;由题图2可知,当电压高于 时,氨气生成速率变
慢,说明部分在阴极得到电子生成氢气,导致混合气体中氮气和氨气的体积分数之和小于 ,D项正确。
2.新考法·通过电解法测定的值[2023北京海淀区练习]阿伏加德罗常数 是一座“桥梁”,连接了宏观世界和微观
世界的数量关系。通过电解法可测得 的数值。
已知:个电子所带电量为 库仑。
(乙二胺四乙酸二钠)能形成可溶含铜配离子。
ⅲ, 。
【实验一】用铜片和铂丝为电极,电解硫酸酸化的溶液。测得通过电路的电量为 库仑。电解完成后,取出
铜片,洗净晾干,铜片质量增加了 。
(1)铜片应连接电源的______(填“正极”或“负极”)。铂丝尖端产生气泡,其电极反应式为
____________________________。理论上,产生气体与析出铜的物质的量之比为_____。
负极
【解题思路】电解完成后,铜片质量增加,则铜片上发生还原反应: ,铜片为阴极,应连接电源
的负极。铂丝为阳极,发生氧化反应: 。根据两电极上通过的电量相等知,产生 与
析出铜的物质的量之比为 。
(2)本实验测得______________ (列出计算式)。
【解题思路】根据通过电路的电量为库仑,知电路中通过电子的数目为,根据 ,知电
路中通过电子的数目为,,则 。
【实验二】为减少含重金属电解液的使用,更换电解液,同时更换电极与电源的连接方式。电解完成后,取出铜
片,洗净晾干,铜片质量减小。
实验 电解液 实验现象
① 溶液 铜片表面为灰蓝色
② 和混合液 铜片表面仍为红色
(3)实验①和②中各配制电解液 ,使用的主要仪器有天平、烧杯、玻璃棒、胶头滴管和______________。
容量瓶
(4)经检验,实验①中的灰蓝色成分主要是。从平衡移动角度解释在测定 的数值中的作用:
___________________________________________________________________________________________________
________________________________________________________________。
,与生成配离子,下降,平衡向溶解方向移动,铜片表面的消失,铜片的质量变化数据准确,可准确测得的数值
(5)电解过程中,若观察到铜片上有小气泡产生,利用铜片质量减小计算 的数值,结果将______(填“偏大”“偏
小”或“不变”)。
偏大
【解题思路】电解过程中,铜电极上单质铜放电生成(Ⅱ),若观察到铜片上有小气泡产生,说明电极上 也
放电,电路中通过的电子数增多,则利用铜片减小的质量计算的 的数值偏大。
(6)实验结束后处理电解液:将取出的电解液加入过量硫酸,过滤,得到白色固体和滤液;向滤液 中先
加入调,再加入,解释不直接加入的原因及 的作用:_____________________________
___________________________________________________________________________________。
若直接加入,可能产生有毒气体;调后,加可进一步降低溶液中铜离子的浓度,同时沉淀转化为
【解题思路】滤液中含有稀硫酸和(Ⅱ),若直接加入,和反应产生有毒气体;调 后,
加可进一步降低溶液中铜离子的浓度,同时可使沉淀转化为 。
命题动向
本题将实验探究与反应原理知识融合,对相关知识进行多维度多层次的考查,有利于促进考生的批判性、缜密性
和系统性思维品质的养成。
考点28 金属的腐蚀与防护
03
经典3+2
1.[2024广东惠州调研]下列现象与电化学腐蚀无关的是( )
B
A.铜锌合金(黄铜)不易被腐蚀 B.银质物品久置表面变黑
C.附有银制配件的铁制品其接触处易生锈 D.铁锅炒菜后未洗净擦干容易生锈
【解析】铜锌合金形成原电池时,锌作负极被腐蚀,铜作正极被保护,A项与电化学腐蚀有关;金属银能和空气中
的二氧化硫、氧气等发生反应,故银质物品久置表面变黑属于化学腐蚀,B项与电化学腐蚀无关;铁制品附有银制
配件时,在接触处形成原电池,铁作负极被氧化,故C项与电化学腐蚀有关;铁锅炒菜后未洗净擦干,铁、碳和电
解质溶液构成原电池, 作负极被腐蚀,D项与电化学腐蚀有关。
2.[2024辽宁部分学校联考]科学研究发现金属生锈时,锈层内如果有硫酸盐
会加快金属的腐蚀,其腐蚀原理如图所示。下列说法错误的是( )
C
A.钢铁的腐蚀中正极电极反应式为
B.酸雨地区的钢铁更易被腐蚀
C.生成 反应的化学方程式为
D.硫酸盐加速电子传递,有一定的催化剂作用
【解析】由图可知钢铁发生吸氧腐蚀,C作正极,氧气在正极得电子,电极反应式为 ,
A项正确; 酸性溶液可以加速铁的腐蚀,B项正确;不稳定,易被氧气氧化生成 ,化学方程式为
,C项错误;根据题干信息可知,锈层内如果有硫酸盐会加快金属的腐蚀,
硫酸盐能增加导电性,加速电子传递,有一定的催化剂作用,D项正确。
3.[2024广东广州阶段训练改编]全世界每年的钢铁锈蚀会造成巨大的损失,
为了保护地下的钢铁输水管所采取的措施如图所示。下列说法不正确的是
( )
D
A.钢铁发生吸氧腐蚀过程中负极反应为
B.导线与 块连接为牺牲阳极法
C.导线应连接外接电源的负极
D.导线与 块连接也可保护钢铁输水管
【解析】钢铁发生吸氧腐蚀过程中,负极上失去电子转化为,A项正确;导线与 块连接,为原电池,属于
牺牲阳极法,B项正确;外接电源时,钢铁作阴极,导线应连接外接电源的负极,C项正确;铜的金属活动性比铁
弱,导线与 块连接不能保护钢铁输水管,D项错误。
4.[2022广东卷]为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放入酸化的 溶液
中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是( )
D
A.加入 溶液产生沉淀 B.加入淀粉碘化钾溶液无蓝色出现
C.加入溶液无红色出现 D.加入 溶液无蓝色沉淀生成
【解析】若铁片被腐蚀,则溶液中含有,在溶液中加入溶液,反应生成蓝色的 沉淀,
D项正确;A项只能检验溶液中含有,B项只能检验溶液中无强氧化性物质,C项只能检验溶液中无 ,三者
均不能说明铁片没有被腐蚀。
4-1.变实验[2023北京101中学质检]实验小组研究金属电化学腐蚀,实验如下:
序号 实验
实验Ⅰ 铁钉表面及周边未见明显变化 铁钉周边零星、随机出现极少量红色和蓝色区
域,有少量红棕色铁锈生成
实验Ⅱ 铁钉周边出现红色区域,未见 蓝色出现; #b# 锌片周边未见明显变化 铁钉周边红色加深,区域变大,未见蓝色出
现;
#b#
锌片周边未见明显变化
下列说法不正确的是( )
A
A.实验Ⅰ的现象说明溶液与反应生成了
B.实验Ⅱ中保护了 ,使铁的腐蚀速率比实验Ⅰ小
C.实验Ⅱ中正极的电极反应式:
D.若将片换成片,推测 片周边会出现红色,铁钉周边会出现蓝色
【解析】根据实验Ⅰ的现象可知,与生成蓝色沉淀(【易错】 与铁氰化钾溶液反
应生成蓝色沉淀,与硫氰化钾反应使溶液呈红色,可分别用来鉴别和。), 使酚酞溶液变红,
最后有少量红棕色铁锈生成,发生了吸氧腐蚀,不能说明与反应生成了 ,A项错误。实验Ⅱ中,
比活泼,故锌片作负极被氧化,保护了,从而使 的腐蚀速率降低,B项正确。实验Ⅱ中的铁钉周边溶液中
出现红色区域说明生成了,则正极反应式为,C项正确。实验Ⅱ中,将片换成
片,则铁钉为负极,被氧化,电极反应式为,生成的与反应生成 ,
则铁钉周边出现蓝色,片为正极,被还原,生成, 片周边出现红色,D项正确。
5.[2023北京清华大学附属中学考试]家庭常用的一种储水式电热水器的结构如图所示,其中、 为水管口。
下列说法不正确的是( )
C
A.电热水器可将电能转化为热能 B.该热水器采用了牺牲阳极的电化学保护法
C.镁棒可以有效防止内部水垢生成 D.应为出水口, 应为进水口
【解析】
6.[2023湘豫名校联考]青铜器文物腐蚀物以粉末状有害锈最为严重,某种碱式氯化铜粉状锈的形成过程分三个阶段:
阶段一:铜在电解质溶液中发生一般腐蚀,; (灰白色);
;
阶段二: ;
阶段三:和具有很强穿透力,可深入铜体内部,产生粉状锈, 。
下列说法正确的是( )
A
A.该粉状锈生成的条件中需要有:潮湿环境、可溶性的氯化物、氧化性的物质
B.上述过程涉及的化学反应有:电解反应、水解反应、氧化还原反应
C.依据反应 ,可以判断氧化亚铜不能溶于盐酸
D.利用外加电流法保护铜制文物时,青铜器应连接电源的正极
【解析】由三个阶段的反应可知,碱式氯化铜粉状锈产生的基本条件是:可溶性的氯化物、潮湿环境和氧化性的物质,A项正确;没有涉及电解反应,题中是原电池原理,没有形成电解池,B项错误;氧化亚铜能溶于盐酸,C项错误;保护铜制文物时,即防止铜失去电子被氧化,则青铜器应该接电源负极,若是接电源正极,则作阳极,会加速失去电子,不能起到保护作用,D项错误。
创新1+1
1.新考法·浓硫酸贮存罐的钝化金属保护法[2022上海卷]浓硫酸贮存罐的钝化
金属保护法示意图如图,其原理是利用可钝化的金属与直流电源相连,控制
合适的电压,使金属贮存罐表面形成致密的钝化膜,以有效减缓金属腐蚀。
下列选项错误的是( )
C
A.金属贮存罐可用钢制材料 B.电子沿导线流入辅助电极
C.贮存浓硫酸的金属罐与电源负极相连 D.电压高到一定程度有可能会加剧腐蚀
【解析】原理分析
钢的主要成分是铁,铁遇冷的浓硫酸发生钝化,因此金属贮存罐可用钢制材料,A正确;贮存浓硫酸的金属罐为阳极,连接电源正极,辅助电极是阴极,电子沿导线流向辅助电极,B正确,C错误;电压过高时,有可能会加剧腐蚀,D正确。
2.新形式·实验装置图+温度、压强与时间关系图[2024四川南充考试改编]某实验小组要定量探究铁锈蚀的因素,设
计如图所示实验装置,检查气密性,将铁粉和碳粉加入三颈烧瓶,加入 饱和氯化钠溶液后,再将一
只装有 稀盐酸的注射器插到烧瓶上,采集数据。下列说法错误的是( )
C
A.铁发生锈蚀的反应是放热反应
B. 温度降低是因为反应速率减慢了
C. 段压强减小是因为铁和氧气直接反应生成了氧化铁
D. 压强变大是因为发生了铁的析氢腐蚀
【解析】由温度与时间的关系曲线可知,温度升高,铁发生锈蚀的反应是放热反应,A项正确; 反应速率
减慢,铁锈蚀放出的热量小于装置散失的热量,温度降低,B项正确;铁在氧气和水共同作用下反应生成铁锈,铁
锈的主要成分为氧化铁,C项错误;铁锈蚀消耗氧气,装置内压强减小,注射器内稀盐酸被吸入烧瓶,反应产生较
多氢气,压强变大(【点拨】铁粉一开始在氯化钠溶液中发生吸氧腐蚀,后期稀盐酸被吸入烧瓶,在酸性条件下
发生析氢腐蚀。),D项正确。
命题动向
本题结合传感器和图像考查铁锈蚀的实验,形象直观,是教材实验的创新设计。
热考题型13 新型电化学装置分析
04
1.新考法·与压力有关的浓差电池[2024湖北部分名校联考]两个负载有不同压力
的氢气的片插入一定浓度的酸性介质中构成的浓差电池如图所示 ,
电池工作时 逐渐增大。下列说法不正确的是( )
A
A.电流方向:电极 电流表 电极
B.电极上发生的反应为
C.电池工作原理为
D. 为质子交换膜
【解析】,该电池工作时电极为负极,发生反应;逐渐增大, 电极为正极,发生反应
;电子流向为电极 电流表电极,电流方向与电子流向相反;电极产生的会穿过
移向电极,则为质子交换膜;电池工作原理为 。由上述分析可知,A项错误,B、C、D项正确。
2.[2024天星原创]在能源短缺、环境污染日益严重的现代社会,太阳能的利用一直是科学研究的热点。一种染料
敏化光伏电池的结构和工作原理如图1、图2所示。下列有关说法错误的是( )
D
A.染料电极为电池的负极 B.石墨电极的电极反应式为
C.电池工作过程中,和的浓度基本保持不变 D.碘系电解液可以用溶液,也可以用 溶液
【解析】
3.[2023湖北卷]我国科学家设计如图所示的电解池,实现了海水直接制备氢气技术的绿色化。该装置工作时阳极无
生成且溶液的浓度不变,电解生成氢气的速率为 。下列说法错误的是( )
D
A.电极反应式为
B.离子交换膜为阴离子交换膜
C.电解时海水中动能高的水分子可穿过 膜
D.海水为电解池补水的速率为
【解析】根据图示, 电极与电源负极相连,为阴极,结合题干信息可知,阴极反应式为
,A正确;该装置工作时阳极无氯气产生,则阳极反应式为
,又阳极溶液的浓度不变,则需要 由阴极移向阳极,故离子交换膜为阴离子
交换膜,B正确;电解过程中,阳极 溶液的浓度不变,而阳极不断有水分子消耗,结合题图,海水中动能高的
水分子 (【提示】气态水分子。)可以穿过 膜,为阳极补充水,C正确;由阴、阳极反应式可知,电解总反
应式为 ,已知电解生成氢气的速率为 ,则海水为电解池补水的速率也为
,D错误。
4.[2024福建福州质检]我国科学家经过研究发明了以下装置从海水中提取锂单质,其工作原理如图所示。该装置运
行期间电极Ⅱ上产生和气体 。下列说法错误的是( )
C
A.该装置实现了“太阳能 电能 化学能”的转化
B.电极Ⅰ连接太阳能电池的负极
C.工作时,电极Ⅱ附近溶液的 增大
D.实验室检验气体可用湿润的淀粉 试纸
【解析】原理分析
根据该装置可知,太阳能电池将太阳能转化为电能,电解装置又将电能转化为化学能,A选项正确;电极Ⅰ为电解
池的阴极,连接太阳能电池的负极,B选项正确;由电极Ⅱ的电极反应式可知,电极Ⅱ上产生 ,则电极Ⅱ附近溶
液降低,C选项错误;气体为(黄绿色气体),实验室检验可用湿润的淀粉 试纸,试纸变蓝即说明
存在,D选项正确。
5.[2023重庆卷]电化学合成是一种绿色高效的合成方法。如图是在酸性介质中电解合成半胱氨酸和烟酸的示意图。
下列叙述错误的是( )
D
A.电极 为阴极
B.从电极移向电极
C.电极 发生的反应为:
D.生成半胱氨酸的同时生成 烟酸
【解析】原理分析
有机反应中“加氢去氧”的反应为还原反应,“加氧去氢”的反应为氧化反应,据此分析电解池中各电极类型及电极反应如下:
由上述分析知,A正确,C正确;电解池中阳离子向阴极移动,故从电极移向电极 ,B正确;根据阴、阳极反
应及得失电子守恒可知,生成半胱氨酸,转移电子,同时生成 烟酸,D错误。
6.[2023广东模拟]我国科学家设计了一种新型的溴基液流可充电电池用
于大规模储能,其放电时的工作原理如图所示。下列有关说法不正确
的是( )
C
A.放电时, 极为正极
B.放电时,极发生的电极反应为
C.充电时,每生成有穿过质子交换膜进入 极室
D.充电时,总反应为
【解析】
放电时,极为正极,A项正确;放电时, 极为负极,电极反应为
,B项正确;充电时, 极为阳极,电极
反应为,则每生成 ,
转移电子,有穿过质子交换膜进入 极室,C项错误;
由阴、阳极反应可知,充电时的总反应为
,D项正确。
命题动向
电化学是高考必考知识,以新型电池为载体考查电化学知识是高考
的高频考查角度,有利于考查考生的知识迁移、应用能力,培养考
生的创新思维。
7.[2023山东卷](双选)利用热再生氨电池可实现 电镀废液的浓缩
再生。电池装置如图所示,甲、乙两室均预加相同的 电镀废液,向甲
室加入足量氨水后电池开始工作。下列说法正确的是( )
CD
A.甲室 电极为正极
B.隔膜为阳离子膜
C.电池总反应为:
D. 扩散到乙室将对电池电动势产生影响
【解析】为实现电镀废液的浓缩再生,据图可知,甲室流出液经低温热解得到和 ,则甲室中生成
了,发生的反应为,甲室电极为负极,A错误;乙室 电极
为正极,发生反应:,消耗,为维持电解质溶液呈电中性, 透过隔膜进入甲室,则隔
膜为阴离子膜,B错误;根据正、负极反应,可知电池总反应为,C正确; 能
与反应生成,因此若扩散到乙室,则乙室 浓度减小,对电池电动势有影响,D正确。
8.[2024天星原创]利用一种微生物燃料电池(原理如图Ⅰ所示),以维生素C的钠盐,简写 为原
料制备维生素,简写,具有弱酸性和还原性,装置如图Ⅱ所示。、 为水电离出来的离子,下列说法
正确的是( )
A
A.图Ⅰ中极的电极反应式为
B.图Ⅱ中极应连接图Ⅰ中的极,和分别代表、
C.将①室的溶液替换为溶液,可发生氧化反应生成
D.若极有(标准状况下)参与反应,则图Ⅱ装置中极产生
【解析】
专题综合训练
05
1.[2024北京石景山区模拟]以氨为燃料的固体氧化物燃料电池具有广阔的应用前景,一种氧离子导电的
的工作原理如图所示在催化剂作用下先分解为和 。下列说法不正确的是( )
C
A.在负极放电 B.正极的电极反应为
C.外电路转移,理论上生成 D. 向负极移动
【解析】
2.[2023湖北武汉武昌区质检]我国科技工作者利用水热法制备了
六方钴纳米片,可应用于高效电催化 的还原。下
列说法错误的是( )
C
A.六方钴纳米片有利于 分子的活化
B.负极的电极反应为:
C.理论上每消耗,可放出
D.该过程的总反应为
【解析】原理分析
由题给条件“可应用于高效电催化的还原”可知,六方钴纳米片有利于分子的活化,A项正确;负极 失电子
转化为,结合电解液环境可知,其电极反应为 ,B项正确;理论上每消耗
,转移电子,根据转化为转移知,生成 ,但没有给出气体所
处的温度和压强,其体积不一定为 ,C项错误;结合正、负极反应可知,总反应为
,D项正确。
3.[2024天星原创]孔蚀(一种集中于金属表面很小的范围并深入到金属
内部的腐蚀形态)是一种常见的电化学腐蚀现象,某铁合金钝化膜破
损后的孔蚀如图。下列关于金属腐蚀与防护的说法错误的是( )
B
A. 的存在会加速该铁合金的腐蚀速率
B.“孔”的表面与内部所发生的腐蚀主要是吸氧腐蚀
C.在表面形成钝化膜可以让铁合金连接外接电源的正极
D.铁合金与锌块连接可有效防止铁被腐蚀
【解析】金属离子不易向外扩散,金属离子增多,会吸引外部 迁入
以维持电中性,“孔”内介质导电性增强,则 的存在会使该铁合金的
腐蚀速率加快,A正确。根据题图可以得出“孔”的表面发生吸氧腐蚀,而其内部介质含有 ,主要发生析氢腐蚀,
B错误。若使铁合金表面被氧化产生钝化,铁合金应该与外接电源的正极连接,充当阳极,发生氧化反应,C正确。
锌的活泼性强于铁,铁合金与锌块连接后可以有效防止金属铁被氧化腐蚀(【原理应用】出海的轮船为了防止船
体被腐蚀,通常在船身外侧放置锌块,原理与此处一致。),D正确。
4.[2023北京东城区练习]用石墨作电极电解 浊液,记录如表。
实验装置 实验现象 Ⅰ.为 Ⅱ.为
两电极均产生气泡,有黑色固体在阴极附 近生成,并沉降在电解槽底部,电解槽中 的液体逐渐变澄清透明 两电极均产生气泡,阴极表面附着少量
银白色固体,电解槽中的液体逐渐变为
棕黄色
下列说法不正确的是( )
C
A.Ⅰ中阳极气体可能为和,Ⅱ中阳极气体为
B.Ⅰ和Ⅱ中阴极生成气体的方程式均为
C.Ⅱ中液体变为棕黄色,说明阳极上发生了反应
D.两实验阴极现象有差异的原因可能是Ⅱ中 比Ⅰ中的小
【解析】原理分析
由实验现象可知,Ⅰ中阳极上和(或)发生氧化反应生成和,阴极上和(或 )发生还原
反应生成和;Ⅱ中阳极上(或)发生氧化反应生成,阴极上(或)和少量 发生还原反应
生成和 。
由上述分析知,A项正确;Ⅰ和Ⅱ中阴极上生成的气体均为,都是(或 )发生还原反应产生的,电极反应
为,B项正确;的溶解度较小,溶液中 小,由电解槽中液体逐渐变为棕黄色知,
阳极生成的将氧化为了,C项错误;的溶解度大于,浊液中大于浊液中 ,所以Ⅰ
中在阴极放电生成,并沉降在电解槽底部,Ⅱ中少量在阴极放电生成 附着在电极上,D项正确。
5.[2023山东济宁模拟](双选)芳香羧酸是一种重要的有机分子骨架,利用电化学方法,芳香烃与 选择性的
键羧基化反应如图所示,下列说法错误的是( )
AB
A.生成芳香羧酸,电路中转移的电子数为(设 为阿伏加德罗常数的值)
B.电池工作过程中需要不断补充
C.不同的取代基 可能影响路径Ⅰ或Ⅱ的选择
D.该反应的原子利用率为
【解析】&16& .
由题图可知,该反应有不同的路径,则不同的取代基 可能影响路径Ⅰ或Ⅱ的选择,C正确。该反应的总化学方程
式为 ,反应物有两种,生成物只有一种,因此该反应是化合反应,原子利用率为 ,
D正确。
6.[2023新课标卷]一种以和为电极、 水溶液为电解质的电池,其示意图如下所示。放电时,
可插入层间形成 。下列说法错误的是( )
C
A.放电时 为正极
B.放电时 由负极向正极迁移
C.充电总反应:
D.充电阳极反应:
【解析】原理分析
放电时失去电子生成,为负极,则为正极,A正确;放电时,阳离子 移向正极,B正确;由上
述分析可知,放电总反应为 ,充电总反应为
,C错误;由上述分析可知,D正确。
7.[2024天星原创]四甲基氢氧化铵
,强有机碱]常用作电子工业清洗
剂。以四甲基氯化铵 为原料,利用
电渗析法合成 的工作原理如图。下
列叙述错误的是( )
C
A.极接电源负极,工作时电极上产生气体
B.膜为阳离子交换膜, 膜为阴离子交换膜
C.工作时电极上产生气体
D.若两极共产生 (标准状况)气体,则
理论上得到
【解析】解题关键
根据进出装置的物质浓度判断粒子移动方向 根据粒子移动方向判断电极类型。
Ⅰ室中稀溶液浓溶液,说明Ⅱ室中的移入Ⅰ室, 为阴极,接电源负极,工作时
电离出的在电极上放电产生气体,A正确;Ⅱ室中的移入Ⅰ室, 膜为阳离子交换膜,Ⅱ室中
浓溶液稀溶液,说明移入Ⅲ室,膜为阴离子交换膜,Ⅲ室中稀溶液 浓溶液,
说明移入Ⅲ室,膜为阳离子交换膜,B正确;工作时电极上产生气体(【点拨】放电产生 ,
。),C错误;综上分析,总反应实质是电解
的反应,根据电路中通过的电流处处相等,可得关系式: ,若两极共产生
气体,则理论上得到 ,D正确。
8.[2024山东青岛调研改编]利用浓差电池电解溶液、电极均为石墨电极,可制得、、 和
,反应原理如图所示。下列说法正确的是( )
D
A.极的电极反应式为
B.、 分别为阴离子交换膜和阳离子交换膜
C.浓差电池放电过程中,电极上的电极反应式为
D.浓差电池从开始工作到放电结束,电解池理论上可制得
【解析】根据电子流动方向可知,极为电解池的阴极,电离出的得电子发生还原反应生成 ,电极反应式
为,为阳离子交换膜,通过阳离子交换膜进入阴极室,阴极区 溶液浓度不
断增大,极为电解池的阳极,失电子发生氧化反应生成,电极反应式为, 为阴
离子交换膜,通过阴离子交换膜进入阳极室,阳极区溶液浓度不断增大,A、B项错误; 为原电池
的正极,电极反应式为,为原电池的负极,电极反应式为 ,C项错误;浓
差电池从开始工作到放电结束,正极区硫酸铜溶液浓度由降低到 ,负极区硫酸铜溶液浓度
由上升到,即正极区被还原的的物质的量为 ,负极
区被氧化的的物质的量为,电路中转移 电子,理论上电解池阴极区生成
,即阴极区可得,其质量为 ,D项正确。
9.[2023江苏卷节选]催化电解吸收的溶液可将 转化为有机物。在相同
条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率
随电解电压的变化如图所示。
其中,,表示电解生成还原产物所转移电子的物质的量, 表示法拉第常数。
①当电解电压为时,电解过程中含碳还原产物的 为0,阴极主要还原产物为____(填化学式)。
【解题思路】当电解电压为时,电解过程中含碳还原产物的 为0,说明阴极无含碳物质生成,则阴极电极
反应为,即阴极主要还原产物为 。
②当电解电压为时,阴极由生成 的电极反应式为_____________________________________。
【解题思路】当电解电压为时,阴极发生还原反应,根据电荷守恒、原子守恒可写出由生成 的电极
反应式为 。
③当电解电压为时,电解生成的和 的物质的量之比为 ______________________________________
__________________________________________________________________________ (写出计算过程)。
【解题思路】由图可知,当电解电压为时,,而转移, 转移
,结合题给信息可知,,所以,即当电解电压为 时,阴极
生成和的物质的量之比为 。
生成转移 电子,生成
转移电子,,
10.[2022北京卷]煤中硫的存在形态分为有机硫和无机硫 、硫
化物及微量单质硫等 。库仑滴定法是常用的快速检测煤中全硫含
量的方法,其主要过程如图所示。
已知:在催化剂作用下,煤在管式炉中燃烧,出口气体中主要含
、、、、 。
(1)煤样需研磨成细小粉末,目的是________________________________________________________。
(2)高温下,煤中的完全转化为 ,该反应的化学方程式为___________________________________。
增大固体与空气的接触面积,加快反应速率,使煤粉完全燃烧
【解题思路】在高温条件下,硫酸钙和C反应生成氧化钙、二氧化硫和二氧化碳。
(3)通过干燥装置后,待测气体进入库仑测硫仪进行测定。
已知:库仑测硫仪中电解原理示意图如图。检测前,电解质溶液中
保持定值时,电解池不工作。待测气体进入电解池后, 溶
解并将还原,测硫仪便立即自动进行电解到 又回到原定值,
测定结束。通过测定电解消耗的电量可以求得煤中含硫量。
① 在电解池中发生反应的离子方程式为___________________________________。
【解题思路】根据题目信息可知,二氧化硫在电解池中与溶液中的 反应生成碘离子、硫酸根离子和氢离子。
②测硫仪工作时电解池的阳极反应式为_________________。
【解题思路】由题意可知,测硫仪工作时,碘离子在阳极失去电子发生氧化反应生成 ,电极反应式为
。
(4)煤样为,电解消耗的电量为 库仑。煤样中硫的质量分数为_______。
已知:电解中转移 电子所消耗的电量为96 500库仑。
【解题思路】根据题意可得关系式:,电解消耗的电量为 库仑,则煤样中硫的质量分数为
。
(5)条件控制和误差分析。
①测定过程中,需要控制电解质溶液的。当时,非电解生成的使测得的全硫含量偏小,生成 的离子
方程式为______________________________。
【解题思路】由已知信息可知,待测气体中含有,可将氧化为 。
②管式炉中煤样燃烧时会有少量 产生,使测得的全硫含量______(填“偏大”或“偏小”),该测量结果可进行校正。
偏小
【解题思路】直接溶解在溶液中生成,会使与反应的 元素偏少,导致测得的全硫含量偏小。
考点26 原电池
考点27 电解池
考点28 金属的腐蚀与防护
专题综合训练
热考题型13 新型电化学装置分析
【考情分析】在高考中,每卷必考。常以新型电化学装置为载体,考查原电池和电解池原理,考查点涉及电极类
型的判断、离子移动方向、电子流向、电极反应式的书写、有关计算等。
考点26 原电池
01
经典3+2
1.[2023辽宁沈阳考试]将反应 设计成如图所示的原电池。开始
时向甲烧杯中加入少量浓硫酸,电流表指针发生偏转,一段时间后,电流表指针回到零,再
向甲烧杯中滴入几滴浓 溶液,电流表指针再次发生偏转。下列判断不正确的是( )
B
A.开始加入少量浓硫酸时,乙中石墨电极上发生氧化反应
B.开始加入少量浓硫酸时,同时在甲、乙烧杯中都加入淀粉溶液,只有乙烧杯中溶液变蓝
C.电流表读数为零时,反应达到化学平衡状态
D.两次电流表指针偏转方向相反
【解析】原理分析
将反应 设计成原电池,当加入少量浓硫酸时,负极的电极反应式为
,正极的电极 反应式为;当加入几滴浓 溶液时,正极
的电极反应式为,负极的电极反应式为 。
开始加入少量浓硫酸时,乙中石墨电极作负极, 发生氧化反应,A项正确;由电极反应式可以看出,开始加入少
量浓硫酸时,甲、乙烧杯中均有 生成,所以加入淀粉溶液,甲、乙烧杯中溶液均变蓝,B项错误;当电流表读数
为零时,反应达到化学平衡状态,C项正确;滴入浓硫酸时与滴入浓 溶液时,电池中两极的电极反应式不同,
总反应进行的方向不同,故两次电流表指针偏转方向相反,D项正确。
2.[2023广东卷]负载有和的活性炭,可选择性去除 实现废酸的纯化,其工作原理如图。下列说法正确的是
( )
B
A. 作原电池正极
B.电子由经活性炭流向
C.表面发生的电极反应:
D.每消耗标准状况下的,最多去除
【解析】原理分析
银比 活泼,银作负极,发生氧化反应,A项错误;原电池工作时,电子由负极流向正极,即电子由银经活性炭流
向,B项正确; 为正极,氧气得电子发生还原反应,由题目信息可知,电解质溶液为酸性溶液,故电极反应为
,C项错误;每消耗标准状况下的,即,转移 电子,根据
可知,最多去除 ,D项错误。
3.[2022湖南卷]海水电池在海洋能源领域备受关注,一种锂 电池构造示意图如下,
下列说法错误的是( )
B
A.海水起电解质溶液作用
B.极仅发生的电极反应:
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂 电池属于一次电池
【解析】原理分析
海水中含有大量的电解质,故A项正确;是活泼金属,作负极,则极是正极,正极上海水中溶解的 也能放
电:,B项错误;由于 易与水反应,故玻璃陶瓷应具有良好的防水功能,同时为形成
闭合的回路,也应具有传导离子的功能,C项正确;该锂 电池放电完成后不可充电再次使用,该电池属于一
次电池,D项正确。
4.[2024江苏苏州调研]氨硼烷 燃料电池装置如图所示,该电池
在常温下即可工作,总反应为
,下列说法不正确的是( )
B
A.氨硼烷与水分子间可形成氢键,故易溶于水
B.电极上的反应为
C.放电过程中 参与反应时,转移的电子数约为
D.其他条件不变,向 溶液中加入适量硫酸能增大电流强度
【解析】原理分析
由总反应方程式可知,电极为负极,电极反应式为, 电极为正极,
电极反应式为 。
氨硼烷分子中含有氮氢键,能与水分子形成分子间氢键,所以氨硼烷易溶于水,A项正确;由上述分析可知,B项
错误;电极的反应式为,参与反应时,转移的电子数约为 ,
C项正确;硫酸为强电解质,加入适量的硫酸,可以增大溶液中离子浓度,增强导电能力,增大电流强度,D项正
确。
4-1.变物质[2024湖南名校联考]某二甲醚-过氧化氢燃料电池的工作原
理如图所示。电池工作时,电极A附近溶液的 ______(填“减小”“增
大”或“不变”);电极B的电极反应式为
________________________________________________。
增大
【解题思路】 电池工作时,电极A上 得到电子发生还原反应生
成,为正极,电极反应式为 ,电极A
附近的溶液中消耗, 增大;电极B上二甲醚失去电子发生氧化反
应生成和 ,电极反应式为
。
5.[2024湖北武汉部分学校调研]我国科技工作者设计了一种转化的多功能光电化学平台,实现了 生产与塑料
到化学品的协同转化,其原理如图所示。下列说法错误的是( )
D
A.光催化电极的电势:
B.电池工作时,负极区溶液的 减小
C.正极区的电极反应为
D.当电路中通过电子时,正极区溶液质量增大
【解析】根据光催化电极上转化为,发生还原反应,知为正极,则为负极,光催化电极的电势: ,
A项正确;负极上 降解为 和,
发生氧化反应转化为,电极反应式为 ,负极区
消耗,溶液的减小,B项正确;正极区转化为 ,电极反应为
,C项正确;由正、负极的电极反应及电解液保持电中性知,当电路中
通过电子时,正极区溶液增加“”,同时 通过阳离子交换膜进入正极区,溶液质量增大
,D项错误。
6.[2023全国乙卷]室温钠-硫电池被认为是一种成本低、比能量高的能源存储系
统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一
个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。 工作时,在硫
电极发生反应:
下列叙述错误的是( )
A
A.充电时从钠电极向硫电极迁移 B.放电时外电路电子流动的方向是
C.放电时正极反应为: D.炭化纤维素纸的作用是增强硫电极导电性能
, ,
【解析】原理分析
充电时,阳离子应向阴极钠电极迁移,A错误;放电时, 失去的电子经外电路流向正极,即电子流向是
,B正确;将题给硫电极发生的反应依次标号为,由 可得正极总反应,C正确;炭化
纤维素纸具有良好的导电性,D正确。
6-1.变载体[2023江西南昌模拟]一种新型的 电池原理如图所示。其电解质溶
液为溶液,正极采用含有、 的水溶液,负极采用固体有机聚合物,
聚合物离子交换膜将正负极分隔开。已知: (棕黄色),下列说
法不正确的是( )
A
A.图甲是原电池工作原理图,图乙是电池充电原理图
B.放电时,正极液态电解质溶液的颜色变浅
C.充电时, 从左向右通过聚合物离子交换膜
D.放电时,负极反应式为&3&
【解析】由题意可知,电池的正极采用含有、 的水溶液且正极发生得电子的还原反应,正极反应式为
;负极固体有机聚合物发生失电子的氧化反应,负极反应式
为 ,再结合题图中电子移动方向可知,图乙是原电池工作原理图,图
甲是电池充电原理图,A错误,D正确。由上述分析可知,放电时,正极反应式为,含 的溶液呈
棕黄色, 减小,则正极液态电解质溶液的颜色变浅,B正确。由上述分析可知,图甲为电解池,根据电子移
动方向可知,左侧电极为阳极,则充电时,由阳极移向阴极,即 从左向右通过聚合物离子交换膜,C正确。
(【必记结论】原电池中,阳离子向正极移动,阴离子向负极移动;电解池中,阳离子向阴极移动,阴离子向阳
极移动。)
创新1+1
1.新角度·双阴极微生物燃料电池处理废水[2024安徽部分学校考试]双阴极微生物燃料电池处理含 的废水的工作
原理如图a所示,双阴极通过的电流相等,废水在电池中的运行模式如图b所示。
下列说法正确的是( )
C
A.Ⅰ室为负极区
B. 离子交换膜为阴离子交换膜
C.Ⅲ室中除了,主要发生的反应为
D.生成,理论上需要消耗
【解析】&6& .
Ⅰ室发生反应,生成,左侧阴极(正极区)转移
电子,消耗,根据题中信息“双阴极通过的电流相等”可知,右侧阴极(正极区)也转移 电子,
右侧阴极(正极区)反应消耗的物质的量为 ,Ⅲ室还发生反应
,Ⅰ室消耗,则Ⅲ室需要生成,消耗 ,理论
上共需要消耗 ,D项错误。
2.新考法·模块融合(结构 电化学)[2023湖南长沙联考]水溶液锌电池(图1)的电极材料是研究热点之一。一种
在晶体中嵌入 的电极材料充放电过程的原理如图2所示。下列叙述正确的是( )
C
A.过程①为活化过程,其中 的化合价不变
B.在晶体中嵌入 的电极材料在锌电池中作为负极材料
C.过程②代表电池放电过程
D.晶体发生过程③时转移电子的物质的量为
【解析】题图2中过程①为晶胞中失去体心的,是产生空穴的过程,该过程为 活化过程,由化合物
中元素化合价的代数和为0可知,的化合价一定发生变化,A错误。由题图1可知, 电极发生失电子的氧化反
应,生成,则为负极材料,故在晶体中嵌入 的电极材料为正极材料,B错误。过程②表示向含有
空穴的氧化锰中嵌入,说明体系中有生成,发生反应, 移向正极补充空穴,因此为
放电过程,C正确。根据“均摊法”可知,晶胞中的个数为,和
晶胞中的个数均为3(脱去晶胞体心的),晶胞中的个数为,因此 与
的个数比为,则中为(【易错警示】容易直接按照个数比进行计算而忽略 的值,
从而计算错误。),过程③为的脱嵌过程,是充电过程,根据得失电子守恒可得, 晶
体发生过程③时转移电子的物质的量为 ,D错误。
3.新装置·协同转化装置[2024江西九校联考]我国科研人员设计的将脱除
的反应与制备 相结合的协同转化装置如图。在电场作用下,双
极膜中间层的解离为和 ,并向两极迁移。已知:
①单独制备 ,不能自发进行;
②单独脱除 ,能自发进行。
下列说法正确的是( )
A
A.正极的电极反应式:
B.单独脱除 的反应为吸热反应
C.反应过程中需补加稀
D.协同转化总反应:
【解析】原理分析
左侧:与反应生成,光催化下失去电子,发生氧化反应生成 ,左侧电极为负极,电极反应
式为 。
右侧:得到电子,发生还原反应生成,右侧电极为正极,电极反应式为 。
右侧电极为正极,正极反应为,A项正确;单独脱除 的反应是一个熵减反应,此反应
可自发进行,根据时反应自发进行,知该反应的 ,为放热反应,B项错误;反应过程中不需
要补加稀硫酸,因为右侧消耗的氢离子可由双极膜中迁移补充,C项错误;根据正负极反应可知,协同转化总反应
为 ,D项错误。
4.新角度·光催化电极产生电子和空穴[2022全国乙卷]
电池比能量高,在汽车、航天等领域具有良好应用前景。近
年来,科学家研究了一种光照充电 电池(如图所示)。
光照时,光催化电极产生电子和空穴 ,驱动阴极反
应和阳极反应
对电池进行充电。下列叙述错误的是( )
C
A.充电时,电池的总反应 B.充电效率与光照产生的电子和空穴量有关
C.放电时,从正极穿过离子交换膜向负极迁移 D.放电时,正极发生反应
【解析】原理分析
由图可知该装置为二次电池,放电时,;充电时, ,由此写出的电极反应
式如下:
电极 电极反应式
电解池 阳极(光催化电极)
阴极(金属锂)
原电池 正极(光催化电极)
负极(金属锂)
充电时为电解池,由题目信息知,光照时,光催化电极产生电子和空穴 ,电子通过外电路转移到锂电极发
生反应,光催化电极上发生反应,总反应为 ,因此充电
效率与光照产生的电子和空穴量有关,A、B项正确;放电时,阳离子移向正极,因此放电时, 从负极穿过离子
交换膜向正极迁移,C项错误;放电时,正极发生还原反应,其电极反应式为 ,D项正确。
考点27 电解池
02
经典3+2
1.[2024贵州贵阳摸底]电解催化 还原为乙烯能缓解碳排放引发的温室效应,
还将成为获得重要化工原料的补充形式,原理如图所示(、 均为惰性电
极)。下列说法正确的是( )
D
A.B为电源负极
B. 从左边透过阳离子交换膜到右边
C.电解一段时间后,阳极区溶液的 增大
D.阴极反应为
【解析】二氧化碳得电子生成乙烯,发生还原反应,所以为阴极, 为阳极,则B为电源正极,A错误;电解池中
阳离子从阳极向阴极移动,故 从右边向左边移动,B错误;由题图知,阳极发生反应:
,故阳极区溶液中 减小,C错误;阴极二氧化碳得电子生成乙烯,发生还原反
应,电极反应式为 ,D正确。
2.[2023广东卷]利用活性石墨电极电解饱和食盐水,进行如图所示实验。
闭合 ,一段时间后,( )
D
A.形管两侧均有气泡冒出,分别是和
B.处布条褪色,说明 具有漂白性
C.处出现蓝色,说明还原性:
D.断开,立刻闭合 ,电流表发生偏转
【解析】闭合,与电源正极相连的一极为阳极,发生反应 ,与电源负极相连的一极为阴极,
发生反应,故形管两侧均有气泡冒出,分别是和,A项错误; 处湿润的红色布
条褪色,是因为氯气与水反应生成的次氯酸具有强氧化性,氯气没有漂白性,B项错误; 处出现蓝色,说明生成
了,即发生反应:,可说明还原性,C项错误;断开,立刻闭合 ,会形成氢
氯燃料电池,电流表发生偏转,D项正确。
命题动向
综合性命题,关注问题的内涵和外延
本题以电解饱和食盐水为载体,综合考查了实验现象分析、物质性质及电化学知识,试题在突出对化学基本概念、
基本原理等内容考查的同时,强化对基础知识深入理解上的综合运用,引导中学教学注重培养考生的综合能力。
多模块知识综合命题不但有利于构建知识体系,更能让考生抓住问题本源、深度理解知识内核。
3.[2024福建漳州考试]是生产航空航天润滑剂的原料。清华大学首创三室膜电解法制备 ,其模拟装置如图
所示。下列有关说法正确的是( )
A
A.极的电极反应式为
B.极为电源的负极, 极上发生氧化反应
C.膜1为阳离子交换膜,膜2为阴离子交换膜
D.每转移电子,理论上生成
【解析】
多解
根据“离子迁移方向”速判电极:极区稀硫酸变为浓硫酸,增大,则通过膜1向 极移动,则膜1为阴离
子交换膜,根据电解池中阴离子移向阳极可知,极为阳极,连接电源正极(极);极区稀 溶液变为浓
溶液,增大,则通过膜2向极移动,则膜2为阳离子交换膜,根据电解池中阳离子移向阴极可知,
极为阴极,发生还原反应,B、C错误。
4.[2022重庆卷]硝酮是重要的有机合成中间体,可采用“成对间接电氧化”法合成。电解槽中水溶液的主要成分及反应过程如图所示。
下列说法错误的是( )
C
A.惰性电极2为阳极 B.反应前后 数量不变
C.消耗氧气,可得到硝酮 D.外电路通过电子,可得到 水
【解析】原理分析
阳极区反应为、 ;阴极区反应为 、
, ;制备硝酮的总反应
为 。
惰性电极2上转化为,发生氧化反应,为阳极,A项正确;由总反应可知,反应前后 数量不变,
B项正确;根据总反应知,消耗氧气,可得到硝酮,C项错误;根据阴极区反应知,外电路通过 电
子,可得到 水,D项正确。
4-1.变物质[2023辽宁沈阳模拟]利用间接成对
电化学法,以间硝基甲苯为原料合成间氨基苯
甲酸的工作原理如图所示。下列说法错误的是
( )
D
A.物质 为间硝基苯甲酸
B.右侧电极电势高于左侧电极电势
C.阳极的电极反应式:
D.当电路中转移 电子时,理论上可得到
间氨基苯甲酸
【解析】由题图可知,被还原为间氨基苯甲酸,则物质 为间硝基苯甲酸,A正确。右侧电极连接电源正极,
为阳极,左侧电极连接电源负极,为阴极,则右侧电极电势高于左侧电极电势(【结论速记】电解池中,阳极电
势高于阴极电势。),B正确。右侧电极为阳极,阳极上失去电子发生氧化反应生成 ,电极反应式为
,C正确。左侧电极为阴极,电极反应式为 ,阴极槽外反
应为间硝基苯甲酸和反应生成间氨基苯甲酸和,即 ,
则当电路中转移电子时,理论上可得到 间氨基苯甲酸(【多解】根据关系式: ,并
结合得失电子守恒可知,电路中每转移电子,生成 间氨基苯甲酸。),D错误。
5.[2024浙江名校协作体考试]以某锂离
子电池、丙烯腈电合成己二腈
的装置如图所示(电极
均为石墨)。该锂离子电池的总反应
是
。下列说法不正确的是( )
B
A.B为正极,电极反应式为
B.阴极区的电极反应为,一段时间后,阴极室的 增大
C.石墨电极C产生 ,稀硫酸的作用为增强溶液导电性
D.当电路中通过时,阳极室溶液质量减少 (不考虑氧气溶解)
【解析】根据装置图及该锂离子电池的总反应知,放电时 向B极移动,则B为正极,电极反应为
,A项正确;A极为负极,则D极为阴极,电极反应为
,阳极区透过质子交换膜进入阴极区,因此阴极室的 不变,B
项错误;C极为阳极,电极反应为 ,稀硫酸的作用为增强溶液导电性,C项正确;根据
阳极反应知,当电路中通过时,阳极室析出,同时有 进入
阴极室,相当于减少,因此阳极室溶液质量减少 ,D项正确。
命题动向
将电化学与实际相联系,从“解题”向“解决问题”转变
本题以锂离子电池和电合成己二腈为载体,考查串联电池分析、电极反应、电解液作用等,引导考生多关注创新
科技,有利于培养考生的证据推理和分析推测能力。电化学知识是高考中的热点和难点,常结合前沿科技、实际
生产生活进行考查,拓展考生视野,提升考生利用所学知识解决实际问题的能力。
6.[2022山东卷](双选)设计如图装置回收金属钴。保持细菌所在环
境稳定,借助其降解乙酸盐生成 ,将废旧锂离子电池的正极
材料转化为 ,工作时保持厌氧环境,并定时将乙
室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电
池。下列说法正确的是( )
BD
A.装置工作时,甲室溶液 逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为
D.若甲室减少,乙室增加 ,则此时已进行过
溶液转移
【解析】原理分析
根据右侧装置为原电池,乙酸盐降解为二氧化碳,发生氧化反应,转化为 ,发生还原反应,知右侧装
置左电极为负极,右电极为正极;左侧装置为电解池,左电极为阳极,乙酸盐转化为 气体,右电极为阴极,
转化为 单质。
装置工作时,甲室为阴极室,阳极发生反应 ,结合阴极反应及电解液呈
电中性知,阳极生成的通过阳膜进入阴极室,故甲室溶液 减小,A项错误;乙室为正极室,正极反应为
,消耗生成 ,电解质溶液酸性减弱,需要补充盐酸,B项正确,C
项错误;根据甲室中电极反应和乙室中电极反应可知,甲室中减少的 的质量为乙室中增加的
的质量的一半,则甲室减少,乙室增加 时已进行过溶液转移,D项正确。
7.[2023北京卷节选]尿素 合成的发展体现了化学科学与技术的不断进步。近
年研究发现,电催化和含氮物质( 等)在常温常压下合成尿素,有助于实现碳
中和及解决含氮废水污染问题。向一定浓度的溶液通 至饱和,在电极上反应生
成 ,电解原理如图所示。
①电极 是电解池的____极。
阳
【解题思路】 电极上失电子发生氧化反应生成 ,是电解池的阳极。
②电解过程中生成尿素的电极反应式是______________________________________________。
【解题思路】 电极 上硝酸根离子得电子发生还原反应生成尿素,再结合电解液环境(酸性)、电荷守恒、原子
守恒可写出电极反应式。
7-1.变物质[2024江苏南京六校调研]隔膜电解法同时脱硫脱硝的装置如图
所示,其中电极A、B均为惰性电极,电解液为稀硫酸。为提高脱除效率,
将阴极室的溶液调至 ,则阴极上的电极反应为________________
___________________。
【解题思路】 惰性电极A侧转变为,元素由价变为 价,
则电极A为电解池的阴极,结合电解液为稀硫酸可得阴极的电极反应式
为 。
创新1+1
1.新角度·与速率图像结合[2024江苏南通如皋考试]科研人员
发现利用低温固体质子导体作电解质,催化合成 ,与
传统的热催化合成氨相比,催化效率较高。其合成原理如
图1所示,电源电压改变与生成 速率的关系如图2所示,
下列说法不正确的是( )
C
A. 是该合成氨装置的阳极
B.电极上发生的反应为
C.若的进出口流量差为,则固体质子导体中的流速为
D.当电压高于时,混合气体中和的体积分数之和小于
【解析】原理分析
由题图1可知,电极上,是电解池的阳极,电极反应式为, 电极为阴极,
电极反应式为 。
由上述分析可知,A、B项正确;未给出气体所处状态,无法计算内氢气的物质的量和反应生成 的物
质的量,所以无法计算固体质子导体中的流速,C项错误;由题图2可知,当电压高于 时,氨气生成速率变
慢,说明部分在阴极得到电子生成氢气,导致混合气体中氮气和氨气的体积分数之和小于 ,D项正确。
2.新考法·通过电解法测定的值[2023北京海淀区练习]阿伏加德罗常数 是一座“桥梁”,连接了宏观世界和微观
世界的数量关系。通过电解法可测得 的数值。
已知:个电子所带电量为 库仑。
(乙二胺四乙酸二钠)能形成可溶含铜配离子。
ⅲ, 。
【实验一】用铜片和铂丝为电极,电解硫酸酸化的溶液。测得通过电路的电量为 库仑。电解完成后,取出
铜片,洗净晾干,铜片质量增加了 。
(1)铜片应连接电源的______(填“正极”或“负极”)。铂丝尖端产生气泡,其电极反应式为
____________________________。理论上,产生气体与析出铜的物质的量之比为_____。
负极
【解题思路】电解完成后,铜片质量增加,则铜片上发生还原反应: ,铜片为阴极,应连接电源
的负极。铂丝为阳极,发生氧化反应: 。根据两电极上通过的电量相等知,产生 与
析出铜的物质的量之比为 。
(2)本实验测得______________ (列出计算式)。
【解题思路】根据通过电路的电量为库仑,知电路中通过电子的数目为,根据 ,知电
路中通过电子的数目为,,则 。
【实验二】为减少含重金属电解液的使用,更换电解液,同时更换电极与电源的连接方式。电解完成后,取出铜
片,洗净晾干,铜片质量减小。
实验 电解液 实验现象
① 溶液 铜片表面为灰蓝色
② 和混合液 铜片表面仍为红色
(3)实验①和②中各配制电解液 ,使用的主要仪器有天平、烧杯、玻璃棒、胶头滴管和______________。
容量瓶
(4)经检验,实验①中的灰蓝色成分主要是。从平衡移动角度解释在测定 的数值中的作用:
___________________________________________________________________________________________________
________________________________________________________________。
,与生成配离子,下降,平衡向溶解方向移动,铜片表面的消失,铜片的质量变化数据准确,可准确测得的数值
(5)电解过程中,若观察到铜片上有小气泡产生,利用铜片质量减小计算 的数值,结果将______(填“偏大”“偏
小”或“不变”)。
偏大
【解题思路】电解过程中,铜电极上单质铜放电生成(Ⅱ),若观察到铜片上有小气泡产生,说明电极上 也
放电,电路中通过的电子数增多,则利用铜片减小的质量计算的 的数值偏大。
(6)实验结束后处理电解液:将取出的电解液加入过量硫酸,过滤,得到白色固体和滤液;向滤液 中先
加入调,再加入,解释不直接加入的原因及 的作用:_____________________________
___________________________________________________________________________________。
若直接加入,可能产生有毒气体;调后,加可进一步降低溶液中铜离子的浓度,同时沉淀转化为
【解题思路】滤液中含有稀硫酸和(Ⅱ),若直接加入,和反应产生有毒气体;调 后,
加可进一步降低溶液中铜离子的浓度,同时可使沉淀转化为 。
命题动向
本题将实验探究与反应原理知识融合,对相关知识进行多维度多层次的考查,有利于促进考生的批判性、缜密性
和系统性思维品质的养成。
考点28 金属的腐蚀与防护
03
经典3+2
1.[2024广东惠州调研]下列现象与电化学腐蚀无关的是( )
B
A.铜锌合金(黄铜)不易被腐蚀 B.银质物品久置表面变黑
C.附有银制配件的铁制品其接触处易生锈 D.铁锅炒菜后未洗净擦干容易生锈
【解析】铜锌合金形成原电池时,锌作负极被腐蚀,铜作正极被保护,A项与电化学腐蚀有关;金属银能和空气中
的二氧化硫、氧气等发生反应,故银质物品久置表面变黑属于化学腐蚀,B项与电化学腐蚀无关;铁制品附有银制
配件时,在接触处形成原电池,铁作负极被氧化,故C项与电化学腐蚀有关;铁锅炒菜后未洗净擦干,铁、碳和电
解质溶液构成原电池, 作负极被腐蚀,D项与电化学腐蚀有关。
2.[2024辽宁部分学校联考]科学研究发现金属生锈时,锈层内如果有硫酸盐
会加快金属的腐蚀,其腐蚀原理如图所示。下列说法错误的是( )
C
A.钢铁的腐蚀中正极电极反应式为
B.酸雨地区的钢铁更易被腐蚀
C.生成 反应的化学方程式为
D.硫酸盐加速电子传递,有一定的催化剂作用
【解析】由图可知钢铁发生吸氧腐蚀,C作正极,氧气在正极得电子,电极反应式为 ,
A项正确; 酸性溶液可以加速铁的腐蚀,B项正确;不稳定,易被氧气氧化生成 ,化学方程式为
,C项错误;根据题干信息可知,锈层内如果有硫酸盐会加快金属的腐蚀,
硫酸盐能增加导电性,加速电子传递,有一定的催化剂作用,D项正确。
3.[2024广东广州阶段训练改编]全世界每年的钢铁锈蚀会造成巨大的损失,
为了保护地下的钢铁输水管所采取的措施如图所示。下列说法不正确的是
( )
D
A.钢铁发生吸氧腐蚀过程中负极反应为
B.导线与 块连接为牺牲阳极法
C.导线应连接外接电源的负极
D.导线与 块连接也可保护钢铁输水管
【解析】钢铁发生吸氧腐蚀过程中,负极上失去电子转化为,A项正确;导线与 块连接,为原电池,属于
牺牲阳极法,B项正确;外接电源时,钢铁作阴极,导线应连接外接电源的负极,C项正确;铜的金属活动性比铁
弱,导线与 块连接不能保护钢铁输水管,D项错误。
4.[2022广东卷]为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放入酸化的 溶液
中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是( )
D
A.加入 溶液产生沉淀 B.加入淀粉碘化钾溶液无蓝色出现
C.加入溶液无红色出现 D.加入 溶液无蓝色沉淀生成
【解析】若铁片被腐蚀,则溶液中含有,在溶液中加入溶液,反应生成蓝色的 沉淀,
D项正确;A项只能检验溶液中含有,B项只能检验溶液中无强氧化性物质,C项只能检验溶液中无 ,三者
均不能说明铁片没有被腐蚀。
4-1.变实验[2023北京101中学质检]实验小组研究金属电化学腐蚀,实验如下:
序号 实验
实验Ⅰ 铁钉表面及周边未见明显变化 铁钉周边零星、随机出现极少量红色和蓝色区
域,有少量红棕色铁锈生成
实验Ⅱ 铁钉周边出现红色区域,未见 蓝色出现; #b# 锌片周边未见明显变化 铁钉周边红色加深,区域变大,未见蓝色出
现;
#b#
锌片周边未见明显变化
下列说法不正确的是( )
A
A.实验Ⅰ的现象说明溶液与反应生成了
B.实验Ⅱ中保护了 ,使铁的腐蚀速率比实验Ⅰ小
C.实验Ⅱ中正极的电极反应式:
D.若将片换成片,推测 片周边会出现红色,铁钉周边会出现蓝色
【解析】根据实验Ⅰ的现象可知,与生成蓝色沉淀(【易错】 与铁氰化钾溶液反
应生成蓝色沉淀,与硫氰化钾反应使溶液呈红色,可分别用来鉴别和。), 使酚酞溶液变红,
最后有少量红棕色铁锈生成,发生了吸氧腐蚀,不能说明与反应生成了 ,A项错误。实验Ⅱ中,
比活泼,故锌片作负极被氧化,保护了,从而使 的腐蚀速率降低,B项正确。实验Ⅱ中的铁钉周边溶液中
出现红色区域说明生成了,则正极反应式为,C项正确。实验Ⅱ中,将片换成
片,则铁钉为负极,被氧化,电极反应式为,生成的与反应生成 ,
则铁钉周边出现蓝色,片为正极,被还原,生成, 片周边出现红色,D项正确。
5.[2023北京清华大学附属中学考试]家庭常用的一种储水式电热水器的结构如图所示,其中、 为水管口。
下列说法不正确的是( )
C
A.电热水器可将电能转化为热能 B.该热水器采用了牺牲阳极的电化学保护法
C.镁棒可以有效防止内部水垢生成 D.应为出水口, 应为进水口
【解析】
6.[2023湘豫名校联考]青铜器文物腐蚀物以粉末状有害锈最为严重,某种碱式氯化铜粉状锈的形成过程分三个阶段:
阶段一:铜在电解质溶液中发生一般腐蚀,; (灰白色);
;
阶段二: ;
阶段三:和具有很强穿透力,可深入铜体内部,产生粉状锈, 。
下列说法正确的是( )
A
A.该粉状锈生成的条件中需要有:潮湿环境、可溶性的氯化物、氧化性的物质
B.上述过程涉及的化学反应有:电解反应、水解反应、氧化还原反应
C.依据反应 ,可以判断氧化亚铜不能溶于盐酸
D.利用外加电流法保护铜制文物时,青铜器应连接电源的正极
【解析】由三个阶段的反应可知,碱式氯化铜粉状锈产生的基本条件是:可溶性的氯化物、潮湿环境和氧化性的物质,A项正确;没有涉及电解反应,题中是原电池原理,没有形成电解池,B项错误;氧化亚铜能溶于盐酸,C项错误;保护铜制文物时,即防止铜失去电子被氧化,则青铜器应该接电源负极,若是接电源正极,则作阳极,会加速失去电子,不能起到保护作用,D项错误。
创新1+1
1.新考法·浓硫酸贮存罐的钝化金属保护法[2022上海卷]浓硫酸贮存罐的钝化
金属保护法示意图如图,其原理是利用可钝化的金属与直流电源相连,控制
合适的电压,使金属贮存罐表面形成致密的钝化膜,以有效减缓金属腐蚀。
下列选项错误的是( )
C
A.金属贮存罐可用钢制材料 B.电子沿导线流入辅助电极
C.贮存浓硫酸的金属罐与电源负极相连 D.电压高到一定程度有可能会加剧腐蚀
【解析】原理分析
钢的主要成分是铁,铁遇冷的浓硫酸发生钝化,因此金属贮存罐可用钢制材料,A正确;贮存浓硫酸的金属罐为阳极,连接电源正极,辅助电极是阴极,电子沿导线流向辅助电极,B正确,C错误;电压过高时,有可能会加剧腐蚀,D正确。
2.新形式·实验装置图+温度、压强与时间关系图[2024四川南充考试改编]某实验小组要定量探究铁锈蚀的因素,设
计如图所示实验装置,检查气密性,将铁粉和碳粉加入三颈烧瓶,加入 饱和氯化钠溶液后,再将一
只装有 稀盐酸的注射器插到烧瓶上,采集数据。下列说法错误的是( )
C
A.铁发生锈蚀的反应是放热反应
B. 温度降低是因为反应速率减慢了
C. 段压强减小是因为铁和氧气直接反应生成了氧化铁
D. 压强变大是因为发生了铁的析氢腐蚀
【解析】由温度与时间的关系曲线可知,温度升高,铁发生锈蚀的反应是放热反应,A项正确; 反应速率
减慢,铁锈蚀放出的热量小于装置散失的热量,温度降低,B项正确;铁在氧气和水共同作用下反应生成铁锈,铁
锈的主要成分为氧化铁,C项错误;铁锈蚀消耗氧气,装置内压强减小,注射器内稀盐酸被吸入烧瓶,反应产生较
多氢气,压强变大(【点拨】铁粉一开始在氯化钠溶液中发生吸氧腐蚀,后期稀盐酸被吸入烧瓶,在酸性条件下
发生析氢腐蚀。),D项正确。
命题动向
本题结合传感器和图像考查铁锈蚀的实验,形象直观,是教材实验的创新设计。
热考题型13 新型电化学装置分析
04
1.新考法·与压力有关的浓差电池[2024湖北部分名校联考]两个负载有不同压力
的氢气的片插入一定浓度的酸性介质中构成的浓差电池如图所示 ,
电池工作时 逐渐增大。下列说法不正确的是( )
A
A.电流方向:电极 电流表 电极
B.电极上发生的反应为
C.电池工作原理为
D. 为质子交换膜
【解析】,该电池工作时电极为负极,发生反应;逐渐增大, 电极为正极,发生反应
;电子流向为电极 电流表电极,电流方向与电子流向相反;电极产生的会穿过
移向电极,则为质子交换膜;电池工作原理为 。由上述分析可知,A项错误,B、C、D项正确。
2.[2024天星原创]在能源短缺、环境污染日益严重的现代社会,太阳能的利用一直是科学研究的热点。一种染料
敏化光伏电池的结构和工作原理如图1、图2所示。下列有关说法错误的是( )
D
A.染料电极为电池的负极 B.石墨电极的电极反应式为
C.电池工作过程中,和的浓度基本保持不变 D.碘系电解液可以用溶液,也可以用 溶液
【解析】
3.[2023湖北卷]我国科学家设计如图所示的电解池,实现了海水直接制备氢气技术的绿色化。该装置工作时阳极无
生成且溶液的浓度不变,电解生成氢气的速率为 。下列说法错误的是( )
D
A.电极反应式为
B.离子交换膜为阴离子交换膜
C.电解时海水中动能高的水分子可穿过 膜
D.海水为电解池补水的速率为
【解析】根据图示, 电极与电源负极相连,为阴极,结合题干信息可知,阴极反应式为
,A正确;该装置工作时阳极无氯气产生,则阳极反应式为
,又阳极溶液的浓度不变,则需要 由阴极移向阳极,故离子交换膜为阴离子
交换膜,B正确;电解过程中,阳极 溶液的浓度不变,而阳极不断有水分子消耗,结合题图,海水中动能高的
水分子 (【提示】气态水分子。)可以穿过 膜,为阳极补充水,C正确;由阴、阳极反应式可知,电解总反
应式为 ,已知电解生成氢气的速率为 ,则海水为电解池补水的速率也为
,D错误。
4.[2024福建福州质检]我国科学家经过研究发明了以下装置从海水中提取锂单质,其工作原理如图所示。该装置运
行期间电极Ⅱ上产生和气体 。下列说法错误的是( )
C
A.该装置实现了“太阳能 电能 化学能”的转化
B.电极Ⅰ连接太阳能电池的负极
C.工作时,电极Ⅱ附近溶液的 增大
D.实验室检验气体可用湿润的淀粉 试纸
【解析】原理分析
根据该装置可知,太阳能电池将太阳能转化为电能,电解装置又将电能转化为化学能,A选项正确;电极Ⅰ为电解
池的阴极,连接太阳能电池的负极,B选项正确;由电极Ⅱ的电极反应式可知,电极Ⅱ上产生 ,则电极Ⅱ附近溶
液降低,C选项错误;气体为(黄绿色气体),实验室检验可用湿润的淀粉 试纸,试纸变蓝即说明
存在,D选项正确。
5.[2023重庆卷]电化学合成是一种绿色高效的合成方法。如图是在酸性介质中电解合成半胱氨酸和烟酸的示意图。
下列叙述错误的是( )
D
A.电极 为阴极
B.从电极移向电极
C.电极 发生的反应为:
D.生成半胱氨酸的同时生成 烟酸
【解析】原理分析
有机反应中“加氢去氧”的反应为还原反应,“加氧去氢”的反应为氧化反应,据此分析电解池中各电极类型及电极反应如下:
由上述分析知,A正确,C正确;电解池中阳离子向阴极移动,故从电极移向电极 ,B正确;根据阴、阳极反
应及得失电子守恒可知,生成半胱氨酸,转移电子,同时生成 烟酸,D错误。
6.[2023广东模拟]我国科学家设计了一种新型的溴基液流可充电电池用
于大规模储能,其放电时的工作原理如图所示。下列有关说法不正确
的是( )
C
A.放电时, 极为正极
B.放电时,极发生的电极反应为
C.充电时,每生成有穿过质子交换膜进入 极室
D.充电时,总反应为
【解析】
放电时,极为正极,A项正确;放电时, 极为负极,电极反应为
,B项正确;充电时, 极为阳极,电极
反应为,则每生成 ,
转移电子,有穿过质子交换膜进入 极室,C项错误;
由阴、阳极反应可知,充电时的总反应为
,D项正确。
命题动向
电化学是高考必考知识,以新型电池为载体考查电化学知识是高考
的高频考查角度,有利于考查考生的知识迁移、应用能力,培养考
生的创新思维。
7.[2023山东卷](双选)利用热再生氨电池可实现 电镀废液的浓缩
再生。电池装置如图所示,甲、乙两室均预加相同的 电镀废液,向甲
室加入足量氨水后电池开始工作。下列说法正确的是( )
CD
A.甲室 电极为正极
B.隔膜为阳离子膜
C.电池总反应为:
D. 扩散到乙室将对电池电动势产生影响
【解析】为实现电镀废液的浓缩再生,据图可知,甲室流出液经低温热解得到和 ,则甲室中生成
了,发生的反应为,甲室电极为负极,A错误;乙室 电极
为正极,发生反应:,消耗,为维持电解质溶液呈电中性, 透过隔膜进入甲室,则隔
膜为阴离子膜,B错误;根据正、负极反应,可知电池总反应为,C正确; 能
与反应生成,因此若扩散到乙室,则乙室 浓度减小,对电池电动势有影响,D正确。
8.[2024天星原创]利用一种微生物燃料电池(原理如图Ⅰ所示),以维生素C的钠盐,简写 为原
料制备维生素,简写,具有弱酸性和还原性,装置如图Ⅱ所示。、 为水电离出来的离子,下列说法
正确的是( )
A
A.图Ⅰ中极的电极反应式为
B.图Ⅱ中极应连接图Ⅰ中的极,和分别代表、
C.将①室的溶液替换为溶液,可发生氧化反应生成
D.若极有(标准状况下)参与反应,则图Ⅱ装置中极产生
【解析】
专题综合训练
05
1.[2024北京石景山区模拟]以氨为燃料的固体氧化物燃料电池具有广阔的应用前景,一种氧离子导电的
的工作原理如图所示在催化剂作用下先分解为和 。下列说法不正确的是( )
C
A.在负极放电 B.正极的电极反应为
C.外电路转移,理论上生成 D. 向负极移动
【解析】
2.[2023湖北武汉武昌区质检]我国科技工作者利用水热法制备了
六方钴纳米片,可应用于高效电催化 的还原。下
列说法错误的是( )
C
A.六方钴纳米片有利于 分子的活化
B.负极的电极反应为:
C.理论上每消耗,可放出
D.该过程的总反应为
【解析】原理分析
由题给条件“可应用于高效电催化的还原”可知,六方钴纳米片有利于分子的活化,A项正确;负极 失电子
转化为,结合电解液环境可知,其电极反应为 ,B项正确;理论上每消耗
,转移电子,根据转化为转移知,生成 ,但没有给出气体所
处的温度和压强,其体积不一定为 ,C项错误;结合正、负极反应可知,总反应为
,D项正确。
3.[2024天星原创]孔蚀(一种集中于金属表面很小的范围并深入到金属
内部的腐蚀形态)是一种常见的电化学腐蚀现象,某铁合金钝化膜破
损后的孔蚀如图。下列关于金属腐蚀与防护的说法错误的是( )
B
A. 的存在会加速该铁合金的腐蚀速率
B.“孔”的表面与内部所发生的腐蚀主要是吸氧腐蚀
C.在表面形成钝化膜可以让铁合金连接外接电源的正极
D.铁合金与锌块连接可有效防止铁被腐蚀
【解析】金属离子不易向外扩散,金属离子增多,会吸引外部 迁入
以维持电中性,“孔”内介质导电性增强,则 的存在会使该铁合金的
腐蚀速率加快,A正确。根据题图可以得出“孔”的表面发生吸氧腐蚀,而其内部介质含有 ,主要发生析氢腐蚀,
B错误。若使铁合金表面被氧化产生钝化,铁合金应该与外接电源的正极连接,充当阳极,发生氧化反应,C正确。
锌的活泼性强于铁,铁合金与锌块连接后可以有效防止金属铁被氧化腐蚀(【原理应用】出海的轮船为了防止船
体被腐蚀,通常在船身外侧放置锌块,原理与此处一致。),D正确。
4.[2023北京东城区练习]用石墨作电极电解 浊液,记录如表。
实验装置 实验现象 Ⅰ.为 Ⅱ.为
两电极均产生气泡,有黑色固体在阴极附 近生成,并沉降在电解槽底部,电解槽中 的液体逐渐变澄清透明 两电极均产生气泡,阴极表面附着少量
银白色固体,电解槽中的液体逐渐变为
棕黄色
下列说法不正确的是( )
C
A.Ⅰ中阳极气体可能为和,Ⅱ中阳极气体为
B.Ⅰ和Ⅱ中阴极生成气体的方程式均为
C.Ⅱ中液体变为棕黄色,说明阳极上发生了反应
D.两实验阴极现象有差异的原因可能是Ⅱ中 比Ⅰ中的小
【解析】原理分析
由实验现象可知,Ⅰ中阳极上和(或)发生氧化反应生成和,阴极上和(或 )发生还原
反应生成和;Ⅱ中阳极上(或)发生氧化反应生成,阴极上(或)和少量 发生还原反应
生成和 。
由上述分析知,A项正确;Ⅰ和Ⅱ中阴极上生成的气体均为,都是(或 )发生还原反应产生的,电极反应
为,B项正确;的溶解度较小,溶液中 小,由电解槽中液体逐渐变为棕黄色知,
阳极生成的将氧化为了,C项错误;的溶解度大于,浊液中大于浊液中 ,所以Ⅰ
中在阴极放电生成,并沉降在电解槽底部,Ⅱ中少量在阴极放电生成 附着在电极上,D项正确。
5.[2023山东济宁模拟](双选)芳香羧酸是一种重要的有机分子骨架,利用电化学方法,芳香烃与 选择性的
键羧基化反应如图所示,下列说法错误的是( )
AB
A.生成芳香羧酸,电路中转移的电子数为(设 为阿伏加德罗常数的值)
B.电池工作过程中需要不断补充
C.不同的取代基 可能影响路径Ⅰ或Ⅱ的选择
D.该反应的原子利用率为
【解析】&16& .
由题图可知,该反应有不同的路径,则不同的取代基 可能影响路径Ⅰ或Ⅱ的选择,C正确。该反应的总化学方程
式为 ,反应物有两种,生成物只有一种,因此该反应是化合反应,原子利用率为 ,
D正确。
6.[2023新课标卷]一种以和为电极、 水溶液为电解质的电池,其示意图如下所示。放电时,
可插入层间形成 。下列说法错误的是( )
C
A.放电时 为正极
B.放电时 由负极向正极迁移
C.充电总反应:
D.充电阳极反应:
【解析】原理分析
放电时失去电子生成,为负极,则为正极,A正确;放电时,阳离子 移向正极,B正确;由上
述分析可知,放电总反应为 ,充电总反应为
,C错误;由上述分析可知,D正确。
7.[2024天星原创]四甲基氢氧化铵
,强有机碱]常用作电子工业清洗
剂。以四甲基氯化铵 为原料,利用
电渗析法合成 的工作原理如图。下
列叙述错误的是( )
C
A.极接电源负极,工作时电极上产生气体
B.膜为阳离子交换膜, 膜为阴离子交换膜
C.工作时电极上产生气体
D.若两极共产生 (标准状况)气体,则
理论上得到
【解析】解题关键
根据进出装置的物质浓度判断粒子移动方向 根据粒子移动方向判断电极类型。
Ⅰ室中稀溶液浓溶液,说明Ⅱ室中的移入Ⅰ室, 为阴极,接电源负极,工作时
电离出的在电极上放电产生气体,A正确;Ⅱ室中的移入Ⅰ室, 膜为阳离子交换膜,Ⅱ室中
浓溶液稀溶液,说明移入Ⅲ室,膜为阴离子交换膜,Ⅲ室中稀溶液 浓溶液,
说明移入Ⅲ室,膜为阳离子交换膜,B正确;工作时电极上产生气体(【点拨】放电产生 ,
。),C错误;综上分析,总反应实质是电解
的反应,根据电路中通过的电流处处相等,可得关系式: ,若两极共产生
气体,则理论上得到 ,D正确。
8.[2024山东青岛调研改编]利用浓差电池电解溶液、电极均为石墨电极,可制得、、 和
,反应原理如图所示。下列说法正确的是( )
D
A.极的电极反应式为
B.、 分别为阴离子交换膜和阳离子交换膜
C.浓差电池放电过程中,电极上的电极反应式为
D.浓差电池从开始工作到放电结束,电解池理论上可制得
【解析】根据电子流动方向可知,极为电解池的阴极,电离出的得电子发生还原反应生成 ,电极反应式
为,为阳离子交换膜,通过阳离子交换膜进入阴极室,阴极区 溶液浓度不
断增大,极为电解池的阳极,失电子发生氧化反应生成,电极反应式为, 为阴
离子交换膜,通过阴离子交换膜进入阳极室,阳极区溶液浓度不断增大,A、B项错误; 为原电池
的正极,电极反应式为,为原电池的负极,电极反应式为 ,C项错误;浓
差电池从开始工作到放电结束,正极区硫酸铜溶液浓度由降低到 ,负极区硫酸铜溶液浓度
由上升到,即正极区被还原的的物质的量为 ,负极
区被氧化的的物质的量为,电路中转移 电子,理论上电解池阴极区生成
,即阴极区可得,其质量为 ,D项正确。
9.[2023江苏卷节选]催化电解吸收的溶液可将 转化为有机物。在相同
条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率
随电解电压的变化如图所示。
其中,,表示电解生成还原产物所转移电子的物质的量, 表示法拉第常数。
①当电解电压为时,电解过程中含碳还原产物的 为0,阴极主要还原产物为____(填化学式)。
【解题思路】当电解电压为时,电解过程中含碳还原产物的 为0,说明阴极无含碳物质生成,则阴极电极
反应为,即阴极主要还原产物为 。
②当电解电压为时,阴极由生成 的电极反应式为_____________________________________。
【解题思路】当电解电压为时,阴极发生还原反应,根据电荷守恒、原子守恒可写出由生成 的电极
反应式为 。
③当电解电压为时,电解生成的和 的物质的量之比为 ______________________________________
__________________________________________________________________________ (写出计算过程)。
【解题思路】由图可知,当电解电压为时,,而转移, 转移
,结合题给信息可知,,所以,即当电解电压为 时,阴极
生成和的物质的量之比为 。
生成转移 电子,生成
转移电子,,
10.[2022北京卷]煤中硫的存在形态分为有机硫和无机硫 、硫
化物及微量单质硫等 。库仑滴定法是常用的快速检测煤中全硫含
量的方法,其主要过程如图所示。
已知:在催化剂作用下,煤在管式炉中燃烧,出口气体中主要含
、、、、 。
(1)煤样需研磨成细小粉末,目的是________________________________________________________。
(2)高温下,煤中的完全转化为 ,该反应的化学方程式为___________________________________。
增大固体与空气的接触面积,加快反应速率,使煤粉完全燃烧
【解题思路】在高温条件下,硫酸钙和C反应生成氧化钙、二氧化硫和二氧化碳。
(3)通过干燥装置后,待测气体进入库仑测硫仪进行测定。
已知:库仑测硫仪中电解原理示意图如图。检测前,电解质溶液中
保持定值时,电解池不工作。待测气体进入电解池后, 溶
解并将还原,测硫仪便立即自动进行电解到 又回到原定值,
测定结束。通过测定电解消耗的电量可以求得煤中含硫量。
① 在电解池中发生反应的离子方程式为___________________________________。
【解题思路】根据题目信息可知,二氧化硫在电解池中与溶液中的 反应生成碘离子、硫酸根离子和氢离子。
②测硫仪工作时电解池的阳极反应式为_________________。
【解题思路】由题意可知,测硫仪工作时,碘离子在阳极失去电子发生氧化反应生成 ,电极反应式为
。
(4)煤样为,电解消耗的电量为 库仑。煤样中硫的质量分数为_______。
已知:电解中转移 电子所消耗的电量为96 500库仑。
【解题思路】根据题意可得关系式:,电解消耗的电量为 库仑,则煤样中硫的质量分数为
。
(5)条件控制和误差分析。
①测定过程中,需要控制电解质溶液的。当时,非电解生成的使测得的全硫含量偏小,生成 的离子
方程式为______________________________。
【解题思路】由已知信息可知,待测气体中含有,可将氧化为 。
②管式炉中煤样燃烧时会有少量 产生,使测得的全硫含量______(填“偏大”或“偏小”),该测量结果可进行校正。
偏小
【解题思路】直接溶解在溶液中生成,会使与反应的 元素偏少,导致测得的全硫含量偏小。
同课章节目录
