第三节 氧气的实验室制取 课件(共38张PPT内嵌视频)
文档属性
| 名称 | 第三节 氧气的实验室制取 课件(共38张PPT内嵌视频) |

|
|
| 格式 | pptx | ||
| 文件大小 | 76.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-07 00:00:00 | ||
图片预览








文档简介
(共38张PPT)
第三节 氧气的实验室制取
氧气与世间万物如影随行,以上的场景都需要用到氧气,那你知道氧气是怎样制取的吗?今天就让我们一起学习吧!
动植物的呼吸
燃料的燃烧
钢铁的冶炼
金属的焊接
学习目标
1、通过讨论和交流,知道实验室制取气体的一般思路,知道催化剂及其对化学反应的作用.(重点)
2、通过实验探究,能完成实验室制取氧气的方法和步骤.(难点)
通电
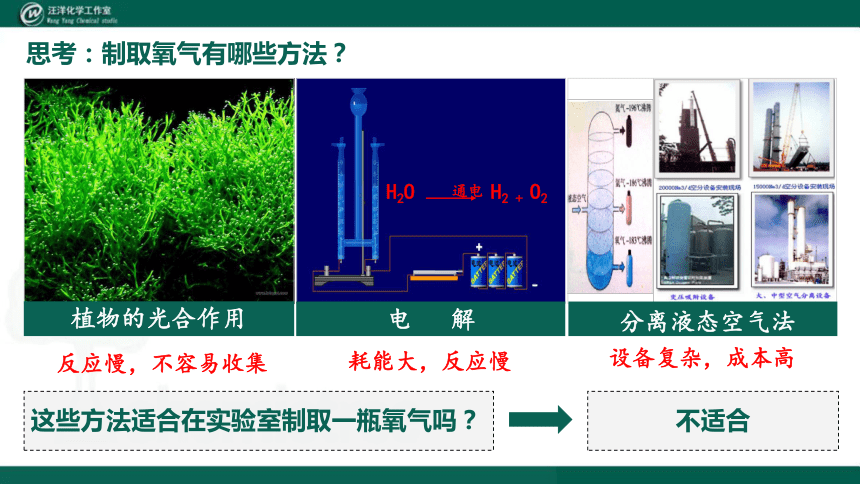
植物的光合作用
电 解 水
分离液态空气法
反应慢,不容易收集
耗能大,反应慢
设备复杂,成本高
思考:制取氧气有哪些方法?
这些方法适合在实验室制取一瓶氧气吗?
H2O H2 + O2
不适合
学习任务一:氧气实验室制取的原理
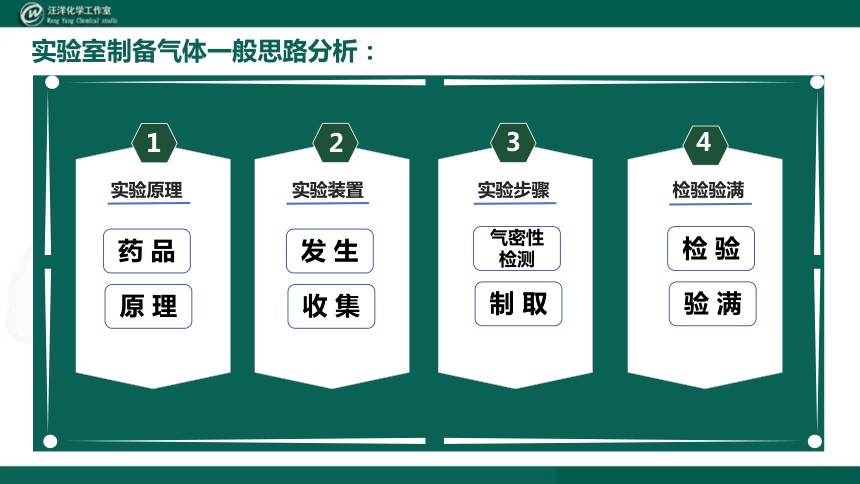
实验室制备气体一般思路分析:
实验原理
实验装置
实验步骤
检验验满
1
2
3
4
药 品
原 理
发 生
收 集
气密性
检测
制 取
检 验
验 满
问题1:你认为下列哪些物质不能作为实验室制取氧气的反应物?
1.选择反应物
水(H2 )
氯化钠
(NaCl)
铜(Cu)
甲烷(CH4)
(H2 2)
过氧化氢溶液
高锰酸钾
KMn 4
氯酸钾
KCl 3
O
O
O
O
首选必要条件:原料中必须含有氧元素。
A.原料是否容易获得
B.实验条件是否容易控制
C.实验装置是否容易装配
D.实验操作是否安全可靠
问题2:小明认为,实验室制取气体的化学反应,应考虑以下几个方面。
2.反应条件
同意,还要考虑成本、是否产生有毒物质、反应速度、反应是否耗能
简便 快捷 安全 可控 节约 环保
物质
相关资料
高锰酸钾(KMnO4) 〈紫黑色固体〉 受热分解放出氧气(O2)
氯酸钾(KClO3) 〈白色晶体〉 400℃时分解放出氧气(O2)
水(H2O) 〈无色液体〉 在通直流电时可以分解得到氧气(O2)和氢气(H2)
过氧化氢(H2O2) 〈无色液体〉 俗称双氧水,易分解,常温下就可以生成氧气和水,价格低廉,产物无污染。
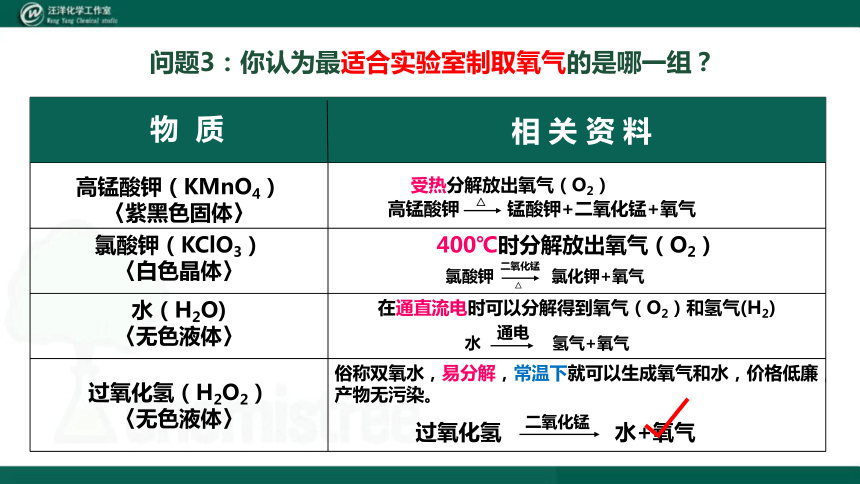
问题3:你认为最适合实验室制取氧气的是哪一组?
过氧化氢 水+氧气
二氧化锰
物 质
相 关 资 料
高锰酸钾 锰酸钾+二氧化锰+氧气
△
氯酸钾 氯化钾+氧气
二氧化锰
△
水 氢气+氧气
通电
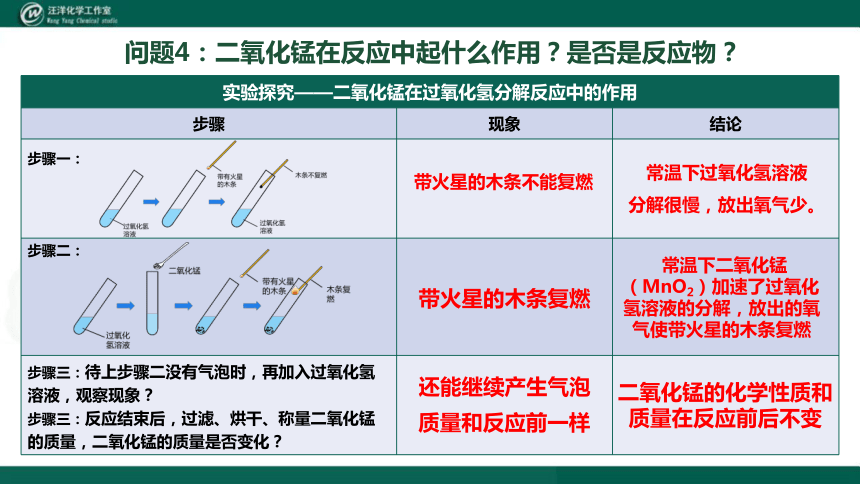
问题4:二氧化锰在反应中起什么作用?是否是反应物?
实验探究——二氧化锰在过氧化氢分解反应中的作用 步骤 现象 结论
步骤一:
步骤二:
步骤三:待上步骤二没有气泡时,再加入过氧化氢溶液,观察现象? 步骤三:反应结束后,过滤、烘干、称量二氧化锰的质量,二氧化锰的质量是否变化?
带火星的木条不能复燃
常温下过氧化氢溶液
分解很慢,放出氧气少。
带火星的木条复燃
常温下二氧化锰(MnO2)加速了过氧化氢溶液的分解,放出的氧气使带火星的木条复燃
还能继续产生气泡
质量和反应前一样
二氧化锰的化学性质和质量在反应前后不变
催化剂
定义:在化学反应中能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫催化剂(又叫触媒)。
(特点:一变二不变)
一 变:
二不变:
改变其它物质的化学反应速率
在化学反应的前后
本身的质量
化学性质
催化
剂
炼油厂使用的催化剂
工业上合成氨气的铁催化剂
生物酶催化剂
硫酸生产中使用的五氧化二钒催化剂
处理汽车尾气的铂催化剂
某些抗衰老化妆品中含有催化剂
多识一点
催化剂针对性训练
(1)催化剂在化学反应前后自身的质量和性质均不变( )
(2)催化剂一定加快化学反应速率 ( )
(3)催化剂参与了化学反应的过程 ( )
(4)使用催化剂可以增加生成物的质量 ( )
(5)二氧化锰是所有化学反应的催化剂 ( )
×
×
√
×
×
1.判断正误:
2.实验室用过氧化氢制氧气的实验中,应加入少量二氧化锰。下列说法中正确的是( )
A. 只有二氧化锰能作过氧化氢分解的催化剂
B. 二氧化锰只能作过氧化氢分解的催化剂
C. 加入二氧化锰可以增加过氧化氢分解产生氧气的质量
D. 二氧化锰能加快过氧化氢分解
D
3.有a、b两份完全相同的过氧化氢溶液,向a份中加入少量二氧化锰。下图是二者产生氧气的质量m与反应时间t的图象。其中正确的是( )
B
学习任务二:发生装置和收集装置的选择
发生装置
收集装置
3.实验装置
A ;
B ;C ;
D ;E .
E
A
B
C
D
分液漏斗
导气管
锥形瓶
集气瓶
水槽
气体发生装置选择依据:1.反应物和生成物的状态 2.反应条件
固 + 固 气
固+液 气(不需加热)
(4)
(1)
(2)
(3)
(5)
装置简单
随时加入液体试剂
可控制反应的速率
氧气发生装置的选择
可控制反应
发生与停止
棉花
高锰酸钾 → 锰酸钾+二氧化锰+氧气
过氧化氢 → 水 + 氧气
二氧化锰
加热
根据提供的资料想一想,若在实验室中收集氧气应选择 ,并说一说你的依据: 。
A.向上排空气法
B.向下排空气法
C.排水集气法
适用于密度比空气大的气体
适用于密度比空气小的气体
适用于不易或难溶于谁的气体
1.气体在水中的溶解性 2.气体的密度
A或C
氧气收集装置的选择
小资料 :通常状况下,氧气不易溶于水,且不与水反应;在 0℃,1个标准大气压下,其密度为1.429g/L,空气的密度为1.293g/L。
排水法收集(纯净但不干燥)
向上排空气法收集(干燥不纯净)
导管口有气泡连续、均匀产生时收集
导管伸入到接近集气瓶底部
探究析思:收集装置的选择
思考回答:排水法收集气体时如果气体不纯,为什么?
学习任务三:氧气的检验、验满及步骤
直接观察:集气瓶口冒出大气泡,说明氧气已经满了。
验满方法: 将带火星的木条放在集气瓶口,若木条复燃,说明氧气已经满了。
4.验满方法
5.检验方法
检验氧气: 将带火星的木条伸入集气瓶中,若木条复燃,证明是氧气。
观察思考——实验步骤
6.总结归纳——实验步骤
1.组装仪器(自下而上,从左往右)
2.检查装置的气密性(手热法)
3.装药品,先加固体(MnO2 ) ,后加液体(H2O2)
4.收集气体
(用向上排空气法收集要验满,带火星木条放瓶口)
5.正放在桌面(氧气密度大于空气密度)
装置气密性检查方法
把导气管末端插到水里,用手紧握试管的外壁。如果导管口处有气泡冒出,则装置的气密性良好。 关闭分液漏斗活塞,导气管末端浸没水中,用手捂住锥形瓶,看到管口有气泡产生,表明不漏气。 向长颈漏斗注水,使漏斗的下端管口浸没在液面以下(液封),将导气管末端浸没水中,双手紧握锥形瓶,导管口有气泡冒出,说明该装置不漏气。
评价练习题
23-24峄城区期中:
集气
知识拓展——多功能瓶
排空气法:
1.密度大于空气的气体,收集时气体由 进入;
2.密度小于空气的气体,收集时气体由 进入;
a
b
排水法:
瓶中先装满水,无论气体的密度大小,只要气体不溶(难溶)于水,收集时气体都是由 进入。
b
氧气
储气
量气
量气原理:
瓶中储存氧气,用水将氧气排出时,水从____端通入
气体进入万能瓶,占据一定的体积,由于气压作用,会有相等体积的水被压入量筒,最后读出量筒内水的体积,这即为进入万能瓶中的气体的体积。
a
水
氧气
氧气
指示
检验
在医院给病人输氧时,瓶中放约半瓶蒸馏水,可观察给病人输氧气的速度,这时氧气从_____端通入。
检验二氧化碳气体:
瓶内装入适量澄清石灰水用于检验CO2时,气体应从_____端管口通入,现象是澄清石灰水变浑浊。
a
氧气
蒸馏水
二氧化碳
a
澄清石灰水
21-22峄城区期中:
关闭分液漏斗活塞,将导气管末端伸入水中,然后双手握住锥形瓶,观察导管口是否有气泡产生
3.如图装置常用于实验室制取气体。
(1)写出如图中指定仪器的名称:① ,组装装置时此仪器应注意 ;
(2)用高锰酸钾制取并收集纯度较大的氧气,可以选择的装置是 (填字母),该反应属于 (填基本反应类型)反应;
H
长颈漏斗
长颈漏斗下端必须伸入液面以下
BG
分解反应
(3)用过氧化氢制取氧气时,如需控制产生气体的速率,发生装置最好选用
(填字母),用装置H进行排空气法收集氧气,气体应从 (选填“a”或“b”)端通入,原因是 ;
(4)实验室制取硫化氢气体的原理:室温下,块状不溶性的硫化亚铁(FeS)固体与稀硫酸反应(另一产物为硫酸亚铁);
①写出该反应的文字表达式: ;
②若想控制反应的发生和停止,可选用的发生装置为 (填字母);
H
a
氧气的密度大于空气的密度
C
硫化亚铁+稀硫酸→硫酸亚铁+硫化氢
D
写出用高锰酸钾制取氧气的文字表达式
高锰酸钾 → 锰酸钾 +二氧化锰 +氧气
△
分解
AE
A
导管口有连续
均匀气泡放出
试管口没有棉花
氧气不易溶于水
用带火星的木条靠近瓶口,看是否复燃
控制反应的发生与停止
将a加长深入水中
课程结束了,祝学习进步哦!
第三节 氧气的实验室制取
氧气与世间万物如影随行,以上的场景都需要用到氧气,那你知道氧气是怎样制取的吗?今天就让我们一起学习吧!
动植物的呼吸
燃料的燃烧
钢铁的冶炼
金属的焊接
学习目标
1、通过讨论和交流,知道实验室制取气体的一般思路,知道催化剂及其对化学反应的作用.(重点)
2、通过实验探究,能完成实验室制取氧气的方法和步骤.(难点)
通电
植物的光合作用
电 解 水
分离液态空气法
反应慢,不容易收集
耗能大,反应慢
设备复杂,成本高
思考:制取氧气有哪些方法?
这些方法适合在实验室制取一瓶氧气吗?
H2O H2 + O2
不适合
学习任务一:氧气实验室制取的原理
实验室制备气体一般思路分析:
实验原理
实验装置
实验步骤
检验验满
1
2
3
4
药 品
原 理
发 生
收 集
气密性
检测
制 取
检 验
验 满
问题1:你认为下列哪些物质不能作为实验室制取氧气的反应物?
1.选择反应物
水(H2 )
氯化钠
(NaCl)
铜(Cu)
甲烷(CH4)
(H2 2)
过氧化氢溶液
高锰酸钾
KMn 4
氯酸钾
KCl 3
O
O
O
O
首选必要条件:原料中必须含有氧元素。
A.原料是否容易获得
B.实验条件是否容易控制
C.实验装置是否容易装配
D.实验操作是否安全可靠
问题2:小明认为,实验室制取气体的化学反应,应考虑以下几个方面。
2.反应条件
同意,还要考虑成本、是否产生有毒物质、反应速度、反应是否耗能
简便 快捷 安全 可控 节约 环保
物质
相关资料
高锰酸钾(KMnO4) 〈紫黑色固体〉 受热分解放出氧气(O2)
氯酸钾(KClO3) 〈白色晶体〉 400℃时分解放出氧气(O2)
水(H2O) 〈无色液体〉 在通直流电时可以分解得到氧气(O2)和氢气(H2)
过氧化氢(H2O2) 〈无色液体〉 俗称双氧水,易分解,常温下就可以生成氧气和水,价格低廉,产物无污染。
问题3:你认为最适合实验室制取氧气的是哪一组?
过氧化氢 水+氧气
二氧化锰
物 质
相 关 资 料
高锰酸钾 锰酸钾+二氧化锰+氧气
△
氯酸钾 氯化钾+氧气
二氧化锰
△
水 氢气+氧气
通电
问题4:二氧化锰在反应中起什么作用?是否是反应物?
实验探究——二氧化锰在过氧化氢分解反应中的作用 步骤 现象 结论
步骤一:
步骤二:
步骤三:待上步骤二没有气泡时,再加入过氧化氢溶液,观察现象? 步骤三:反应结束后,过滤、烘干、称量二氧化锰的质量,二氧化锰的质量是否变化?
带火星的木条不能复燃
常温下过氧化氢溶液
分解很慢,放出氧气少。
带火星的木条复燃
常温下二氧化锰(MnO2)加速了过氧化氢溶液的分解,放出的氧气使带火星的木条复燃
还能继续产生气泡
质量和反应前一样
二氧化锰的化学性质和质量在反应前后不变
催化剂
定义:在化学反应中能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫催化剂(又叫触媒)。
(特点:一变二不变)
一 变:
二不变:
改变其它物质的化学反应速率
在化学反应的前后
本身的质量
化学性质
催化
剂
炼油厂使用的催化剂
工业上合成氨气的铁催化剂
生物酶催化剂
硫酸生产中使用的五氧化二钒催化剂
处理汽车尾气的铂催化剂
某些抗衰老化妆品中含有催化剂
多识一点
催化剂针对性训练
(1)催化剂在化学反应前后自身的质量和性质均不变( )
(2)催化剂一定加快化学反应速率 ( )
(3)催化剂参与了化学反应的过程 ( )
(4)使用催化剂可以增加生成物的质量 ( )
(5)二氧化锰是所有化学反应的催化剂 ( )
×
×
√
×
×
1.判断正误:
2.实验室用过氧化氢制氧气的实验中,应加入少量二氧化锰。下列说法中正确的是( )
A. 只有二氧化锰能作过氧化氢分解的催化剂
B. 二氧化锰只能作过氧化氢分解的催化剂
C. 加入二氧化锰可以增加过氧化氢分解产生氧气的质量
D. 二氧化锰能加快过氧化氢分解
D
3.有a、b两份完全相同的过氧化氢溶液,向a份中加入少量二氧化锰。下图是二者产生氧气的质量m与反应时间t的图象。其中正确的是( )
B
学习任务二:发生装置和收集装置的选择
发生装置
收集装置
3.实验装置
A ;
B ;C ;
D ;E .
E
A
B
C
D
分液漏斗
导气管
锥形瓶
集气瓶
水槽
气体发生装置选择依据:1.反应物和生成物的状态 2.反应条件
固 + 固 气
固+液 气(不需加热)
(4)
(1)
(2)
(3)
(5)
装置简单
随时加入液体试剂
可控制反应的速率
氧气发生装置的选择
可控制反应
发生与停止
棉花
高锰酸钾 → 锰酸钾+二氧化锰+氧气
过氧化氢 → 水 + 氧气
二氧化锰
加热
根据提供的资料想一想,若在实验室中收集氧气应选择 ,并说一说你的依据: 。
A.向上排空气法
B.向下排空气法
C.排水集气法
适用于密度比空气大的气体
适用于密度比空气小的气体
适用于不易或难溶于谁的气体
1.气体在水中的溶解性 2.气体的密度
A或C
氧气收集装置的选择
小资料 :通常状况下,氧气不易溶于水,且不与水反应;在 0℃,1个标准大气压下,其密度为1.429g/L,空气的密度为1.293g/L。
排水法收集(纯净但不干燥)
向上排空气法收集(干燥不纯净)
导管口有气泡连续、均匀产生时收集
导管伸入到接近集气瓶底部
探究析思:收集装置的选择
思考回答:排水法收集气体时如果气体不纯,为什么?
学习任务三:氧气的检验、验满及步骤
直接观察:集气瓶口冒出大气泡,说明氧气已经满了。
验满方法: 将带火星的木条放在集气瓶口,若木条复燃,说明氧气已经满了。
4.验满方法
5.检验方法
检验氧气: 将带火星的木条伸入集气瓶中,若木条复燃,证明是氧气。
观察思考——实验步骤
6.总结归纳——实验步骤
1.组装仪器(自下而上,从左往右)
2.检查装置的气密性(手热法)
3.装药品,先加固体(MnO2 ) ,后加液体(H2O2)
4.收集气体
(用向上排空气法收集要验满,带火星木条放瓶口)
5.正放在桌面(氧气密度大于空气密度)
装置气密性检查方法
把导气管末端插到水里,用手紧握试管的外壁。如果导管口处有气泡冒出,则装置的气密性良好。 关闭分液漏斗活塞,导气管末端浸没水中,用手捂住锥形瓶,看到管口有气泡产生,表明不漏气。 向长颈漏斗注水,使漏斗的下端管口浸没在液面以下(液封),将导气管末端浸没水中,双手紧握锥形瓶,导管口有气泡冒出,说明该装置不漏气。
评价练习题
23-24峄城区期中:
集气
知识拓展——多功能瓶
排空气法:
1.密度大于空气的气体,收集时气体由 进入;
2.密度小于空气的气体,收集时气体由 进入;
a
b
排水法:
瓶中先装满水,无论气体的密度大小,只要气体不溶(难溶)于水,收集时气体都是由 进入。
b
氧气
储气
量气
量气原理:
瓶中储存氧气,用水将氧气排出时,水从____端通入
气体进入万能瓶,占据一定的体积,由于气压作用,会有相等体积的水被压入量筒,最后读出量筒内水的体积,这即为进入万能瓶中的气体的体积。
a
水
氧气
氧气
指示
检验
在医院给病人输氧时,瓶中放约半瓶蒸馏水,可观察给病人输氧气的速度,这时氧气从_____端通入。
检验二氧化碳气体:
瓶内装入适量澄清石灰水用于检验CO2时,气体应从_____端管口通入,现象是澄清石灰水变浑浊。
a
氧气
蒸馏水
二氧化碳
a
澄清石灰水
21-22峄城区期中:
关闭分液漏斗活塞,将导气管末端伸入水中,然后双手握住锥形瓶,观察导管口是否有气泡产生
3.如图装置常用于实验室制取气体。
(1)写出如图中指定仪器的名称:① ,组装装置时此仪器应注意 ;
(2)用高锰酸钾制取并收集纯度较大的氧气,可以选择的装置是 (填字母),该反应属于 (填基本反应类型)反应;
H
长颈漏斗
长颈漏斗下端必须伸入液面以下
BG
分解反应
(3)用过氧化氢制取氧气时,如需控制产生气体的速率,发生装置最好选用
(填字母),用装置H进行排空气法收集氧气,气体应从 (选填“a”或“b”)端通入,原因是 ;
(4)实验室制取硫化氢气体的原理:室温下,块状不溶性的硫化亚铁(FeS)固体与稀硫酸反应(另一产物为硫酸亚铁);
①写出该反应的文字表达式: ;
②若想控制反应的发生和停止,可选用的发生装置为 (填字母);
H
a
氧气的密度大于空气的密度
C
硫化亚铁+稀硫酸→硫酸亚铁+硫化氢
D
写出用高锰酸钾制取氧气的文字表达式
高锰酸钾 → 锰酸钾 +二氧化锰 +氧气
△
分解
AE
A
导管口有连续
均匀气泡放出
试管口没有棉花
氧气不易溶于水
用带火星的木条靠近瓶口,看是否复燃
控制反应的发生与停止
将a加长深入水中
课程结束了,祝学习进步哦!
同课章节目录
