第一节 空气的组成第一课时课件(共28张PPT内嵌视频)
文档属性
| 名称 | 第一节 空气的组成第一课时课件(共28张PPT内嵌视频) |

|
|
| 格式 | pptx | ||
| 文件大小 | 204.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-07 00:00:00 | ||
图片预览








文档简介
(共28张PPT)
第一节 空气的组成(1)
小游戏—试试你的憋气能力
学习目标
课标定位
1.了解空气的主要成分,认识空气对人类生活的重要作用。
2.学生通过亲身经历和体验科学探究活动,激发化学学习的兴趣,增进对科学的情感,理解科学的本质,学习科学探究的方法,初步形成科学探究能力。
学标定位
1.通过追寻科学家研究空气成分的足迹结合自学探究,能说出空气的主要成分。
2.通过对空气中氧气含量的定量测定,学会从混合物中除去某种气体进而测定其含量的方法。
3.通过认识空气的成分,能对所学物质从宏观和微观两个角度进行分类,进一步形成物质分类观,同时进行“宏观—微观—符号”三重表征思维构建,促进化学学科核心素养的提升。
学习任务一:认识空气的成分
活动1
猜想与事实
根据生活经验你认为空气中有哪些物质?用什么生活事实可以证明你的猜想。
手持式氧气检测仪
大型实验室空气成分检测
现代科学技术的发展让空气成分的测定变得更加直观、简洁、精确!
(宏观 —— 微观 —— 符号)
干燥洁净 空气的成分 成分名称 体积分数 微观构成 符号
从空气的组成
来分析,空气属于 物
氮气 氧气 氩气 (最多的稀有气体) 二氧化碳 其他气体 78%
氮分子
N2
21%
氧分子
O2
0.934%
氩原子
Ar
0.038%
二氧化碳分子
CO2
0.002%
多种微粒
无
混合
活动2
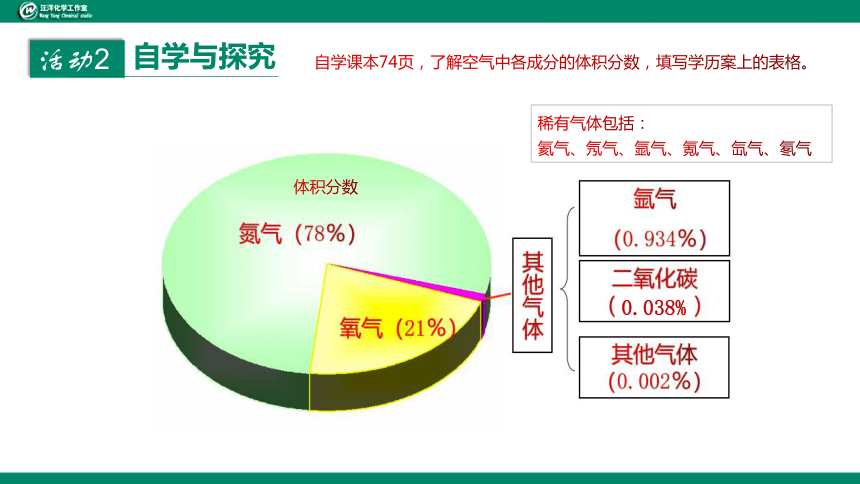
自学与探究
自学课本74页,了解空气中各成分的体积分数,填写学历案上的表格。
稀有气体包括:
氦气、氖气、氩气、氪气、氙气、氡气
体积分数
0.038%
巧记空气组成成分
空气本是混合物,主要成分氮氧气。
氮七八,氧二一,氩气零点九三四。
还有二氧化碳气,百分零点零三八。
以上均以体积计,莫要当成质量比。
1.我们学校的几名同学对空气成分的描述如下,你认为不正确的是:( )
A.空气是由多种气体组成的,并不是单一的物质
B.空气是相对均一、稳定的物质,从某种意义上说也是一种溶液
C.按质量分数计算,空气中含氧气21%,含氮气78%
D.空气中含有多种分子或原子,因此空气属于混合物
C
【评价练习一】
2.请沿用科学家认识事物的方式认识“空气”。
⑴从分类角度:空气属于 (填“混合物”或“纯净物”)。
⑵从微观角度:用“ ”表示氮原子,“ ”表示氧原子。
①用“ ”可表示的微粒是 (填名称)。
②同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,下图中可表示空气微观模型的是 (填标号)。
混合物
氧分子
B
学习任务二:测定空气中氧气的含量
活动1
提出问题 寻找思路
如何测定一定量空气中氧气的含量?小组讨论后交流思路(结合76页课本拉瓦锡的实验原理去思考)。
氮气
稀有气体
二氧化碳
氧气
其他气体
思路1:用药品通过化学反应将一定量的空气中其他气体除去,只剩下氧气,测定氧气体积。
思路2:用药品通过化学反应除去一定量的空气中所有的氧气,减少的体积即为氧气的体积。
需要除去很多气体,难!!!!
只需除去氧气即可,且氧气有助燃性,可以和很多物质反应,相对容易!
氮气
稀有气体
二氧化碳
氧气
其他气体
密闭空间内一定体积的空气
活动2
明确原理 选择药品
实验原理:
药品选择:
一些物质在空气中燃烧或加热的表达式如下,根据实验原理选择能完成此实验的物质是 ,原则是 。
在 的容器中留有一定体积的空气,利用 只除去其中的 ,而且不产生 新的 ,减少的体积就是空气中 的体积。
反应表达式 生成物状态 反应表达式 生成物状态
①木炭+氧气 → 二氧化碳 气体 ⑤铜+氧气 → 氧化铜 黑色固体
②硫+氧气 → 二氧化硫 气体 ⑥镁+氧气 → 氧化镁 白色固体 镁+氮气 → 氮化镁 淡黄色固体 ③磷+氧气 → 五氧化二磷 白色固体 ④蜡烛+氧气 → 二氧化碳+水 气体+液体 ⑦汞+氧气 → 氧化汞 红色固体
③⑤⑦
只与氧气反应,生成物不为气体
点燃
点燃
点燃
点燃
加热
点燃
点燃
点燃
密闭
化学反应
氧气
气体
氧气
(此反应需要12天,且汞有毒)
活动3
设计方案 实验探究
如果选择磷或铜作为除氧药品,同学们设计实验装置和具体实验方案,装置图如下。
燃磷法
烧铜法
铜丝
实验设计拓展:
2.利用有刻度的容器测出密闭体系气体减小的体积
1.氧气被消耗,气压减小,使水进入密闭容器内,测定进入的水的体积
3.利用氧气传感器测出燃烧后密闭体系中氧气的含量
核心思想点:利用物质性质的差异引起量的变化,将不可测的量转化成可测的物理量,达到实验的目的!
以铜丝为除氧药品,按照实验步骤进行分组实验,注意实验安全,将实验现象、数据等记录在学历案上。(分工参考:1点灯加热,1手扶紧橡胶塞,1推拉注射器,1观察铜丝颜色变化记录现象、1记录各项体积数据)
1.连接仪器,检验气密性(已检验,已连接)
2.记录加热之前硬质玻璃管中气体体积V1= 65mL和注射器中预留气体的体积V2=20mL。 (已预留)
3.点燃酒精灯,先预热,后对准有铜丝的部位加热,
同时不断的慢慢推拉注射器活塞。
4.停止加热后 ,待玻璃管冷却至室温,将气球内的气体全部挤入注射器内。待注射器稳定后,记录注射器内气体的体积V3,最后根据公式进行计算!
活动3
设计方案 实验探究
铜丝
收集数据 获得结论
数据
组别
氧气的体积分数
反应消耗的氧气的体积/mL
=V2-V3
(注射器实验前-注射器反应后)
封闭体系中空气的体积/mL
=V1+V2
(注射器空气+玻璃管内空气)
六组
五组
四组
三组
二组
一组
七组
(1)实验现象: 色铜丝变成 色,注射器内气体体积减少;
(2)反应原理:
文字表达式为 ;属于 反应(填“分解”或“化合”);
(3)小气球的作用: ;
(4)实验过程中不断推拉注射器的原因 ;
(5)实验结论:氧气体积大约占空气体积的 ;
收集数据 获得结论
观察实验完成下列内容,写在学历案相应位置。
红
黑
化合
缓冲作用
增加空气的流通,有利于氧气的消耗
五分之一
铜+氧气→氧化铜
分析数据 交流反思
上述实验中,各小组间的实验结果差别较大,你认为可能的原因有哪些?
实验结果偏小,不足1/5
药品的量不足,没将氧气耗尽
装置的气密性不好,外界空气进入
反应完毕,未冷却至室温就观察读数
加热时间太短或温度不够高,反应不充分
活塞推拉次数太少,氧气没充分反应
实验完毕冷却后,气球内的气体未全部挤入注射器内
实验结果偏大,大于1/5
【评价性练习二】
1.某同学利用燃烧法测定空气中氧气含量,查阅资料得知五氧化二磷会污染空气,于是将实验装置改进为如右图所示装置。
(1)你认为此装置的缺点是 ;
(2)不能用木炭代替白磷,因为 ;
(3)若实验成功,最终量筒中液面约降至 mL刻度线处;
(4)该实验得出的结论是 。
没有缓冲装置
生成二氧化碳气体,测试结果不准确
24
氧气约占空气总体积的1/5
东风夜放花千树,更吹落,星如雨。请同学们谈一谈本节课你有什么收获或者感悟!
[检测与作业] A.基础巩固
1.2021年12月9日,航天员翟志刚、王亚平、叶光富在中国“天和号”空间站进行“天宫课堂”第一课。水球光学实验中打入的“人造空气”与我们身边的空气成分含量基本相同,“人造空气”中氧气含量约为( )
A.78% B.21% C.0.934% D.0.034%
2.法国化学家拉瓦锡将汞放在密闭容器里加热12天,发现容器里空气的体积减少了约五分之一。减少的气体是( )
A.氮气 B.稀有气体 C.氧气 D.二氧化碳
B
C
[检测与作业] B.能力提升
第一节 空气的组成(1)
小游戏—试试你的憋气能力
学习目标
课标定位
1.了解空气的主要成分,认识空气对人类生活的重要作用。
2.学生通过亲身经历和体验科学探究活动,激发化学学习的兴趣,增进对科学的情感,理解科学的本质,学习科学探究的方法,初步形成科学探究能力。
学标定位
1.通过追寻科学家研究空气成分的足迹结合自学探究,能说出空气的主要成分。
2.通过对空气中氧气含量的定量测定,学会从混合物中除去某种气体进而测定其含量的方法。
3.通过认识空气的成分,能对所学物质从宏观和微观两个角度进行分类,进一步形成物质分类观,同时进行“宏观—微观—符号”三重表征思维构建,促进化学学科核心素养的提升。
学习任务一:认识空气的成分
活动1
猜想与事实
根据生活经验你认为空气中有哪些物质?用什么生活事实可以证明你的猜想。
手持式氧气检测仪
大型实验室空气成分检测
现代科学技术的发展让空气成分的测定变得更加直观、简洁、精确!
(宏观 —— 微观 —— 符号)
干燥洁净 空气的成分 成分名称 体积分数 微观构成 符号
从空气的组成
来分析,空气属于 物
氮气 氧气 氩气 (最多的稀有气体) 二氧化碳 其他气体 78%
氮分子
N2
21%
氧分子
O2
0.934%
氩原子
Ar
0.038%
二氧化碳分子
CO2
0.002%
多种微粒
无
混合
活动2
自学与探究
自学课本74页,了解空气中各成分的体积分数,填写学历案上的表格。
稀有气体包括:
氦气、氖气、氩气、氪气、氙气、氡气
体积分数
0.038%
巧记空气组成成分
空气本是混合物,主要成分氮氧气。
氮七八,氧二一,氩气零点九三四。
还有二氧化碳气,百分零点零三八。
以上均以体积计,莫要当成质量比。
1.我们学校的几名同学对空气成分的描述如下,你认为不正确的是:( )
A.空气是由多种气体组成的,并不是单一的物质
B.空气是相对均一、稳定的物质,从某种意义上说也是一种溶液
C.按质量分数计算,空气中含氧气21%,含氮气78%
D.空气中含有多种分子或原子,因此空气属于混合物
C
【评价练习一】
2.请沿用科学家认识事物的方式认识“空气”。
⑴从分类角度:空气属于 (填“混合物”或“纯净物”)。
⑵从微观角度:用“ ”表示氮原子,“ ”表示氧原子。
①用“ ”可表示的微粒是 (填名称)。
②同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,下图中可表示空气微观模型的是 (填标号)。
混合物
氧分子
B
学习任务二:测定空气中氧气的含量
活动1
提出问题 寻找思路
如何测定一定量空气中氧气的含量?小组讨论后交流思路(结合76页课本拉瓦锡的实验原理去思考)。
氮气
稀有气体
二氧化碳
氧气
其他气体
思路1:用药品通过化学反应将一定量的空气中其他气体除去,只剩下氧气,测定氧气体积。
思路2:用药品通过化学反应除去一定量的空气中所有的氧气,减少的体积即为氧气的体积。
需要除去很多气体,难!!!!
只需除去氧气即可,且氧气有助燃性,可以和很多物质反应,相对容易!
氮气
稀有气体
二氧化碳
氧气
其他气体
密闭空间内一定体积的空气
活动2
明确原理 选择药品
实验原理:
药品选择:
一些物质在空气中燃烧或加热的表达式如下,根据实验原理选择能完成此实验的物质是 ,原则是 。
在 的容器中留有一定体积的空气,利用 只除去其中的 ,而且不产生 新的 ,减少的体积就是空气中 的体积。
反应表达式 生成物状态 反应表达式 生成物状态
①木炭+氧气 → 二氧化碳 气体 ⑤铜+氧气 → 氧化铜 黑色固体
②硫+氧气 → 二氧化硫 气体 ⑥镁+氧气 → 氧化镁 白色固体 镁+氮气 → 氮化镁 淡黄色固体 ③磷+氧气 → 五氧化二磷 白色固体 ④蜡烛+氧气 → 二氧化碳+水 气体+液体 ⑦汞+氧气 → 氧化汞 红色固体
③⑤⑦
只与氧气反应,生成物不为气体
点燃
点燃
点燃
点燃
加热
点燃
点燃
点燃
密闭
化学反应
氧气
气体
氧气
(此反应需要12天,且汞有毒)
活动3
设计方案 实验探究
如果选择磷或铜作为除氧药品,同学们设计实验装置和具体实验方案,装置图如下。
燃磷法
烧铜法
铜丝
实验设计拓展:
2.利用有刻度的容器测出密闭体系气体减小的体积
1.氧气被消耗,气压减小,使水进入密闭容器内,测定进入的水的体积
3.利用氧气传感器测出燃烧后密闭体系中氧气的含量
核心思想点:利用物质性质的差异引起量的变化,将不可测的量转化成可测的物理量,达到实验的目的!
以铜丝为除氧药品,按照实验步骤进行分组实验,注意实验安全,将实验现象、数据等记录在学历案上。(分工参考:1点灯加热,1手扶紧橡胶塞,1推拉注射器,1观察铜丝颜色变化记录现象、1记录各项体积数据)
1.连接仪器,检验气密性(已检验,已连接)
2.记录加热之前硬质玻璃管中气体体积V1= 65mL和注射器中预留气体的体积V2=20mL。 (已预留)
3.点燃酒精灯,先预热,后对准有铜丝的部位加热,
同时不断的慢慢推拉注射器活塞。
4.停止加热后 ,待玻璃管冷却至室温,将气球内的气体全部挤入注射器内。待注射器稳定后,记录注射器内气体的体积V3,最后根据公式进行计算!
活动3
设计方案 实验探究
铜丝
收集数据 获得结论
数据
组别
氧气的体积分数
反应消耗的氧气的体积/mL
=V2-V3
(注射器实验前-注射器反应后)
封闭体系中空气的体积/mL
=V1+V2
(注射器空气+玻璃管内空气)
六组
五组
四组
三组
二组
一组
七组
(1)实验现象: 色铜丝变成 色,注射器内气体体积减少;
(2)反应原理:
文字表达式为 ;属于 反应(填“分解”或“化合”);
(3)小气球的作用: ;
(4)实验过程中不断推拉注射器的原因 ;
(5)实验结论:氧气体积大约占空气体积的 ;
收集数据 获得结论
观察实验完成下列内容,写在学历案相应位置。
红
黑
化合
缓冲作用
增加空气的流通,有利于氧气的消耗
五分之一
铜+氧气→氧化铜
分析数据 交流反思
上述实验中,各小组间的实验结果差别较大,你认为可能的原因有哪些?
实验结果偏小,不足1/5
药品的量不足,没将氧气耗尽
装置的气密性不好,外界空气进入
反应完毕,未冷却至室温就观察读数
加热时间太短或温度不够高,反应不充分
活塞推拉次数太少,氧气没充分反应
实验完毕冷却后,气球内的气体未全部挤入注射器内
实验结果偏大,大于1/5
【评价性练习二】
1.某同学利用燃烧法测定空气中氧气含量,查阅资料得知五氧化二磷会污染空气,于是将实验装置改进为如右图所示装置。
(1)你认为此装置的缺点是 ;
(2)不能用木炭代替白磷,因为 ;
(3)若实验成功,最终量筒中液面约降至 mL刻度线处;
(4)该实验得出的结论是 。
没有缓冲装置
生成二氧化碳气体,测试结果不准确
24
氧气约占空气总体积的1/5
东风夜放花千树,更吹落,星如雨。请同学们谈一谈本节课你有什么收获或者感悟!
[检测与作业] A.基础巩固
1.2021年12月9日,航天员翟志刚、王亚平、叶光富在中国“天和号”空间站进行“天宫课堂”第一课。水球光学实验中打入的“人造空气”与我们身边的空气成分含量基本相同,“人造空气”中氧气含量约为( )
A.78% B.21% C.0.934% D.0.034%
2.法国化学家拉瓦锡将汞放在密闭容器里加热12天,发现容器里空气的体积减少了约五分之一。减少的气体是( )
A.氮气 B.稀有气体 C.氧气 D.二氧化碳
B
C
[检测与作业] B.能力提升
同课章节目录
