2.1.2 碳酸钠和碳酸氢钠 焰色试验 课时同步练(含解析)
文档属性
| 名称 | 2.1.2 碳酸钠和碳酸氢钠 焰色试验 课时同步练(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 287.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-06 00:00:00 | ||
图片预览



文档简介
碳酸钠和碳酸氢钠 焰色试验
◆ 知识点一 碳酸钠和碳酸氢钠的性质
1.下列有关NaHCO3和 Na2CO3性质的叙述中正确的是( )
A.碳酸钠可用于治疗胃溃疡病人的胃酸过多
B.发酵粉中主要含有碳酸钠,能使焙制出的糕点疏松多孔
C.在Na2CO3和 NaHCO3溶液中滴加石灰水均产生白色沉淀
D.Na2CO3和 NaHCO3均能与盐酸或 NaOH 溶液反应
2. 关于NaHCO3和Na2CO3性质的说法不正确的是 ( )
A.相同温度下,在水中的溶解度:Na2CO3>NaHCO3
B.质量相等的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3放出的CO2比Na2CO3多
C.与等质量分数、等体积盐酸反应放出气体的快慢:Na2CO3D.Na2CO3不能转化成NaHCO3,而NaHCO3能转化成Na2CO3
3. 下列是某兴趣小组根据教材实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验。查阅资料可知白色的无水硫酸铜粉末遇水变蓝。请观察如图L2-1-11所示的实验装置,分析实验原理,并判断下列说法和做法,其中不科学的是 ( )
图L2-1-11
A.甲为小苏打,乙为纯碱
B.要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球
C.加热不久就能看到A烧杯的澄清石灰水变浑浊
D.B烧杯中发生反应的化学方程式为Ca(OH)2+CO2CaCO3↓+H2O
4. 加热10.0 g碳酸钠和碳酸氢钠的混合物至质量不再变化,剩余固体的质量为8.45 g,则混合物中碳酸钠的质量分数为 ( )
A.42% B.58% C.29% D.50%
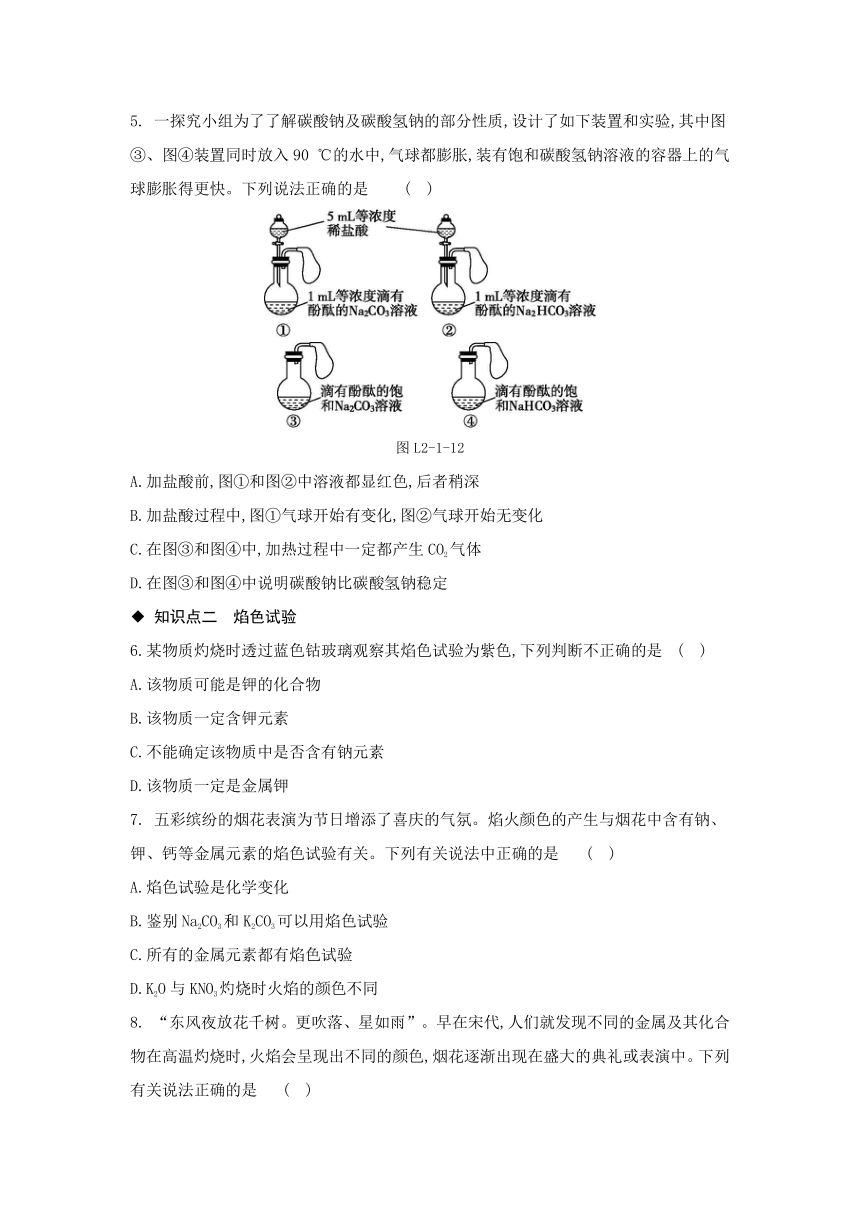
5. 一探究小组为了了解碳酸钠及碳酸氢钠的部分性质,设计了如下装置和实验,其中图③、图④装置同时放入90 ℃的水中,气球都膨胀,装有饱和碳酸氢钠溶液的容器上的气球膨胀得更快。下列说法正确的是 ( )
图L2-1-12
A.加盐酸前,图①和图②中溶液都显红色,后者稍深
B.加盐酸过程中,图①气球开始有变化,图②气球开始无变化
C.在图③和图④中,加热过程中一定都产生CO2气体
D.在图③和图④中说明碳酸钠比碳酸氢钠稳定
◆ 知识点二 焰色试验
6.某物质灼烧时透过蓝色钴玻璃观察其焰色试验为紫色,下列判断不正确的是 ( )
A.该物质可能是钾的化合物
B.该物质一定含钾元素
C.不能确定该物质中是否含有钠元素
D.该物质一定是金属钾
7. 五彩缤纷的烟花表演为节日增添了喜庆的气氛。焰火颜色的产生与烟花中含有钠、钾、钙等金属元素的焰色试验有关。下列有关说法中正确的是 ( )
A.焰色试验是化学变化
B.鉴别Na2CO3和K2CO3可以用焰色试验
C.所有的金属元素都有焰色试验
D.K2O与KNO3灼烧时火焰的颜色不同
8. “东风夜放花千树。更吹落、星如雨”。早在宋代,人们就发现不同的金属及其化合物在高温灼烧时,火焰会呈现出不同的颜色,烟花逐渐出现在盛大的典礼或表演中。下列有关说法正确的是 ( )
A.高温灼烧时,铜元素的焰色为黄色
B.焰色试验利用了金属元素的物理性质
C.某物质在灼烧时焰色为黄色,则该物质一定不含K元素
D.将铂丝(或无绣铁丝)用盐酸洗涤后,可直接蘸取药品灼烧
◆ 知识点三 碳酸钠和碳酸氢钠的鉴别与除杂
9. 下列说法正确的是 ( )
A.鉴别NaHCO3与Na2CO3溶液,可用Ca(OH)2溶液
B.质量相等的NaHCO3与Na2CO3分别与足量盐酸完全反应,产生CO2的质量后者更大
C.NaHCO3粉末中混有Na2CO3,可配制成溶液,通入过量的CO2,再低温结晶进行提纯
D.取a g Na2CO3和NaHCO3混合物,与足量稀硫酸充分反应,逸出的气体用碱石灰吸收,碱石灰质量增加b g,能测定Na2CO3和NaHCO3混合物中Na2CO3的质量分数
10.为除去括号内的杂质,所选用的试剂或方法不正确的是 ( )
A.NaCl溶液(Na2SO4),加入适量的Ba(NO3)2溶液,过滤
B.NaOH溶液(Na2CO3),加入适量的Ca(OH)2溶液,过滤
C.Na2O2粉末(Na2O),将混合物在氧气中加热
D.Na2CO3溶液(NaHCO3),加入适量的NaOH溶液
11.某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法进行以下实验,如图L2-1-13Ⅰ~Ⅳ所示。
图L2-1-13
(1)只根据图Ⅰ所示实验,能否达到实验目的 (填“能”或“否”)。
(2)图Ⅱ所示的实验,若固体质量相同且稀盐酸足量时,气球鼓起较小的装有 (填化学式)。
(3)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,与实验Ⅲ相比,实验Ⅳ的优点是 (填选项序号)。
A.Ⅳ比Ⅲ复杂
B.Ⅳ比Ⅲ安全
C.Ⅳ可一套装置同时进行两个对比实验,而Ⅲ不行
(4)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是 (填化学式)。
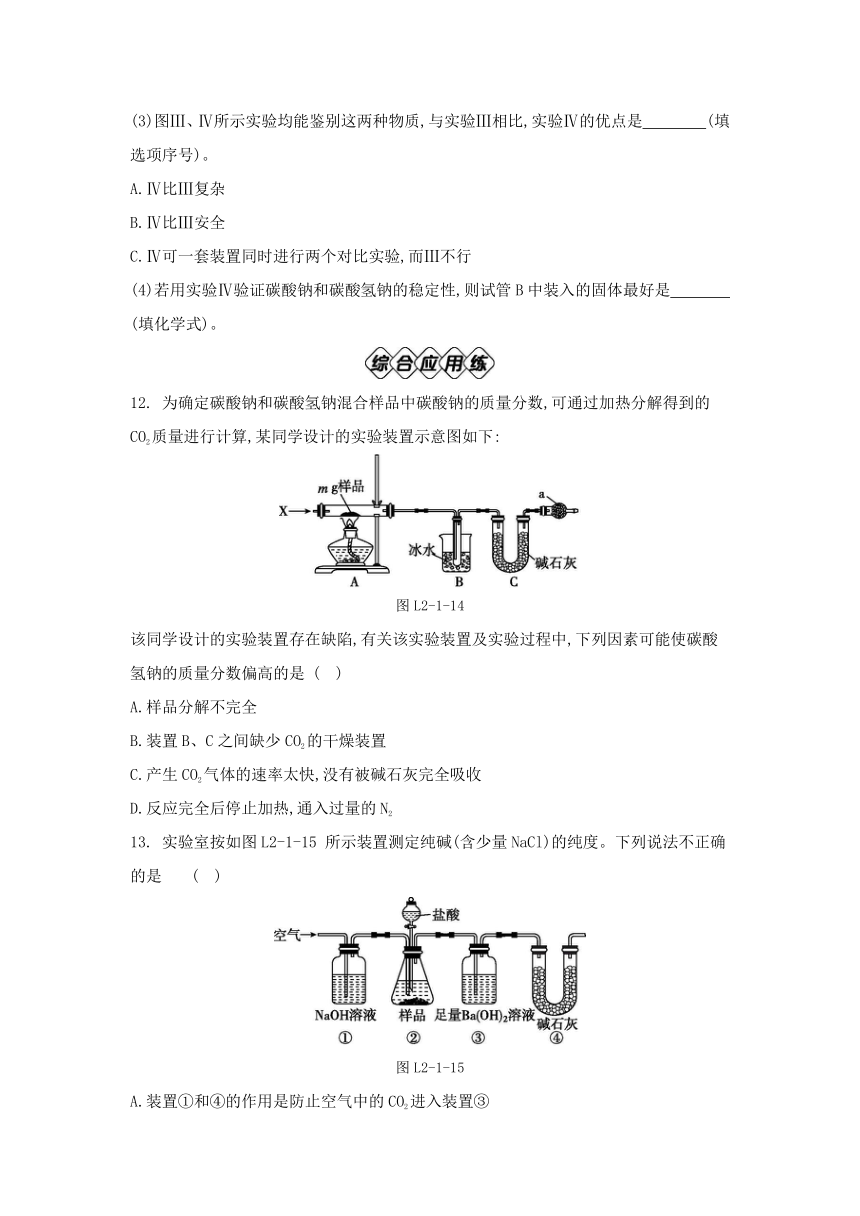
12. 为确定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,可通过加热分解得到的CO2质量进行计算,某同学设计的实验装置示意图如下:
图L2-1-14
该同学设计的实验装置存在缺陷,有关该实验装置及实验过程中,下列因素可能使碳酸氢钠的质量分数偏高的是 ( )
A.样品分解不完全
B.装置B、C之间缺少CO2的干燥装置
C.产生CO2气体的速率太快,没有被碱石灰完全吸收
D.反应完全后停止加热,通入过量的N2
13. 实验室按如图L2-1-15 所示装置测定纯碱(含少量NaCl)的纯度。下列说法不正确的是 ( )
图L2-1-15
A.装置①和④的作用是防止空气中的CO2进入装置③
B.②中的盐酸可以用稀硫酸代替
C.必须在装置②和③间添加盛有饱和NaHCO3溶液的洗气瓶
D.反应结束时,应再通入空气将装置②中CO2转移到装置③中
14.已知A是一种金属单质,焰色试验呈黄色,各物质间转化关系如图L2-1-16所示,则以下叙述正确的是 ( )
图L2-1-16
A.C溶液呈碱性,所以C属于碱
B.B与水反应产生的气体具有可燃性
C.D能与硫酸铜溶液反应生成蓝色沉淀
D.C受热易分解,产物能使澄清石灰水变浑浊
15. 通过测定混合气体中O2的含量可计算已变质的Na2O2(含Na2CO3)纯度,实验装置如图L2-1-17(Q为弹性良好的气囊)。下列分析错误的是 ( )
图L2-1-17
A.干燥管b中装入无水氯化钙
B.Q气球中产生的气体主要成分是O2、CO2
C.测定气体总体积必须关闭K1、K2,打开K3
D.读完气体总体积后,关闭K3,缓缓打开K1、K2,可观察到Q气球慢慢缩小
16. 2022年6月5日,神舟十四号载人飞船顺利进入预定轨道。飞船的轨道舱内安装盛有Na2O2颗粒的装置,为宇航员供氧。回答下列问题:
(1)Na2O2的供氧。过氧化钠能与人体呼出的酸性氧化物发生反应,其化学方程式为 ,该反应中的还原剂是 (填写化学式)。
(2)反应后组成的探究。Na2O2使用后会失去供氧
能力(又称失效供氧剂),某“失效供氧剂”的化学组成可能是Na2CO3或NaHCO3或两者的混合物。为探究“失效供氧剂”的化学组成,化学探究小组进行如下实验:
取适量“失效供氧剂”于试管中,加热,产生能使澄清石灰水变浑浊的气体,产生该气体的化学方程式为 。
②称取19.0 g“失效供氧剂”,加入足量稀硫酸,将生成的气体用浓硫酸干燥后,再用碱石灰完全吸收,碱石灰质量增加8.8 g,该“失效供氧剂”的化学组成为 (填写化学式)。
17. 碳酸氢钠俗称小苏打,在医疗、食品、橡胶工业中有广泛应用。某NaHCO3晶体中含有NaCl等与酸不反应且受热不易分解的杂质,为测定NaHCO3的质量分数,甲同学设计了以下两种方案。
方案一:滴定法
称取8.4 g样品溶于水,逐滴加入质量分数为19.6%的稀硫酸(密度约为1.0 g·cm-3),待不再产生气体时,测定所消耗稀硫酸的体积。
(1)甲同学共进行3次测定,每次称取8.2 g样品,消耗质量分数为19.6%的稀硫酸的体积如下表:
实验序号 ① ② ③
V[H2SO4(aq)]/mL 20.10 20.00 19.90
样品中NaHCO3的质量分数为 。
方案二:称量法
乙同学按如图L2-1-18所示操作流程进行测定。
图L2-1-18
(2)操作Ⅰ后所得溶液中的主要溶质是 (填化学式)。
(3)操作Ⅱ的名称是 。
(4)样品中NaHCO3的质量分数为 (用含a的代数式表示)。
碳酸钠和碳酸氢钠 焰色试验
1.C [解析] 碳酸钠溶液的碱性较强,具有较强腐蚀性,不能用于治疗胃溃疡病人的胃酸过多,A错误;发酵粉中含有NaHCO3,受热分解产生CO2,能使焙制出的糕点疏松多孔,B错误;在Na2CO3和 NaHCO3溶液中滴加石灰水均产生白色沉淀CaCO3,C正确;Na2CO3不能与NaOH溶液反应,D错误。
2.D [解析] 相同温度下Na2CO3在水中的溶解度大于NaHCO3,故A正确;质量相等的NaCO3和NaHCO3,相对分子质量:NaHCO33.C [解析] 碳酸氢钠在小试管,碳酸钠在大试管,大试管直接加热,温度较高,如温度较高的不分解,而加热温度较低的物质分解,可判断稳定性强弱,故甲为小苏打、乙为纯碱,A正确;小苏打为NaHCO3,其受热易分解产生Na2CO3、H2O和CO2,白色的无水硫酸铜遇到水显蓝色,则证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球,如果变蓝则说明有水生成,B正确;碳酸钠较稳定,加热过程中不会分解,连接A烧杯的试管不会产生二氧化碳,则A烧杯的澄清石灰水不变浑浊,C错误;NaHCO3受热分解产生的CO2与Ca(OH)2反应的化学方程式为CO2+Ca(OH)2CaCO3↓+H2O,D正确。
4.B [解析] 碳酸钠加热不反应,碳酸氢钠加热分解为碳酸钠、二氧化碳、水,加热10.0 g碳酸钠和碳酸氢钠的混合物至质量不再变化,剩余固体的质量为8.45 g。设10.0 g混合物中碳酸氢钠的质量为x,则有
2NaHCO3Na2CO3+CO2↑+H2O↑ Δm
168 106 62
x (10.0-8.45) g
列式:=,解得x=4.2 g,故混合物中碳酸钠的质量分数为×100%=58%。
5.D [解析] 碳酸钠及碳酸氢钠溶液都显碱性,其中碳酸钠溶液的碱性更强,酚酞在碱性溶液中显红色,则图①和图②中溶液都显红色,前者稍深,故A错误。碳酸钠和少量盐酸反应生成的是碳酸氢钠,没有气体生成,继续滴加盐酸,生成氯化钠、二氧化碳和水,有气泡产生;碳酸氢钠与盐酸反应直接产生二氧化碳气体,则加盐酸过程中,图①气球开始无变化,图②气球开始有变化,故B错误。③中可能是由于温度高导致瓶内气体的压强增大,而④中气球膨胀得更快,说明除此原因外,NaHCO3受热分解产生CO2,故C错误。图③、图④装置同时放入90 ℃的水中,气球都膨胀,装有饱和碳酸氢钠溶液的容器上的气球膨胀得更快,说明碳酸氢钠不稳定,受热分解,则碳酸钠比碳酸氢钠稳定,故D正确。
6.D [解析] 钾的化合物中含有钾元素,灼烧时透过蓝色钴玻璃观察其焰色试验为紫色,A正确;某物质灼烧时透过蓝色钴玻璃观察其焰色试验为紫色,说明该物质中一定含有钾元素,B正确;蓝色钴玻璃可以过滤黄光,所以无法确定是否含有钠元素,C正确;该物质含有钾元素,可以是钾单质,也可以是钾的化合物,D错误。
7.B [解析] 焰色试验没有生成新物质,属于物理变化,故A错误;钠的焰色试验是黄色,钾的焰色试验是紫色(透过蓝色钴玻璃),故鉴别Na2CO3和K2CO3可以用焰色试验,故B正确;有些金属的焰色试验是无色的,如铂丝,故C错误;焰色试验是某种金属元素的特性,K2O与KNO3都含有K元素,焰色试验(透过蓝色钴玻璃)都显紫色,灼烧时火焰的颜色相同,故D错误。
8.B [解析] 铜元素的焰色为绿色,A错误;焰色试验没有生成新物质,利用了金属元素的物理性质,B正确;K元素的焰色要透过蓝色钴玻璃观察,C错误;铂丝(或无锈铁丝)用盐酸洗涤后,要先在酒精灯外焰灼烧至与原来的火焰颜色相同,再蘸取药品灼烧,D错误。
9.C [解析] NaHCO3和Na2CO3溶液都能与Ca(OH)2溶液反应生成CaCO3沉淀,无法鉴别,A错误;NaHCO3中C元素的质量分数大于Na2CO3,质量相等的NaHCO3和Na2CO3分别与足量的盐酸反应,产生CO2的质量前者更大,B错误;Na2CO3溶液中通入过量的CO2可以转化为NaHCO3,因此NaHCO3粉末中混有Na2CO3,可配制成溶液,通入过量的CO2,再低温结晶进行提纯,C正确;Na2CO3和NaHCO3混合物与足量稀硫酸充分反应后,逸出的CO2气体中含有水蒸气,无法通过碱石灰增加的质量测定混合物中Na2CO3的质量分数,D错误。
10.A [解析] 加入适量Ba(NO3)2溶液,反应生成BaSO4和NaNO3,过滤后,滤液中引入新杂质NaNO3,A错误;加入适量Ca(OH)2溶液,发生反应:Ca(OH)2+Na2CO3CaCO3↓+2NaOH,过滤除去CaCO3,得到NaOH溶液,B正确;在氧气中加热,Na2O与O2反应转化为Na2O2,C正确;NaHCO3与适量NaOH溶液反应生成Na2CO3和H2O,从而除去杂质,D正确。
11.(1)否 (2)Na2CO3 (3)C (4)NaHCO3
[解析] (1)无论碳酸钠还是碳酸氢钠都能和盐酸反应生成二氧化碳,二氧化碳能使澄清石灰水变浑浊,故实验Ⅰ无法鉴别。(2)稀盐酸足量,说明两种固体完全反应,质量相同,含碳量越高,完全反应生成二氧化碳越多,碳酸钠中含碳量为×100%≈11.3%,而碳酸氢钠中含碳量为×100%≈14.3%,所以碳酸钠放出二氧化碳量少,气球鼓起较小。(3)实验Ⅲ、Ⅳ相比,Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行,C符合题意。(4)碳酸钠直接加热不产生气体,而碳酸氢钠不直接加热就能产生气体,更能说明碳酸氢钠不稳定,受热易分解,所以试管B中装入的固体应该是NaHCO3。
12.B [解析] 样品分解不完全,测定二氧化碳的质量偏小,碳酸氢钠质量偏小,碳酸氢钠的质量分数偏低,A错误;装置B、C之间缺少CO2的干燥装置,水蒸气进入装置C导致测定的二氧化碳质量偏大,碳酸氢钠质量偏大,故碳酸氢钠的质量分数偏高,B正确;产生CO2气体的速率太快,没有被碱石灰完全吸收,测定二氧化碳质量偏小,碳酸氢钠质量偏小,则碳酸氢钠的质量分数偏低,C错误;反应完全后停止加热,通入过量的N2,N2不会被装置C吸收,测得二氧化碳的质量不变,则碳酸氢钠的质量分数不会偏高也不会偏低,D错误。
13.C [解析] 测定纯碱(含少量NaCl)的纯度,由实验装置可知,先通入空气,在①中除去CO2,利用氮气等将装置内的二氧化碳排出,然后关闭①和②之间的橡皮管,打开分液漏斗的活塞,盐酸与样品反应生成二氧化碳,③中二氧化碳与氢氧化钡反应生成白色沉淀,反应结束后,再打开①和②之间的橡皮管,继续通入空气使生成的二氧化碳被③中溶液完全吸收,④中碱石灰可防止空气中的二氧化碳被氢氧化钡吸收。装置①和④的作用是防止空气中的CO2进入装置③,可准确测定生成二氧化碳的量,故A正确;硫酸和碳酸钠反应也可以生成二氧化碳,②中的盐酸可以用稀硫酸代替,故B正确;在装置②和③间不需要添加盛有饱和NaHCO3溶液的洗气瓶,HCl与氢氧化钡不生成沉淀,且Ba(OH)2溶液足量,最后测定沉淀的质量,结合守恒法可计算纯度,故C错误;反应结束后,继续通入空气使生成的二氧化碳被③中溶液完全吸收,保证测定结果更准确,故D正确。
14.C [解析] A是一种金属单质,焰色试验呈黄色,可知A是Na;钠和氧气在加热条件下反应生成过氧化钠,B是Na2O2;Na2O2和二氧化碳反应生成碳酸钠和氧气,C是Na2CO3;Na2O2和水反应生成氢氧化钠和氧气,D是NaOH;NaOH和CO2可反应生成Na2CO3。C是Na2CO3,Na2CO3溶液呈碱性,但Na2CO3属于盐,故A错误;B是Na2O2,Na2O2与水反应生成氢氧化钠和氧气,氧气没有可燃性,故B错误;D是NaOH,NaOH与硫酸铜溶液反应生成蓝色氢氧化铜沉淀,故C正确;C是Na2CO3,Na2CO3受热不分解,故D错误。
15.A [解析] 已变质的Na2O2(含Na2CO3)滴入稀H2SO4,发生反应:2Na2O2+2H2SO42Na2SO4+O2↑+2H2O、Na2CO3+H2SO4Na2SO4+CO2↑+H2O,反应产生CO2、O2气体,用碱石灰吸收CO2,在量筒Ⅱ中利用排水法测得O2的量,进而求出Na2O2的量,A错误,B正确;关闭K1、K2,打开K3,CO2、O2使气球变大,将广口瓶中气体排出,水进入量筒Ⅰ中,故量筒Ⅰ中水的体积即为O2、CO2的总体积,C正确;读完气体总体积后,关闭K3,缓缓打开K1、K2,才能观察到Q气球慢慢缩小,D正确。
16.(1)2Na2O2+2CO22Na2CO3+O2 Na2O2
(2)①2NaHCO3Na2CO3+CO2↑+H2O
②Na2CO3和NaHCO3
[解析] (1)人体呼出的酸性氧化物是二氧化碳,过氧化钠能与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO22Na2CO3+O2,Na2O2中氧元素一部分由-1价降低为-2价,一部分由-1价升高为0价,该反应中Na2O2既是氧化剂又是还原剂。(2)①取适量“失效供氧剂”于试管中,加热,产生能使澄清石灰水变浑浊的气体,说明碳酸氢钠受热分解生成二氧化碳。②称取19.0 g“失效供氧剂”,加入足量稀硫酸,将生成的气体用浓硫酸干燥后,再用碱石灰完全吸收,碱石灰质量增加8.8 g,生成的二氧化碳质量为8.8 g,根据Na2CO3~CO2,若二氧化碳全部是碳酸钠反应生成的,则碳酸钠质量为21.2 g;根据NaHCO3~CO2,若二氧化碳全部是碳酸氢钠反应生成的,则碳酸氢钠质量为16.8 g;样品的质量为19.0 g,可知该“失效供氧剂”的化学组成为Na2CO3和NaHCO3。
17.(1)80% (2)NaCl
(3)蒸发结晶 (4)×100%
[解析] (1)由表中数据可知,平均消耗质量分数为19.6%的稀硫酸的体积为20.00 mL,则消耗H2SO4的质量为20.00 mL×1.0 g·cm-3×19.6%=3.92 g。 设样品中NaHCO3的质量为x,则:
2NaHCO3+H2SO4Na2SO4+2CO2↑+2H2O
2×84 98
x 3.92 g
列式:=,解得x=6.72 g,故样品中NaHCO3的质量分数为×100%=80%。(2)准确称取2.0 g NaHCO3样品,向其中滴加足量稀盐酸,发生反应:NaHCO3+HClNaCl+H2O+CO2↑,至不再逸出气体后停止滴加,此时得到的溶液中溶质的主要成分是NaCl。(3)将反应后的溶液转移至蒸发皿中蒸发水分,待仅剩余少量液体时,停止加热,利用余热将残留水分蒸干,然后冷却、干燥、称量,此时得到固体质量是a g,则操作Ⅱ是蒸发结晶。(4)根据反应方程式NaHCO3+HClNaCl+H2O+CO2↑可知:每有84 g NaHCO3发生反应,产生58.5 g NaCl,反应后固体质量减少84 g-58.5 g=25.5 g。此实验中固体充分反应后质量减轻(2.0-a) g,则样品中含有NaHCO3的质量为m(NaHCO3)=×84 g,故样品中NaHCO3的质量分数为×100%=×100%。
◆ 知识点一 碳酸钠和碳酸氢钠的性质
1.下列有关NaHCO3和 Na2CO3性质的叙述中正确的是( )
A.碳酸钠可用于治疗胃溃疡病人的胃酸过多
B.发酵粉中主要含有碳酸钠,能使焙制出的糕点疏松多孔
C.在Na2CO3和 NaHCO3溶液中滴加石灰水均产生白色沉淀
D.Na2CO3和 NaHCO3均能与盐酸或 NaOH 溶液反应
2. 关于NaHCO3和Na2CO3性质的说法不正确的是 ( )
A.相同温度下,在水中的溶解度:Na2CO3>NaHCO3
B.质量相等的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3放出的CO2比Na2CO3多
C.与等质量分数、等体积盐酸反应放出气体的快慢:Na2CO3
3. 下列是某兴趣小组根据教材实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验。查阅资料可知白色的无水硫酸铜粉末遇水变蓝。请观察如图L2-1-11所示的实验装置,分析实验原理,并判断下列说法和做法,其中不科学的是 ( )
图L2-1-11
A.甲为小苏打,乙为纯碱
B.要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球
C.加热不久就能看到A烧杯的澄清石灰水变浑浊
D.B烧杯中发生反应的化学方程式为Ca(OH)2+CO2CaCO3↓+H2O
4. 加热10.0 g碳酸钠和碳酸氢钠的混合物至质量不再变化,剩余固体的质量为8.45 g,则混合物中碳酸钠的质量分数为 ( )
A.42% B.58% C.29% D.50%
5. 一探究小组为了了解碳酸钠及碳酸氢钠的部分性质,设计了如下装置和实验,其中图③、图④装置同时放入90 ℃的水中,气球都膨胀,装有饱和碳酸氢钠溶液的容器上的气球膨胀得更快。下列说法正确的是 ( )
图L2-1-12
A.加盐酸前,图①和图②中溶液都显红色,后者稍深
B.加盐酸过程中,图①气球开始有变化,图②气球开始无变化
C.在图③和图④中,加热过程中一定都产生CO2气体
D.在图③和图④中说明碳酸钠比碳酸氢钠稳定
◆ 知识点二 焰色试验
6.某物质灼烧时透过蓝色钴玻璃观察其焰色试验为紫色,下列判断不正确的是 ( )
A.该物质可能是钾的化合物
B.该物质一定含钾元素
C.不能确定该物质中是否含有钠元素
D.该物质一定是金属钾
7. 五彩缤纷的烟花表演为节日增添了喜庆的气氛。焰火颜色的产生与烟花中含有钠、钾、钙等金属元素的焰色试验有关。下列有关说法中正确的是 ( )
A.焰色试验是化学变化
B.鉴别Na2CO3和K2CO3可以用焰色试验
C.所有的金属元素都有焰色试验
D.K2O与KNO3灼烧时火焰的颜色不同
8. “东风夜放花千树。更吹落、星如雨”。早在宋代,人们就发现不同的金属及其化合物在高温灼烧时,火焰会呈现出不同的颜色,烟花逐渐出现在盛大的典礼或表演中。下列有关说法正确的是 ( )
A.高温灼烧时,铜元素的焰色为黄色
B.焰色试验利用了金属元素的物理性质
C.某物质在灼烧时焰色为黄色,则该物质一定不含K元素
D.将铂丝(或无绣铁丝)用盐酸洗涤后,可直接蘸取药品灼烧
◆ 知识点三 碳酸钠和碳酸氢钠的鉴别与除杂
9. 下列说法正确的是 ( )
A.鉴别NaHCO3与Na2CO3溶液,可用Ca(OH)2溶液
B.质量相等的NaHCO3与Na2CO3分别与足量盐酸完全反应,产生CO2的质量后者更大
C.NaHCO3粉末中混有Na2CO3,可配制成溶液,通入过量的CO2,再低温结晶进行提纯
D.取a g Na2CO3和NaHCO3混合物,与足量稀硫酸充分反应,逸出的气体用碱石灰吸收,碱石灰质量增加b g,能测定Na2CO3和NaHCO3混合物中Na2CO3的质量分数
10.为除去括号内的杂质,所选用的试剂或方法不正确的是 ( )
A.NaCl溶液(Na2SO4),加入适量的Ba(NO3)2溶液,过滤
B.NaOH溶液(Na2CO3),加入适量的Ca(OH)2溶液,过滤
C.Na2O2粉末(Na2O),将混合物在氧气中加热
D.Na2CO3溶液(NaHCO3),加入适量的NaOH溶液
11.某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法进行以下实验,如图L2-1-13Ⅰ~Ⅳ所示。
图L2-1-13
(1)只根据图Ⅰ所示实验,能否达到实验目的 (填“能”或“否”)。
(2)图Ⅱ所示的实验,若固体质量相同且稀盐酸足量时,气球鼓起较小的装有 (填化学式)。
(3)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,与实验Ⅲ相比,实验Ⅳ的优点是 (填选项序号)。
A.Ⅳ比Ⅲ复杂
B.Ⅳ比Ⅲ安全
C.Ⅳ可一套装置同时进行两个对比实验,而Ⅲ不行
(4)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是 (填化学式)。
12. 为确定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,可通过加热分解得到的CO2质量进行计算,某同学设计的实验装置示意图如下:
图L2-1-14
该同学设计的实验装置存在缺陷,有关该实验装置及实验过程中,下列因素可能使碳酸氢钠的质量分数偏高的是 ( )
A.样品分解不完全
B.装置B、C之间缺少CO2的干燥装置
C.产生CO2气体的速率太快,没有被碱石灰完全吸收
D.反应完全后停止加热,通入过量的N2
13. 实验室按如图L2-1-15 所示装置测定纯碱(含少量NaCl)的纯度。下列说法不正确的是 ( )
图L2-1-15
A.装置①和④的作用是防止空气中的CO2进入装置③
B.②中的盐酸可以用稀硫酸代替
C.必须在装置②和③间添加盛有饱和NaHCO3溶液的洗气瓶
D.反应结束时,应再通入空气将装置②中CO2转移到装置③中
14.已知A是一种金属单质,焰色试验呈黄色,各物质间转化关系如图L2-1-16所示,则以下叙述正确的是 ( )
图L2-1-16
A.C溶液呈碱性,所以C属于碱
B.B与水反应产生的气体具有可燃性
C.D能与硫酸铜溶液反应生成蓝色沉淀
D.C受热易分解,产物能使澄清石灰水变浑浊
15. 通过测定混合气体中O2的含量可计算已变质的Na2O2(含Na2CO3)纯度,实验装置如图L2-1-17(Q为弹性良好的气囊)。下列分析错误的是 ( )
图L2-1-17
A.干燥管b中装入无水氯化钙
B.Q气球中产生的气体主要成分是O2、CO2
C.测定气体总体积必须关闭K1、K2,打开K3
D.读完气体总体积后,关闭K3,缓缓打开K1、K2,可观察到Q气球慢慢缩小
16. 2022年6月5日,神舟十四号载人飞船顺利进入预定轨道。飞船的轨道舱内安装盛有Na2O2颗粒的装置,为宇航员供氧。回答下列问题:
(1)Na2O2的供氧。过氧化钠能与人体呼出的酸性氧化物发生反应,其化学方程式为 ,该反应中的还原剂是 (填写化学式)。
(2)反应后组成的探究。Na2O2使用后会失去供氧
能力(又称失效供氧剂),某“失效供氧剂”的化学组成可能是Na2CO3或NaHCO3或两者的混合物。为探究“失效供氧剂”的化学组成,化学探究小组进行如下实验:
取适量“失效供氧剂”于试管中,加热,产生能使澄清石灰水变浑浊的气体,产生该气体的化学方程式为 。
②称取19.0 g“失效供氧剂”,加入足量稀硫酸,将生成的气体用浓硫酸干燥后,再用碱石灰完全吸收,碱石灰质量增加8.8 g,该“失效供氧剂”的化学组成为 (填写化学式)。
17. 碳酸氢钠俗称小苏打,在医疗、食品、橡胶工业中有广泛应用。某NaHCO3晶体中含有NaCl等与酸不反应且受热不易分解的杂质,为测定NaHCO3的质量分数,甲同学设计了以下两种方案。
方案一:滴定法
称取8.4 g样品溶于水,逐滴加入质量分数为19.6%的稀硫酸(密度约为1.0 g·cm-3),待不再产生气体时,测定所消耗稀硫酸的体积。
(1)甲同学共进行3次测定,每次称取8.2 g样品,消耗质量分数为19.6%的稀硫酸的体积如下表:
实验序号 ① ② ③
V[H2SO4(aq)]/mL 20.10 20.00 19.90
样品中NaHCO3的质量分数为 。
方案二:称量法
乙同学按如图L2-1-18所示操作流程进行测定。
图L2-1-18
(2)操作Ⅰ后所得溶液中的主要溶质是 (填化学式)。
(3)操作Ⅱ的名称是 。
(4)样品中NaHCO3的质量分数为 (用含a的代数式表示)。
碳酸钠和碳酸氢钠 焰色试验
1.C [解析] 碳酸钠溶液的碱性较强,具有较强腐蚀性,不能用于治疗胃溃疡病人的胃酸过多,A错误;发酵粉中含有NaHCO3,受热分解产生CO2,能使焙制出的糕点疏松多孔,B错误;在Na2CO3和 NaHCO3溶液中滴加石灰水均产生白色沉淀CaCO3,C正确;Na2CO3不能与NaOH溶液反应,D错误。
2.D [解析] 相同温度下Na2CO3在水中的溶解度大于NaHCO3,故A正确;质量相等的NaCO3和NaHCO3,相对分子质量:NaHCO3
4.B [解析] 碳酸钠加热不反应,碳酸氢钠加热分解为碳酸钠、二氧化碳、水,加热10.0 g碳酸钠和碳酸氢钠的混合物至质量不再变化,剩余固体的质量为8.45 g。设10.0 g混合物中碳酸氢钠的质量为x,则有
2NaHCO3Na2CO3+CO2↑+H2O↑ Δm
168 106 62
x (10.0-8.45) g
列式:=,解得x=4.2 g,故混合物中碳酸钠的质量分数为×100%=58%。
5.D [解析] 碳酸钠及碳酸氢钠溶液都显碱性,其中碳酸钠溶液的碱性更强,酚酞在碱性溶液中显红色,则图①和图②中溶液都显红色,前者稍深,故A错误。碳酸钠和少量盐酸反应生成的是碳酸氢钠,没有气体生成,继续滴加盐酸,生成氯化钠、二氧化碳和水,有气泡产生;碳酸氢钠与盐酸反应直接产生二氧化碳气体,则加盐酸过程中,图①气球开始无变化,图②气球开始有变化,故B错误。③中可能是由于温度高导致瓶内气体的压强增大,而④中气球膨胀得更快,说明除此原因外,NaHCO3受热分解产生CO2,故C错误。图③、图④装置同时放入90 ℃的水中,气球都膨胀,装有饱和碳酸氢钠溶液的容器上的气球膨胀得更快,说明碳酸氢钠不稳定,受热分解,则碳酸钠比碳酸氢钠稳定,故D正确。
6.D [解析] 钾的化合物中含有钾元素,灼烧时透过蓝色钴玻璃观察其焰色试验为紫色,A正确;某物质灼烧时透过蓝色钴玻璃观察其焰色试验为紫色,说明该物质中一定含有钾元素,B正确;蓝色钴玻璃可以过滤黄光,所以无法确定是否含有钠元素,C正确;该物质含有钾元素,可以是钾单质,也可以是钾的化合物,D错误。
7.B [解析] 焰色试验没有生成新物质,属于物理变化,故A错误;钠的焰色试验是黄色,钾的焰色试验是紫色(透过蓝色钴玻璃),故鉴别Na2CO3和K2CO3可以用焰色试验,故B正确;有些金属的焰色试验是无色的,如铂丝,故C错误;焰色试验是某种金属元素的特性,K2O与KNO3都含有K元素,焰色试验(透过蓝色钴玻璃)都显紫色,灼烧时火焰的颜色相同,故D错误。
8.B [解析] 铜元素的焰色为绿色,A错误;焰色试验没有生成新物质,利用了金属元素的物理性质,B正确;K元素的焰色要透过蓝色钴玻璃观察,C错误;铂丝(或无锈铁丝)用盐酸洗涤后,要先在酒精灯外焰灼烧至与原来的火焰颜色相同,再蘸取药品灼烧,D错误。
9.C [解析] NaHCO3和Na2CO3溶液都能与Ca(OH)2溶液反应生成CaCO3沉淀,无法鉴别,A错误;NaHCO3中C元素的质量分数大于Na2CO3,质量相等的NaHCO3和Na2CO3分别与足量的盐酸反应,产生CO2的质量前者更大,B错误;Na2CO3溶液中通入过量的CO2可以转化为NaHCO3,因此NaHCO3粉末中混有Na2CO3,可配制成溶液,通入过量的CO2,再低温结晶进行提纯,C正确;Na2CO3和NaHCO3混合物与足量稀硫酸充分反应后,逸出的CO2气体中含有水蒸气,无法通过碱石灰增加的质量测定混合物中Na2CO3的质量分数,D错误。
10.A [解析] 加入适量Ba(NO3)2溶液,反应生成BaSO4和NaNO3,过滤后,滤液中引入新杂质NaNO3,A错误;加入适量Ca(OH)2溶液,发生反应:Ca(OH)2+Na2CO3CaCO3↓+2NaOH,过滤除去CaCO3,得到NaOH溶液,B正确;在氧气中加热,Na2O与O2反应转化为Na2O2,C正确;NaHCO3与适量NaOH溶液反应生成Na2CO3和H2O,从而除去杂质,D正确。
11.(1)否 (2)Na2CO3 (3)C (4)NaHCO3
[解析] (1)无论碳酸钠还是碳酸氢钠都能和盐酸反应生成二氧化碳,二氧化碳能使澄清石灰水变浑浊,故实验Ⅰ无法鉴别。(2)稀盐酸足量,说明两种固体完全反应,质量相同,含碳量越高,完全反应生成二氧化碳越多,碳酸钠中含碳量为×100%≈11.3%,而碳酸氢钠中含碳量为×100%≈14.3%,所以碳酸钠放出二氧化碳量少,气球鼓起较小。(3)实验Ⅲ、Ⅳ相比,Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行,C符合题意。(4)碳酸钠直接加热不产生气体,而碳酸氢钠不直接加热就能产生气体,更能说明碳酸氢钠不稳定,受热易分解,所以试管B中装入的固体应该是NaHCO3。
12.B [解析] 样品分解不完全,测定二氧化碳的质量偏小,碳酸氢钠质量偏小,碳酸氢钠的质量分数偏低,A错误;装置B、C之间缺少CO2的干燥装置,水蒸气进入装置C导致测定的二氧化碳质量偏大,碳酸氢钠质量偏大,故碳酸氢钠的质量分数偏高,B正确;产生CO2气体的速率太快,没有被碱石灰完全吸收,测定二氧化碳质量偏小,碳酸氢钠质量偏小,则碳酸氢钠的质量分数偏低,C错误;反应完全后停止加热,通入过量的N2,N2不会被装置C吸收,测得二氧化碳的质量不变,则碳酸氢钠的质量分数不会偏高也不会偏低,D错误。
13.C [解析] 测定纯碱(含少量NaCl)的纯度,由实验装置可知,先通入空气,在①中除去CO2,利用氮气等将装置内的二氧化碳排出,然后关闭①和②之间的橡皮管,打开分液漏斗的活塞,盐酸与样品反应生成二氧化碳,③中二氧化碳与氢氧化钡反应生成白色沉淀,反应结束后,再打开①和②之间的橡皮管,继续通入空气使生成的二氧化碳被③中溶液完全吸收,④中碱石灰可防止空气中的二氧化碳被氢氧化钡吸收。装置①和④的作用是防止空气中的CO2进入装置③,可准确测定生成二氧化碳的量,故A正确;硫酸和碳酸钠反应也可以生成二氧化碳,②中的盐酸可以用稀硫酸代替,故B正确;在装置②和③间不需要添加盛有饱和NaHCO3溶液的洗气瓶,HCl与氢氧化钡不生成沉淀,且Ba(OH)2溶液足量,最后测定沉淀的质量,结合守恒法可计算纯度,故C错误;反应结束后,继续通入空气使生成的二氧化碳被③中溶液完全吸收,保证测定结果更准确,故D正确。
14.C [解析] A是一种金属单质,焰色试验呈黄色,可知A是Na;钠和氧气在加热条件下反应生成过氧化钠,B是Na2O2;Na2O2和二氧化碳反应生成碳酸钠和氧气,C是Na2CO3;Na2O2和水反应生成氢氧化钠和氧气,D是NaOH;NaOH和CO2可反应生成Na2CO3。C是Na2CO3,Na2CO3溶液呈碱性,但Na2CO3属于盐,故A错误;B是Na2O2,Na2O2与水反应生成氢氧化钠和氧气,氧气没有可燃性,故B错误;D是NaOH,NaOH与硫酸铜溶液反应生成蓝色氢氧化铜沉淀,故C正确;C是Na2CO3,Na2CO3受热不分解,故D错误。
15.A [解析] 已变质的Na2O2(含Na2CO3)滴入稀H2SO4,发生反应:2Na2O2+2H2SO42Na2SO4+O2↑+2H2O、Na2CO3+H2SO4Na2SO4+CO2↑+H2O,反应产生CO2、O2气体,用碱石灰吸收CO2,在量筒Ⅱ中利用排水法测得O2的量,进而求出Na2O2的量,A错误,B正确;关闭K1、K2,打开K3,CO2、O2使气球变大,将广口瓶中气体排出,水进入量筒Ⅰ中,故量筒Ⅰ中水的体积即为O2、CO2的总体积,C正确;读完气体总体积后,关闭K3,缓缓打开K1、K2,才能观察到Q气球慢慢缩小,D正确。
16.(1)2Na2O2+2CO22Na2CO3+O2 Na2O2
(2)①2NaHCO3Na2CO3+CO2↑+H2O
②Na2CO3和NaHCO3
[解析] (1)人体呼出的酸性氧化物是二氧化碳,过氧化钠能与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO22Na2CO3+O2,Na2O2中氧元素一部分由-1价降低为-2价,一部分由-1价升高为0价,该反应中Na2O2既是氧化剂又是还原剂。(2)①取适量“失效供氧剂”于试管中,加热,产生能使澄清石灰水变浑浊的气体,说明碳酸氢钠受热分解生成二氧化碳。②称取19.0 g“失效供氧剂”,加入足量稀硫酸,将生成的气体用浓硫酸干燥后,再用碱石灰完全吸收,碱石灰质量增加8.8 g,生成的二氧化碳质量为8.8 g,根据Na2CO3~CO2,若二氧化碳全部是碳酸钠反应生成的,则碳酸钠质量为21.2 g;根据NaHCO3~CO2,若二氧化碳全部是碳酸氢钠反应生成的,则碳酸氢钠质量为16.8 g;样品的质量为19.0 g,可知该“失效供氧剂”的化学组成为Na2CO3和NaHCO3。
17.(1)80% (2)NaCl
(3)蒸发结晶 (4)×100%
[解析] (1)由表中数据可知,平均消耗质量分数为19.6%的稀硫酸的体积为20.00 mL,则消耗H2SO4的质量为20.00 mL×1.0 g·cm-3×19.6%=3.92 g。 设样品中NaHCO3的质量为x,则:
2NaHCO3+H2SO4Na2SO4+2CO2↑+2H2O
2×84 98
x 3.92 g
列式:=,解得x=6.72 g,故样品中NaHCO3的质量分数为×100%=80%。(2)准确称取2.0 g NaHCO3样品,向其中滴加足量稀盐酸,发生反应:NaHCO3+HClNaCl+H2O+CO2↑,至不再逸出气体后停止滴加,此时得到的溶液中溶质的主要成分是NaCl。(3)将反应后的溶液转移至蒸发皿中蒸发水分,待仅剩余少量液体时,停止加热,利用余热将残留水分蒸干,然后冷却、干燥、称量,此时得到固体质量是a g,则操作Ⅱ是蒸发结晶。(4)根据反应方程式NaHCO3+HClNaCl+H2O+CO2↑可知:每有84 g NaHCO3发生反应,产生58.5 g NaCl,反应后固体质量减少84 g-58.5 g=25.5 g。此实验中固体充分反应后质量减轻(2.0-a) g,则样品中含有NaHCO3的质量为m(NaHCO3)=×84 g,故样品中NaHCO3的质量分数为×100%=×100%。
