江苏省2025年1月普通高中学业水平合格性考试 导学案 课时7 铁、铜及其化合物(含解析)
文档属性
| 名称 | 江苏省2025年1月普通高中学业水平合格性考试 导学案 课时7 铁、铜及其化合物(含解析) |
|
|
| 格式 | doc | ||
| 文件大小 | 205.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-06 00:00:00 | ||
图片预览



文档简介
课时7 铁、铜及其化合物
知 识 梳 理
知识点1 铁的性质
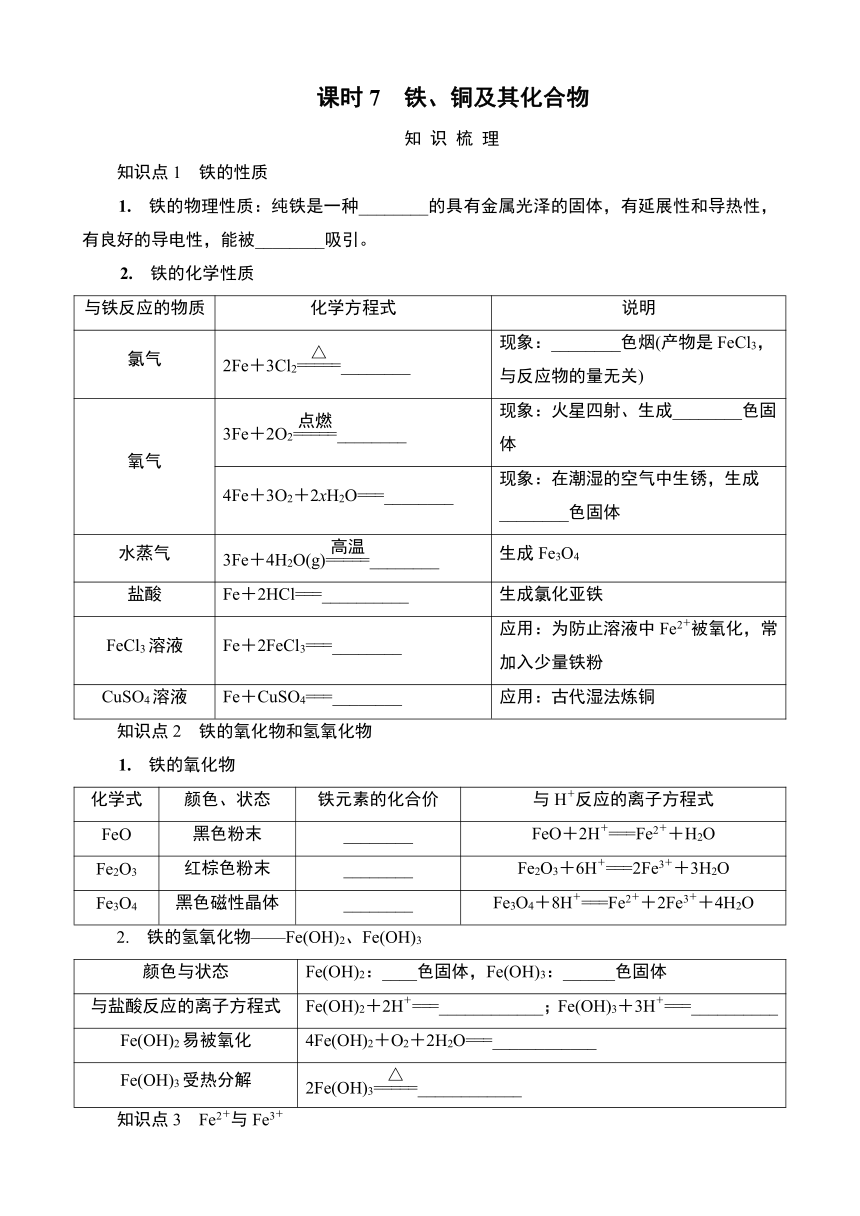
1. 铁的物理性质:纯铁是一种________的具有金属光泽的固体,有延展性和导热性,有良好的导电性,能被________吸引。
2. 铁的化学性质
与铁反应的物质 化学方程式 说明
氯气 2Fe+3Cl2________ 现象:________色烟(产物是FeCl3,与反应物的量无关)
氧气 3Fe+2O2________ 现象:火星四射、生成________色固体
4Fe+3O2+2xH2O===________ 现象:在潮湿的空气中生锈,生成________色固体
水蒸气 3Fe+4H2O(g)________ 生成Fe3O4
盐酸 Fe+2HCl===__________ 生成氯化亚铁
FeCl3溶液 Fe+2FeCl3===________ 应用:为防止溶液中Fe2+被氧化,常加入少量铁粉
CuSO4溶液 Fe+CuSO4===________ 应用:古代湿法炼铜
知识点2 铁的氧化物和氢氧化物
1. 铁的氧化物
化学式 颜色、状态 铁元素的化合价 与H+反应的离子方程式
FeO 黑色粉末 ________ FeO+2H+===Fe2++H2O
Fe2O3 红棕色粉末 ________ Fe2O3+6H+===2Fe3++3H2O
Fe3O4 黑色磁性晶体 ________ Fe3O4+8H+===Fe2++2Fe3++4H2O
2. 铁的氢氧化物——Fe(OH)2、Fe(OH)3
颜色与状态 Fe(OH)2:____色固体,Fe(OH)3:______色固体
与盐酸反应的离子方程式 Fe(OH)2+2H+===____________;Fe(OH)3+3H+===__________
Fe(OH)2易被氧化 4Fe(OH)2+O2+2H2O===____________
Fe(OH)3受热分解 2Fe(OH)3____________
知识点3 Fe2+与Fe3+
1. Fe3+和Fe2+的检验方法
Fe3+的检验方法 Fe2+的检验方法
特别提醒:①检验Fe2+应先加KSCN溶液,无明显现象,再加氯水(或双氧水);加入试剂的顺序绝不能颠倒;②在含Fe3+溶液中加入KSCN溶液,溶液变红,不是产生红色沉淀
2. Fe2+与Fe3+的相互转化
转化 化学(或离子)方程式 说明
Fe2+→Fe3+ 2FeCl2+Cl2===________;2Fe2++Cl2===____________ 加入强氧化剂
Fe3+→Fe2+ Fe+2FeCl3===________;Fe+2Fe3+===________;Cu+2Fe3+===2Fe2++Cu2+ 加入还原剂
3. 有关含铁物质的除杂
主要成分 杂质 所加试剂 离子方程式
FeCl3溶液 FeCl2溶液 氯气 ____________________________
FeCl2溶液 FeCl3溶液 铁粉 ____________________________
FeCl2溶液 CuCl2溶液 铁粉 ____________________________
Fe Al 过量NaOH溶液 2Al+2OH-+6H2O===2[Al(OH)4]-+3H2↑
Fe2O3 Al2O3 过量NaOH溶液 ____________________________
知识点4 铜及其化合物
1. 铜及其常见化合物的颜色
Cu CuSO4 Cu(OH)2 CuSO4·5H2O CuO
紫红色 白色 蓝色 黑色
2. CuSO4(重金属盐,有毒,能使蛋白质变性)
(1) 无水CuSO4遇水变蓝色(生成CuSO4·5H2O),可用无水CuSO4检验水。
(2) 胆矾与石灰乳混合配制农药波尔多液(用来杀灭植物的病毒)。
(3) CuSO4·5H2O俗称蓝矾或胆矾,受热易分解:CuSO4·5H2OCuSO4+5H2O。
典 型 例 题
类型1 俗名
(2022·江苏学测)化学与生活密切相关。下列生活中常见物质的俗名(或主要成分)与化学式相对应的是( )
A. 苏打——NaHCO3 B. 胆矾——CuSO4
C. 铁红——Fe2O3 D. 生石灰——Ca(OH)2
下列物质的俗名(或主要成分)与化学式对应正确的是( )
A. 磁性氧化铁——Fe2O3 B. 食盐——NaCl
C. 大理石——CaSO4 D. 绿矾——CuSO4·5H2O
类型2 铁及其化合物的性质
(2022·江苏学测)铁粉活化用于污水处理。活化方法如下:向一定量表面被部分氧化的铁粉中加入少量稀盐酸和H2O2(少量H2O2有利于铁粉活化),搅拌。一段时间后,铁粉吸附Fe2+形成胶体。活化过程中,溶液中c(Fe2+)、c(Fe3+)随时间的变化如图所示。下列说法不合理的是( )
A. 盐酸能与铁粉表面的Fe2O3反应
B. 0~2.5 min,溶液的pH不断升高
C. 2.5~5 min,c(Fe3+)减小,c(Fe2+)增大,可能发生反应为2Fe3++Fe===3Fe2+
D. 5 min后,c(Fe2+)减小,可能是H2O2将Fe2+还原为Fe
(2024·扬州合格考模拟)下列有关物质的性质与用途不具有对应关系的是( )
A. NaClO有氧化性,可用于消毒杀菌
B. NaHCO3受热易分解,可用于制胃酸中和剂
C. FeCl3具有氧化性,可用于腐蚀印刷电路板上的Cu
D. Fe粉能与O2反应,可用作食品保存的吸氧剂
(2023·盐城学测合格考)医学发现一种Fe3O4纳米粒子具有肝靶向功能。利用废旧镀锌铁皮制备Fe3O4胶体粒子的流程图如下:
已知:Zn溶于强碱时生成[Zn(OH)4]2-。下列有关说法正确的是( )
A. Fe3O4俗称铁红
B. “碱洗”是为了洗去废旧镀锌铁皮表面的油污
C. “酸溶”中发生反应的离子方程式为Fe(OH)3+3H+===Fe3++3H2O
D. “氧化”后溶液中存在的离子有:H+、Fe2+、Fe3+、SO
类型3 Fe3+的检验
(2007·江苏学测)某溶液中滴入KSCN溶液后变红,说明该溶液中存在( )
A. NO B. Fe3+
C. SO D. Mg2+
(2023·江苏六校联考学测合格考)某溶液滴加硫氰化钾(KSCN)溶液时无明显现象,再向其中滴加适量双氧水后溶液变红,则原溶液中一定有( )
A. Fe3+ B. Fe2+
C. HCO D. Al3+
课时7 铁、铜及其化合物
[知识梳理]
[知识点1] 1. 银白色 磁铁 2. 2FeCl3 棕褐 Fe3O4 黑 2[Fe2O3·xH2O] 红棕 Fe3O4+4H2 FeCl2+H2↑ 3FeCl2 FeSO4+Cu
[知识点2] 1. +2 +3 +2、+3
2. 白 红褐 Fe2++2H2O Fe3++3H2O 4Fe(OH)3 Fe2O3+3H2O
[知识点3] 2. 2FeCl3 2Fe3++2Cl- 3FeCl2 3Fe2+
3. 2Fe2++Cl2===2Cl-+2Fe3+ 2Fe3++Fe===3Fe2+
Cu2++Fe===Cu+Fe2+ Al2O3+2OH-+3H2O===2[Al(OH)4]-
[典型例题]
例题1 C 【解析】苏打为Na2CO3,A错误;胆矾化学式为CuSO4·5H2O,B错误;铁红的主要成分为Fe2O3 ,C正确;生石灰为CaO,D错误。
变式1 B 【解析】磁性氧化铁为Fe3O4,A错误;大理石的主要成分是CaCO3,C错误;绿矾为FeSO4·7H2O,D错误。
例题2 D 【解析】开始时Fe3+和Fe2+同时产生,Fe3+来自Fe2O3与盐酸的反应,Fe2+来自Fe与盐酸的反应,A正确;0~2.5 min,生成的Fe3+和Fe2+的速率都比较快,消耗H+较快,所以pH不断升高,B正确;2.5~5 min,c(Fe3+)减小,c(Fe2+)增大,可能发生的反应为2Fe3++Fe===3Fe2+,C正确;5 min后,c(Fe2+)减小是因为部分Fe2+被铁粉吸附形成胶体,H2O2不能还原Fe2+,D错误。
变式2 B 【解析】NaHCO3与胃酸中的HCl反应,与受热易分解无关,B错误。
变式3 D 【解析】由信息可知,Zn能溶于强碱溶液,则加入氢氧化钠溶液反应,锌转化为[Zn(OH)4]2-进入溶液,铁不溶解,分离出不溶物为Fe,加入稀硫酸与Fe反应生成硫酸亚铁,再加入适量H2O2溶液,部分亚铁离子被氧化为铁离子,得到含Fe2+、Fe3+的溶液,再通入氮气排出空气,防止亚铁离子被氧化,加入氢氧化钠溶液,最终生成四氧化三铁胶体粒子。Fe3O4为黑色固体,Fe2O3俗称铁红,常用作红色油漆和涂料,A错误;氢氧化钠溶液具有去除油污作用,但是本流程中“碱洗”的作用是将Zn转化为可溶于水的 [Zn(OH)4]2-,即起到溶解镀锌层的作用,B错误;“酸溶”的离子方程式为Fe+2H+===Fe2++H2↑,C错误;酸溶生成硫酸亚铁溶液,加过氧化氢氧化部分亚铁离子,则“氧化”后溶液中存在的离子有:H+、Fe2+、Fe3+、SO,D正确。
例题3 B 【解析】 若某溶液中滴入KSCN溶液后变红,说明该溶液中含有Fe3+,B正确。
变式4 B
知 识 梳 理
知识点1 铁的性质
1. 铁的物理性质:纯铁是一种________的具有金属光泽的固体,有延展性和导热性,有良好的导电性,能被________吸引。
2. 铁的化学性质
与铁反应的物质 化学方程式 说明
氯气 2Fe+3Cl2________ 现象:________色烟(产物是FeCl3,与反应物的量无关)
氧气 3Fe+2O2________ 现象:火星四射、生成________色固体
4Fe+3O2+2xH2O===________ 现象:在潮湿的空气中生锈,生成________色固体
水蒸气 3Fe+4H2O(g)________ 生成Fe3O4
盐酸 Fe+2HCl===__________ 生成氯化亚铁
FeCl3溶液 Fe+2FeCl3===________ 应用:为防止溶液中Fe2+被氧化,常加入少量铁粉
CuSO4溶液 Fe+CuSO4===________ 应用:古代湿法炼铜
知识点2 铁的氧化物和氢氧化物
1. 铁的氧化物
化学式 颜色、状态 铁元素的化合价 与H+反应的离子方程式
FeO 黑色粉末 ________ FeO+2H+===Fe2++H2O
Fe2O3 红棕色粉末 ________ Fe2O3+6H+===2Fe3++3H2O
Fe3O4 黑色磁性晶体 ________ Fe3O4+8H+===Fe2++2Fe3++4H2O
2. 铁的氢氧化物——Fe(OH)2、Fe(OH)3
颜色与状态 Fe(OH)2:____色固体,Fe(OH)3:______色固体
与盐酸反应的离子方程式 Fe(OH)2+2H+===____________;Fe(OH)3+3H+===__________
Fe(OH)2易被氧化 4Fe(OH)2+O2+2H2O===____________
Fe(OH)3受热分解 2Fe(OH)3____________
知识点3 Fe2+与Fe3+
1. Fe3+和Fe2+的检验方法
Fe3+的检验方法 Fe2+的检验方法
特别提醒:①检验Fe2+应先加KSCN溶液,无明显现象,再加氯水(或双氧水);加入试剂的顺序绝不能颠倒;②在含Fe3+溶液中加入KSCN溶液,溶液变红,不是产生红色沉淀
2. Fe2+与Fe3+的相互转化
转化 化学(或离子)方程式 说明
Fe2+→Fe3+ 2FeCl2+Cl2===________;2Fe2++Cl2===____________ 加入强氧化剂
Fe3+→Fe2+ Fe+2FeCl3===________;Fe+2Fe3+===________;Cu+2Fe3+===2Fe2++Cu2+ 加入还原剂
3. 有关含铁物质的除杂
主要成分 杂质 所加试剂 离子方程式
FeCl3溶液 FeCl2溶液 氯气 ____________________________
FeCl2溶液 FeCl3溶液 铁粉 ____________________________
FeCl2溶液 CuCl2溶液 铁粉 ____________________________
Fe Al 过量NaOH溶液 2Al+2OH-+6H2O===2[Al(OH)4]-+3H2↑
Fe2O3 Al2O3 过量NaOH溶液 ____________________________
知识点4 铜及其化合物
1. 铜及其常见化合物的颜色
Cu CuSO4 Cu(OH)2 CuSO4·5H2O CuO
紫红色 白色 蓝色 黑色
2. CuSO4(重金属盐,有毒,能使蛋白质变性)
(1) 无水CuSO4遇水变蓝色(生成CuSO4·5H2O),可用无水CuSO4检验水。
(2) 胆矾与石灰乳混合配制农药波尔多液(用来杀灭植物的病毒)。
(3) CuSO4·5H2O俗称蓝矾或胆矾,受热易分解:CuSO4·5H2OCuSO4+5H2O。
典 型 例 题
类型1 俗名
(2022·江苏学测)化学与生活密切相关。下列生活中常见物质的俗名(或主要成分)与化学式相对应的是( )
A. 苏打——NaHCO3 B. 胆矾——CuSO4
C. 铁红——Fe2O3 D. 生石灰——Ca(OH)2
下列物质的俗名(或主要成分)与化学式对应正确的是( )
A. 磁性氧化铁——Fe2O3 B. 食盐——NaCl
C. 大理石——CaSO4 D. 绿矾——CuSO4·5H2O
类型2 铁及其化合物的性质
(2022·江苏学测)铁粉活化用于污水处理。活化方法如下:向一定量表面被部分氧化的铁粉中加入少量稀盐酸和H2O2(少量H2O2有利于铁粉活化),搅拌。一段时间后,铁粉吸附Fe2+形成胶体。活化过程中,溶液中c(Fe2+)、c(Fe3+)随时间的变化如图所示。下列说法不合理的是( )
A. 盐酸能与铁粉表面的Fe2O3反应
B. 0~2.5 min,溶液的pH不断升高
C. 2.5~5 min,c(Fe3+)减小,c(Fe2+)增大,可能发生反应为2Fe3++Fe===3Fe2+
D. 5 min后,c(Fe2+)减小,可能是H2O2将Fe2+还原为Fe
(2024·扬州合格考模拟)下列有关物质的性质与用途不具有对应关系的是( )
A. NaClO有氧化性,可用于消毒杀菌
B. NaHCO3受热易分解,可用于制胃酸中和剂
C. FeCl3具有氧化性,可用于腐蚀印刷电路板上的Cu
D. Fe粉能与O2反应,可用作食品保存的吸氧剂
(2023·盐城学测合格考)医学发现一种Fe3O4纳米粒子具有肝靶向功能。利用废旧镀锌铁皮制备Fe3O4胶体粒子的流程图如下:
已知:Zn溶于强碱时生成[Zn(OH)4]2-。下列有关说法正确的是( )
A. Fe3O4俗称铁红
B. “碱洗”是为了洗去废旧镀锌铁皮表面的油污
C. “酸溶”中发生反应的离子方程式为Fe(OH)3+3H+===Fe3++3H2O
D. “氧化”后溶液中存在的离子有:H+、Fe2+、Fe3+、SO
类型3 Fe3+的检验
(2007·江苏学测)某溶液中滴入KSCN溶液后变红,说明该溶液中存在( )
A. NO B. Fe3+
C. SO D. Mg2+
(2023·江苏六校联考学测合格考)某溶液滴加硫氰化钾(KSCN)溶液时无明显现象,再向其中滴加适量双氧水后溶液变红,则原溶液中一定有( )
A. Fe3+ B. Fe2+
C. HCO D. Al3+
课时7 铁、铜及其化合物
[知识梳理]
[知识点1] 1. 银白色 磁铁 2. 2FeCl3 棕褐 Fe3O4 黑 2[Fe2O3·xH2O] 红棕 Fe3O4+4H2 FeCl2+H2↑ 3FeCl2 FeSO4+Cu
[知识点2] 1. +2 +3 +2、+3
2. 白 红褐 Fe2++2H2O Fe3++3H2O 4Fe(OH)3 Fe2O3+3H2O
[知识点3] 2. 2FeCl3 2Fe3++2Cl- 3FeCl2 3Fe2+
3. 2Fe2++Cl2===2Cl-+2Fe3+ 2Fe3++Fe===3Fe2+
Cu2++Fe===Cu+Fe2+ Al2O3+2OH-+3H2O===2[Al(OH)4]-
[典型例题]
例题1 C 【解析】苏打为Na2CO3,A错误;胆矾化学式为CuSO4·5H2O,B错误;铁红的主要成分为Fe2O3 ,C正确;生石灰为CaO,D错误。
变式1 B 【解析】磁性氧化铁为Fe3O4,A错误;大理石的主要成分是CaCO3,C错误;绿矾为FeSO4·7H2O,D错误。
例题2 D 【解析】开始时Fe3+和Fe2+同时产生,Fe3+来自Fe2O3与盐酸的反应,Fe2+来自Fe与盐酸的反应,A正确;0~2.5 min,生成的Fe3+和Fe2+的速率都比较快,消耗H+较快,所以pH不断升高,B正确;2.5~5 min,c(Fe3+)减小,c(Fe2+)增大,可能发生的反应为2Fe3++Fe===3Fe2+,C正确;5 min后,c(Fe2+)减小是因为部分Fe2+被铁粉吸附形成胶体,H2O2不能还原Fe2+,D错误。
变式2 B 【解析】NaHCO3与胃酸中的HCl反应,与受热易分解无关,B错误。
变式3 D 【解析】由信息可知,Zn能溶于强碱溶液,则加入氢氧化钠溶液反应,锌转化为[Zn(OH)4]2-进入溶液,铁不溶解,分离出不溶物为Fe,加入稀硫酸与Fe反应生成硫酸亚铁,再加入适量H2O2溶液,部分亚铁离子被氧化为铁离子,得到含Fe2+、Fe3+的溶液,再通入氮气排出空气,防止亚铁离子被氧化,加入氢氧化钠溶液,最终生成四氧化三铁胶体粒子。Fe3O4为黑色固体,Fe2O3俗称铁红,常用作红色油漆和涂料,A错误;氢氧化钠溶液具有去除油污作用,但是本流程中“碱洗”的作用是将Zn转化为可溶于水的 [Zn(OH)4]2-,即起到溶解镀锌层的作用,B错误;“酸溶”的离子方程式为Fe+2H+===Fe2++H2↑,C错误;酸溶生成硫酸亚铁溶液,加过氧化氢氧化部分亚铁离子,则“氧化”后溶液中存在的离子有:H+、Fe2+、Fe3+、SO,D正确。
例题3 B 【解析】 若某溶液中滴入KSCN溶液后变红,说明该溶液中含有Fe3+,B正确。
变式4 B
同课章节目录
