5.1.2酶的特性(共31张ppt)生物人教版(2019)必修一
文档属性
| 名称 | 5.1.2酶的特性(共31张ppt)生物人教版(2019)必修一 |  | |
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 生物学 | ||
| 更新时间 | 2024-12-07 12:08:02 | ||
图片预览








文档简介
(共31张PPT)
降低化学反应活化能的酶
第2课时
温故
酶在代谢中的作用
酶的
本质
比较过氧化氢在
不同条件下的分解
酶具有催化作用,能显著降低化学反应的活化能
关于酶本质的探索
绝大多数酶是蛋白质
少数酶是RNA——核酶
知新
酶的定义:
酶是活细胞产生的具有催化作用的有机物,其中绝大多数酶是蛋白质。
酶的定义:
酶是活细胞产生的具有催化作用的有机物,其中绝大多数酶是蛋白质。
①酶只有一个作用:催化作用,不具有传递信息、调节的作用。
②有些酶在细胞内发挥作用,有些酶在细胞外发挥作用(如:消化酶)。
酶也可以在体外发挥作用(如:加酶洗衣粉中的酶)
③酶的基本单位是氨基酸或核糖核苷酸。
酶与无机催化剂相比有哪些共性和特性呢?
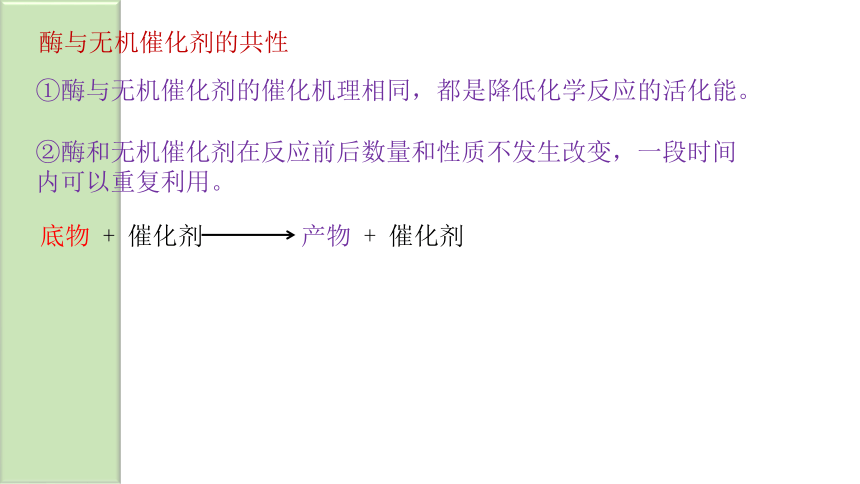
酶与无机催化剂的共性
①酶与无机催化剂的催化机理相同,都是降低化学反应的活化能。
②酶和无机催化剂在反应前后数量和性质不发生改变,一段时间内可以重复利用。
底物 + 催化剂
产物 + 催化剂
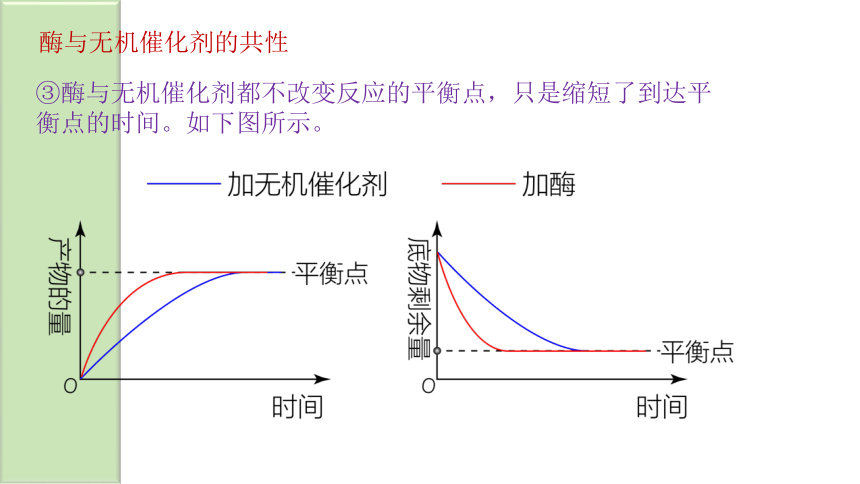
酶与无机催化剂的共性
③酶与无机催化剂都不改变反应的平衡点,只是缩短了到达平衡点的时间。如下图所示。
二、酶的特性
1.高效性
与无机催化剂相比,酶的催化效率高,是无机催化剂的107~1013倍
保证了细胞内化学反应的顺利进行,
保证了细胞内能量供应稳定。
与无机催化剂相比,酶能显著降低化学反应的活化能。
①内容
②意义
③原因
二、酶的特性
1.高效性
④实验设计思路及预测结果与结论
项目 对照组 实验组
材料 等量的同一种底物 试剂 一定量的无机催化剂 等量的底物对应的酶溶液
现象 反应速率慢 或反应时间长 反应速率快
或反应时间短
结论 酶具有高效性 二、酶的特性
1.高效性
(5)实验验证
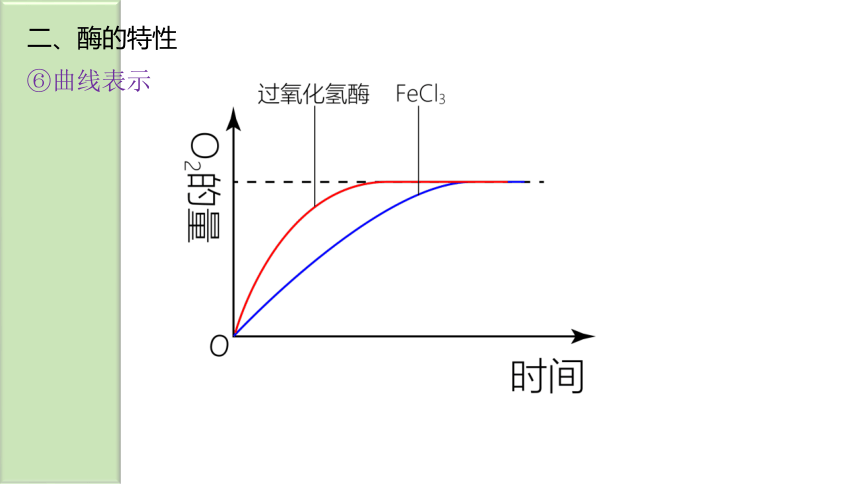
在相同条件下,比较FeCl3和过氧化氢酶对过氧化氢的分解速率。如图中的3和4。
⑥曲线表示
二、酶的特性
二、酶的特性
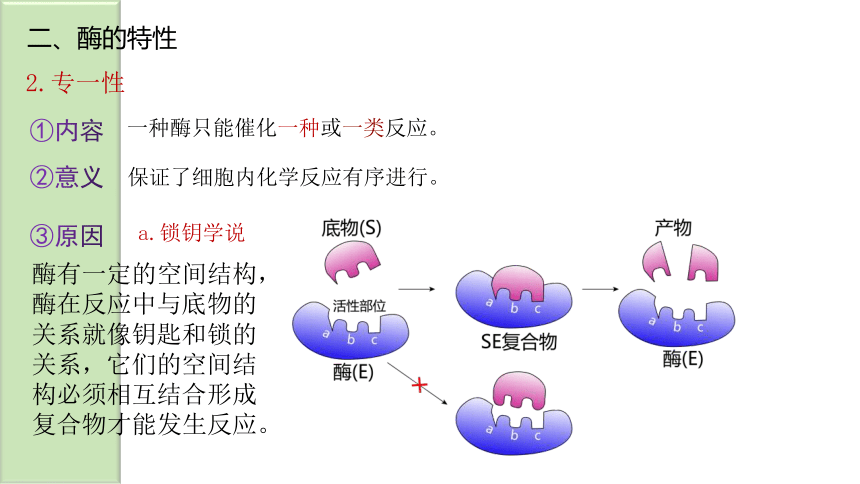
2.专一性
一种酶只能催化一种或一类反应。
保证了细胞内化学反应有序进行。
a.锁钥学说
①内容
②意义
③原因
酶有一定的空间结构,酶在反应中与底物的关系就像钥匙和锁的关系,它们的空间结构必须相互结合形成复合物才能发生反应。
2.专一性
b.诱导契合学说
③原因
酶活性部位不是刚性不变的,其形状可在结合底物时有所改变,即底物与酶活性部位结合,会诱导酶发生构象变化,使酶的活性中心变得与底物的结构互补,两者相互契合,从而发挥催化功能。
2.专一性
④实验设计思路及预测结果与结论
项目 对照组 实验组
材料 底物A 底物B
试剂 酶A 酶A
现象 发生反应 不发生反应
结论 酶具有专一性 2.专一性
⑤实验验证
原理
淀粉和蔗糖都是非还原糖。它们在酶的催化下都能水解呈还原糖。在淀粉溶液和蔗糖溶液中分别加入淀粉酶,再用斐林试剂鉴定溶液中有无还原糖,就可以看出淀粉酶是否只能催化特定的化学反应了。
步骤 项目 试管1 试管2
1 注入可溶性淀粉溶液
2 注入蔗糖溶液
3 注入新鲜的淀粉酶溶液
4 保温 5 加斐林试剂 6 水浴加热 7 观察颜色变化
2mL
—
—
2mL
2mL
2mL
60℃保温5min
各加入2mL
沸水浴1min
砖红色
无砖红色
2.专一性
⑤实验验证
思考:能否用碘液对实验结果进行检测?
不能,因为碘液无法检测蔗糖是否发生水解
改进实验设计
步骤 项目 1 2 3 4 5 6
1 加淀粉溶液 2mL 2mL 2mL
2 加蔗糖溶液 2mL 2mL 2mL
3 加淀粉酶 1mL 1mL
4 加蔗糖酶 1mL 1mL
5 保温 各自在60℃下保温5min 6 加斐林试剂 各加入2mL斐林试剂 7 沸水浴加热
观察颜色 8 沸水浴1min
无砖红色
无砖红色
有砖红色
无砖红色
无砖红色
有砖红色
实验结论:
淀粉酶只能催化淀粉水解,不能催化蔗糖水解;蔗糖酶只能催化蔗糖水解,不能催化淀粉水解。即酶具有专一性。
2.专一性
⑥曲线表示
3.条件温和
①含义
酶通常在一定pH范围和一定温度范围内才能起作用,而且在某一pH、某一温度下作用最强。
②意义
保证细胞代谢能够在温和条件下高效进行。
③原因
过酸、过碱、高温,会使酶的空间结构遭到破坏,甚至使酶永久失活,
低温使酶的活性抑制,空间结构稳定,在适宜温度下酶的活性会升高。
因此,酶制剂需要在低温和适宜的pH下保存。
④实验设计思路(探究温度对酶活性的影响)
实验过程与结果(探究温度对酶活性的影响)
操作 1试管 2试管 3试管 4试管 5试管 6试管
0℃ 0℃ 60℃ 60℃ 100℃ 100℃
加淀粉 2mL — 2mL — 2mL —
加淀粉酶 — 2mL — 2mL — 2mL
保温 在各自温度下保温5min 混合 将2加入1中 将4加入3中 将6加入5中 保温 在各自温度下保温5min 加碘液 2滴 2滴 2滴 观察颜色 实验结论
温度过低或过高酶的活性都较低。
变蓝
不变蓝
变蓝
思考·讨论
1.如何进一步探究淀粉酶的最适温度?
缩小温度梯度,重复进行上述实验。
2.为什么不能用斐林试剂对实验结果进行检测?
该实验的自变量是温度,用斐林试剂检测时需要水浴加热,
这样会干扰自变量。
3.为什么不能用过氧化氢酶和过氧化氢来探究温度对酶活性的影响?
因为过氧化氢本身受热易分解,会对实验结果造成干扰。
④实验设计思路(探究pH对酶活性的影响)
探究pH对酶活性影响的实验方案
步 骤 项目 试管1 试管2 试管3
1 注入新鲜的肝脏研磨液 2滴 2滴 2滴
2 注入不同pH的溶液 1 mL 蒸馏水 1 mL 盐酸 1 mL
NaOH
溶液
3 注入等量的H2O2溶液 2 mL 2 mL 2 mL
4 观察现象
有大量气泡
产生
无气泡产生
无气泡产生
实验结论:
过氧化氢酶的最适pH接近7.0,过酸或过碱,
都会使其催化活性下降。
1.该实验中,能否将步骤2、3调换 为什么
2.该实验不宜选用淀粉酶催化淀粉的水解做实验,为什么
因为淀粉酶催化的底物——淀粉在酸性条件下也会发生水解反应,无法排除无关变量的干扰。
不能。若调换2、3步骤,在调节pH之前,试管中已经发生了反应,从而影响实验结果。
思考:
⑥曲线
在一定条件下,酶活性最大时的温度称为该酶的最适温度。
在一定温度范围内,酶促反应速率随温度的升高而加快;但当温度升高到一定限度后,酶促反应速率随着温度的升高而下降。
曲线解读
⑥曲线
最适pH
最适pH
曲线解读:
在一定条件下,酶活性最大时的pH称为该酶的最适pH。
pH偏高或偏低,酶促反应速率都会下降。
三、影响酶促反应速率的因素
1.酶促反应:
由酶催化的化学反应,生物体内的化学反应绝大多数属于酶促反应。
2.酶促反应速率:
单位时间内反应物或生成物浓度的改变量。
3.影响酶促反应速率的因素:
pH
温度
抑制剂
激活剂
活性
浓度
底物浓度
酶
酶促反应速率
甲
乙
丙
丁
①图甲中,温度从a降低或升高,酶促反速率均下降,但是下降的原因不同。
1.温度、pH、底物浓度、酶浓度
②图乙中,pH从b降低或升高,酶促反速率均下降,但是下降的原因相同。
③图丙中,底物浓度为c时,酶促反应速率达到最大,因为,酶数量有限。
课后习题
2.下图表示最适温度下反应物浓度对酶所催化的化学反应速率的影响。
(1)请解释在A、B、C三点时该化学反应的状况。
A 点:随着反应底物浓度的增加,反应速率加快。
B 点:反应速率在此时达到最高
C 点:反应速率不再随反应底物浓度的增加而升高,维持在相对稳定的水平。
2.下图表示最适温度下反应物浓度对酶所催化的化学反应速率的影响。
(2)如果从A点开始温度升高10℃,曲线会发生什么变化 为什么 请画出变化后的曲线。
如果 A 点时温度升高 10℃,曲线上升的幅度变小因为图中原曲线表示在最适温度下催化速率随底物浓度的变化。温度高于或低于最适温度,反应速率都会变慢。
2.下图表示最适温度下反应物浓度对酶所催化的化学反应速率的影响。
(3)如果在B点时向反应混合物中加入少量同样的酶,曲线会发生什么变化 为什么 请画出相应的曲线。
该曲线表明,B 点的反应底物的浓度足够大,是酶的数量限制了反应速率的提高,这时加入少量的酶,会使反应速率加快。
降低化学反应活化能的酶
第2课时
温故
酶在代谢中的作用
酶的
本质
比较过氧化氢在
不同条件下的分解
酶具有催化作用,能显著降低化学反应的活化能
关于酶本质的探索
绝大多数酶是蛋白质
少数酶是RNA——核酶
知新
酶的定义:
酶是活细胞产生的具有催化作用的有机物,其中绝大多数酶是蛋白质。
酶的定义:
酶是活细胞产生的具有催化作用的有机物,其中绝大多数酶是蛋白质。
①酶只有一个作用:催化作用,不具有传递信息、调节的作用。
②有些酶在细胞内发挥作用,有些酶在细胞外发挥作用(如:消化酶)。
酶也可以在体外发挥作用(如:加酶洗衣粉中的酶)
③酶的基本单位是氨基酸或核糖核苷酸。
酶与无机催化剂相比有哪些共性和特性呢?
酶与无机催化剂的共性
①酶与无机催化剂的催化机理相同,都是降低化学反应的活化能。
②酶和无机催化剂在反应前后数量和性质不发生改变,一段时间内可以重复利用。
底物 + 催化剂
产物 + 催化剂
酶与无机催化剂的共性
③酶与无机催化剂都不改变反应的平衡点,只是缩短了到达平衡点的时间。如下图所示。
二、酶的特性
1.高效性
与无机催化剂相比,酶的催化效率高,是无机催化剂的107~1013倍
保证了细胞内化学反应的顺利进行,
保证了细胞内能量供应稳定。
与无机催化剂相比,酶能显著降低化学反应的活化能。
①内容
②意义
③原因
二、酶的特性
1.高效性
④实验设计思路及预测结果与结论
项目 对照组 实验组
材料 等量的同一种底物 试剂 一定量的无机催化剂 等量的底物对应的酶溶液
现象 反应速率慢 或反应时间长 反应速率快
或反应时间短
结论 酶具有高效性 二、酶的特性
1.高效性
(5)实验验证
在相同条件下,比较FeCl3和过氧化氢酶对过氧化氢的分解速率。如图中的3和4。
⑥曲线表示
二、酶的特性
二、酶的特性
2.专一性
一种酶只能催化一种或一类反应。
保证了细胞内化学反应有序进行。
a.锁钥学说
①内容
②意义
③原因
酶有一定的空间结构,酶在反应中与底物的关系就像钥匙和锁的关系,它们的空间结构必须相互结合形成复合物才能发生反应。
2.专一性
b.诱导契合学说
③原因
酶活性部位不是刚性不变的,其形状可在结合底物时有所改变,即底物与酶活性部位结合,会诱导酶发生构象变化,使酶的活性中心变得与底物的结构互补,两者相互契合,从而发挥催化功能。
2.专一性
④实验设计思路及预测结果与结论
项目 对照组 实验组
材料 底物A 底物B
试剂 酶A 酶A
现象 发生反应 不发生反应
结论 酶具有专一性 2.专一性
⑤实验验证
原理
淀粉和蔗糖都是非还原糖。它们在酶的催化下都能水解呈还原糖。在淀粉溶液和蔗糖溶液中分别加入淀粉酶,再用斐林试剂鉴定溶液中有无还原糖,就可以看出淀粉酶是否只能催化特定的化学反应了。
步骤 项目 试管1 试管2
1 注入可溶性淀粉溶液
2 注入蔗糖溶液
3 注入新鲜的淀粉酶溶液
4 保温 5 加斐林试剂 6 水浴加热 7 观察颜色变化
2mL
—
—
2mL
2mL
2mL
60℃保温5min
各加入2mL
沸水浴1min
砖红色
无砖红色
2.专一性
⑤实验验证
思考:能否用碘液对实验结果进行检测?
不能,因为碘液无法检测蔗糖是否发生水解
改进实验设计
步骤 项目 1 2 3 4 5 6
1 加淀粉溶液 2mL 2mL 2mL
2 加蔗糖溶液 2mL 2mL 2mL
3 加淀粉酶 1mL 1mL
4 加蔗糖酶 1mL 1mL
5 保温 各自在60℃下保温5min 6 加斐林试剂 各加入2mL斐林试剂 7 沸水浴加热
观察颜色 8 沸水浴1min
无砖红色
无砖红色
有砖红色
无砖红色
无砖红色
有砖红色
实验结论:
淀粉酶只能催化淀粉水解,不能催化蔗糖水解;蔗糖酶只能催化蔗糖水解,不能催化淀粉水解。即酶具有专一性。
2.专一性
⑥曲线表示
3.条件温和
①含义
酶通常在一定pH范围和一定温度范围内才能起作用,而且在某一pH、某一温度下作用最强。
②意义
保证细胞代谢能够在温和条件下高效进行。
③原因
过酸、过碱、高温,会使酶的空间结构遭到破坏,甚至使酶永久失活,
低温使酶的活性抑制,空间结构稳定,在适宜温度下酶的活性会升高。
因此,酶制剂需要在低温和适宜的pH下保存。
④实验设计思路(探究温度对酶活性的影响)
实验过程与结果(探究温度对酶活性的影响)
操作 1试管 2试管 3试管 4试管 5试管 6试管
0℃ 0℃ 60℃ 60℃ 100℃ 100℃
加淀粉 2mL — 2mL — 2mL —
加淀粉酶 — 2mL — 2mL — 2mL
保温 在各自温度下保温5min 混合 将2加入1中 将4加入3中 将6加入5中 保温 在各自温度下保温5min 加碘液 2滴 2滴 2滴 观察颜色 实验结论
温度过低或过高酶的活性都较低。
变蓝
不变蓝
变蓝
思考·讨论
1.如何进一步探究淀粉酶的最适温度?
缩小温度梯度,重复进行上述实验。
2.为什么不能用斐林试剂对实验结果进行检测?
该实验的自变量是温度,用斐林试剂检测时需要水浴加热,
这样会干扰自变量。
3.为什么不能用过氧化氢酶和过氧化氢来探究温度对酶活性的影响?
因为过氧化氢本身受热易分解,会对实验结果造成干扰。
④实验设计思路(探究pH对酶活性的影响)
探究pH对酶活性影响的实验方案
步 骤 项目 试管1 试管2 试管3
1 注入新鲜的肝脏研磨液 2滴 2滴 2滴
2 注入不同pH的溶液 1 mL 蒸馏水 1 mL 盐酸 1 mL
NaOH
溶液
3 注入等量的H2O2溶液 2 mL 2 mL 2 mL
4 观察现象
有大量气泡
产生
无气泡产生
无气泡产生
实验结论:
过氧化氢酶的最适pH接近7.0,过酸或过碱,
都会使其催化活性下降。
1.该实验中,能否将步骤2、3调换 为什么
2.该实验不宜选用淀粉酶催化淀粉的水解做实验,为什么
因为淀粉酶催化的底物——淀粉在酸性条件下也会发生水解反应,无法排除无关变量的干扰。
不能。若调换2、3步骤,在调节pH之前,试管中已经发生了反应,从而影响实验结果。
思考:
⑥曲线
在一定条件下,酶活性最大时的温度称为该酶的最适温度。
在一定温度范围内,酶促反应速率随温度的升高而加快;但当温度升高到一定限度后,酶促反应速率随着温度的升高而下降。
曲线解读
⑥曲线
最适pH
最适pH
曲线解读:
在一定条件下,酶活性最大时的pH称为该酶的最适pH。
pH偏高或偏低,酶促反应速率都会下降。
三、影响酶促反应速率的因素
1.酶促反应:
由酶催化的化学反应,生物体内的化学反应绝大多数属于酶促反应。
2.酶促反应速率:
单位时间内反应物或生成物浓度的改变量。
3.影响酶促反应速率的因素:
pH
温度
抑制剂
激活剂
活性
浓度
底物浓度
酶
酶促反应速率
甲
乙
丙
丁
①图甲中,温度从a降低或升高,酶促反速率均下降,但是下降的原因不同。
1.温度、pH、底物浓度、酶浓度
②图乙中,pH从b降低或升高,酶促反速率均下降,但是下降的原因相同。
③图丙中,底物浓度为c时,酶促反应速率达到最大,因为,酶数量有限。
课后习题
2.下图表示最适温度下反应物浓度对酶所催化的化学反应速率的影响。
(1)请解释在A、B、C三点时该化学反应的状况。
A 点:随着反应底物浓度的增加,反应速率加快。
B 点:反应速率在此时达到最高
C 点:反应速率不再随反应底物浓度的增加而升高,维持在相对稳定的水平。
2.下图表示最适温度下反应物浓度对酶所催化的化学反应速率的影响。
(2)如果从A点开始温度升高10℃,曲线会发生什么变化 为什么 请画出变化后的曲线。
如果 A 点时温度升高 10℃,曲线上升的幅度变小因为图中原曲线表示在最适温度下催化速率随底物浓度的变化。温度高于或低于最适温度,反应速率都会变慢。
2.下图表示最适温度下反应物浓度对酶所催化的化学反应速率的影响。
(3)如果在B点时向反应混合物中加入少量同样的酶,曲线会发生什么变化 为什么 请画出相应的曲线。
该曲线表明,B 点的反应底物的浓度足够大,是酶的数量限制了反应速率的提高,这时加入少量的酶,会使反应速率加快。
同课章节目录
- 第1章 走近细胞
- 第1节 细胞是生命活动的基本单位
- 第2节 细胞的多样性和统一性
- 第2章 组成细胞的分子
- 第1节 细胞中的元素和化合物
- 第2节 细胞中的无机物
- 第3节 细胞中的糖类和脂质
- 第4节 蛋白质是生命活动的主要承担者
- 第5节 核酸是遗传信息的携带者
- 第3章 细胞的基本结构
- 第1节 细胞膜的结构和功能
- 第2节 细胞器之间的分工合作
- 第3节 细胞核的结构和功能
- 第4章 细胞的物质输入和输出
- 第1节 被动运输
- 第2节 主动运输与胞吞、胞吐
- 第5章 细胞的能量供应和利用
- 第1节 降低化学反应活化能的酶
- 第2节 细胞的能量“货币”ATP
- 第3节 细胞呼吸的原理和应用
- 第4节 光合作用与能量转化
- 第6章 细胞的生命历程
- 第1节 细胞的增殖
- 第2节 细胞的分化
- 第3节 细胞的衰老和死亡
