江苏2025年1月普通高中学业水平合格性考试化学复习 课时练14 反应热 原电池(含解析)
文档属性
| 名称 | 江苏2025年1月普通高中学业水平合格性考试化学复习 课时练14 反应热 原电池(含解析) |

|
|
| 格式 | DOC | ||
| 文件大小 | 430.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-07 00:00:00 | ||
图片预览



文档简介
课时14 反应热 原电池
1. (2024·扬州合格考模拟)下列过程放出热量的是( )
A. 碘的升华 B. 水的分解
C. 冰的融化 D. CaO溶于水
2. (2023·南京学测合格考)6NO+4NH35N2+6H2O,该反应过程中物质的能量变化如图所示。下列关于该反应说法正确的是( )
A. 该反应为吸热反应
B. 反应时热能转化为化学能
C. 断裂N—H会吸收能量
D. NO常温时是红棕色气体
3. (2023·镇江学测合格考)下列图示变化为吸热反应的是( )
4. (2023·盐城学测合格考)下列图示变化为吸热反应的是( )
5. (2024·常州合格考模拟)已知:Mg+2HCl===MgCl2+H2↑,测得反应过程中溶液温度升高。下列关于该反应的说法不正确的是( )
A. 属于吸热反应
B. 属于氧化还原反应
C. 反应物的总能量高于生成物的总能量
D. 化学键的断裂与形成是化学反应中能量变化的主要原因
6. (2024·无锡合格考模拟)氢气在氯气中燃烧为放热反应。下列关于该反应的说法正确的是( )
A. 断开Cl—Cl键放出能量
B. 形成H—Cl键吸收能量
C. 燃烧都是放热反应
D. 反应物的总能量小于生成物的总能量
7. (2024·淮安合格考模拟二)先进的甲醇蒸气重整-变压吸附技术可得到高浓度CO2混合气、H2,化学反应原理是CH3OH+H2O===CO2+3H2,其能量变化如图所示。下列说法正确的是( )
A. CH3OH转变成H2的过程是一个吸收能量的过程
B. 反应物的总能量大于生成物的总能量
C. 形成H—H键吸收能量
D. 断开H—C键放出能量
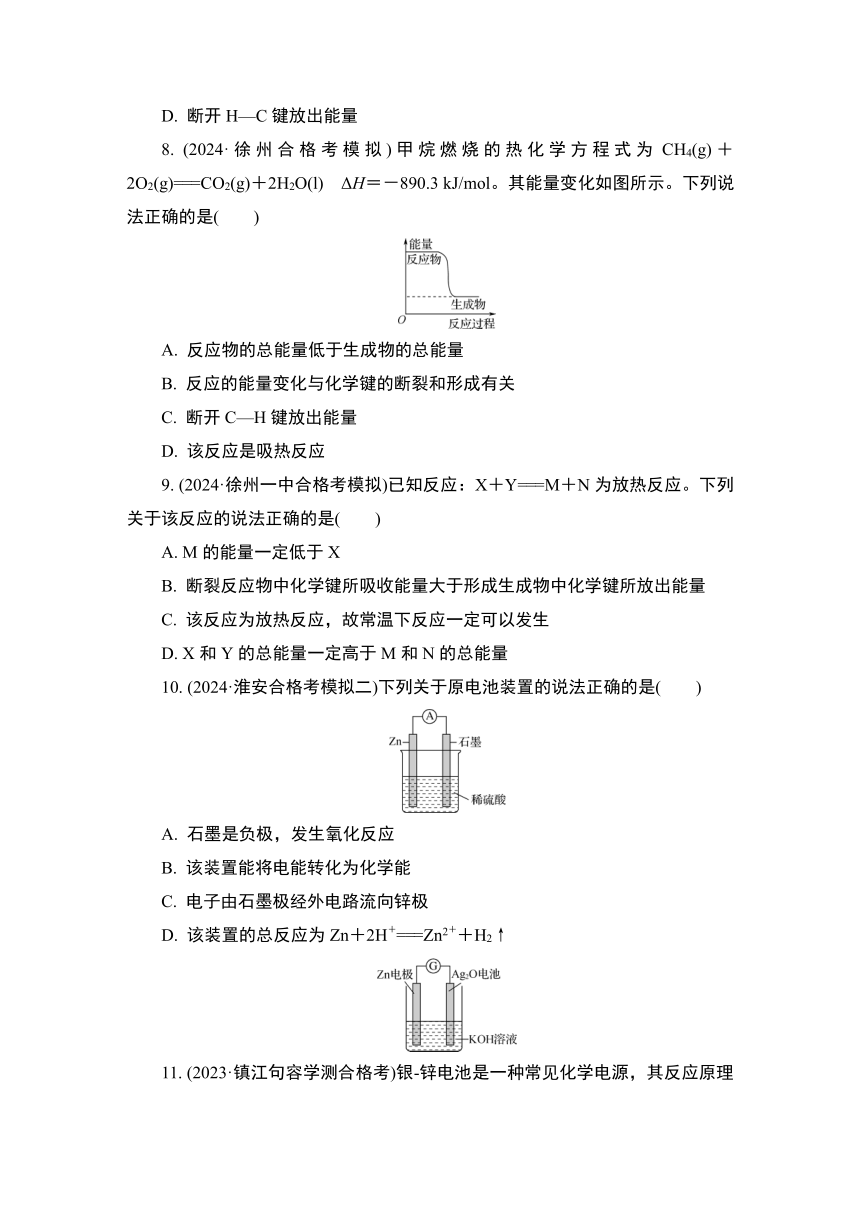
8. (2024·徐州合格考模拟)甲烷燃烧的热化学方程式为CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3 kJ/mol。其能量变化如图所示。下列说法正确的是( )
A. 反应物的总能量低于生成物的总能量
B. 反应的能量变化与化学键的断裂和形成有关
C. 断开C—H键放出能量
D. 该反应是吸热反应
9. (2024·徐州一中合格考模拟)已知反应:X+Y===M+N为放热反应。下列关于该反应的说法正确的是( )
A. M的能量一定低于X
B. 断裂反应物中化学键所吸收能量大于形成生成物中化学键所放出能量
C. 该反应为放热反应,故常温下反应一定可以发生
D. X和Y的总能量一定高于M和N的总能量
10. (2024·淮安合格考模拟二)下列关于原电池装置的说法正确的是( )
A. 石墨是负极,发生氧化反应
B. 该装置能将电能转化为化学能
C. 电子由石墨极经外电路流向锌极
D. 该装置的总反应为Zn+2H+===Zn2++H2↑
11. (2023·镇江句容学测合格考)银-锌电池是一种常见化学电源,其反应原理为Zn+Ag2O+H2O===Zn(OH)2+2Ag,其装置如图所示。下列说法不正确的是( )
A. 锌是负极
B. Zn电极的电极反应式:
Zn-2e-+2OH-===Zn(OH)2
C. Ag2O电极发生氧化反应
D. 电子从锌电极经外电路转移到Ag2O电极
12. (2024·徐州合格考模)NH3-O2燃料电池装置如图所示。下列说法错误的是( )
A. 该NH3-O2燃料电池是将化学能转化为电能的装置
B. 电极a是负极
C. NH3发生还原反应
D. 电极b上的电极反应式为O2+2H2O+4e-===4OH-
13. (2024·无锡合格考模拟)用锌片、铜片、西红柿等材料可以制作如图所示的西红柿电池。电池工作时,下列有关说法正确的是( )
A. Zn片作正极
B. Cu片质量减小
C. 电子由Zn片经导线流向Cu片
D. 实现了电能向化学能的转化
14. (2024·无锡合格考模拟)2019年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如图所示。下列说法不正确的是( )
A. 该装置实现了化学能转化为电能
B. 电极A为电池的正极
C. 电池工作时负极失去电子发生氧化反应
D. 电池工作时,电池内部的锂离子向电极B移动
15. (2024·常州合格考模拟)锌(Zn)-空气电池的总反应:2Zn+O2+2H2O===2Zn(OH)2,装置如图所示。下列说法不正确的是( )
A. 多孔石墨电极上发生还原反应
B. 电子从锌电极经过KOH溶液流向石墨电极
C. 负极的电极反应式:Zn-2e-+2OH-===Zn(OH)2
D. 电池工作时,电解质溶液中K+的数目保持不变
16. (2024·徐州一中合格考模拟)某原电池装置如图所示。下列说法正确的是( )
A. Fe作负极
B. 碳棒上有O2生成
C. 可将电能转化为化学能
D. 电子从碳棒经导线流向Fe
17. (2022·连云港学测合格考)如图所示的原电池的反应原理为2NH+Zn===Zn2++2NH3↑+H2↑。下列说法正确的是( )
A. 石墨为电池的负极
B. 电池工作时,Zn逐渐被消耗
C. 电子由石墨电极经外电路流向Zn电极
D. 反应2NH+2e-===2NH3↑+H2↑在负极上发生
18. (2023·南京六校联合学业调研)火星大气中含有大量CO2,一种有CO2参加反应的新型全固态电池有望为火星探测器供电。电池以金属钠为负极,碳纳米管为正极。放电时,下列说法正确的是( )
A. 负极上发生还原反应
B. CO2在正极上得电子
C. 工作时电子由碳纳米管经外电路流向金属钠
D. 将电能转化为化学能
课时14 反应热 原电池
1. D
2. C 【解析】由图可知,该反应的反应物的总能量高于生成物的总能量,是放热反应,A错误;反应时是化学能转化为热能,B错误;断裂化学键要吸收热量,C正确;NO是无色气体,NO2是红棕色气体,D错误。
3. A 【解析】图中反应物的总能量小于生成物的总能量,是吸热反应,A正确;反应物的总能量大于生成物的总能量,是放热反应,B错误;浓硫酸溶于水虽放出热量,但其是物理变化,不属于放热反应,C错误;稀盐酸与锌反应放出热量,是放热反应,D错误。
4. A 【解析】Ba(OH)2·8H2O晶体与NH4Cl 晶体反应为吸热反应,A正确;酸碱中和反应为放热反应,燃烧为放热反应,反应物总能量高于生成物的总能量为放热反应,B、C、D错误。
5. A 【解析】该反应属于放热反应,A错误;该反应中有元素化合价的变化,属于氧化还原反应,B正确;放热反应中反应物的总能量高于生成物的总能量,C正确;断裂化学键时吸收能量,形成化学键时放出能量,反应的能量变化由这两个过程能量变化决定,D正确。
6. C 【解析】断裂化学键吸收能量,形成化学键放出能量,A、B错误;放热反应中,反应物的总能量大于生成物的总能量,D错误。
7. B 【解析】由图示能量变化可知,反应物的总能量大于生成物的总能量,则CH3OH转变成H2的过程是放出热量的过程,A错误;反应物的总能量大于生成物的总能量,B正确;化学键的形成需要释放能量,形成H—H键放出能量,C错误;化学键的断裂需要吸收能量,D错误。
8. B 9. D
10. D 【解析】锌电极为负极,锌失去电子发生氧化反应,A错误;该装置是原电池,能将化学能转化为电能,B错误;原电池中电子由负极(锌极)经外电路流向正极(石墨极),C错误;负极Zn失去电子变为Zn2+进入溶液,负极的电极反应式为Zn-2e-===Zn2+;石墨为正极,正极上溶液中的H+得到电子发生还原反应,正极的电极反应式为2H++2e-===H2↑,总反应为Zn+2H+===Zn2++H2↑,D正确。
11. C 【解析】银-锌电池中,锌是负极,A正确;负极锌失电子生成氢氧化锌,其电极的电极反应式:Zn-2e-+2OH-===Zn(OH)2,B正确;Ag2O电极为正极,发生还原反应,C错误;原电池中电子由负极经过导线转移到正极,则电子从锌电极经外电路转移到Ag2O电极,D正确。
12. C 【解析】燃料电池是将化学能转化为电能的装置,通入燃料的一极为负极,则电极a为负极,电极b为正极,负极中NH3失去电子,发生氧化反应,电极b上的电极反应式为O2+2H2O+4e-===4OH-,C错误。
13. C
14. B 【解析】该装置为原电池装置,实现了化学能转化为电能,A正确;根据电子的流向,电极A为电池的负极,B错误;电池工作时,负极失去电子,发生氧化反应,C正确;根据图像,电池工作时,电池内部的锂离子向正极(电极B)移动,D正确。
15. B 【解析】由装置图可知,在多孔石墨电极上空气中的O2得到电子,发生还原反应,A正确;该装置为原电池,Zn为负极,多孔石墨电极为正极,电子由Zn经外电路流向正极石墨,而不能进入电解质溶液中,B错误;该装置为原电池,Zn为负极,Zn失去电子变为Zn2+,然后结合溶液中的OH-变为Zn(OH)2,故负极的电极反应式为Zn-2e-+2OH-===Zn(OH)2,C正确;在反应过程中,K+没有参与反应,因此电池工作时,电解质溶液中K+的数目保持不变,D正确。
16. A
17. B 【解析】由原电池反应原理可知,Zn失去电子作负极,被消耗,A错误、B正确;电子由负极(Zn极)流出,C错误;2NH+2e-===2NH3↑+H2↑在正极上发生,D错误。
18. B 【解析】该电池以金属钠为负极,碳纳米管为正极。放电时,负极失电子,发生了氧化反应,A错误;CO2在正极上得电子,B正确;放电时,电子由负极金属钠经外电路流向碳纳米管,C错误;该电池放电时,将化学能转化为电能,D错误。
1. (2024·扬州合格考模拟)下列过程放出热量的是( )
A. 碘的升华 B. 水的分解
C. 冰的融化 D. CaO溶于水
2. (2023·南京学测合格考)6NO+4NH35N2+6H2O,该反应过程中物质的能量变化如图所示。下列关于该反应说法正确的是( )
A. 该反应为吸热反应
B. 反应时热能转化为化学能
C. 断裂N—H会吸收能量
D. NO常温时是红棕色气体
3. (2023·镇江学测合格考)下列图示变化为吸热反应的是( )
4. (2023·盐城学测合格考)下列图示变化为吸热反应的是( )
5. (2024·常州合格考模拟)已知:Mg+2HCl===MgCl2+H2↑,测得反应过程中溶液温度升高。下列关于该反应的说法不正确的是( )
A. 属于吸热反应
B. 属于氧化还原反应
C. 反应物的总能量高于生成物的总能量
D. 化学键的断裂与形成是化学反应中能量变化的主要原因
6. (2024·无锡合格考模拟)氢气在氯气中燃烧为放热反应。下列关于该反应的说法正确的是( )
A. 断开Cl—Cl键放出能量
B. 形成H—Cl键吸收能量
C. 燃烧都是放热反应
D. 反应物的总能量小于生成物的总能量
7. (2024·淮安合格考模拟二)先进的甲醇蒸气重整-变压吸附技术可得到高浓度CO2混合气、H2,化学反应原理是CH3OH+H2O===CO2+3H2,其能量变化如图所示。下列说法正确的是( )
A. CH3OH转变成H2的过程是一个吸收能量的过程
B. 反应物的总能量大于生成物的总能量
C. 形成H—H键吸收能量
D. 断开H—C键放出能量
8. (2024·徐州合格考模拟)甲烷燃烧的热化学方程式为CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3 kJ/mol。其能量变化如图所示。下列说法正确的是( )
A. 反应物的总能量低于生成物的总能量
B. 反应的能量变化与化学键的断裂和形成有关
C. 断开C—H键放出能量
D. 该反应是吸热反应
9. (2024·徐州一中合格考模拟)已知反应:X+Y===M+N为放热反应。下列关于该反应的说法正确的是( )
A. M的能量一定低于X
B. 断裂反应物中化学键所吸收能量大于形成生成物中化学键所放出能量
C. 该反应为放热反应,故常温下反应一定可以发生
D. X和Y的总能量一定高于M和N的总能量
10. (2024·淮安合格考模拟二)下列关于原电池装置的说法正确的是( )
A. 石墨是负极,发生氧化反应
B. 该装置能将电能转化为化学能
C. 电子由石墨极经外电路流向锌极
D. 该装置的总反应为Zn+2H+===Zn2++H2↑
11. (2023·镇江句容学测合格考)银-锌电池是一种常见化学电源,其反应原理为Zn+Ag2O+H2O===Zn(OH)2+2Ag,其装置如图所示。下列说法不正确的是( )
A. 锌是负极
B. Zn电极的电极反应式:
Zn-2e-+2OH-===Zn(OH)2
C. Ag2O电极发生氧化反应
D. 电子从锌电极经外电路转移到Ag2O电极
12. (2024·徐州合格考模)NH3-O2燃料电池装置如图所示。下列说法错误的是( )
A. 该NH3-O2燃料电池是将化学能转化为电能的装置
B. 电极a是负极
C. NH3发生还原反应
D. 电极b上的电极反应式为O2+2H2O+4e-===4OH-
13. (2024·无锡合格考模拟)用锌片、铜片、西红柿等材料可以制作如图所示的西红柿电池。电池工作时,下列有关说法正确的是( )
A. Zn片作正极
B. Cu片质量减小
C. 电子由Zn片经导线流向Cu片
D. 实现了电能向化学能的转化
14. (2024·无锡合格考模拟)2019年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如图所示。下列说法不正确的是( )
A. 该装置实现了化学能转化为电能
B. 电极A为电池的正极
C. 电池工作时负极失去电子发生氧化反应
D. 电池工作时,电池内部的锂离子向电极B移动
15. (2024·常州合格考模拟)锌(Zn)-空气电池的总反应:2Zn+O2+2H2O===2Zn(OH)2,装置如图所示。下列说法不正确的是( )
A. 多孔石墨电极上发生还原反应
B. 电子从锌电极经过KOH溶液流向石墨电极
C. 负极的电极反应式:Zn-2e-+2OH-===Zn(OH)2
D. 电池工作时,电解质溶液中K+的数目保持不变
16. (2024·徐州一中合格考模拟)某原电池装置如图所示。下列说法正确的是( )
A. Fe作负极
B. 碳棒上有O2生成
C. 可将电能转化为化学能
D. 电子从碳棒经导线流向Fe
17. (2022·连云港学测合格考)如图所示的原电池的反应原理为2NH+Zn===Zn2++2NH3↑+H2↑。下列说法正确的是( )
A. 石墨为电池的负极
B. 电池工作时,Zn逐渐被消耗
C. 电子由石墨电极经外电路流向Zn电极
D. 反应2NH+2e-===2NH3↑+H2↑在负极上发生
18. (2023·南京六校联合学业调研)火星大气中含有大量CO2,一种有CO2参加反应的新型全固态电池有望为火星探测器供电。电池以金属钠为负极,碳纳米管为正极。放电时,下列说法正确的是( )
A. 负极上发生还原反应
B. CO2在正极上得电子
C. 工作时电子由碳纳米管经外电路流向金属钠
D. 将电能转化为化学能
课时14 反应热 原电池
1. D
2. C 【解析】由图可知,该反应的反应物的总能量高于生成物的总能量,是放热反应,A错误;反应时是化学能转化为热能,B错误;断裂化学键要吸收热量,C正确;NO是无色气体,NO2是红棕色气体,D错误。
3. A 【解析】图中反应物的总能量小于生成物的总能量,是吸热反应,A正确;反应物的总能量大于生成物的总能量,是放热反应,B错误;浓硫酸溶于水虽放出热量,但其是物理变化,不属于放热反应,C错误;稀盐酸与锌反应放出热量,是放热反应,D错误。
4. A 【解析】Ba(OH)2·8H2O晶体与NH4Cl 晶体反应为吸热反应,A正确;酸碱中和反应为放热反应,燃烧为放热反应,反应物总能量高于生成物的总能量为放热反应,B、C、D错误。
5. A 【解析】该反应属于放热反应,A错误;该反应中有元素化合价的变化,属于氧化还原反应,B正确;放热反应中反应物的总能量高于生成物的总能量,C正确;断裂化学键时吸收能量,形成化学键时放出能量,反应的能量变化由这两个过程能量变化决定,D正确。
6. C 【解析】断裂化学键吸收能量,形成化学键放出能量,A、B错误;放热反应中,反应物的总能量大于生成物的总能量,D错误。
7. B 【解析】由图示能量变化可知,反应物的总能量大于生成物的总能量,则CH3OH转变成H2的过程是放出热量的过程,A错误;反应物的总能量大于生成物的总能量,B正确;化学键的形成需要释放能量,形成H—H键放出能量,C错误;化学键的断裂需要吸收能量,D错误。
8. B 9. D
10. D 【解析】锌电极为负极,锌失去电子发生氧化反应,A错误;该装置是原电池,能将化学能转化为电能,B错误;原电池中电子由负极(锌极)经外电路流向正极(石墨极),C错误;负极Zn失去电子变为Zn2+进入溶液,负极的电极反应式为Zn-2e-===Zn2+;石墨为正极,正极上溶液中的H+得到电子发生还原反应,正极的电极反应式为2H++2e-===H2↑,总反应为Zn+2H+===Zn2++H2↑,D正确。
11. C 【解析】银-锌电池中,锌是负极,A正确;负极锌失电子生成氢氧化锌,其电极的电极反应式:Zn-2e-+2OH-===Zn(OH)2,B正确;Ag2O电极为正极,发生还原反应,C错误;原电池中电子由负极经过导线转移到正极,则电子从锌电极经外电路转移到Ag2O电极,D正确。
12. C 【解析】燃料电池是将化学能转化为电能的装置,通入燃料的一极为负极,则电极a为负极,电极b为正极,负极中NH3失去电子,发生氧化反应,电极b上的电极反应式为O2+2H2O+4e-===4OH-,C错误。
13. C
14. B 【解析】该装置为原电池装置,实现了化学能转化为电能,A正确;根据电子的流向,电极A为电池的负极,B错误;电池工作时,负极失去电子,发生氧化反应,C正确;根据图像,电池工作时,电池内部的锂离子向正极(电极B)移动,D正确。
15. B 【解析】由装置图可知,在多孔石墨电极上空气中的O2得到电子,发生还原反应,A正确;该装置为原电池,Zn为负极,多孔石墨电极为正极,电子由Zn经外电路流向正极石墨,而不能进入电解质溶液中,B错误;该装置为原电池,Zn为负极,Zn失去电子变为Zn2+,然后结合溶液中的OH-变为Zn(OH)2,故负极的电极反应式为Zn-2e-+2OH-===Zn(OH)2,C正确;在反应过程中,K+没有参与反应,因此电池工作时,电解质溶液中K+的数目保持不变,D正确。
16. A
17. B 【解析】由原电池反应原理可知,Zn失去电子作负极,被消耗,A错误、B正确;电子由负极(Zn极)流出,C错误;2NH+2e-===2NH3↑+H2↑在正极上发生,D错误。
18. B 【解析】该电池以金属钠为负极,碳纳米管为正极。放电时,负极失电子,发生了氧化反应,A错误;CO2在正极上得电子,B正确;放电时,电子由负极金属钠经外电路流向碳纳米管,C错误;该电池放电时,将化学能转化为电能,D错误。
同课章节目录
