7.3.2 配制一定溶质质量分数的溶液 课件 (共21张PPT内嵌视频)2024-2025学年化学科粤版九年级下册
文档属性
| 名称 | 7.3.2 配制一定溶质质量分数的溶液 课件 (共21张PPT内嵌视频)2024-2025学年化学科粤版九年级下册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 41.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-09 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
1.能配制一定溶质质量分数的溶液。
2.通过练习一定质量分数溶液的配制,使学生掌握溶液配制的基本步骤。
①溶液的质量 = 溶质的质量 + 溶剂的质量
②溶液的质量 = 溶液的密度×溶液的体积
③溶质的质量分数 =
溶质质量
溶液质量
×100%
溶质质量
溶质质量+溶剂质量
=
×100%
溶解度+100 g
溶解度
④饱和溶液的质量分数 =
×100%
复习回顾
氯化钠注射液
[规格] 溶液质量分数为0.9%
[注意] 使用前发现溶液中有絮状物、
瓶身细微裂缝等均不可使用
[贮存] 密封保存
医用生理盐水的标签。
此信息中的0.9%表明的含义有哪些?
思考 如何配制一定溶质质量分数的溶液?
学生实验探究>>>
设计实验方案
【实验7-5】配制溶质质量分数为 3% 的硝酸钾营养液。
实验用品:硝酸钾固体、托盘天平、药匙、烧杯(100mL、 250mL、 500mL )、量筒( 50mL、 100mL、 250mL )、玻璃棒、试剂瓶、标签。
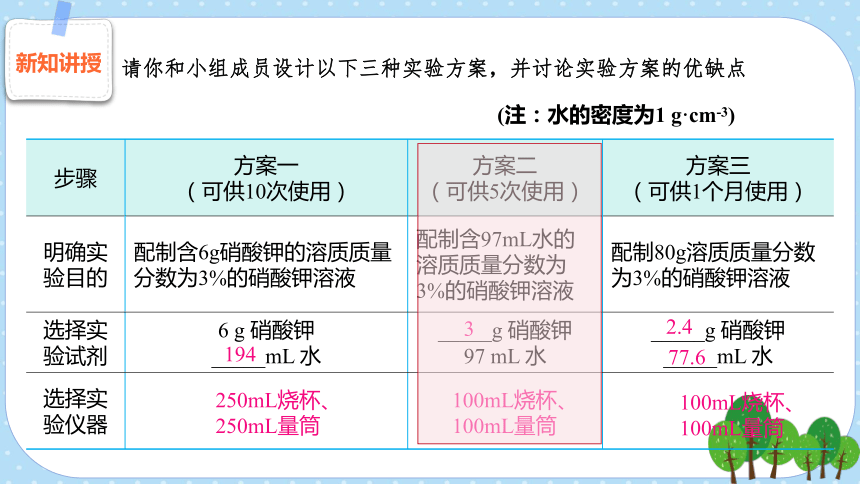
请你和小组成员设计以下三种实验方案,并讨论实验方案的优缺点
(注:水的密度为1 g·cm-3)
步骤 方案一 (可供10次使用) 方案二 (可供5次使用) 方案三
(可供1个月使用)
明确实验目的 配制含6g硝酸钾的溶质质量分数为3%的硝酸钾溶液 配制含97mL水的溶质质量分数为3%的硝酸钾溶液 配制80g溶质质量分数为3%的硝酸钾溶液
选择实验试剂 6 g 硝酸钾 _____mL 水 _____g 硝酸钾 97 mL 水 _____g 硝酸钾
_____mL 水
选择实验仪器
194
3
2.4
77.6
250mL烧杯、
250mL量筒
100mL烧杯、
100mL量筒
100mL烧杯、
100mL量筒
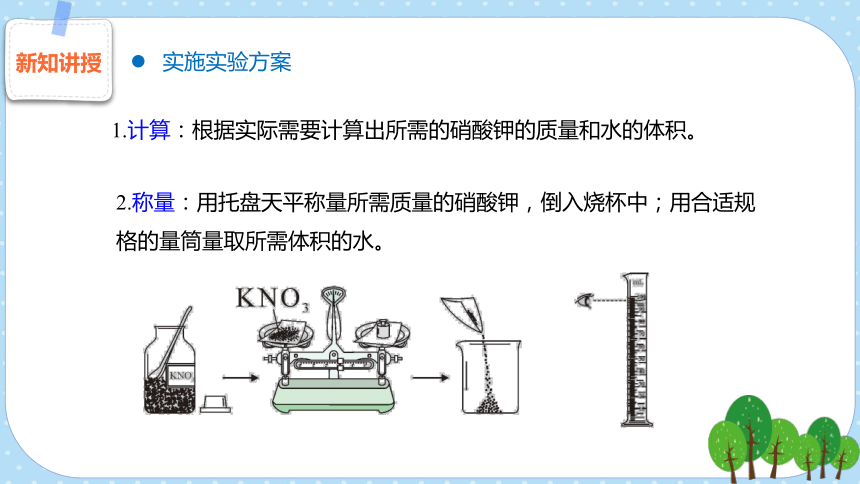
实施实验方案
1.计算:根据实际需要计算出所需的硝酸钾的质量和水的体积。
2.称量:用托盘天平称量所需质量的硝酸钾,倒入烧杯中;用合适规格的量筒量取所需体积的水。
固体称量操作要点:
①“左物右码”;
②两托盘上放上质量相等的称量纸,调节天平平衡,准备进行称量。
③先将砝码以及游码调整到所需硝酸钾的质量的刻度,然后逐渐添加硝酸钾直到天平平衡;
④称量完毕,砝码和游码还归原位。
注意:溶质若为易潮解或有腐蚀性的试剂,称量时不能再天平的托盘上垫纸片,应将溶质装在玻璃器皿(如小烧杯)中。
液体量取操作要点:
视线要与液体凹液面的最低处保持水平。
3.溶解:将量筒里的水注入盛有硝酸钾的烧杯中,并用玻璃棒搅拌使硝酸钾充分溶解。
倾倒操作要点:将量筒中的水沿烧杯壁倒入烧杯中,切勿洒出。
搅拌操作要点:搅拌时玻璃棒不要碰烧杯内壁。
4.装瓶:把上述硝酸钾溶液装入贴有试剂名称和溶质质量分数标签的试剂瓶中,盖好瓶塞,放到指定的液体试剂柜中。
请填写该瓶溶液的标签
名称:KNO3溶液
质量分数:3%
配制溶质质量分数为10%、20%的氯化钠溶液
所得溶液的溶质质量分数误差分析
操作 溶质 溶剂 对溶质质量
分数的影响
试剂不纯
仰视读数(量筒)
俯视读数(量筒)
烧杯内壁有水
溶解时溶质洒出
减少
偏小
增大
偏小
减少
偏大
增大
偏小
减少
偏小
操作 溶质 溶剂 对溶质质量
分数的影响
试剂瓶用 水润洗过
砝码生锈
砝码放反
往烧杯中倒 水时有水溅出
增大
偏小
增大
偏大
减少
偏小
减少
偏大
1. 配制一定溶质质量分数的溶液,正确的操作步骤( )
A.称量(量取)、计算、溶解
B.计算、称量(量取)、溶解
C.计算、溶解、称量(量取)
D.溶解、计算、称量(量取)
B
2.要配制100g溶质质量分数为10%的氯化钠溶液,下列操作正确的是( )
A.将10g氯化钠固体直接放在天平的托盘上称量
B.量取90mL水时,俯视读数
C.为加快固体溶解,用温度计搅拌溶液
D.将配好的溶液倒入细口瓶中,盖紧瓶塞,并贴上标签
D
3. 在配制一定质量分数的氯化钠溶液时,下列出现的操作失误,会引起所配溶液的溶质质量分数降低的是 ( )
A.用托盘天平称量氯化钠时,将砝码放在左盘,但未使用游码;
B.用量筒量取蒸馏水读数时,仰视凹液面的最低处;
C.将量筒中的水倒入烧杯时,有水洒出;
D.将配好的氯化钠溶液转移到细口瓶时,不慎撒出部分溶液。
B
4. 某同学配制60 g溶质质量分数为5%的NaCl溶液,准备了下列实验用品。回答下列问题:
(1)该同学按下列实验步骤进行:①计算,②称量,③量取,④______(填步骤名称)。
(2)配制过程还缺少的一种玻璃仪器是_______(填名称)。
(3)计算所需NaCl的质量为_____g,称量时,NaCl应放在托盘天平的_____(填“左盘”、“右盘”)上。
溶解
玻璃棒
3
左盘
(4)量取蒸馏水操作如下:将蒸馏水注入量筒,待液面接近量取体积对应刻度线时,改用_________(填仪器名称)滴加蒸馏水至刻度线。
(5)若量取水的体积时俯视读数,所配制溶液的溶质质量分数会_____(填“偏大”、“偏小”或“无影响”)。
胶头滴管
偏大
配制一定溶质质量分数的溶液:
步骤
1. 计算
根据实际需要计算出所需试剂及水的量
固体试剂用托盘天平称量好后倒入烧杯中;液体试剂用合适规格的量筒量取。
将量筒里的液体注入盛有试剂的烧杯中,并用玻璃棒搅拌使试剂充分溶解。
把溶液装入试剂瓶中,盖好瓶塞,放到指定的液体试剂柜中。
2. 称量
3. 溶解
4. 装瓶
1.能配制一定溶质质量分数的溶液。
2.通过练习一定质量分数溶液的配制,使学生掌握溶液配制的基本步骤。
①溶液的质量 = 溶质的质量 + 溶剂的质量
②溶液的质量 = 溶液的密度×溶液的体积
③溶质的质量分数 =
溶质质量
溶液质量
×100%
溶质质量
溶质质量+溶剂质量
=
×100%
溶解度+100 g
溶解度
④饱和溶液的质量分数 =
×100%
复习回顾
氯化钠注射液
[规格] 溶液质量分数为0.9%
[注意] 使用前发现溶液中有絮状物、
瓶身细微裂缝等均不可使用
[贮存] 密封保存
医用生理盐水的标签。
此信息中的0.9%表明的含义有哪些?
思考 如何配制一定溶质质量分数的溶液?
学生实验探究>>>
设计实验方案
【实验7-5】配制溶质质量分数为 3% 的硝酸钾营养液。
实验用品:硝酸钾固体、托盘天平、药匙、烧杯(100mL、 250mL、 500mL )、量筒( 50mL、 100mL、 250mL )、玻璃棒、试剂瓶、标签。
请你和小组成员设计以下三种实验方案,并讨论实验方案的优缺点
(注:水的密度为1 g·cm-3)
步骤 方案一 (可供10次使用) 方案二 (可供5次使用) 方案三
(可供1个月使用)
明确实验目的 配制含6g硝酸钾的溶质质量分数为3%的硝酸钾溶液 配制含97mL水的溶质质量分数为3%的硝酸钾溶液 配制80g溶质质量分数为3%的硝酸钾溶液
选择实验试剂 6 g 硝酸钾 _____mL 水 _____g 硝酸钾 97 mL 水 _____g 硝酸钾
_____mL 水
选择实验仪器
194
3
2.4
77.6
250mL烧杯、
250mL量筒
100mL烧杯、
100mL量筒
100mL烧杯、
100mL量筒
实施实验方案
1.计算:根据实际需要计算出所需的硝酸钾的质量和水的体积。
2.称量:用托盘天平称量所需质量的硝酸钾,倒入烧杯中;用合适规格的量筒量取所需体积的水。
固体称量操作要点:
①“左物右码”;
②两托盘上放上质量相等的称量纸,调节天平平衡,准备进行称量。
③先将砝码以及游码调整到所需硝酸钾的质量的刻度,然后逐渐添加硝酸钾直到天平平衡;
④称量完毕,砝码和游码还归原位。
注意:溶质若为易潮解或有腐蚀性的试剂,称量时不能再天平的托盘上垫纸片,应将溶质装在玻璃器皿(如小烧杯)中。
液体量取操作要点:
视线要与液体凹液面的最低处保持水平。
3.溶解:将量筒里的水注入盛有硝酸钾的烧杯中,并用玻璃棒搅拌使硝酸钾充分溶解。
倾倒操作要点:将量筒中的水沿烧杯壁倒入烧杯中,切勿洒出。
搅拌操作要点:搅拌时玻璃棒不要碰烧杯内壁。
4.装瓶:把上述硝酸钾溶液装入贴有试剂名称和溶质质量分数标签的试剂瓶中,盖好瓶塞,放到指定的液体试剂柜中。
请填写该瓶溶液的标签
名称:KNO3溶液
质量分数:3%
配制溶质质量分数为10%、20%的氯化钠溶液
所得溶液的溶质质量分数误差分析
操作 溶质 溶剂 对溶质质量
分数的影响
试剂不纯
仰视读数(量筒)
俯视读数(量筒)
烧杯内壁有水
溶解时溶质洒出
减少
偏小
增大
偏小
减少
偏大
增大
偏小
减少
偏小
操作 溶质 溶剂 对溶质质量
分数的影响
试剂瓶用 水润洗过
砝码生锈
砝码放反
往烧杯中倒 水时有水溅出
增大
偏小
增大
偏大
减少
偏小
减少
偏大
1. 配制一定溶质质量分数的溶液,正确的操作步骤( )
A.称量(量取)、计算、溶解
B.计算、称量(量取)、溶解
C.计算、溶解、称量(量取)
D.溶解、计算、称量(量取)
B
2.要配制100g溶质质量分数为10%的氯化钠溶液,下列操作正确的是( )
A.将10g氯化钠固体直接放在天平的托盘上称量
B.量取90mL水时,俯视读数
C.为加快固体溶解,用温度计搅拌溶液
D.将配好的溶液倒入细口瓶中,盖紧瓶塞,并贴上标签
D
3. 在配制一定质量分数的氯化钠溶液时,下列出现的操作失误,会引起所配溶液的溶质质量分数降低的是 ( )
A.用托盘天平称量氯化钠时,将砝码放在左盘,但未使用游码;
B.用量筒量取蒸馏水读数时,仰视凹液面的最低处;
C.将量筒中的水倒入烧杯时,有水洒出;
D.将配好的氯化钠溶液转移到细口瓶时,不慎撒出部分溶液。
B
4. 某同学配制60 g溶质质量分数为5%的NaCl溶液,准备了下列实验用品。回答下列问题:
(1)该同学按下列实验步骤进行:①计算,②称量,③量取,④______(填步骤名称)。
(2)配制过程还缺少的一种玻璃仪器是_______(填名称)。
(3)计算所需NaCl的质量为_____g,称量时,NaCl应放在托盘天平的_____(填“左盘”、“右盘”)上。
溶解
玻璃棒
3
左盘
(4)量取蒸馏水操作如下:将蒸馏水注入量筒,待液面接近量取体积对应刻度线时,改用_________(填仪器名称)滴加蒸馏水至刻度线。
(5)若量取水的体积时俯视读数,所配制溶液的溶质质量分数会_____(填“偏大”、“偏小”或“无影响”)。
胶头滴管
偏大
配制一定溶质质量分数的溶液:
步骤
1. 计算
根据实际需要计算出所需试剂及水的量
固体试剂用托盘天平称量好后倒入烧杯中;液体试剂用合适规格的量筒量取。
将量筒里的液体注入盛有试剂的烧杯中,并用玻璃棒搅拌使试剂充分溶解。
把溶液装入试剂瓶中,盖好瓶塞,放到指定的液体试剂柜中。
2. 称量
3. 溶解
4. 装瓶
