第2讲 课时2 常见的碱 课件(共43张PPT) 2025年中考化学一轮考点研究(人教版)
文档属性
| 名称 | 第2讲 课时2 常见的碱 课件(共43张PPT) 2025年中考化学一轮考点研究(人教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 30.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-09 00:00:00 | ||
图片预览







文档简介
(共43张PPT)
第2讲 常见的酸碱盐
2025广东化学
课时2 常见的碱
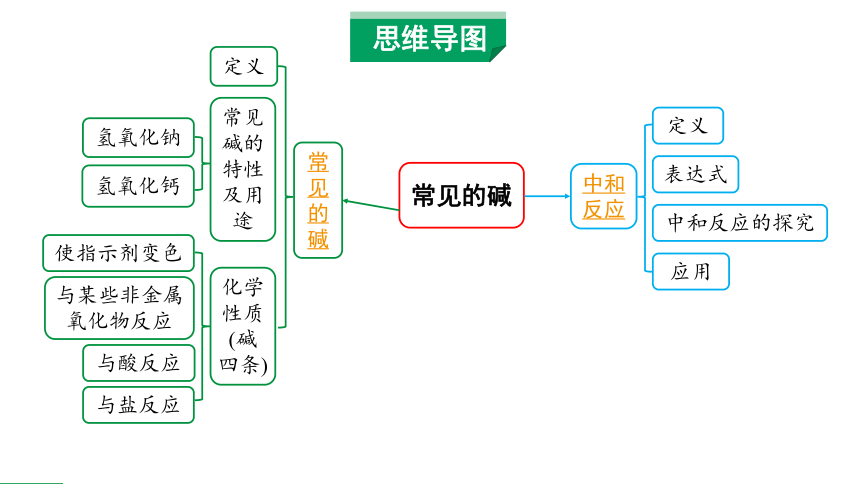
常见的碱
常见的碱
中和反应
定义
应用
表达式
中和反应的探究
定义
常见碱的特性及用途
氢氧化钠
氢氧化钙
化学性质(碱四条)
使指示剂变色
与某些非金属氧化物反应
与酸反应
与盐反应
思维导图
考点梳理
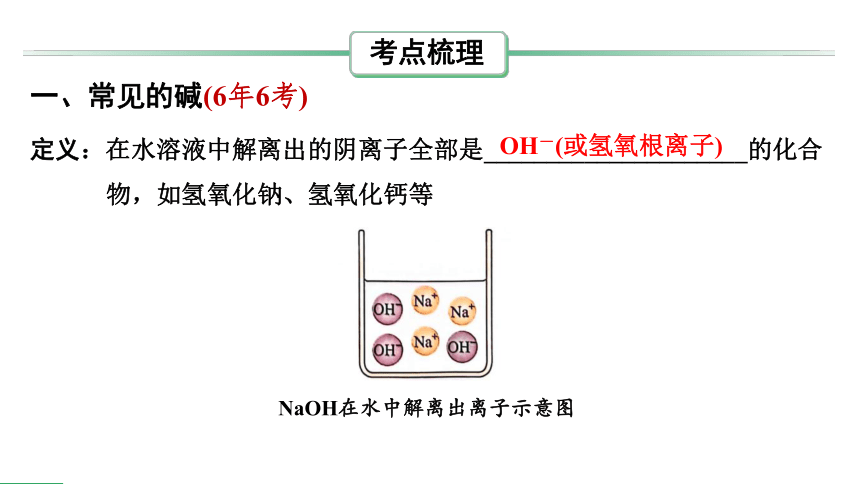
定义:在水溶液中解离出的阴离子全部是_____________________的化合
物,如氢氧化钠、氢氧化钙等
一、常见的碱(6年6考)
OH-(或氢氧根离子)
NaOH在水中解离出离子示意图
常见碱的特性及用途
物质 氢氧化钠(NaOH) 氢氧化钙[Ca(OH)2]
俗名 ________、火碱、苛性钠 ________、消石灰
物理 性质 白色固体,易溶于水,溶解时________(填“吸收”或“放出”)热量 白色粉末状物质,微溶于水,溶解度随温度的升高而________
一、常见的碱(6年6考)
烧碱
熟石灰
放出
减小
常见碱的特性及用途
物质 氢氧化钠(NaOH) 氢氧化钙[Ca(OH)2]
特性 在空气中易潮解、有强烈的腐蚀性 有腐蚀性
用途 实验室可用作某些气体(中性或碱性)的干燥剂;炉具清洁剂的成分之一,可用于除油污 作建筑材料;改良酸性土壤;配制农药波尔多液;保护树木,防止冻伤等
一、常见的碱(6年6考)
熟石灰改良酸性土壤
一、常见的碱(6年6考)
氢氧化钠变质的探究(详见微专题4)
化学性质
(碱四条)
使指示剂变色:能使紫色石蕊溶液变_____,使无色酚酞溶液变____
与某些非金属
氧化物反应
通式:碱+非金属氧化物→盐+水
举例
2NaOH+CO2=== ________________(实验室吸收二
氧化碳)
Ca(OH)2+CO2=== ________________(实验室检验二
氧化碳),现象为澄清石灰水变浑浊
蓝
红
Na2CO3+H2O
CaCO3↓+H2O
一、常见的碱(6年6考)
与酸反应
化学性质
(碱四条)
通式:碱+酸→盐+水
举例:氢氧化钠与稀盐酸:
___________________________
与盐反应
通式:可溶性碱+可溶性盐→新碱+新盐
举例:2NaOH+MgCl2=== __________________,现象
__________________
总结
不同碱具有通性的原因:_________________________________
不同碱具有个性的原因:___________________
NaOH+HCl === NaCl+H2O
Mg(OH)2↓+2NaCl
有白色沉淀产生
在水溶液中解离出的阴离子都是OH-
所含阳离子不同
氢氧化镁沉淀
农业:调节土壤的酸碱性,如用________改良酸性土壤
工业:处理工厂废水,如用熟石灰处理酸性废水
医药:用于医药,如胃酸过多时可服用含有碱性物质的药物
生活:蜂或蚂蚁叮咬后涂抹含有碱性物质的溶液,可减轻肿、痛
或瘙痒等症状
二、中和反应(6年4考)
定义:_____与_____作用生成_____和_____的反应
表达式:酸+碱→盐+水
中和反应的探究(详见微专题3)
应用
酸
碱
盐
水
熟石灰
中和胃酸——氢氧化铝
易错点判断
判断下列说法的正误,正确的打“√”,错误的打“×”。
1. 碱中一定含有氢元素、氧元素和金属元素。( )
2. 氢氧化钠固体可用于干燥氯化氢和二氧化碳气体。( )
3. 熟石灰可用于改良酸性土壤,则氢氧化钠也可用于改良酸性土壤。( )
4. 能与碱反应生成盐和水的物质一定是酸。( )
×
×
×
×
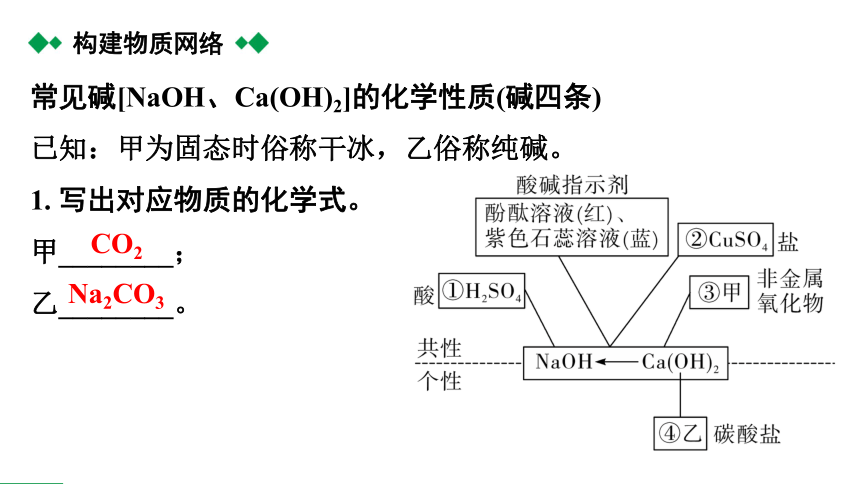
常见碱[NaOH、Ca(OH)2]的化学性质(碱四条)
已知:甲为固态时俗称干冰,乙俗称纯碱。
1. 写出对应物质的化学式。
甲________;
乙________。
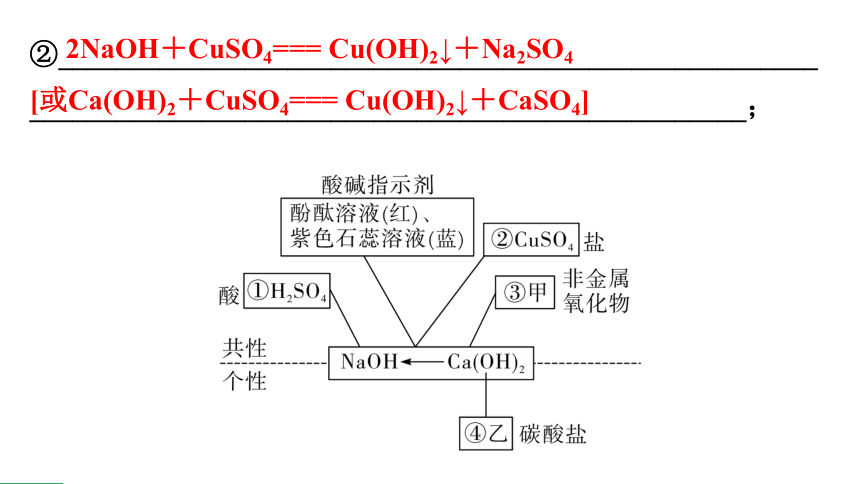
构建物质网络
CO2
Na2CO3
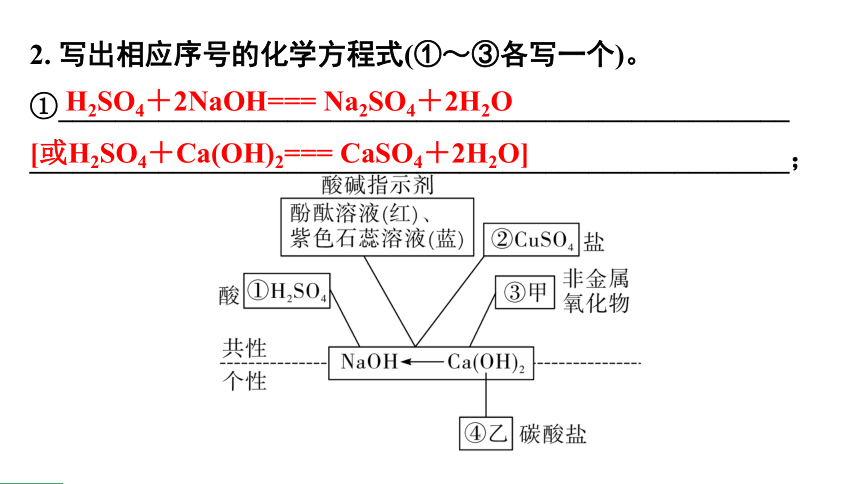
2. 写出相应序号的化学方程式(①~③各写一个)。
①___________________________________________________
_____________________________________________________;
H2SO4+2NaOH=== Na2SO4+2H2O
[或H2SO4+Ca(OH)2=== CaSO4+2H2O]
②_______________________________________________________________________________________________________;
2NaOH+CuSO4=== Cu(OH)2↓+Na2SO4
[或Ca(OH)2+CuSO4=== Cu(OH)2↓+CaSO4]
③_____________________________________________________;
______________________________________________________④_____________________________________________________。
CO2+Ca(OH)2=== CaCO3↓+H2O
(或CO2+2NaOH=== Na2CO3+H2O)
Ca(OH)2+Na2CO3=== CaCO3↓+2NaOH
甲________;
乙________。
CO2
Na2CO3
广东真题练基础
1. (省卷真题组合)判断下列说法的正误:
(1)用炉具清洁剂去除油污,NaOH可与油脂反应。(2022.14B)
( )
(2)KOH在水中解离出K+和OH-。(2020.11A)( )
命题点
1
常见碱的特性及用途(6年4考)
√
√
2. (2023省卷9题3分)下列与制作叶脉书签项目有关的说法错误的是( )
A. NaOH溶液可以腐蚀叶肉
B. 制作过程涉及化学变化
C. 制作完成后废液需回收处理
D. NaOH固体存放处应张贴如图所示标志
D
3. (2023深圳改编)有关NaOH说法错误的是( )
A. NaOH固体溶解时放出热量
B. NaOH固体吸水易潮解
C. NaOH是所有气体的干燥剂
D. NaOH应密封保存
C
4. [2021省卷18(4)题第1空2分](4)某同学在学习氮肥时,查阅资料:①氨气极易溶于水,其水溶液称为氨水;②氨水在浓度大或受热时易分解放出氨气。
实验室用生石灰和浓氨水能快速制取氨气的原因是___________
__________________________________________________。
生石灰和水反应消耗水,并且放出热量,可加快浓氨水分解
5. [人教素材改编]每年冬季,园林工人总会在景观树树干下部涂上“白浆”,同学们通过询问得知该“白浆”是含有硫黄粉等的石灰浆,石灰浆的主要成分是熟石灰,请回答下列问题。
(1)生石灰可用于制取熟石灰,该反应属于______(填“吸热”或“放热”)反应。
(2)树干上涂抹含有硫黄粉等的石灰浆的主要目的是___________
_________________________。
放热
保护树木,防止冻伤,并防止害虫产卵
(3)用石灰浆粉刷树干,干燥后石灰浆变硬,其原因是_______________________________(用化学方程式解释)。
(4)熟石灰在农业生产上的另一种用途是______________________。
Ca(OH)2+CO2 === CaCO3↓+H2O
改良酸性土壤(合理即可)
6. [人教探究改编]若利用碱的化学性质进行下列实验,能达到相应目的的是( )
A. 用Ba(OH)2溶液鉴别稀盐酸和稀硫酸
B. 用KOH溶液鉴别Cu(NO3)2溶液和CuCl2溶液
C. 用NaOH溶液鉴别MgCl2溶液和MgSO4溶液
D. 用澄清石灰水鉴别氧气和一氧化碳
命题点
2
碱的化学性质(6年6考)
A
7. [2020省卷18(3)题2分](3)滴加过量NaOH溶液除去MgCl2,反应的化学方程式是_______________________________________。
8. (2023广州节选)(1)向少量Fe(OH)3沉淀中加入稀盐酸,观察到______________________________,可判断发生了反应。
(2)向Ca(OH)2溶液中通入CO2,观察到______________________
_________,可判断发生了反应。
2NaOH+MgCl2 === Mg(OH)2↓+2NaCl
红褐色沉淀溶解,溶液变为黄色
有白色沉淀产生(或溶液
变浑浊)
9. [人教探究改编]如图是关于碱的化学性质的思维导图。
(1)性质①:碱能使无色酚酞溶液变____。
(2)性质②:若碱为氢氧化钠,酸为稀硫酸,则反应的微观实质是_____________________________________________________
________。
红
氢离子与氢氧根离子结合生成水分子(或H+与OH-结合生成
H2O)
(3)性质③:将一定量二氧化碳通入氢氧化钠溶液中,发生反应的化学方程式为_______________________________。
(4)性质④:若碱为氢氧化钙,写出一个符合性质④的盐的化学式:_________________。
CO2+2NaOH === Na2CO3+H2O
Na2CO3(合理即可)
10. [人教图片改编]黄蜂的毒液呈碱性,若被黄蜂蜇了,涂抹下列物质可缓解疼痛的是( )
A. 食盐水(pH≈7) B. 牙膏(pH≈9)
C. 肥皂水(pH≈10) D. 米醋(pH≈3)
命题点
3
中和反应及其应用(6年4考)
D
11. [人教图片改编]如图是氢氧化钠与盐酸反应的微观示意图,下列有关该图示的说法正确的是( )
A. 反应前后,溶液的pH不变
B. 向反应后溶液中滴加酚酞,溶液呈红色
C. 该图表示氢氧化钠和盐酸恰好完全反应
D. 该反应后溶液中
的微观粒子只有Na+
和Cl-
C
12. [2024省卷20(5)题2分](5)“酸洗”后,用熟石灰中和酸性废液(含硫酸),其反应的化学方程式为
______________________________________。
Ca(OH)2+H2SO4 === CaSO4+2H2O
13. [2020省卷18(4)题2分](4)实验室对含有MgCl2的粗盐进行提纯,步骤如图。步骤⑤中,为中和过量的NaOH,应滴加的“试剂a”是____(填字母)。
A. 稀盐酸 B. 稀硫酸 C. 稀硝酸
A
14. [2022省卷18Ⅱ(2)题2分](2)稀盐酸和NaOH溶液反应无明显现象。为使该反应“可视化”,小英向NaOH溶液中滴加_______
_____溶液,再逐滴加入稀盐酸至过量,观察到溶液由_____色变为无色。
【温馨提示】更多试题详见微专题3
无色
酚酞
红
情境素材提能力
1. [健康安全](2024吉林改编)化学活动小组对可缓解胃酸过多的食物和药物进行了分类整理。下列说法不正确的是( )
A. 胃酸的主要成分是盐酸
B. 轻度胃酸过多时可食用馒头、皮蛋等食物调理
C. 加大剂量服用含氢氧化镁的药物可快速缓解胃酸过多
D. 也可以服用含碳酸氢钠的药物治疗胃酸过多症
食物 馒头、皮蛋、苏打饼干、花生等 药物 有效成分 氢氧化镁 碳酸镁 氧化镁 食品级铁粉
类别 碱 盐 氧化物 单质
C
2. [食品安全][人教习题改编]某产品的包装袋内,有一个装有白色颗粒状固体的小纸袋,上面写着“强力干燥剂”,该干燥剂的主要成分为生石灰,下列说法不正确的是( )
A. 禁止食用食品干燥剂
B. 该干燥剂能够吸收食品袋中的水分
C. 曝露在空气中的生石灰可能会转变成碳酸钙
D. 可利用稀盐酸检验生石灰中是否含有熟石灰
D
3. [传统文化]《天工开物》记载:“凡造淀(靛),叶者茎多者入窖,少者入桶与缸。水浸七日,其汁自来。每水浆一石下石灰五升,搅冲数十下,淀信即结……其掠出浮沫晒干者曰靛花。”这里的“靛花”无法直接染色,先转为可溶性靛白,进入纺织品的纤维,透风后被氧化成靛蓝固着在纤维制品上。
(1)“水浸七日,其汁自来”“晒干者曰靛花”,相当于实验操作中的_____、______。
溶解
蒸发
(2)“每水浆一石下石灰五升”,该过程生成的氢氧化钙能中和“水浸七日”时发酵生成的酸,使溶液的pH______(填“增大”或“减小”);氢氧化钙还能与发酵过程产生的二氧化碳反应,反应的化学方程式为____________________________________,加快沉降速度。
(3)透风的目的是与空气中的__________接触,使靛白变成靛蓝。
增大
CO2+Ca(OH)2 === CaCO3↓+H2O
O2(或氧气)
4. [日常生活](2024成都)皮蛋是成渝等地人们喜爱的食品,制作流程如图。
资料:1. 草木灰(含K2CO3)中常含有砂石和未燃尽的秸秆等固体。
2. 碱,有涩味,可与蛋白质作用,使其凝固。回答下列问题。
(1)选料:“过筛”的目的是_______________________________
__________。
除去砂石和未燃尽的秸秆等颗粒较
大的固体
(2)调浆:调浆过程发生的复分解反应的化学方程式为___________________________________________________________________________________________,料浆浸出液中一定含有的阴离子有___________(填离子符号)。
Ca(OH)2+Na2CO3 === CaCO3↓+2NaOH[或
Ca(OH)2+K2CO3 === CaCO3↓+2KOH]
OH-和Cl-
(3)裹泥:裹泥时,不慎皮肤接触料浆,处理方法为___________
______。
(4)封存:需要“密封”的主要原因是减少水分蒸发和_________
________________________________________________。
用大量清水
冲洗
减少空气中二氧化碳与皮蛋表面的碱反应,避免皮蛋制作失败
(5)食用皮蛋时加醋能去除涩味的原因是_____________________
___________。
醋能与皮蛋中的碱性物质发生反应
纵横过实验·纵向实验分层练
实验
常见碱的化学性质(6年6考)
如图是探究碱的化学性质的实验。
【实验操作和现象】
(1)图1实验,向氢氧化钠和氢氧化钙溶液中分别滴加酸碱指示剂,观察到的现象是_________________________________________
___________,得出的结论是________
_________________________________。
基础巩固
——教材要点梳理
滴加紫色石蕊溶液的孔穴变蓝,滴加酚酞溶液的孔穴变红
碱能使紫色石蕊溶液变蓝,能使酚酞溶液变红
(2)图2实验,向盛有氢氧化钠溶液的试管中滴加几滴硫酸铜溶液,观察到的现象是________________,反应的化学方程式为________________________________________。
有蓝色沉淀生成
CuSO4+2NaOH === Na2SO4+Cu(OH)2↓
(3)图3实验中,发生反应的化学方程式为___________________________________,该反应原理常用来__________。
CO2+Ca(OH)2 === CaCO3↓+H2O
检验CO2
(4)图4实验中,向两支试管中各加入0.2 g氢氧化钙粉末,然后各加入约1 mL水,振荡,再各滴入2滴酚酞溶液,观察到的现象是两支试管底部均有固体剩余,___________________________;继续向其中一支试管中加入约1 mL水,振荡,观察到的现象是试管中存在不溶物,_____________;向另一支试管中加入
约1 mL稀盐酸,振荡,观察到的现象是试管中固
体全部溶解,_______________________;比较两支
试管中的现象,可得出氢氧化钙的化学性质是__________________________________。
两支试管中溶液均变为红色
溶液颜色不变
溶液由红色逐渐变为无色
能使酚酞溶液变红、能与酸反应
【实验结论】
(5)通过上述实验可知,碱的化学性质为能使指示剂变色、与酸反应、与某些_______________________(填物质类别)反应。
可溶性盐、非金属氧化物
(6)[替换试剂]某同学将图3实验中的氢氧化钙溶液换成了氢氧化钠溶液,未观察到明显现象,为验证反应已发生,请设计实验:_________________________________________________________________________(写出实验操作及现象)。
能力提升
——全国视野·新考法
取少量反应后的溶液于另一支试管中,滴加过量的稀盐酸,有气泡产生(合理即可)
第2讲 常见的酸碱盐
2025广东化学
课时2 常见的碱
常见的碱
常见的碱
中和反应
定义
应用
表达式
中和反应的探究
定义
常见碱的特性及用途
氢氧化钠
氢氧化钙
化学性质(碱四条)
使指示剂变色
与某些非金属氧化物反应
与酸反应
与盐反应
思维导图
考点梳理
定义:在水溶液中解离出的阴离子全部是_____________________的化合
物,如氢氧化钠、氢氧化钙等
一、常见的碱(6年6考)
OH-(或氢氧根离子)
NaOH在水中解离出离子示意图
常见碱的特性及用途
物质 氢氧化钠(NaOH) 氢氧化钙[Ca(OH)2]
俗名 ________、火碱、苛性钠 ________、消石灰
物理 性质 白色固体,易溶于水,溶解时________(填“吸收”或“放出”)热量 白色粉末状物质,微溶于水,溶解度随温度的升高而________
一、常见的碱(6年6考)
烧碱
熟石灰
放出
减小
常见碱的特性及用途
物质 氢氧化钠(NaOH) 氢氧化钙[Ca(OH)2]
特性 在空气中易潮解、有强烈的腐蚀性 有腐蚀性
用途 实验室可用作某些气体(中性或碱性)的干燥剂;炉具清洁剂的成分之一,可用于除油污 作建筑材料;改良酸性土壤;配制农药波尔多液;保护树木,防止冻伤等
一、常见的碱(6年6考)
熟石灰改良酸性土壤
一、常见的碱(6年6考)
氢氧化钠变质的探究(详见微专题4)
化学性质
(碱四条)
使指示剂变色:能使紫色石蕊溶液变_____,使无色酚酞溶液变____
与某些非金属
氧化物反应
通式:碱+非金属氧化物→盐+水
举例
2NaOH+CO2=== ________________(实验室吸收二
氧化碳)
Ca(OH)2+CO2=== ________________(实验室检验二
氧化碳),现象为澄清石灰水变浑浊
蓝
红
Na2CO3+H2O
CaCO3↓+H2O
一、常见的碱(6年6考)
与酸反应
化学性质
(碱四条)
通式:碱+酸→盐+水
举例:氢氧化钠与稀盐酸:
___________________________
与盐反应
通式:可溶性碱+可溶性盐→新碱+新盐
举例:2NaOH+MgCl2=== __________________,现象
__________________
总结
不同碱具有通性的原因:_________________________________
不同碱具有个性的原因:___________________
NaOH+HCl === NaCl+H2O
Mg(OH)2↓+2NaCl
有白色沉淀产生
在水溶液中解离出的阴离子都是OH-
所含阳离子不同
氢氧化镁沉淀
农业:调节土壤的酸碱性,如用________改良酸性土壤
工业:处理工厂废水,如用熟石灰处理酸性废水
医药:用于医药,如胃酸过多时可服用含有碱性物质的药物
生活:蜂或蚂蚁叮咬后涂抹含有碱性物质的溶液,可减轻肿、痛
或瘙痒等症状
二、中和反应(6年4考)
定义:_____与_____作用生成_____和_____的反应
表达式:酸+碱→盐+水
中和反应的探究(详见微专题3)
应用
酸
碱
盐
水
熟石灰
中和胃酸——氢氧化铝
易错点判断
判断下列说法的正误,正确的打“√”,错误的打“×”。
1. 碱中一定含有氢元素、氧元素和金属元素。( )
2. 氢氧化钠固体可用于干燥氯化氢和二氧化碳气体。( )
3. 熟石灰可用于改良酸性土壤,则氢氧化钠也可用于改良酸性土壤。( )
4. 能与碱反应生成盐和水的物质一定是酸。( )
×
×
×
×
常见碱[NaOH、Ca(OH)2]的化学性质(碱四条)
已知:甲为固态时俗称干冰,乙俗称纯碱。
1. 写出对应物质的化学式。
甲________;
乙________。
构建物质网络
CO2
Na2CO3
2. 写出相应序号的化学方程式(①~③各写一个)。
①___________________________________________________
_____________________________________________________;
H2SO4+2NaOH=== Na2SO4+2H2O
[或H2SO4+Ca(OH)2=== CaSO4+2H2O]
②_______________________________________________________________________________________________________;
2NaOH+CuSO4=== Cu(OH)2↓+Na2SO4
[或Ca(OH)2+CuSO4=== Cu(OH)2↓+CaSO4]
③_____________________________________________________;
______________________________________________________④_____________________________________________________。
CO2+Ca(OH)2=== CaCO3↓+H2O
(或CO2+2NaOH=== Na2CO3+H2O)
Ca(OH)2+Na2CO3=== CaCO3↓+2NaOH
甲________;
乙________。
CO2
Na2CO3
广东真题练基础
1. (省卷真题组合)判断下列说法的正误:
(1)用炉具清洁剂去除油污,NaOH可与油脂反应。(2022.14B)
( )
(2)KOH在水中解离出K+和OH-。(2020.11A)( )
命题点
1
常见碱的特性及用途(6年4考)
√
√
2. (2023省卷9题3分)下列与制作叶脉书签项目有关的说法错误的是( )
A. NaOH溶液可以腐蚀叶肉
B. 制作过程涉及化学变化
C. 制作完成后废液需回收处理
D. NaOH固体存放处应张贴如图所示标志
D
3. (2023深圳改编)有关NaOH说法错误的是( )
A. NaOH固体溶解时放出热量
B. NaOH固体吸水易潮解
C. NaOH是所有气体的干燥剂
D. NaOH应密封保存
C
4. [2021省卷18(4)题第1空2分](4)某同学在学习氮肥时,查阅资料:①氨气极易溶于水,其水溶液称为氨水;②氨水在浓度大或受热时易分解放出氨气。
实验室用生石灰和浓氨水能快速制取氨气的原因是___________
__________________________________________________。
生石灰和水反应消耗水,并且放出热量,可加快浓氨水分解
5. [人教素材改编]每年冬季,园林工人总会在景观树树干下部涂上“白浆”,同学们通过询问得知该“白浆”是含有硫黄粉等的石灰浆,石灰浆的主要成分是熟石灰,请回答下列问题。
(1)生石灰可用于制取熟石灰,该反应属于______(填“吸热”或“放热”)反应。
(2)树干上涂抹含有硫黄粉等的石灰浆的主要目的是___________
_________________________。
放热
保护树木,防止冻伤,并防止害虫产卵
(3)用石灰浆粉刷树干,干燥后石灰浆变硬,其原因是_______________________________(用化学方程式解释)。
(4)熟石灰在农业生产上的另一种用途是______________________。
Ca(OH)2+CO2 === CaCO3↓+H2O
改良酸性土壤(合理即可)
6. [人教探究改编]若利用碱的化学性质进行下列实验,能达到相应目的的是( )
A. 用Ba(OH)2溶液鉴别稀盐酸和稀硫酸
B. 用KOH溶液鉴别Cu(NO3)2溶液和CuCl2溶液
C. 用NaOH溶液鉴别MgCl2溶液和MgSO4溶液
D. 用澄清石灰水鉴别氧气和一氧化碳
命题点
2
碱的化学性质(6年6考)
A
7. [2020省卷18(3)题2分](3)滴加过量NaOH溶液除去MgCl2,反应的化学方程式是_______________________________________。
8. (2023广州节选)(1)向少量Fe(OH)3沉淀中加入稀盐酸,观察到______________________________,可判断发生了反应。
(2)向Ca(OH)2溶液中通入CO2,观察到______________________
_________,可判断发生了反应。
2NaOH+MgCl2 === Mg(OH)2↓+2NaCl
红褐色沉淀溶解,溶液变为黄色
有白色沉淀产生(或溶液
变浑浊)
9. [人教探究改编]如图是关于碱的化学性质的思维导图。
(1)性质①:碱能使无色酚酞溶液变____。
(2)性质②:若碱为氢氧化钠,酸为稀硫酸,则反应的微观实质是_____________________________________________________
________。
红
氢离子与氢氧根离子结合生成水分子(或H+与OH-结合生成
H2O)
(3)性质③:将一定量二氧化碳通入氢氧化钠溶液中,发生反应的化学方程式为_______________________________。
(4)性质④:若碱为氢氧化钙,写出一个符合性质④的盐的化学式:_________________。
CO2+2NaOH === Na2CO3+H2O
Na2CO3(合理即可)
10. [人教图片改编]黄蜂的毒液呈碱性,若被黄蜂蜇了,涂抹下列物质可缓解疼痛的是( )
A. 食盐水(pH≈7) B. 牙膏(pH≈9)
C. 肥皂水(pH≈10) D. 米醋(pH≈3)
命题点
3
中和反应及其应用(6年4考)
D
11. [人教图片改编]如图是氢氧化钠与盐酸反应的微观示意图,下列有关该图示的说法正确的是( )
A. 反应前后,溶液的pH不变
B. 向反应后溶液中滴加酚酞,溶液呈红色
C. 该图表示氢氧化钠和盐酸恰好完全反应
D. 该反应后溶液中
的微观粒子只有Na+
和Cl-
C
12. [2024省卷20(5)题2分](5)“酸洗”后,用熟石灰中和酸性废液(含硫酸),其反应的化学方程式为
______________________________________。
Ca(OH)2+H2SO4 === CaSO4+2H2O
13. [2020省卷18(4)题2分](4)实验室对含有MgCl2的粗盐进行提纯,步骤如图。步骤⑤中,为中和过量的NaOH,应滴加的“试剂a”是____(填字母)。
A. 稀盐酸 B. 稀硫酸 C. 稀硝酸
A
14. [2022省卷18Ⅱ(2)题2分](2)稀盐酸和NaOH溶液反应无明显现象。为使该反应“可视化”,小英向NaOH溶液中滴加_______
_____溶液,再逐滴加入稀盐酸至过量,观察到溶液由_____色变为无色。
【温馨提示】更多试题详见微专题3
无色
酚酞
红
情境素材提能力
1. [健康安全](2024吉林改编)化学活动小组对可缓解胃酸过多的食物和药物进行了分类整理。下列说法不正确的是( )
A. 胃酸的主要成分是盐酸
B. 轻度胃酸过多时可食用馒头、皮蛋等食物调理
C. 加大剂量服用含氢氧化镁的药物可快速缓解胃酸过多
D. 也可以服用含碳酸氢钠的药物治疗胃酸过多症
食物 馒头、皮蛋、苏打饼干、花生等 药物 有效成分 氢氧化镁 碳酸镁 氧化镁 食品级铁粉
类别 碱 盐 氧化物 单质
C
2. [食品安全][人教习题改编]某产品的包装袋内,有一个装有白色颗粒状固体的小纸袋,上面写着“强力干燥剂”,该干燥剂的主要成分为生石灰,下列说法不正确的是( )
A. 禁止食用食品干燥剂
B. 该干燥剂能够吸收食品袋中的水分
C. 曝露在空气中的生石灰可能会转变成碳酸钙
D. 可利用稀盐酸检验生石灰中是否含有熟石灰
D
3. [传统文化]《天工开物》记载:“凡造淀(靛),叶者茎多者入窖,少者入桶与缸。水浸七日,其汁自来。每水浆一石下石灰五升,搅冲数十下,淀信即结……其掠出浮沫晒干者曰靛花。”这里的“靛花”无法直接染色,先转为可溶性靛白,进入纺织品的纤维,透风后被氧化成靛蓝固着在纤维制品上。
(1)“水浸七日,其汁自来”“晒干者曰靛花”,相当于实验操作中的_____、______。
溶解
蒸发
(2)“每水浆一石下石灰五升”,该过程生成的氢氧化钙能中和“水浸七日”时发酵生成的酸,使溶液的pH______(填“增大”或“减小”);氢氧化钙还能与发酵过程产生的二氧化碳反应,反应的化学方程式为____________________________________,加快沉降速度。
(3)透风的目的是与空气中的__________接触,使靛白变成靛蓝。
增大
CO2+Ca(OH)2 === CaCO3↓+H2O
O2(或氧气)
4. [日常生活](2024成都)皮蛋是成渝等地人们喜爱的食品,制作流程如图。
资料:1. 草木灰(含K2CO3)中常含有砂石和未燃尽的秸秆等固体。
2. 碱,有涩味,可与蛋白质作用,使其凝固。回答下列问题。
(1)选料:“过筛”的目的是_______________________________
__________。
除去砂石和未燃尽的秸秆等颗粒较
大的固体
(2)调浆:调浆过程发生的复分解反应的化学方程式为___________________________________________________________________________________________,料浆浸出液中一定含有的阴离子有___________(填离子符号)。
Ca(OH)2+Na2CO3 === CaCO3↓+2NaOH[或
Ca(OH)2+K2CO3 === CaCO3↓+2KOH]
OH-和Cl-
(3)裹泥:裹泥时,不慎皮肤接触料浆,处理方法为___________
______。
(4)封存:需要“密封”的主要原因是减少水分蒸发和_________
________________________________________________。
用大量清水
冲洗
减少空气中二氧化碳与皮蛋表面的碱反应,避免皮蛋制作失败
(5)食用皮蛋时加醋能去除涩味的原因是_____________________
___________。
醋能与皮蛋中的碱性物质发生反应
纵横过实验·纵向实验分层练
实验
常见碱的化学性质(6年6考)
如图是探究碱的化学性质的实验。
【实验操作和现象】
(1)图1实验,向氢氧化钠和氢氧化钙溶液中分别滴加酸碱指示剂,观察到的现象是_________________________________________
___________,得出的结论是________
_________________________________。
基础巩固
——教材要点梳理
滴加紫色石蕊溶液的孔穴变蓝,滴加酚酞溶液的孔穴变红
碱能使紫色石蕊溶液变蓝,能使酚酞溶液变红
(2)图2实验,向盛有氢氧化钠溶液的试管中滴加几滴硫酸铜溶液,观察到的现象是________________,反应的化学方程式为________________________________________。
有蓝色沉淀生成
CuSO4+2NaOH === Na2SO4+Cu(OH)2↓
(3)图3实验中,发生反应的化学方程式为___________________________________,该反应原理常用来__________。
CO2+Ca(OH)2 === CaCO3↓+H2O
检验CO2
(4)图4实验中,向两支试管中各加入0.2 g氢氧化钙粉末,然后各加入约1 mL水,振荡,再各滴入2滴酚酞溶液,观察到的现象是两支试管底部均有固体剩余,___________________________;继续向其中一支试管中加入约1 mL水,振荡,观察到的现象是试管中存在不溶物,_____________;向另一支试管中加入
约1 mL稀盐酸,振荡,观察到的现象是试管中固
体全部溶解,_______________________;比较两支
试管中的现象,可得出氢氧化钙的化学性质是__________________________________。
两支试管中溶液均变为红色
溶液颜色不变
溶液由红色逐渐变为无色
能使酚酞溶液变红、能与酸反应
【实验结论】
(5)通过上述实验可知,碱的化学性质为能使指示剂变色、与酸反应、与某些_______________________(填物质类别)反应。
可溶性盐、非金属氧化物
(6)[替换试剂]某同学将图3实验中的氢氧化钙溶液换成了氢氧化钠溶液,未观察到明显现象,为验证反应已发生,请设计实验:_________________________________________________________________________(写出实验操作及现象)。
能力提升
——全国视野·新考法
取少量反应后的溶液于另一支试管中,滴加过量的稀盐酸,有气泡产生(合理即可)
同课章节目录
