第12讲 质量守恒定律 化学方程式 课件(共42张PPT) 2025年中考化学一轮考点研究(人教版)
文档属性
| 名称 | 第12讲 质量守恒定律 化学方程式 课件(共42张PPT) 2025年中考化学一轮考点研究(人教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 30.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-09 00:00:00 | ||
图片预览









文档简介
(共42张PPT)
第12讲 质量守恒定律
化学方程式
2025广东化学
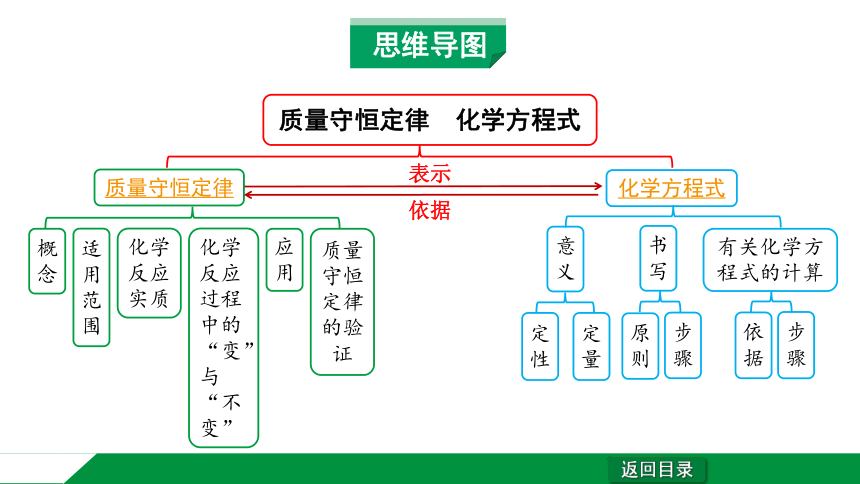
思维导图
质量守恒定律 化学方程式
化学方程式
质量守恒定律
依据
表示
意义
有关化学方程式的计算
书写
定性
定量
原则
步骤
依据
步骤
适用范围
化学反应过程中的“变”与“不变”
应用
概念
化学反应实质
质量守恒定律的验证
考点梳理
一、质量守恒定律(6年6考)
概念:参加化学反应的各物质的_________等于反应后生成的各物质的
_________
适用范围:只适用于所有的________变化;只适用于________守恒,不
包括体积、分子数目等的守恒
化学反应实质:分子分为原子,原子结合成新的分子
质量总和
质量总和
化学
质量
宏观:元素的化合价可能改变
微观:分子的_______可能改变
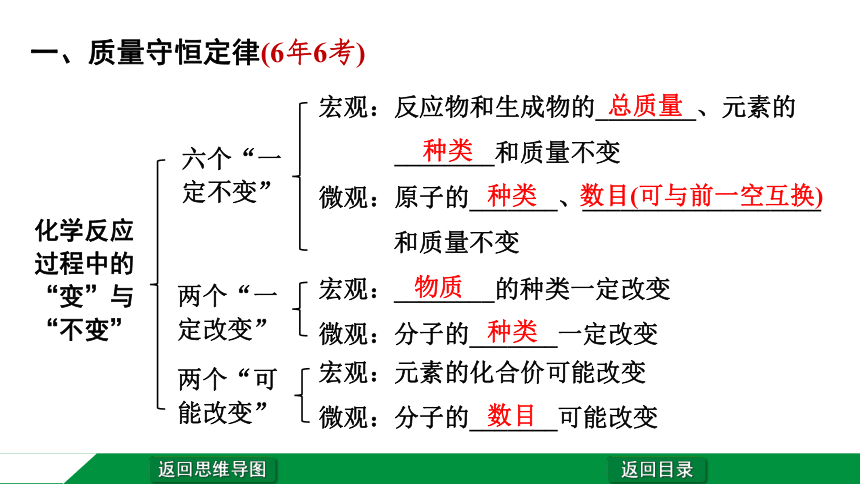
一、质量守恒定律(6年6考)
化学反应过程中的
“变”与“不变”
六个“一定不变”
宏观:反应物和生成物的________、元素的
________和质量不变
微观:原子的_______、___________________
和质量不变
两个“一定改变”
宏观:________的种类一定改变
微观:分子的_______一定改变
两个“可能改变”
总质量
种类
种类
数目(可与前一空互换)
物质
种类
数目
推断物质的元素组成及组成元素的质量——依据化学反应前后元
素的________和质量不变
推断化学反应中未知物的化学式或化学计量数、配平化学方程
式——依据化学反应前后原子的____________不变
对微观反应示意图进行分析、判断——依据化学反应前后原子的
种类和数目不变
一、质量守恒定律(6年6考)
应用
质量守恒定律的验证(详见纵横过实验·纵向实验分层练)
种类
种类和数目
宏观:表示各物质间的质量关系(即质量比),如
该化学反应中C、O2、CO2的质量比为
_________(写最简整数比,下同)
微观:表示各物质间的微观粒子个数关系(即微观
粒子个数比),如该化学反应中C、O2、
CO2的分子个数比为__________
二、化学方程式(6年6考)
意义(以“C+
O2 CO2”
为例)
定性:体现化学反应中的物质转化关系,如该化学反应
中的反应物为________、生成物为_______、反
应条件为________
定量
C、O2
CO2
点燃
3∶8∶11
1∶1∶1
二、化学方程式(6年6考)
书写
原则:以客观事实为基础,遵守________________
步骤:写→配→标→查
一查化学式是否正确
二查是否配平
三查生成物状态是否标注,标注是否恰当
四查反应条件是否标明
【特别提醒】如果生成物中有气体,在气体物质的化学式右边要注
“↑”号。对于溶液中的反应,如果生成物中有固体,在
固体物质的化学式右边要注“↓”号。若反应前后均有气
体或固体,则不标“↑”和“↓”
质量守恒定律
设:设未知量(不带单位)
写:正确书写有关反应的化学方程式
找:找出已知量、未知量的质量关系
列:列出比例式,求解(求得的数值带单位)
答:简明地写出答案
二、化学方程式(6年6考)
有关化学方程式的计算
依据:_______________
步骤
质量守恒定律
广东真题练基础
命题点
1
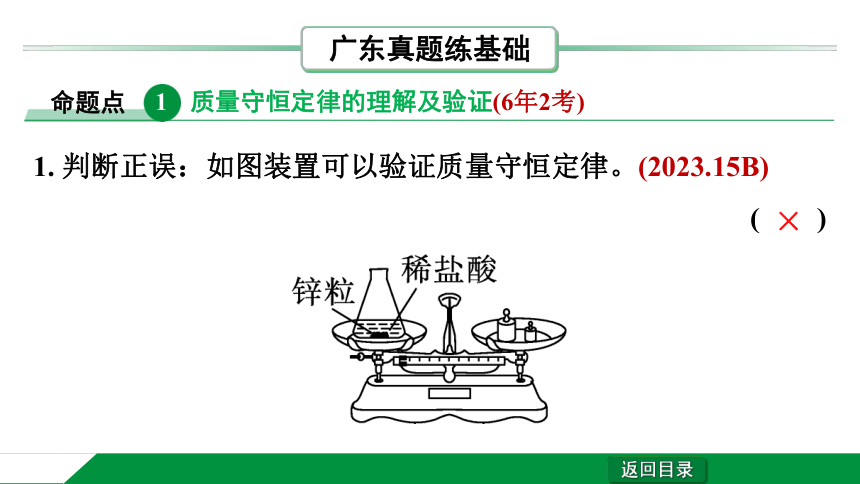
质量守恒定律的理解及验证(6年2考)
1. 判断正误:如图装置可以验证质量守恒定律。(2023.15B)
( )
×
2. [人教习题改编]下列有关质量守恒定律的说法正确的是( )
A. 蜡烛燃烧后质量减少,不遵守质量守恒定律
B. 冰块化成水后质量不变,遵守质量守恒定律
C. 2 L氢气和1 L氧气在一定条件下反应会生成3 L水
D. 在氧气中燃烧生成二氧化碳的物质中一定含有碳元素
D
命题点
2
质量守恒定律的应用(6年6考)
考向1 推断未知物的化学式(6年2考)
3. [人教新增习题改编]黑火药是我国古代“四大发明”之一,其爆炸时发生反应的化学方程式为
S+2KNO3+3C K2S+X↑+3CO2↑,则X的化学式为( )
A. N2 B. N2O C. NO D. NO2
A
4. (2024广州节选)制备供氧剂用于水产养殖。查阅资料后动手实践:往CaCl2溶液中通入足量的NH3后加入H2O2溶液,保持0~5 ℃充分反应,过滤、水洗并烘干后得到CaO2。
(1)原理分析:补充完整制备CaO2的化学方程式
CaCl2+2NH3+H2O2===CaO2↓+2________。
(2)供氧剂使用:水产养殖中,CaO2与水缓慢反应释放出O2为鱼类供氧,反应的另一产物属于微溶于水的碱,该产物的化学式为__________。
NH4Cl
Ca(OH)2
考向2 微观反应示意图(6年6考)
5. (2024省卷13题3分)我国科学家利用光催化技术实现了绿色制取H2O2, 反应的微观示意图如图所示。下列说法正确的是( )
A. 反应后氧原子个数减少
B. 反应后催化剂的质量增加
C. b的化学式为H2O
D. 参加反应的a、b分子个数
比为1∶1
C
6. [2022省卷17(1)(2)题4分]我国科学家研制了一种新型催化剂,实现了甲烷向重要化工原料甲醇的高效转化。反应过程的微观示意图如图所示。
(1)该反应涉及________种单质。反应前后催化剂的化学性质______。
2(或两)
不变
(2)该反应的化学方程式为________________________________。
【温馨提示】更多试题详见微专题8
CH4+H2+O2 CH3OH+H2O
命题点
3
化学方程式的书写(6年6考)
7. [2022省卷20(5)题2分](5)孔雀石[主要成分为Cu2(OH)2CO3]受热分解,生成三种氧化物,其中一种为黑色固体。该反应的化学方程式为___________________________________。
Cu2(OH)2CO3 2CuO+H2O+CO2↑
8. [2024省卷16(2)(3)题5分]《天工开物》蕴含丰富的化学知识和化学思想。书中记载了银朱的制备过程,如图所示。
(2)“研磨”时,水银与石亭脂充分反应生成银朱,化学方程式为_______________, 有剩余的反应物是________________。
S(或硫或石亭脂)
Hg+S===HgS
(3)“加热”时,银朱______(填“升华”或“凝华”),再经“蘸水擦盏”形成粉末贴于泥罐内壁,达到银朱从混合物中_______
______的目的。
升华
分离
提纯
命题点
4
有关化学方程式的计算(6年6考)
9. [2022省卷21(3)(4)题8分]铁铜双金属粉末可用于生产机械零件。利用还原铁粉和CuSO4溶液制备该产品的工艺流程如图1所示。(可能用到的相对原子质量:Fe-56 Cu-64)
图1
(3)若用该工艺制备了1 000 g铁铜双金属粉末产品,其中Cu单质的质量分数为19.2%。计算置换这些Cu单质所需还原铁粉的质量。(写出计算过程)
图1
(3)解:置换出的铜的质量为1 000 g×19.2%=192 g,设所需还原铁粉的质量为x
Fe+CuSO4===FeSO4+Cu
56 64
x 192 g
x=168 g
答:所需还原铁粉的质量为168 g。
(4)“干燥还原”可在不同的温度下进行,产品中氧元素的质量分数随温度的变化如图2所示。
若(3)中产品是在500 ℃时干燥
还原后得到的,则其中最多含
Fe元素______g(产品中只含三
种元素)。
图2
804
10. [2020省卷21(2)(3)(4)题8分]某实验小组探究了溶质的质量分数对H2O2分解速率的影响。实验装置如图1所示,用注射器加入不同浓度的H2O2溶液(见下表)
实验编号 H2O2的质量分数/% H2O2溶液的体积/mL 对应曲线
Ⅰ 3.4 10.0 a
Ⅱ 2.4 10.0 b
Ⅲ 1.7 10.0 c(待绘制)
实验中使用传感器装置测算生成O2的质量(圆底烧瓶内气压变化在安全范围内),绘制氧气的质量随时间变化的曲线,如图2所示。(可能用到的相对原子质量:H-1 O-16)
实验编号 H2O2的质量分数/% H2O2溶液的体积/mL 对应曲线
Ⅰ 3.4 10.0 a
Ⅱ 2.4 10.0 b
Ⅲ 1.7 10.0 c(待绘制)
(2)根据实验探究目的,从曲线a、b中,可得
出的结论是____________________________
________。
实验编号 H2O2的质量分数/% H2O2溶液的体积/mL 对应曲线
Ⅰ 3.4 10.0 a
Ⅱ 2.4 10.0 b
Ⅲ 1.7 10.0 c(待绘制)
H2O2的溶质质量分数越大,分
解越快
(3)计算实验Ⅰ条件下H2O2完全分解所得氧气的质量,并写出具体计算过程。(1.5%~5.0% H2O2溶液的密度取值1.0 g/mL)
实验编号 H2O2的质量分数/% H2O2溶液的体积/mL 对应曲线
Ⅰ 3.4 10.0 a
(3)解:10.0 mL 3.4% H2O2溶液中溶质质量为10.0 mL×1.0 g/mL×
3.4%=0.34 g,设实验Ⅰ条件下H2O2完全分解生成氧气的质量为 x
2H2O2 2H2O+O2↑
68 32
0.34 g x
x=0.16 g
答:实验 Ⅰ 条件下H2O2完全分解生成氧气的质量为0.16 g。
实验编号 H2O2的质量分数/% H2O2溶液的体积/mL 对应
曲线
Ⅰ 3.4 10.0 a
(4)在图2中画出曲线c的大致位置及趋势。
图2
实验编号 H2O2的质量分数/% H2O2溶液的体积/mL 对应
曲线
Ⅰ 3.4 10.0 a
Ⅱ 2.4 10.0 b
Ⅲ 1.7 10.0 c(待
绘制)
情境素材提能力
1. [热点信息·奥运会]北京时间2024年7月27日,第33届夏季奥林匹克运动会开幕式在巴黎举行,传递火炬所用的燃料为生物丙烷,丙烷燃烧的化学方程式为C3H8+5O2 3CO2+mH2O,则m的值为( )
A. 1 B. 2 C. 3 D. 4
D
2. [科技信息](2024佛山顺德二模)二氧化钛(TiO2)是优秀的光催化剂,可催化分解细菌和有机污染物等。在TiO2催化下,O3降解CH3CHO的过程如图所示,下列说法正确的是( )
A. 反应前后TiO2的性质一定不变
B. CH3CHO为有机高分子化合物
C. 参加反应的物质分子个数比1∶1
D. CH3CHO中氢、氧元素质量比为1∶4
D
3. [科学家探究精神](2024深圳模拟)“侯氏制碱法”的主要过程是利用饱和食盐水先后吸收两种气体,生成碳酸氢钠(NaHCO3)和氯化铵(NH4Cl),再加热碳酸氢钠即可制得纯碱。
(1)“侯氏制碱法”的主要过程中需要吸收的两种气体是_____(填字母)。
A. NH3 B. Cl2 C. CO2 D. SO2
(2)加热碳酸氢钠可制得纯碱,同时生成水和二氧化碳,写出该反应的化学方程式:__________________________________。
AC
2NaHCO3 Na2CO3+H2O+CO2↑
4. [中国科技](2024佛山南海一模节选)纳米零价铁(nZVI)除废水中金属离子的性能优越,制备示意图为:
(1)“聚集”过程,铁元素化合价_______(填“升高”“降低”或“不变”)。
不变
(2)“还原”过程,一定量焦炭与232 g Fe3O4作用,生成CO2,反应的化学方程式为____________________________。
(3)“雾化”过程,发生反应:
FeCl3+3H2O===Fe(OH)3+3______(补充完整该化学方程式)。
HCl
Fe3O4+2C 3Fe+2CO2↑
某兴趣小组同学设计如下实验验证质量守恒定律(反应前已调节天平平衡)。
图1
基础巩固
———教材要点梳理
【实验原理】
(1)实验甲、乙、丙、丁的反应原理用化学方程式可表示为____________________、__________________________、____________________________________、
____________________。
2Cu+O2 2CuO
Fe+CuSO4===FeSO4+Cu
2HCl+Na2CO3===2NaCl+H2O+CO2↑
2Mg+O2 2MgO
【实验操作及现象】
(2)实验甲:将装置放在天平上称量,然后再将锥形瓶置于陶土网上,用酒精灯加热,观察到_____________
___________________________,一段时间后
停止加热,待装置冷却后再次称量,可观察
到天平示数______(填“变大”“变小”或
“不变”,后同)。
铜粉由红色变
为黑色,小气球先变大后变瘪
不变
(3)实验乙:锥形瓶内硫酸铜溶液和铁丝接触后,观察到的现象是_________________________________________________,实验结束后再次称量,可观察到天平示数______。
(4)实验丙:烧杯中碳酸钠粉末
和稀盐酸接触后,观察到的现
象是______________________
______,实验结束后再次称量,
可观察到天平示数______。
铁丝表面有红色固体析出,溶液由蓝色逐渐变为浅绿色
不变
固体粉末溶解,有气泡
产生
变小
(5)实验丁:点燃镁条后观察到____________________________
_____________________,实验结束后再次称量固体质量,观察到天平示数改变。
镁条燃烧,发出耀眼的白光,生
成白色固体,放出热量
【实验结论】
(6)上述实验中能直接验证质量守恒定律的是________(填“甲”
“乙”“丙”或“丁”,后同),由此可知,化学反应前后______________不变。
甲、乙
物质的总质量
【实验反思】
(7)实验甲中小气球的作用是______________________________
_______________;该实验结束后,锥形瓶底部有铜粉剩余,对实验结果______(填“有”或“没有”)影响。
调节锥形瓶内的压强、形成密闭
装置(合理即可)
没有
(8)通过上述实验,同学们总结出验证质量守恒定律的条件:
①物质间发生_______(填“物理”或“化学”)反应;②有气体参与或生成的反应必须在__________中进行。
化学
密闭容器
能力提升
——全国视野·新考法
(9)[试剂改进]用上述实验丙验证质量守恒定律,
同学们在不改变装置的情况下设计了如图2所示
三个实验,其中能验证质量守恒定律的是_____(填字母)。
图2
C
第12讲 质量守恒定律
化学方程式
2025广东化学
思维导图
质量守恒定律 化学方程式
化学方程式
质量守恒定律
依据
表示
意义
有关化学方程式的计算
书写
定性
定量
原则
步骤
依据
步骤
适用范围
化学反应过程中的“变”与“不变”
应用
概念
化学反应实质
质量守恒定律的验证
考点梳理
一、质量守恒定律(6年6考)
概念:参加化学反应的各物质的_________等于反应后生成的各物质的
_________
适用范围:只适用于所有的________变化;只适用于________守恒,不
包括体积、分子数目等的守恒
化学反应实质:分子分为原子,原子结合成新的分子
质量总和
质量总和
化学
质量
宏观:元素的化合价可能改变
微观:分子的_______可能改变
一、质量守恒定律(6年6考)
化学反应过程中的
“变”与“不变”
六个“一定不变”
宏观:反应物和生成物的________、元素的
________和质量不变
微观:原子的_______、___________________
和质量不变
两个“一定改变”
宏观:________的种类一定改变
微观:分子的_______一定改变
两个“可能改变”
总质量
种类
种类
数目(可与前一空互换)
物质
种类
数目
推断物质的元素组成及组成元素的质量——依据化学反应前后元
素的________和质量不变
推断化学反应中未知物的化学式或化学计量数、配平化学方程
式——依据化学反应前后原子的____________不变
对微观反应示意图进行分析、判断——依据化学反应前后原子的
种类和数目不变
一、质量守恒定律(6年6考)
应用
质量守恒定律的验证(详见纵横过实验·纵向实验分层练)
种类
种类和数目
宏观:表示各物质间的质量关系(即质量比),如
该化学反应中C、O2、CO2的质量比为
_________(写最简整数比,下同)
微观:表示各物质间的微观粒子个数关系(即微观
粒子个数比),如该化学反应中C、O2、
CO2的分子个数比为__________
二、化学方程式(6年6考)
意义(以“C+
O2 CO2”
为例)
定性:体现化学反应中的物质转化关系,如该化学反应
中的反应物为________、生成物为_______、反
应条件为________
定量
C、O2
CO2
点燃
3∶8∶11
1∶1∶1
二、化学方程式(6年6考)
书写
原则:以客观事实为基础,遵守________________
步骤:写→配→标→查
一查化学式是否正确
二查是否配平
三查生成物状态是否标注,标注是否恰当
四查反应条件是否标明
【特别提醒】如果生成物中有气体,在气体物质的化学式右边要注
“↑”号。对于溶液中的反应,如果生成物中有固体,在
固体物质的化学式右边要注“↓”号。若反应前后均有气
体或固体,则不标“↑”和“↓”
质量守恒定律
设:设未知量(不带单位)
写:正确书写有关反应的化学方程式
找:找出已知量、未知量的质量关系
列:列出比例式,求解(求得的数值带单位)
答:简明地写出答案
二、化学方程式(6年6考)
有关化学方程式的计算
依据:_______________
步骤
质量守恒定律
广东真题练基础
命题点
1
质量守恒定律的理解及验证(6年2考)
1. 判断正误:如图装置可以验证质量守恒定律。(2023.15B)
( )
×
2. [人教习题改编]下列有关质量守恒定律的说法正确的是( )
A. 蜡烛燃烧后质量减少,不遵守质量守恒定律
B. 冰块化成水后质量不变,遵守质量守恒定律
C. 2 L氢气和1 L氧气在一定条件下反应会生成3 L水
D. 在氧气中燃烧生成二氧化碳的物质中一定含有碳元素
D
命题点
2
质量守恒定律的应用(6年6考)
考向1 推断未知物的化学式(6年2考)
3. [人教新增习题改编]黑火药是我国古代“四大发明”之一,其爆炸时发生反应的化学方程式为
S+2KNO3+3C K2S+X↑+3CO2↑,则X的化学式为( )
A. N2 B. N2O C. NO D. NO2
A
4. (2024广州节选)制备供氧剂用于水产养殖。查阅资料后动手实践:往CaCl2溶液中通入足量的NH3后加入H2O2溶液,保持0~5 ℃充分反应,过滤、水洗并烘干后得到CaO2。
(1)原理分析:补充完整制备CaO2的化学方程式
CaCl2+2NH3+H2O2===CaO2↓+2________。
(2)供氧剂使用:水产养殖中,CaO2与水缓慢反应释放出O2为鱼类供氧,反应的另一产物属于微溶于水的碱,该产物的化学式为__________。
NH4Cl
Ca(OH)2
考向2 微观反应示意图(6年6考)
5. (2024省卷13题3分)我国科学家利用光催化技术实现了绿色制取H2O2, 反应的微观示意图如图所示。下列说法正确的是( )
A. 反应后氧原子个数减少
B. 反应后催化剂的质量增加
C. b的化学式为H2O
D. 参加反应的a、b分子个数
比为1∶1
C
6. [2022省卷17(1)(2)题4分]我国科学家研制了一种新型催化剂,实现了甲烷向重要化工原料甲醇的高效转化。反应过程的微观示意图如图所示。
(1)该反应涉及________种单质。反应前后催化剂的化学性质______。
2(或两)
不变
(2)该反应的化学方程式为________________________________。
【温馨提示】更多试题详见微专题8
CH4+H2+O2 CH3OH+H2O
命题点
3
化学方程式的书写(6年6考)
7. [2022省卷20(5)题2分](5)孔雀石[主要成分为Cu2(OH)2CO3]受热分解,生成三种氧化物,其中一种为黑色固体。该反应的化学方程式为___________________________________。
Cu2(OH)2CO3 2CuO+H2O+CO2↑
8. [2024省卷16(2)(3)题5分]《天工开物》蕴含丰富的化学知识和化学思想。书中记载了银朱的制备过程,如图所示。
(2)“研磨”时,水银与石亭脂充分反应生成银朱,化学方程式为_______________, 有剩余的反应物是________________。
S(或硫或石亭脂)
Hg+S===HgS
(3)“加热”时,银朱______(填“升华”或“凝华”),再经“蘸水擦盏”形成粉末贴于泥罐内壁,达到银朱从混合物中_______
______的目的。
升华
分离
提纯
命题点
4
有关化学方程式的计算(6年6考)
9. [2022省卷21(3)(4)题8分]铁铜双金属粉末可用于生产机械零件。利用还原铁粉和CuSO4溶液制备该产品的工艺流程如图1所示。(可能用到的相对原子质量:Fe-56 Cu-64)
图1
(3)若用该工艺制备了1 000 g铁铜双金属粉末产品,其中Cu单质的质量分数为19.2%。计算置换这些Cu单质所需还原铁粉的质量。(写出计算过程)
图1
(3)解:置换出的铜的质量为1 000 g×19.2%=192 g,设所需还原铁粉的质量为x
Fe+CuSO4===FeSO4+Cu
56 64
x 192 g
x=168 g
答:所需还原铁粉的质量为168 g。
(4)“干燥还原”可在不同的温度下进行,产品中氧元素的质量分数随温度的变化如图2所示。
若(3)中产品是在500 ℃时干燥
还原后得到的,则其中最多含
Fe元素______g(产品中只含三
种元素)。
图2
804
10. [2020省卷21(2)(3)(4)题8分]某实验小组探究了溶质的质量分数对H2O2分解速率的影响。实验装置如图1所示,用注射器加入不同浓度的H2O2溶液(见下表)
实验编号 H2O2的质量分数/% H2O2溶液的体积/mL 对应曲线
Ⅰ 3.4 10.0 a
Ⅱ 2.4 10.0 b
Ⅲ 1.7 10.0 c(待绘制)
实验中使用传感器装置测算生成O2的质量(圆底烧瓶内气压变化在安全范围内),绘制氧气的质量随时间变化的曲线,如图2所示。(可能用到的相对原子质量:H-1 O-16)
实验编号 H2O2的质量分数/% H2O2溶液的体积/mL 对应曲线
Ⅰ 3.4 10.0 a
Ⅱ 2.4 10.0 b
Ⅲ 1.7 10.0 c(待绘制)
(2)根据实验探究目的,从曲线a、b中,可得
出的结论是____________________________
________。
实验编号 H2O2的质量分数/% H2O2溶液的体积/mL 对应曲线
Ⅰ 3.4 10.0 a
Ⅱ 2.4 10.0 b
Ⅲ 1.7 10.0 c(待绘制)
H2O2的溶质质量分数越大,分
解越快
(3)计算实验Ⅰ条件下H2O2完全分解所得氧气的质量,并写出具体计算过程。(1.5%~5.0% H2O2溶液的密度取值1.0 g/mL)
实验编号 H2O2的质量分数/% H2O2溶液的体积/mL 对应曲线
Ⅰ 3.4 10.0 a
(3)解:10.0 mL 3.4% H2O2溶液中溶质质量为10.0 mL×1.0 g/mL×
3.4%=0.34 g,设实验Ⅰ条件下H2O2完全分解生成氧气的质量为 x
2H2O2 2H2O+O2↑
68 32
0.34 g x
x=0.16 g
答:实验 Ⅰ 条件下H2O2完全分解生成氧气的质量为0.16 g。
实验编号 H2O2的质量分数/% H2O2溶液的体积/mL 对应
曲线
Ⅰ 3.4 10.0 a
(4)在图2中画出曲线c的大致位置及趋势。
图2
实验编号 H2O2的质量分数/% H2O2溶液的体积/mL 对应
曲线
Ⅰ 3.4 10.0 a
Ⅱ 2.4 10.0 b
Ⅲ 1.7 10.0 c(待
绘制)
情境素材提能力
1. [热点信息·奥运会]北京时间2024年7月27日,第33届夏季奥林匹克运动会开幕式在巴黎举行,传递火炬所用的燃料为生物丙烷,丙烷燃烧的化学方程式为C3H8+5O2 3CO2+mH2O,则m的值为( )
A. 1 B. 2 C. 3 D. 4
D
2. [科技信息](2024佛山顺德二模)二氧化钛(TiO2)是优秀的光催化剂,可催化分解细菌和有机污染物等。在TiO2催化下,O3降解CH3CHO的过程如图所示,下列说法正确的是( )
A. 反应前后TiO2的性质一定不变
B. CH3CHO为有机高分子化合物
C. 参加反应的物质分子个数比1∶1
D. CH3CHO中氢、氧元素质量比为1∶4
D
3. [科学家探究精神](2024深圳模拟)“侯氏制碱法”的主要过程是利用饱和食盐水先后吸收两种气体,生成碳酸氢钠(NaHCO3)和氯化铵(NH4Cl),再加热碳酸氢钠即可制得纯碱。
(1)“侯氏制碱法”的主要过程中需要吸收的两种气体是_____(填字母)。
A. NH3 B. Cl2 C. CO2 D. SO2
(2)加热碳酸氢钠可制得纯碱,同时生成水和二氧化碳,写出该反应的化学方程式:__________________________________。
AC
2NaHCO3 Na2CO3+H2O+CO2↑
4. [中国科技](2024佛山南海一模节选)纳米零价铁(nZVI)除废水中金属离子的性能优越,制备示意图为:
(1)“聚集”过程,铁元素化合价_______(填“升高”“降低”或“不变”)。
不变
(2)“还原”过程,一定量焦炭与232 g Fe3O4作用,生成CO2,反应的化学方程式为____________________________。
(3)“雾化”过程,发生反应:
FeCl3+3H2O===Fe(OH)3+3______(补充完整该化学方程式)。
HCl
Fe3O4+2C 3Fe+2CO2↑
某兴趣小组同学设计如下实验验证质量守恒定律(反应前已调节天平平衡)。
图1
基础巩固
———教材要点梳理
【实验原理】
(1)实验甲、乙、丙、丁的反应原理用化学方程式可表示为____________________、__________________________、____________________________________、
____________________。
2Cu+O2 2CuO
Fe+CuSO4===FeSO4+Cu
2HCl+Na2CO3===2NaCl+H2O+CO2↑
2Mg+O2 2MgO
【实验操作及现象】
(2)实验甲:将装置放在天平上称量,然后再将锥形瓶置于陶土网上,用酒精灯加热,观察到_____________
___________________________,一段时间后
停止加热,待装置冷却后再次称量,可观察
到天平示数______(填“变大”“变小”或
“不变”,后同)。
铜粉由红色变
为黑色,小气球先变大后变瘪
不变
(3)实验乙:锥形瓶内硫酸铜溶液和铁丝接触后,观察到的现象是_________________________________________________,实验结束后再次称量,可观察到天平示数______。
(4)实验丙:烧杯中碳酸钠粉末
和稀盐酸接触后,观察到的现
象是______________________
______,实验结束后再次称量,
可观察到天平示数______。
铁丝表面有红色固体析出,溶液由蓝色逐渐变为浅绿色
不变
固体粉末溶解,有气泡
产生
变小
(5)实验丁:点燃镁条后观察到____________________________
_____________________,实验结束后再次称量固体质量,观察到天平示数改变。
镁条燃烧,发出耀眼的白光,生
成白色固体,放出热量
【实验结论】
(6)上述实验中能直接验证质量守恒定律的是________(填“甲”
“乙”“丙”或“丁”,后同),由此可知,化学反应前后______________不变。
甲、乙
物质的总质量
【实验反思】
(7)实验甲中小气球的作用是______________________________
_______________;该实验结束后,锥形瓶底部有铜粉剩余,对实验结果______(填“有”或“没有”)影响。
调节锥形瓶内的压强、形成密闭
装置(合理即可)
没有
(8)通过上述实验,同学们总结出验证质量守恒定律的条件:
①物质间发生_______(填“物理”或“化学”)反应;②有气体参与或生成的反应必须在__________中进行。
化学
密闭容器
能力提升
——全国视野·新考法
(9)[试剂改进]用上述实验丙验证质量守恒定律,
同学们在不改变装置的情况下设计了如图2所示
三个实验,其中能验证质量守恒定律的是_____(填字母)。
图2
C
同课章节目录
