浙教版初三科学期末简答题专训(高频版)
图片预览


文档简介
初三科学期末简答题专训(高频版)
一、解答题
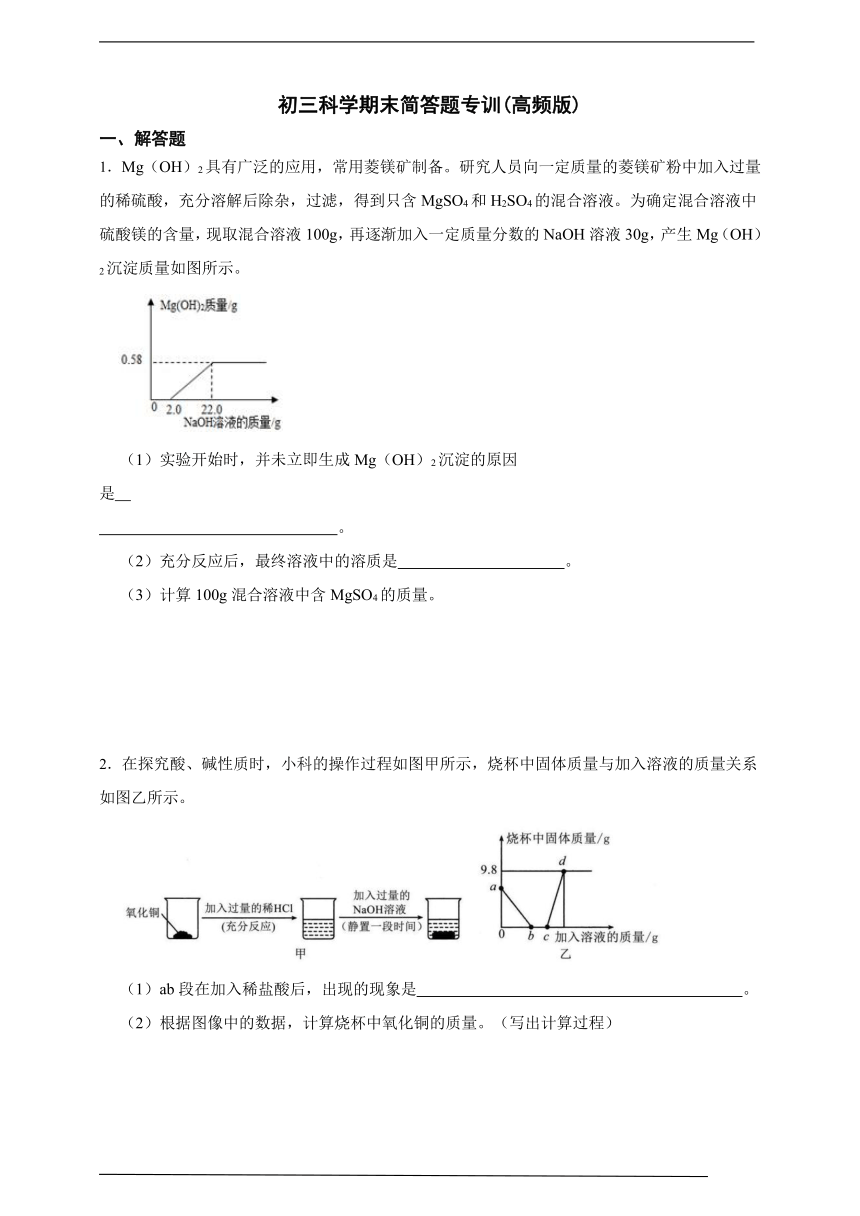
1.Mg(OH)2具有广泛的应用,常用菱镁矿制备。研究人员向一定质量的菱镁矿粉中加入过量的稀硫酸,充分溶解后除杂,过滤,得到只含MgSO4和H2SO4的混合溶液。为确定混合溶液中硫酸镁的含量,现取混合溶液100g,再逐渐加入一定质量分数的NaOH溶液30g,产生Mg(OH)2沉淀质量如图所示。
(1)实验开始时,并未立即生成Mg(OH)2沉淀的原因是 。
(2)充分反应后,最终溶液中的溶质是 。
(3)计算100g混合溶液中含MgSO4的质量。
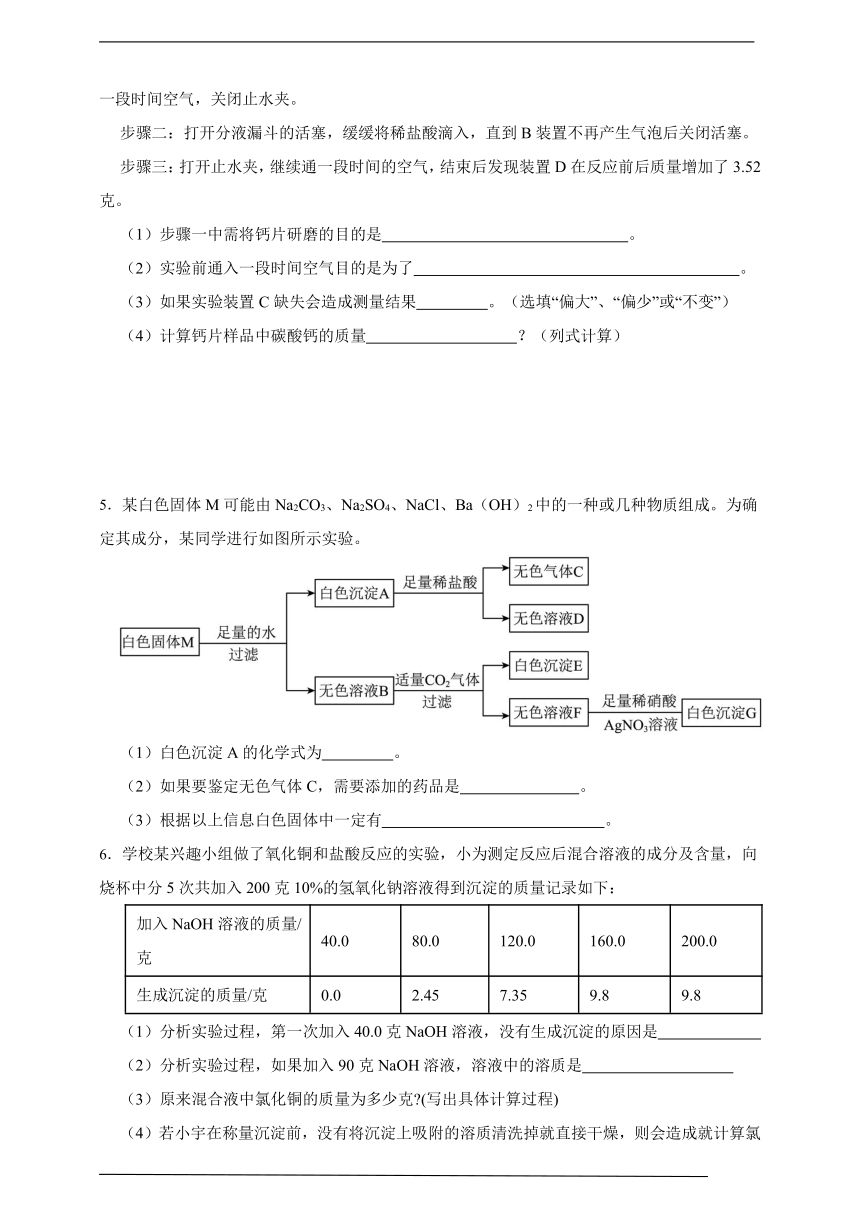
2.在探究酸、碱性质时,小科的操作过程如图甲所示,烧杯中固体质量与加入溶液的质量关系如图乙所示。
(1)ab段在加入稀盐酸后,出现的现象是 。
(2)根据图像中的数据,计算烧杯中氧化铜的质量。(写出计算过程)
3.“低钠盐”(如图)是在精盐中加入适量的食用氯化钾,以降低食盐中钠元素的含量。生产厂家为改善“低钠盐”的味道会添加少量食用硫酸镁。
(1)小科欲测定“低钠盐”中硫酸镁的质量分数:取40g样品于烧杯中加入适量蒸馏水,使其完全溶解;将100g10%的氯化钡溶液分五次加入烧杯中,生成的沉淀经过洗涤、过滤、烘干后称量,沉淀质量如下表(“低钠盐”中其他成分都能溶于水且不参与反应)。
实验次数 第1次 第2次 第3次 第4次 第5次
加入的氯化钡溶液质量/g 20 20 20 20 20
沉淀总质量/g 2.24 m 6.72 6.99 6.99
①上表中m的值为 ▲ 。
②样品中硫酸镁的质量分数为多少?
(2)测量后,小科反思:实验过程中如果沉淀洗涤不干净,会使测量结果偏大。要判断沉淀是否洗涤干净,下列试剂可用来检验的是____。
A.NaOH B.Na2CO3 C.AgNO3 D.Na2SO4
4.钙是人体内最普遍的元素之一,补钙可以预防骨质疏松。某同学为了测定某钙片中CaCO3的含量,设计了如下实验:(已知该钙片中其他成分不与酸反应)
步骤一:实验前称取10克研磨过的固体样品,加入锥形瓶中,打开止水夹,从左侧缓慢通入一段时间空气,关闭止水夹。
步骤二:打开分液漏斗的活塞,缓缓将稀盐酸滴入,直到B装置不再产生气泡后关闭活塞。
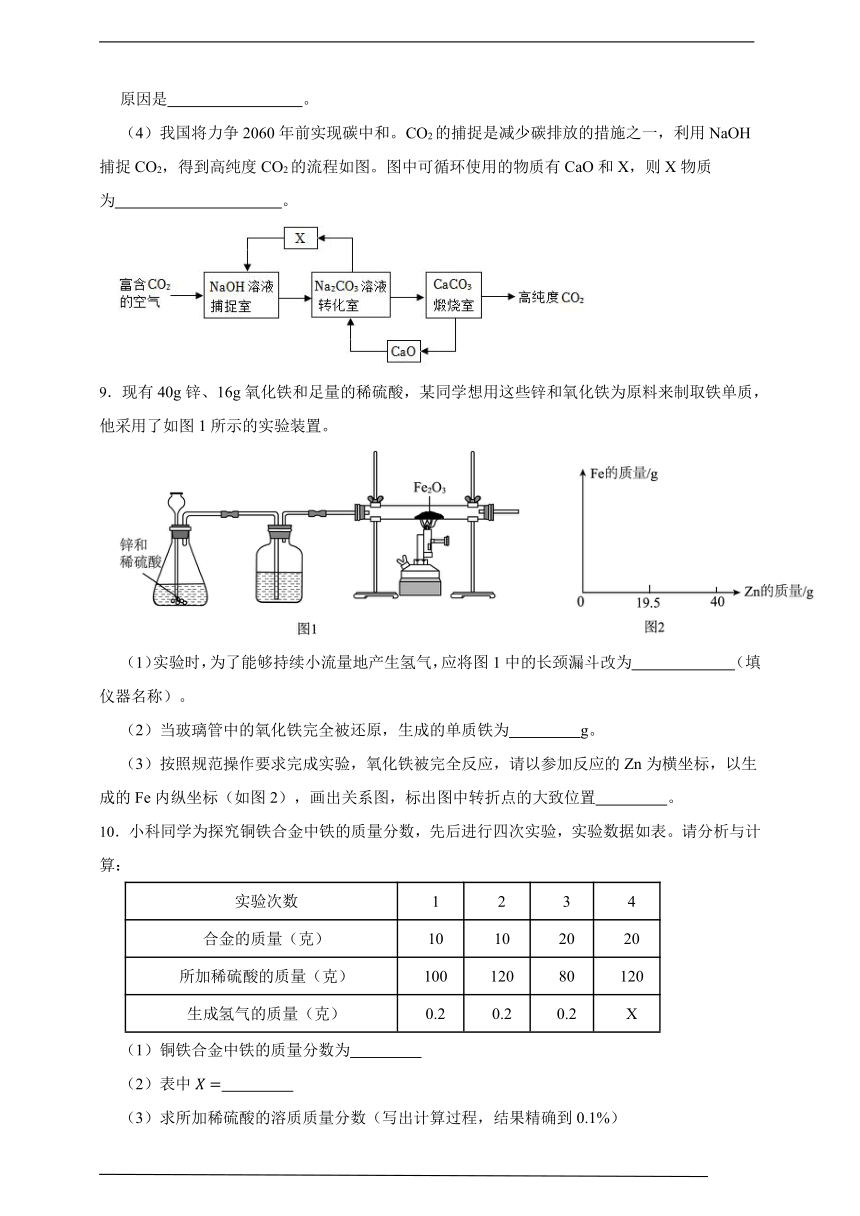
步骤三:打开止水夹,继续通一段时间的空气,结束后发现装置D在反应前后质量增加了3.52克。
(1)步骤一中需将钙片研磨的目的是 。
(2)实验前通入一段时间空气目的是为了 。
(3)如果实验装置C缺失会造成测量结果 。(选填“偏大”、“偏少”或“不变”)
(4)计算钙片样品中碳酸钙的质量 ?(列式计算)
5.某白色固体M可能由Na2CO3、Na2SO4、NaCl、Ba(OH)2中的一种或几种物质组成。为确定其成分,某同学进行如图所示实验。
(1)白色沉淀A的化学式为 。
(2)如果要鉴定无色气体C,需要添加的药品是 。
(3)根据以上信息白色固体中一定有 。
6.学校某兴趣小组做了氧化铜和盐酸反应的实验,小为测定反应后混合溶液的成分及含量,向烧杯中分5次共加入200克10%的氢氧化钠溶液得到沉淀的质量记录如下:
加入NaOH溶液的质量/克 40.0 80.0 120.0 160.0 200.0
生成沉淀的质量/克 0.0 2.45 7.35 9.8 9.8
(1)分析实验过程,第一次加入40.0克NaOH溶液,没有生成沉淀的原因是
(2)分析实验过程,如果加入90克NaOH溶液,溶液中的溶质是
(3)原来混合液中氯化铜的质量为多少克 (写出具体计算过程)
(4)若小宇在称量沉淀前,没有将沉淀上吸附的溶质清洗掉就直接干燥,则会造成就计算氯化铜的含量____
A.偏高 B.偏低 C.不变
7.往200克含有稀硝酸和硝酸钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图(假设生成的气体全部逸出),试分析计算:
(1)a→b段发生反应的化学方程式为 ;
(2)c→d段溶液的pH大于7 的原因是 ;
(3)反应到c点时,所得溶液的溶质质量分数是多少 (写出计算过程,精确到0.1%)
8.新中国成立以来,我国科技发展日新月异,国力的日益强大印证了科技兴则民族兴的道理。
(1)我国“蛟龙”号载人潜水器上使用了钛合金,主要利用了钛合金的化学性质是____(填字母)。
A.硬度大 B.抗腐蚀性能好
C.密度小 D.熔点高
(2)世界最高5G基站在中国,信号覆盖整个珠穆朗玛峰。其发射铁塔表面采用冷喷涂层,其防锈的原理是 。
(3)火星探测器天问一号的控制系统使用了导电性优良的金属铜。铜可采用如下方法制备:
方法一:火法炼铜:Cu2S+O22Cu+SO2
方法二:湿法炼铜:Fe+CuSO4=Cu+FeSO4
上述两种方法中,你认为方法 (填“—”或“二”)更好,
原因是 。
(4)我国将力争2060年前实现碳中和。CO2的捕捉是减少碳排放的措施之一,利用NaOH捕捉CO2,得到高纯度CO2的流程如图。图中可循环使用的物质有CaO和X,则X物质为 。
9.现有40g锌、16g氧化铁和足量的稀硫酸,某同学想用这些锌和氧化铁为原料来制取铁单质,他采用了如图1所示的实验装置。
(1)实验时,为了能够持续小流量地产生氢气,应将图1中的长颈漏斗改为 (填仪器名称)。
(2)当玻璃管中的氧化铁完全被还原,生成的单质铁为 g。
(3)按照规范操作要求完成实验,氧化铁被完全反应,请以参加反应的Zn为横坐标,以生成的Fe内纵坐标(如图2),画出关系图,标出图中转折点的大致位置 。
10.小科同学为探究铜铁合金中铁的质量分数,先后进行四次实验,实验数据如表。请分析与计算:
实验次数 1 2 3 4
合金的质量(克) 10 10 20 20
所加稀硫酸的质量(克) 100 120 80 120
生成氢气的质量(克) 0.2 0.2 0.2 X
(1)铜铁合金中铁的质量分数为
(2)表中
(3)求所加稀硫酸的溶质质量分数(写出计算过程,结果精确到0.1%)
11.黄铜(由铜和锌形成的合金)有较强的耐磨性能,在生活中有广泛的用途。某同学为了测定黄铜屑样品组成,分四组取样品与稀硫酸反应,其实验数据记录如下表:
样品 第1份 第2份 第3份 第4份
取样品质量(g) 25.0 25.0 25.0 25.0
取稀硫酸质量(g) 40.0 80.0 120.0 160.0
产生气体质量(g) 0.2 0.4 m 0.5
试计算:
(1)上表中m的数值是 ;
(2)通过分析上述数据可知,当25克黄铜样品完全反应所需稀硫酸为 克。
(3)求此黄铜的含锌量 ?(列式计算)
12.有一包固体粉末,可能是CaCO3、Na2SO4、CuSO4、Na2CO3口中的一种或多种,某实验小组对其组成
成分进行了以下探究活动。
【资料查阅】Na2CO3溶液与CuSO4溶液混合能产生蓝色沉淀。
【活动与探究】取一定量上述固体粉末,加足量水溶解。
(1)【现象与结论】经上述操作.得到蓝色澄清溶液,则原固体粉末中一定没有 和 *填化学式)。
(2)【探索与拓展】为进一步确定原固体粉末的组成,该实验小组同学先用托盘天平称
取46.2g该粉末,溶于水配成174.6g溶液,再往其中加入溶质质量分数为8%的NaOH溶液,产生沉淀的质量与所加NaOH溶液质量的关系如图所示。据图回答:
①计算产生最大沉淀量时所加NaOH溶液的质量。
②通过计算确定46.2g固体粉末的组成。(回答出物质名称和其质量)
13.图甲中 A 是一种常见的酸,它能与黑色固体 B 反应,B 质量为 8 克。将 NaOH溶液缓缓加入到 C 中,生成的蓝色沉淀 E 与加入 NaOH 溶液的质量关系如图乙所示。在D 中加入 Ba(NO3)2 溶液能生成一种不溶于稀硝酸的白色沉淀。请回答:
(1)A 溶液中溶质的化学式为 ;
(2)NaOH 溶液的溶质质量分数是多少?(列式计算)
(3)C 溶液中加入 NaOH 溶液至恰好完全反应时,所得溶液溶质质量是多少?(列式计算)
14.某工地上用如图所示的滑轮组,匀速提升质量为240kg的物体,在物体上升0.8m的过程中,此滑轮组的机械效率为80%,不计绳重和摩擦,求:
(1)滑轮组做的有用功。
(2)拉力F的大小。
(3)动滑轮的重力。
(4)若用该滑轮组吊起4400N的重物,则此时滑轮组的机械效率为多少?
15.如图所示,小乐用燃气灶烧水。在一个标准大气压下,将一壶初温为20℃的水烧开,消耗了0.02m3的天然气。已知该燃气灶的效率为40%,水的比热容为4.2×103J/(kg ℃),天然气的热值为8.4×107J/m3。求:
(1)0.02m3的天然气完全燃烧所放出的热量;
(2)壶中的水温度的升高是通过 ▲ (选填“做功”或“热传递”)的方式改变了其内能,请求水壶中水吸收的热量;
(3)水壶中水的质量。
16.空气炸锅,因其烹制食物脂肪含量低,美味酥脆,无油烟味,深受广大市民青睐。如图甲所示为某品牌空气炸锅,有低温、中温、高温三档调节。其发热元件为两个电阻,R1=50Ω,R2=200Ω,额定工作电压为220V,发热部分内部电路可简化为图乙所示电路。请回答下列问题:
(1)当S1闭合,S接a处时,炸锅处于中温档工作,求此时电路中的电流。
(2)从中温档调至高温档工作,两个开关应如何操作。
(3)求空气炸锅处于高温档时的实际功率。
17.本届杭州亚运会科技满满,其中两只“呆萌”的四足机械狗成为亮点,它们变身铁饼“搬运工”,这是世界首次使用机械狗在赛场搬运体育器械。工作人员只需将铁饼放置在卡槽上,便可在第一时间操控机械狗将铁饼运输回起点处。
(1)机械狗在平地上运输铁饼,是将电能转化为 。
(2)已知机械狗的牵引力为100牛,将铁饼从65米的落地点径直运到起点用时13秒,求该机械狗的功率。
(3)机械狗除了能在平地上行走外,它还能进行负重登楼。已知机械狗自重12千克,现携带重为2千克的标准铁饼上五楼。试通过计算,求整个过程中机械狗克服重力所做的功。(每层楼高3米)
18.一辆在水平路面上沿直线匀速行驶的货车,行驶时所受的阻力为车总重的0.1,货车(含驾驶员)空载时重为1.5×104N.
(1)求货车空载行驶时所受的阻力大小;
(2)求货车以36km/h的速度空载匀速行驶时,10s内货车牵引力做的功;
(3)当货车以80kW的额定功率、72km/h的速度匀速行驶时,求货车最多可装载多重的货物.
19.如图为我国自行研制“寰岛蛟龙1号”载人潜水器,它的研制成功填补了国内观光潜水器的空白,具有里程碑的意义。该观光潜水器最大下潜深度40米,未搭乘乘客时的质量为23.9吨。
(1)该潜水器在水面下10米到20米的下潜过程中,受到水的压强如何变化? 。
(2)潜水器在下潜前,静止在海面上,若此时潜水器上有5人,总质量为300千克,计算该潜水器排开水的体积为多少?(ρ海水取1×103千克/米3)
(3)若潜水器在水下运动,所受海水阻力与速度的关系如图所示。当它在水下以0.2米/秒的水平速度匀速前进了10秒,则在此过程中潜水器的水平推力做了多少功?
20.在一次学农活动中,小江用一根扁担挑起了两桶水,水桶挂在扁担两端,扁担保持水平状态(扁担和水桶的质量,手对扁担和水桶的作用力均忽略不计)。扁担的A处挂的水重20牛,AB之间的距离为1.2米,肩上支点O与A的距离为0.9米。
(1)扁担B处挂的水受到的重力是多少
(2)小江肩膀受到扁担的压力大小是多少
(3)到达某处后,小江将B处的水倒出20牛,在不改变水桶悬挂位置的情况下,需要将肩上支点O向A移动多少距离,才能再次平衡
21.如图是一个定滑轮(质量为)和一个动滑轮(质量为)组成的滑轮组。用该滑轮组在4秒内将重物竖直向上匀速提升,所用拉力F=100N,不考虑绳重和摩擦的影响。
(1)在该滑轮组中滑轮的作用是: 。
(2)拉力F做功的功率为 。
(3)在提升该重物时滑轮组的机械效率为 。
22.在水平地面上有一长方体木箱。小林用水平推力F把木箱向前推,如图甲所示。此过程中,推力F随时间t的变化情况如图乙所示,木块前进的速度v的大小随时间t的变化情况如图丙所示。
(1)0至1秒内,推力F对木箱是否做功 (选填“是”或“否”);
(2)1至3秒内,木箱所受的摩擦力为 ;
(3)3至5秒内,推力F做的功为 。
23.如图所示,小科骑着电动平衡车,在水平路面上沿直线匀速行驶。若小科的质量为60kg,电动平衡车的质量是20kg,行驶时电动平衡车受到的阻力为车总重的0.05倍,求:
(1)电动平衡车行驶时所受的阻力;
(2)若小科在10分钟内,行驶了3千米,求电动平衡车牵引力做的功;
(3)当电动平衡车以100W的恒定功率匀速行驶时,求电动平衡车行驶的速度。
24.如图所示为太阳能LED路灯,白天有日照时,电池板将太阳能转化为电能并储存在锂电池中,晚上锂电池给LED路灯系统供电提供照明。已知:太阳能电池板输出参数为“20V 5A”,有效面积为0.5m2;正常日照时,太阳每秒辐射到每平方米电池板上的能量为
(1) 若每天正常日照8h,锂电池一天可以储存多少电能
(2) 该太阳能电池板的光电转换效率为多少
(3)若路灯每晚从20:00持续工作到凌晨5:00,为了节能,LED 路灯系统安装雷达感应装置,20:00至24:00人群活动密集时功率为20W,24:00至凌晨5:00夜深人静时功率为4 W。已知锂电池最多能储存, 的电能,则充满电可以提供LED路灯系统在阴雨天(无日照)持续工作多少个晚上
25.如图甲所示的电饭锅,额定电压为220V,加热功率为1210W。从铭牌上可知该电饭锅能效等级为三级,简化电路图如图乙所示,有加热和保温两挡,由开关S调节,其中R1和R2均为发热电阻,且阻值不随着温度的变化而改变。求:
(1)电阻R1的阻值:
(2)小明利用电能表测量电饭锅的保温功率,他关闭家里的其它用电器,让电饭锅处于“保温”状态下正常工作,观察在10min内电能表转盘转了30圈。求该电饭锅保温功率。
(3)小明上网查询了解,国家标准中规定电饭锅在该加热功率下正常工作时,三级能效的热效率值范围为81%≤η<86%(热效率是指装置的有效输出能量与输入能量的比值)。他用学过的知识对电饭锅进行测试:在加热状态下,将温度为23℃、质量为2.2kg的水加热到100℃,电饭锅正常工作用时700s。已知c水=4.2×103J/(kg·℃),请你通过计算帮助小明判断该电饭锅的热效率值是否达到三级能效。
26.如图-1,是某型号电暖器。它有高温、低温两个挡位,其简化电路图如图-2所示。R1和R2均为发热电阻,其部分参数如图表所示。请完成下列问题:
额定电压 220V
额定功率 高温挡 2200W
低温挡 1100W
(1)当开关S1、S2均闭合时,电暖器处于 挡;
(2)求该电暖器在低温挡正常工作时,电路中的电流大小;
(3)在某次用电高峰期,小金用如图-3所示的电力监测仪,测出该电暖器在低温挡工作时的实际电压为210V,实际功率为900W。小金由此认为实际功率小于额定功率,只是因为实际电压小于额定电压造成的。小兰和小江却一致认为小金的观点不全面。请你根据题中信息和所学知识,解释实际功率小于额定功率的原因。
27. 人体各个系统协调配合才能使各项生命活动正常进行,如图甲是人体相关生理过程的示意图,其中①②表示气体,③④表示尿液形成过程。请根据图回答下列问题:
(1) 青少年要合理膳食,小琳的早餐既丰富又营养,有牛奶、麦香面包和苹果,这些食物被消化吸收的主要场所是 ,其中牛奶中的蛋白质被彻底消化为 才能被吸收。
(2)一个健康成人每天形成的原尿大约有 150升,而每天排出的尿液一般约为1.5升,这与图中④表示的 的重吸收作用有关。
(3)①表示 进入血液循环后,最先到达心脏的哪个腔 (填结构名称)。
(4)在抽血或输液时,护士要将针头刺入部位的 (填“近心端”或“远心端”)用橡皮管捆扎起来便于针头刺入血管。
(5)某人患急性肾炎,尿液中检测出血细胞,这可能是图甲中的③表示的肾小球的 作用发生障碍;静脉注射青霉素治疗,在心脏中最先发现药物的是图乙中的标号 。
28.运动需要多个器官、系统协调配合。右图是某同学踢足球时心脏与相关器官X的关系示意图,据图回答下列问题。
(1) 运动后补充的糖类被小肠吸收进入血液,首先到达心脏的 (填字母)。心脏内有防止血液倒流的 ,以保证血液将营养物质运送到骨骼肌细胞,供运动所需。
(2)若血液从B出发,经血管①→X后,变为含氧丰富的动脉血,则X代表的器官是 ,血液经血管② 回到C左心房。
(3)该同学进食一段时间后,血液中葡萄糖的浓度会暂时上升,此时X代表的内分泌腺是 ,其分泌的激素增多,以调节葡萄糖在人体内的吸收、利用和转化。
(4)人体生命活动中产生的尿素等废物,主要通过尿液排出体外。尿的形成要经过肾小球和肾小囊内壁的滤过作用和肾小管的 作用。
(5)如果你是一个足球迷,看一场激烈比赛时大脑皮层会特别兴奋,因而促使肾上腺分泌较多的肾上腺素,使人心跳加快、血压升高、面红耳赤。以上生命活动主要受到 系统的影响,但也受到激素调节的影响。
29.小明同学在使用显微镜观察小鱼尾鳍内血液流动的实验时,看到了如图乙所示的视野。请结合学过的知识回答:
(1)小明使用显微镜时因粗心导致刚开始的视野中一片黑暗,他很可能是忘记了 。
(2)图甲中,用湿棉絮将小鱼头部的鳃盖和躯干部包裹起来,观察过程中,时常用滴管往棉絮上滴水以保持湿润,目的是 ,尽量使小鱼少受伤害。
(3) 在观察小鱼尾鳍的实验中,小明应该选用 (填“高”或“低”)倍物镜进行观察。
(4)“3”所指血管位于视野的右下方,小明想把它移到视野的中央观察,他应该往 移动玻片标本。
(5)图乙中涉及了三种血管,人体也同样具有这三种血管,图中数字可代表人体相应的血管。若某人患肺炎,医生会往他手背上的“青筋”注射消炎药,则消炎药通过三种血管的先后顺序是 (用图中数字和“→”表示)。
30. 动物的能量都来自食物,各种食物中所含的能量是不同的。某同学要比较花生仁、大米、牛肉干在体内所能提供的能量的大小,采用了下列实验方法:
①分别称取1克花生仁、大米、牛肉干,并将它们分别粉碎。
②在如图所示装置的试管中加入10毫升水。
③测量并记录加热前的水温。
④将粉碎后的花生仁放在燃烧匙中,然后在酒精灯上加热到自行燃烧,马上放于试管下方,使其完全燃烧干净。
⑤在同样条件下,再分别用大米和牛肉干重复以上实验。
(1)上述实验步骤尚不完整,请补充实验步骤⑥: 。
(2)这个实验误差较大,为了减小误差,可采用 的措施。
(3) 花生仁含有的主要物质的化学式可表示为CaHbOc,如果要验证花生仁燃烧的生成物中有水和二氧化碳,可让产物依次通过____(填字母)。
A.无水硫酸铜和澄清石灰水 B.澄清石灰水和无水硫酸铜
31.如图表示人体循环系统中部分结构示意图,分析图像,回答下列问题。
(1)甲图为心脏结构示意图,①与②、③与④之间,能控制血液定向流动的结构是 。
(2)若静脉注射消炎药,则药物通过心脏的途径是____。
A.①→②→③→④ B.③→④→①→②
C.②→①→④→③ D.④→③→②→①
(3)图乙为某部位毛细血管示意图,根据血流方向,血管A名称是 。
(4)当血液从A流向C的过程中,血液中气体的含量发生了变化,如图丙所示,则乙图中的B在人体哪个器官内?
32.球形火焰实验、奇妙乒乓球实验、动量守恒实验以及又见陀螺实验,这些都是我们熟悉的“天宫课堂”的精彩实验。
(1)空间站利用电解水来产生人体呼吸所需要的氧气,在电解水过程中的能量转化是将电能转化为 能。同时还配备有二氧化碳还原系统,在催化剂作用下,将电解水产生的氢气和人体产生的二氧化碳进行反应,产生水和甲烷(化学式为),请写出上述反应的化学方程式: 。
(2)以下科学实验能在太空站完成的是:____。
A.测定小灯泡额定功率 B.验证植物的根具有向地性
(3)航天员为了对抗失重对身体造成的影响,需要加强体育锻炼,常见的器械有弹力带和太空自行车,他们运动过后也会感觉到肌肉酸胀,是因为肌肉细胞内发生了 (选填“有氧呼吸”或“无氧呼吸”),该过程属于 (选填“同化作用”或“异化作用”)。
答案解析部分
1.【答案】(1)MgSO4和H2SO4的混合溶液的烧杯中滴加NaOH溶液时,氢氧化钠先与硫酸反应,后与硫酸镁反应生成氢氧化镁沉淀和硫酸钠
(2)硫酸钠、氢氧化钠
(3)解:设100g混合溶液中含MgSO4的质量为x
MgSO4+2NaOH= Mg(OH)2↓+Na2SO4
120 58
x 0.58g
=
解得:x=1.2g
答:100g混合溶液中含MgSO4的质量为1.2g。
2.【答案】(1)黑色固体逐渐消失,溶液由无色变为蓝色
(2)解:设溶液中的质量为。
设烧杯中CuO的质量为。
3.【答案】(1)解:①4.48;
②设样品中硫酸镁的质量为
(2)A;B;C;D
4.【答案】(1)增大接触面积,加快反应速率
(2)排除装置内的二氧化碳对实验结果的干扰
(3)偏大
(4)设参加反应的碳酸钙质量为x
解得:x=8g
答:钙片样品中碳酸钙的质量8g。
5.【答案】(1)BaCO3
(2)澄清石灰水
(3)Na2CO3、NaCl、Ba(OH)2
6.【答案】(1)溶液为盐酸和氯化铜的混合溶液,氢氧化钠先和盐酸反应生成氯化钠和水
(2)氯化铜和氯化钠
(3)设原来混合溶液中氯化铜的质量为x,
CuCl2+2NaOH=2NaCl+Cu(OH)2↓
135 98
x 9.8g
x=13.5g
答:原来混合溶液中氯化铜的质量为13.5g。
(4)A
7.【答案】(1)Na2CO3+2HNO32NaNO3+H2O+CO2↑
(2)碳酸钠溶液过量,碳酸钠溶液显碱性
(3)解:设 HNO3与 Na2CO3反应时,生成 NaNO3质量为x,生成 CO2气体质量为y,则
Na2CO3+2HNO3=2NaNO3+H2O+CO2↑
106 170 44
50g×21.2% X Y
X=17g Y=4.4g
设 与 反应生成 质量为 z,生成CaCO3质量为m,则
Na2CO3+ Ca(NO3)2=CaCO3↓+2NaNO3
106 100 170
100g×21.2% m z
m=20g z=34g
所得NaNO3溶液的溶质质量分数:
8.【答案】(1)B
(2)隔绝氧气和水
(3)二;能耗低和污染
(4)氢氧化钠(NaOH)
9.【答案】(1)分液漏斗
(2)11.2
(3)
10.【答案】(1)56%
(2)0.3
(3)12.25%
11.【答案】(1)0.5
(2)100
(3)设:此黄铜的含锌量为x。
x=65%
答:此黄铜的含锌量为65%。
12.【答案】(1)CaCO3;Na2CO3
(2)①设生成19.6g氢氧化铜沉淀需要NaOH溶液的质量为x,需要硫酸铜的质量为y
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
160 80 98
y x×8% 19.6g
x=200g
y=32.0g
②因此46.2g的粉末中含有硫酸钠,且Na2SO4的质量=46.2g-32g=14.2g
46.2g固体粉末由14.2g硫酸钠和32.0g硫酸铜组成。
13.【答案】(1)H2SO4
(2)根据图像可知,反应生成沉淀氢氧化铜的质量为9.8g,
设与CuSO4反应的NaOH的质量为x,同时生成Na2SO4的质量为y,
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
80 98 142
x 9.8g y
;
解得:x=8g,y=14.2g;
所用氢氧化钠溶液中溶质的质量分数为:;
(3)设硫酸与氢氧化钠反应生成硫酸钠质量为z,
H2SO4+2NaOH=Na2SO4+2H2O
80 142
60g×20% z
;
解得:z=21.3g
所得溶液中溶质的质量为:21.3g+14.2g=35.5g
14.【答案】(1)解:W有=Gh=2400N×0.8m=1920J
(2)解:根据可知,
(3)解:根据();
(4)解:
15.【答案】(1)qev:Q放=Vq=0.02m3×8.4×107J/m3=1.68×106J
(2)解:热传递;
由得水吸收的热量:
(3)解:在一个标准大气压下,水的沸点为100℃,即水的末温,
由得水的质量:
16.【答案】(1)1.1A
(2)S1闭合,S接b处
(3)高温挡正常工作时,R1、R2并联,
并联电路总功率等于各部分功率之和,即高温挡功率。
17.【答案】(1)动能
(2)W=FS=100牛×65米=6500焦,P==500瓦
(3)W=Gh=mgh=(12千克+2千克)×10牛/千克×4×3米=1680焦
18.【答案】(1)解:货车空载行驶时所受的阻力大小:
f=0.1G=0.1×1.5×104N=1.5×103N;
(2)解:V=36km/h=10m/s
由s=vt=10m/s×10s=100m,
∵汽车匀速行驶,
∴牵引力F=f=1.5×103N,
10s内货车牵引力做的功:
W=Fs=1.5×103N×100m=1.5×105J;
(3)解:v=72km/h=20m/s
由p=FvF=p/v=80000w/20m/s=4000N
∵汽车匀速行驶,
∴此时汽车受到的阻力:
f=F=4000N,
∵f=0.1G,
∴货车总重:
G'=f/0.1=4×104N,
货车最多可装载货物的重:
G货=G'-G=4×104N-1.5×104N=2.5×104N.
19.【答案】增大;24.2m3;500J
20.【答案】(1)60N;(2)80N;(3)0.1m
21.【答案】(1)改变力的方向
(2)200
(3)90%
22.【答案】(1)否
(2)200N
(3)400J
23.【答案】(1)解:G总=(m车+m人)g=(20kg+60kg)×10N/kg=800N
f=0.05G总=0.05×800N=40N
答:电动平衡车行驶时所受的阻力为40N.
(2)解:F=f=40N
W=F·s=40N×3000m=1.2×105J
答:电动平衡车牵引力做的功为1.2×105J.
(3)解:v===2.5m/s
答:动平衡车行驶的速度为2.5m/s.
24.【答案】(1)若每天正常日照8h,则锂电池一天可以储存的电能W=UIt=20V×5A×8×3600s=2.88×106J
(2)由太阳每秒辐射到每平方米电池板上的能量为0.8×103 J 知: 由太阳能电池板输出参数为“20 V 5 A”知: 5A×1 s=100 J,根据效率公式
(3)LED路灯系统每个晚上所消耗能量W'=20W×4×3600s+4W×5×3600s=3.6×105 J,充满电的锂电池可以提供LED路灯系统在阴雨天(无日照)持续工作晚上的个数为 个
25.【答案】(1)由电路图知,S断开时两电阻串联,电路中电阻较大,功率较小,为保温状态,
当S闭合时,只有R1接入电路中,电阻较小,功率较大,为加热状态,
则R1的电阻:。
(2)“3000r/(kW h)”表示每消耗1kW h电能,电能表转盘转3000圈,
只让电饭煲在“保温”状态下工作,转盘在10min内转了30转,
则电饭锅消耗的电能为:,
电饭锅处于“保温”状态时的功率为:。
(3)该电饭锅的热效率值达到三级能效
水吸收的热量为:
Q吸=c水mΔt=4.2×103J/(kg ℃)×2.2kg×(100℃-23℃)=7.1148×105J;
用时700s消耗的电能为:
W'=P加热t'=1210W×700s=8.47×105J,
该电饭锅的热效率为:,
故该电饭锅的热效率值达到三级能效。
26.【答案】(1)高温挡
(2)电暖器在低温挡正常工作时的功率为1100W,电路中的电流大小为
(3)由题意知,用电高峰期电暖器在低温挡工作时,实际电压为210V,实际功率为900W,根据P=U2/R可得,此时R1的阻值为49Ω。由此可知,原电阻发生了变化。所以造成实际功率小于额定功率的原因,不只是因为实际电压小于额定电压造成的,用电器电阻变大也是其中一个原因。
27.【答案】(1)小肠;氨基酸
(2)肾小管
(3)氧气;左心房
(4)近心端
(5)滤过;C
28.【答案】(1)A;瓣膜
(2)肺;肺静脉
(3)胰岛
(4)重吸收
(5)神经
29.【答案】(1)对光
(2)保证小鱼正常呼吸
(3)低
(4)右下方
(5)3→1→2
30.【答案】(1)测量并记录加热后水的温度
(2)在相对密闭的环境中做实验
(3)A
31.【答案】(1)房室瓣
(2)B
(3)动脉
(4)肺
32.【答案】(1)化学;
(2)A
(3)无氧呼吸;异化作用
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
一、解答题
1.Mg(OH)2具有广泛的应用,常用菱镁矿制备。研究人员向一定质量的菱镁矿粉中加入过量的稀硫酸,充分溶解后除杂,过滤,得到只含MgSO4和H2SO4的混合溶液。为确定混合溶液中硫酸镁的含量,现取混合溶液100g,再逐渐加入一定质量分数的NaOH溶液30g,产生Mg(OH)2沉淀质量如图所示。
(1)实验开始时,并未立即生成Mg(OH)2沉淀的原因是 。
(2)充分反应后,最终溶液中的溶质是 。
(3)计算100g混合溶液中含MgSO4的质量。
2.在探究酸、碱性质时,小科的操作过程如图甲所示,烧杯中固体质量与加入溶液的质量关系如图乙所示。
(1)ab段在加入稀盐酸后,出现的现象是 。
(2)根据图像中的数据,计算烧杯中氧化铜的质量。(写出计算过程)
3.“低钠盐”(如图)是在精盐中加入适量的食用氯化钾,以降低食盐中钠元素的含量。生产厂家为改善“低钠盐”的味道会添加少量食用硫酸镁。
(1)小科欲测定“低钠盐”中硫酸镁的质量分数:取40g样品于烧杯中加入适量蒸馏水,使其完全溶解;将100g10%的氯化钡溶液分五次加入烧杯中,生成的沉淀经过洗涤、过滤、烘干后称量,沉淀质量如下表(“低钠盐”中其他成分都能溶于水且不参与反应)。
实验次数 第1次 第2次 第3次 第4次 第5次
加入的氯化钡溶液质量/g 20 20 20 20 20
沉淀总质量/g 2.24 m 6.72 6.99 6.99
①上表中m的值为 ▲ 。
②样品中硫酸镁的质量分数为多少?
(2)测量后,小科反思:实验过程中如果沉淀洗涤不干净,会使测量结果偏大。要判断沉淀是否洗涤干净,下列试剂可用来检验的是____。
A.NaOH B.Na2CO3 C.AgNO3 D.Na2SO4
4.钙是人体内最普遍的元素之一,补钙可以预防骨质疏松。某同学为了测定某钙片中CaCO3的含量,设计了如下实验:(已知该钙片中其他成分不与酸反应)
步骤一:实验前称取10克研磨过的固体样品,加入锥形瓶中,打开止水夹,从左侧缓慢通入一段时间空气,关闭止水夹。
步骤二:打开分液漏斗的活塞,缓缓将稀盐酸滴入,直到B装置不再产生气泡后关闭活塞。
步骤三:打开止水夹,继续通一段时间的空气,结束后发现装置D在反应前后质量增加了3.52克。
(1)步骤一中需将钙片研磨的目的是 。
(2)实验前通入一段时间空气目的是为了 。
(3)如果实验装置C缺失会造成测量结果 。(选填“偏大”、“偏少”或“不变”)
(4)计算钙片样品中碳酸钙的质量 ?(列式计算)
5.某白色固体M可能由Na2CO3、Na2SO4、NaCl、Ba(OH)2中的一种或几种物质组成。为确定其成分,某同学进行如图所示实验。
(1)白色沉淀A的化学式为 。
(2)如果要鉴定无色气体C,需要添加的药品是 。
(3)根据以上信息白色固体中一定有 。
6.学校某兴趣小组做了氧化铜和盐酸反应的实验,小为测定反应后混合溶液的成分及含量,向烧杯中分5次共加入200克10%的氢氧化钠溶液得到沉淀的质量记录如下:
加入NaOH溶液的质量/克 40.0 80.0 120.0 160.0 200.0
生成沉淀的质量/克 0.0 2.45 7.35 9.8 9.8
(1)分析实验过程,第一次加入40.0克NaOH溶液,没有生成沉淀的原因是
(2)分析实验过程,如果加入90克NaOH溶液,溶液中的溶质是
(3)原来混合液中氯化铜的质量为多少克 (写出具体计算过程)
(4)若小宇在称量沉淀前,没有将沉淀上吸附的溶质清洗掉就直接干燥,则会造成就计算氯化铜的含量____
A.偏高 B.偏低 C.不变
7.往200克含有稀硝酸和硝酸钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图(假设生成的气体全部逸出),试分析计算:
(1)a→b段发生反应的化学方程式为 ;
(2)c→d段溶液的pH大于7 的原因是 ;
(3)反应到c点时,所得溶液的溶质质量分数是多少 (写出计算过程,精确到0.1%)
8.新中国成立以来,我国科技发展日新月异,国力的日益强大印证了科技兴则民族兴的道理。
(1)我国“蛟龙”号载人潜水器上使用了钛合金,主要利用了钛合金的化学性质是____(填字母)。
A.硬度大 B.抗腐蚀性能好
C.密度小 D.熔点高
(2)世界最高5G基站在中国,信号覆盖整个珠穆朗玛峰。其发射铁塔表面采用冷喷涂层,其防锈的原理是 。
(3)火星探测器天问一号的控制系统使用了导电性优良的金属铜。铜可采用如下方法制备:
方法一:火法炼铜:Cu2S+O22Cu+SO2
方法二:湿法炼铜:Fe+CuSO4=Cu+FeSO4
上述两种方法中,你认为方法 (填“—”或“二”)更好,
原因是 。
(4)我国将力争2060年前实现碳中和。CO2的捕捉是减少碳排放的措施之一,利用NaOH捕捉CO2,得到高纯度CO2的流程如图。图中可循环使用的物质有CaO和X,则X物质为 。
9.现有40g锌、16g氧化铁和足量的稀硫酸,某同学想用这些锌和氧化铁为原料来制取铁单质,他采用了如图1所示的实验装置。
(1)实验时,为了能够持续小流量地产生氢气,应将图1中的长颈漏斗改为 (填仪器名称)。
(2)当玻璃管中的氧化铁完全被还原,生成的单质铁为 g。
(3)按照规范操作要求完成实验,氧化铁被完全反应,请以参加反应的Zn为横坐标,以生成的Fe内纵坐标(如图2),画出关系图,标出图中转折点的大致位置 。
10.小科同学为探究铜铁合金中铁的质量分数,先后进行四次实验,实验数据如表。请分析与计算:
实验次数 1 2 3 4
合金的质量(克) 10 10 20 20
所加稀硫酸的质量(克) 100 120 80 120
生成氢气的质量(克) 0.2 0.2 0.2 X
(1)铜铁合金中铁的质量分数为
(2)表中
(3)求所加稀硫酸的溶质质量分数(写出计算过程,结果精确到0.1%)
11.黄铜(由铜和锌形成的合金)有较强的耐磨性能,在生活中有广泛的用途。某同学为了测定黄铜屑样品组成,分四组取样品与稀硫酸反应,其实验数据记录如下表:
样品 第1份 第2份 第3份 第4份
取样品质量(g) 25.0 25.0 25.0 25.0
取稀硫酸质量(g) 40.0 80.0 120.0 160.0
产生气体质量(g) 0.2 0.4 m 0.5
试计算:
(1)上表中m的数值是 ;
(2)通过分析上述数据可知,当25克黄铜样品完全反应所需稀硫酸为 克。
(3)求此黄铜的含锌量 ?(列式计算)
12.有一包固体粉末,可能是CaCO3、Na2SO4、CuSO4、Na2CO3口中的一种或多种,某实验小组对其组成
成分进行了以下探究活动。
【资料查阅】Na2CO3溶液与CuSO4溶液混合能产生蓝色沉淀。
【活动与探究】取一定量上述固体粉末,加足量水溶解。
(1)【现象与结论】经上述操作.得到蓝色澄清溶液,则原固体粉末中一定没有 和 *填化学式)。
(2)【探索与拓展】为进一步确定原固体粉末的组成,该实验小组同学先用托盘天平称
取46.2g该粉末,溶于水配成174.6g溶液,再往其中加入溶质质量分数为8%的NaOH溶液,产生沉淀的质量与所加NaOH溶液质量的关系如图所示。据图回答:
①计算产生最大沉淀量时所加NaOH溶液的质量。
②通过计算确定46.2g固体粉末的组成。(回答出物质名称和其质量)
13.图甲中 A 是一种常见的酸,它能与黑色固体 B 反应,B 质量为 8 克。将 NaOH溶液缓缓加入到 C 中,生成的蓝色沉淀 E 与加入 NaOH 溶液的质量关系如图乙所示。在D 中加入 Ba(NO3)2 溶液能生成一种不溶于稀硝酸的白色沉淀。请回答:
(1)A 溶液中溶质的化学式为 ;
(2)NaOH 溶液的溶质质量分数是多少?(列式计算)
(3)C 溶液中加入 NaOH 溶液至恰好完全反应时,所得溶液溶质质量是多少?(列式计算)
14.某工地上用如图所示的滑轮组,匀速提升质量为240kg的物体,在物体上升0.8m的过程中,此滑轮组的机械效率为80%,不计绳重和摩擦,求:
(1)滑轮组做的有用功。
(2)拉力F的大小。
(3)动滑轮的重力。
(4)若用该滑轮组吊起4400N的重物,则此时滑轮组的机械效率为多少?
15.如图所示,小乐用燃气灶烧水。在一个标准大气压下,将一壶初温为20℃的水烧开,消耗了0.02m3的天然气。已知该燃气灶的效率为40%,水的比热容为4.2×103J/(kg ℃),天然气的热值为8.4×107J/m3。求:
(1)0.02m3的天然气完全燃烧所放出的热量;
(2)壶中的水温度的升高是通过 ▲ (选填“做功”或“热传递”)的方式改变了其内能,请求水壶中水吸收的热量;
(3)水壶中水的质量。
16.空气炸锅,因其烹制食物脂肪含量低,美味酥脆,无油烟味,深受广大市民青睐。如图甲所示为某品牌空气炸锅,有低温、中温、高温三档调节。其发热元件为两个电阻,R1=50Ω,R2=200Ω,额定工作电压为220V,发热部分内部电路可简化为图乙所示电路。请回答下列问题:
(1)当S1闭合,S接a处时,炸锅处于中温档工作,求此时电路中的电流。
(2)从中温档调至高温档工作,两个开关应如何操作。
(3)求空气炸锅处于高温档时的实际功率。
17.本届杭州亚运会科技满满,其中两只“呆萌”的四足机械狗成为亮点,它们变身铁饼“搬运工”,这是世界首次使用机械狗在赛场搬运体育器械。工作人员只需将铁饼放置在卡槽上,便可在第一时间操控机械狗将铁饼运输回起点处。
(1)机械狗在平地上运输铁饼,是将电能转化为 。
(2)已知机械狗的牵引力为100牛,将铁饼从65米的落地点径直运到起点用时13秒,求该机械狗的功率。
(3)机械狗除了能在平地上行走外,它还能进行负重登楼。已知机械狗自重12千克,现携带重为2千克的标准铁饼上五楼。试通过计算,求整个过程中机械狗克服重力所做的功。(每层楼高3米)
18.一辆在水平路面上沿直线匀速行驶的货车,行驶时所受的阻力为车总重的0.1,货车(含驾驶员)空载时重为1.5×104N.
(1)求货车空载行驶时所受的阻力大小;
(2)求货车以36km/h的速度空载匀速行驶时,10s内货车牵引力做的功;
(3)当货车以80kW的额定功率、72km/h的速度匀速行驶时,求货车最多可装载多重的货物.
19.如图为我国自行研制“寰岛蛟龙1号”载人潜水器,它的研制成功填补了国内观光潜水器的空白,具有里程碑的意义。该观光潜水器最大下潜深度40米,未搭乘乘客时的质量为23.9吨。
(1)该潜水器在水面下10米到20米的下潜过程中,受到水的压强如何变化? 。
(2)潜水器在下潜前,静止在海面上,若此时潜水器上有5人,总质量为300千克,计算该潜水器排开水的体积为多少?(ρ海水取1×103千克/米3)
(3)若潜水器在水下运动,所受海水阻力与速度的关系如图所示。当它在水下以0.2米/秒的水平速度匀速前进了10秒,则在此过程中潜水器的水平推力做了多少功?
20.在一次学农活动中,小江用一根扁担挑起了两桶水,水桶挂在扁担两端,扁担保持水平状态(扁担和水桶的质量,手对扁担和水桶的作用力均忽略不计)。扁担的A处挂的水重20牛,AB之间的距离为1.2米,肩上支点O与A的距离为0.9米。
(1)扁担B处挂的水受到的重力是多少
(2)小江肩膀受到扁担的压力大小是多少
(3)到达某处后,小江将B处的水倒出20牛,在不改变水桶悬挂位置的情况下,需要将肩上支点O向A移动多少距离,才能再次平衡
21.如图是一个定滑轮(质量为)和一个动滑轮(质量为)组成的滑轮组。用该滑轮组在4秒内将重物竖直向上匀速提升,所用拉力F=100N,不考虑绳重和摩擦的影响。
(1)在该滑轮组中滑轮的作用是: 。
(2)拉力F做功的功率为 。
(3)在提升该重物时滑轮组的机械效率为 。
22.在水平地面上有一长方体木箱。小林用水平推力F把木箱向前推,如图甲所示。此过程中,推力F随时间t的变化情况如图乙所示,木块前进的速度v的大小随时间t的变化情况如图丙所示。
(1)0至1秒内,推力F对木箱是否做功 (选填“是”或“否”);
(2)1至3秒内,木箱所受的摩擦力为 ;
(3)3至5秒内,推力F做的功为 。
23.如图所示,小科骑着电动平衡车,在水平路面上沿直线匀速行驶。若小科的质量为60kg,电动平衡车的质量是20kg,行驶时电动平衡车受到的阻力为车总重的0.05倍,求:
(1)电动平衡车行驶时所受的阻力;
(2)若小科在10分钟内,行驶了3千米,求电动平衡车牵引力做的功;
(3)当电动平衡车以100W的恒定功率匀速行驶时,求电动平衡车行驶的速度。
24.如图所示为太阳能LED路灯,白天有日照时,电池板将太阳能转化为电能并储存在锂电池中,晚上锂电池给LED路灯系统供电提供照明。已知:太阳能电池板输出参数为“20V 5A”,有效面积为0.5m2;正常日照时,太阳每秒辐射到每平方米电池板上的能量为
(1) 若每天正常日照8h,锂电池一天可以储存多少电能
(2) 该太阳能电池板的光电转换效率为多少
(3)若路灯每晚从20:00持续工作到凌晨5:00,为了节能,LED 路灯系统安装雷达感应装置,20:00至24:00人群活动密集时功率为20W,24:00至凌晨5:00夜深人静时功率为4 W。已知锂电池最多能储存, 的电能,则充满电可以提供LED路灯系统在阴雨天(无日照)持续工作多少个晚上
25.如图甲所示的电饭锅,额定电压为220V,加热功率为1210W。从铭牌上可知该电饭锅能效等级为三级,简化电路图如图乙所示,有加热和保温两挡,由开关S调节,其中R1和R2均为发热电阻,且阻值不随着温度的变化而改变。求:
(1)电阻R1的阻值:
(2)小明利用电能表测量电饭锅的保温功率,他关闭家里的其它用电器,让电饭锅处于“保温”状态下正常工作,观察在10min内电能表转盘转了30圈。求该电饭锅保温功率。
(3)小明上网查询了解,国家标准中规定电饭锅在该加热功率下正常工作时,三级能效的热效率值范围为81%≤η<86%(热效率是指装置的有效输出能量与输入能量的比值)。他用学过的知识对电饭锅进行测试:在加热状态下,将温度为23℃、质量为2.2kg的水加热到100℃,电饭锅正常工作用时700s。已知c水=4.2×103J/(kg·℃),请你通过计算帮助小明判断该电饭锅的热效率值是否达到三级能效。
26.如图-1,是某型号电暖器。它有高温、低温两个挡位,其简化电路图如图-2所示。R1和R2均为发热电阻,其部分参数如图表所示。请完成下列问题:
额定电压 220V
额定功率 高温挡 2200W
低温挡 1100W
(1)当开关S1、S2均闭合时,电暖器处于 挡;
(2)求该电暖器在低温挡正常工作时,电路中的电流大小;
(3)在某次用电高峰期,小金用如图-3所示的电力监测仪,测出该电暖器在低温挡工作时的实际电压为210V,实际功率为900W。小金由此认为实际功率小于额定功率,只是因为实际电压小于额定电压造成的。小兰和小江却一致认为小金的观点不全面。请你根据题中信息和所学知识,解释实际功率小于额定功率的原因。
27. 人体各个系统协调配合才能使各项生命活动正常进行,如图甲是人体相关生理过程的示意图,其中①②表示气体,③④表示尿液形成过程。请根据图回答下列问题:
(1) 青少年要合理膳食,小琳的早餐既丰富又营养,有牛奶、麦香面包和苹果,这些食物被消化吸收的主要场所是 ,其中牛奶中的蛋白质被彻底消化为 才能被吸收。
(2)一个健康成人每天形成的原尿大约有 150升,而每天排出的尿液一般约为1.5升,这与图中④表示的 的重吸收作用有关。
(3)①表示 进入血液循环后,最先到达心脏的哪个腔 (填结构名称)。
(4)在抽血或输液时,护士要将针头刺入部位的 (填“近心端”或“远心端”)用橡皮管捆扎起来便于针头刺入血管。
(5)某人患急性肾炎,尿液中检测出血细胞,这可能是图甲中的③表示的肾小球的 作用发生障碍;静脉注射青霉素治疗,在心脏中最先发现药物的是图乙中的标号 。
28.运动需要多个器官、系统协调配合。右图是某同学踢足球时心脏与相关器官X的关系示意图,据图回答下列问题。
(1) 运动后补充的糖类被小肠吸收进入血液,首先到达心脏的 (填字母)。心脏内有防止血液倒流的 ,以保证血液将营养物质运送到骨骼肌细胞,供运动所需。
(2)若血液从B出发,经血管①→X后,变为含氧丰富的动脉血,则X代表的器官是 ,血液经血管② 回到C左心房。
(3)该同学进食一段时间后,血液中葡萄糖的浓度会暂时上升,此时X代表的内分泌腺是 ,其分泌的激素增多,以调节葡萄糖在人体内的吸收、利用和转化。
(4)人体生命活动中产生的尿素等废物,主要通过尿液排出体外。尿的形成要经过肾小球和肾小囊内壁的滤过作用和肾小管的 作用。
(5)如果你是一个足球迷,看一场激烈比赛时大脑皮层会特别兴奋,因而促使肾上腺分泌较多的肾上腺素,使人心跳加快、血压升高、面红耳赤。以上生命活动主要受到 系统的影响,但也受到激素调节的影响。
29.小明同学在使用显微镜观察小鱼尾鳍内血液流动的实验时,看到了如图乙所示的视野。请结合学过的知识回答:
(1)小明使用显微镜时因粗心导致刚开始的视野中一片黑暗,他很可能是忘记了 。
(2)图甲中,用湿棉絮将小鱼头部的鳃盖和躯干部包裹起来,观察过程中,时常用滴管往棉絮上滴水以保持湿润,目的是 ,尽量使小鱼少受伤害。
(3) 在观察小鱼尾鳍的实验中,小明应该选用 (填“高”或“低”)倍物镜进行观察。
(4)“3”所指血管位于视野的右下方,小明想把它移到视野的中央观察,他应该往 移动玻片标本。
(5)图乙中涉及了三种血管,人体也同样具有这三种血管,图中数字可代表人体相应的血管。若某人患肺炎,医生会往他手背上的“青筋”注射消炎药,则消炎药通过三种血管的先后顺序是 (用图中数字和“→”表示)。
30. 动物的能量都来自食物,各种食物中所含的能量是不同的。某同学要比较花生仁、大米、牛肉干在体内所能提供的能量的大小,采用了下列实验方法:
①分别称取1克花生仁、大米、牛肉干,并将它们分别粉碎。
②在如图所示装置的试管中加入10毫升水。
③测量并记录加热前的水温。
④将粉碎后的花生仁放在燃烧匙中,然后在酒精灯上加热到自行燃烧,马上放于试管下方,使其完全燃烧干净。
⑤在同样条件下,再分别用大米和牛肉干重复以上实验。
(1)上述实验步骤尚不完整,请补充实验步骤⑥: 。
(2)这个实验误差较大,为了减小误差,可采用 的措施。
(3) 花生仁含有的主要物质的化学式可表示为CaHbOc,如果要验证花生仁燃烧的生成物中有水和二氧化碳,可让产物依次通过____(填字母)。
A.无水硫酸铜和澄清石灰水 B.澄清石灰水和无水硫酸铜
31.如图表示人体循环系统中部分结构示意图,分析图像,回答下列问题。
(1)甲图为心脏结构示意图,①与②、③与④之间,能控制血液定向流动的结构是 。
(2)若静脉注射消炎药,则药物通过心脏的途径是____。
A.①→②→③→④ B.③→④→①→②
C.②→①→④→③ D.④→③→②→①
(3)图乙为某部位毛细血管示意图,根据血流方向,血管A名称是 。
(4)当血液从A流向C的过程中,血液中气体的含量发生了变化,如图丙所示,则乙图中的B在人体哪个器官内?
32.球形火焰实验、奇妙乒乓球实验、动量守恒实验以及又见陀螺实验,这些都是我们熟悉的“天宫课堂”的精彩实验。
(1)空间站利用电解水来产生人体呼吸所需要的氧气,在电解水过程中的能量转化是将电能转化为 能。同时还配备有二氧化碳还原系统,在催化剂作用下,将电解水产生的氢气和人体产生的二氧化碳进行反应,产生水和甲烷(化学式为),请写出上述反应的化学方程式: 。
(2)以下科学实验能在太空站完成的是:____。
A.测定小灯泡额定功率 B.验证植物的根具有向地性
(3)航天员为了对抗失重对身体造成的影响,需要加强体育锻炼,常见的器械有弹力带和太空自行车,他们运动过后也会感觉到肌肉酸胀,是因为肌肉细胞内发生了 (选填“有氧呼吸”或“无氧呼吸”),该过程属于 (选填“同化作用”或“异化作用”)。
答案解析部分
1.【答案】(1)MgSO4和H2SO4的混合溶液的烧杯中滴加NaOH溶液时,氢氧化钠先与硫酸反应,后与硫酸镁反应生成氢氧化镁沉淀和硫酸钠
(2)硫酸钠、氢氧化钠
(3)解:设100g混合溶液中含MgSO4的质量为x
MgSO4+2NaOH= Mg(OH)2↓+Na2SO4
120 58
x 0.58g
=
解得:x=1.2g
答:100g混合溶液中含MgSO4的质量为1.2g。
2.【答案】(1)黑色固体逐渐消失,溶液由无色变为蓝色
(2)解:设溶液中的质量为。
设烧杯中CuO的质量为。
3.【答案】(1)解:①4.48;
②设样品中硫酸镁的质量为
(2)A;B;C;D
4.【答案】(1)增大接触面积,加快反应速率
(2)排除装置内的二氧化碳对实验结果的干扰
(3)偏大
(4)设参加反应的碳酸钙质量为x
解得:x=8g
答:钙片样品中碳酸钙的质量8g。
5.【答案】(1)BaCO3
(2)澄清石灰水
(3)Na2CO3、NaCl、Ba(OH)2
6.【答案】(1)溶液为盐酸和氯化铜的混合溶液,氢氧化钠先和盐酸反应生成氯化钠和水
(2)氯化铜和氯化钠
(3)设原来混合溶液中氯化铜的质量为x,
CuCl2+2NaOH=2NaCl+Cu(OH)2↓
135 98
x 9.8g
x=13.5g
答:原来混合溶液中氯化铜的质量为13.5g。
(4)A
7.【答案】(1)Na2CO3+2HNO32NaNO3+H2O+CO2↑
(2)碳酸钠溶液过量,碳酸钠溶液显碱性
(3)解:设 HNO3与 Na2CO3反应时,生成 NaNO3质量为x,生成 CO2气体质量为y,则
Na2CO3+2HNO3=2NaNO3+H2O+CO2↑
106 170 44
50g×21.2% X Y
X=17g Y=4.4g
设 与 反应生成 质量为 z,生成CaCO3质量为m,则
Na2CO3+ Ca(NO3)2=CaCO3↓+2NaNO3
106 100 170
100g×21.2% m z
m=20g z=34g
所得NaNO3溶液的溶质质量分数:
8.【答案】(1)B
(2)隔绝氧气和水
(3)二;能耗低和污染
(4)氢氧化钠(NaOH)
9.【答案】(1)分液漏斗
(2)11.2
(3)
10.【答案】(1)56%
(2)0.3
(3)12.25%
11.【答案】(1)0.5
(2)100
(3)设:此黄铜的含锌量为x。
x=65%
答:此黄铜的含锌量为65%。
12.【答案】(1)CaCO3;Na2CO3
(2)①设生成19.6g氢氧化铜沉淀需要NaOH溶液的质量为x,需要硫酸铜的质量为y
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
160 80 98
y x×8% 19.6g
x=200g
y=32.0g
②因此46.2g的粉末中含有硫酸钠,且Na2SO4的质量=46.2g-32g=14.2g
46.2g固体粉末由14.2g硫酸钠和32.0g硫酸铜组成。
13.【答案】(1)H2SO4
(2)根据图像可知,反应生成沉淀氢氧化铜的质量为9.8g,
设与CuSO4反应的NaOH的质量为x,同时生成Na2SO4的质量为y,
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
80 98 142
x 9.8g y
;
解得:x=8g,y=14.2g;
所用氢氧化钠溶液中溶质的质量分数为:;
(3)设硫酸与氢氧化钠反应生成硫酸钠质量为z,
H2SO4+2NaOH=Na2SO4+2H2O
80 142
60g×20% z
;
解得:z=21.3g
所得溶液中溶质的质量为:21.3g+14.2g=35.5g
14.【答案】(1)解:W有=Gh=2400N×0.8m=1920J
(2)解:根据可知,
(3)解:根据();
(4)解:
15.【答案】(1)qev:Q放=Vq=0.02m3×8.4×107J/m3=1.68×106J
(2)解:热传递;
由得水吸收的热量:
(3)解:在一个标准大气压下,水的沸点为100℃,即水的末温,
由得水的质量:
16.【答案】(1)1.1A
(2)S1闭合,S接b处
(3)高温挡正常工作时,R1、R2并联,
并联电路总功率等于各部分功率之和,即高温挡功率。
17.【答案】(1)动能
(2)W=FS=100牛×65米=6500焦,P==500瓦
(3)W=Gh=mgh=(12千克+2千克)×10牛/千克×4×3米=1680焦
18.【答案】(1)解:货车空载行驶时所受的阻力大小:
f=0.1G=0.1×1.5×104N=1.5×103N;
(2)解:V=36km/h=10m/s
由s=vt=10m/s×10s=100m,
∵汽车匀速行驶,
∴牵引力F=f=1.5×103N,
10s内货车牵引力做的功:
W=Fs=1.5×103N×100m=1.5×105J;
(3)解:v=72km/h=20m/s
由p=FvF=p/v=80000w/20m/s=4000N
∵汽车匀速行驶,
∴此时汽车受到的阻力:
f=F=4000N,
∵f=0.1G,
∴货车总重:
G'=f/0.1=4×104N,
货车最多可装载货物的重:
G货=G'-G=4×104N-1.5×104N=2.5×104N.
19.【答案】增大;24.2m3;500J
20.【答案】(1)60N;(2)80N;(3)0.1m
21.【答案】(1)改变力的方向
(2)200
(3)90%
22.【答案】(1)否
(2)200N
(3)400J
23.【答案】(1)解:G总=(m车+m人)g=(20kg+60kg)×10N/kg=800N
f=0.05G总=0.05×800N=40N
答:电动平衡车行驶时所受的阻力为40N.
(2)解:F=f=40N
W=F·s=40N×3000m=1.2×105J
答:电动平衡车牵引力做的功为1.2×105J.
(3)解:v===2.5m/s
答:动平衡车行驶的速度为2.5m/s.
24.【答案】(1)若每天正常日照8h,则锂电池一天可以储存的电能W=UIt=20V×5A×8×3600s=2.88×106J
(2)由太阳每秒辐射到每平方米电池板上的能量为0.8×103 J 知: 由太阳能电池板输出参数为“20 V 5 A”知: 5A×1 s=100 J,根据效率公式
(3)LED路灯系统每个晚上所消耗能量W'=20W×4×3600s+4W×5×3600s=3.6×105 J,充满电的锂电池可以提供LED路灯系统在阴雨天(无日照)持续工作晚上的个数为 个
25.【答案】(1)由电路图知,S断开时两电阻串联,电路中电阻较大,功率较小,为保温状态,
当S闭合时,只有R1接入电路中,电阻较小,功率较大,为加热状态,
则R1的电阻:。
(2)“3000r/(kW h)”表示每消耗1kW h电能,电能表转盘转3000圈,
只让电饭煲在“保温”状态下工作,转盘在10min内转了30转,
则电饭锅消耗的电能为:,
电饭锅处于“保温”状态时的功率为:。
(3)该电饭锅的热效率值达到三级能效
水吸收的热量为:
Q吸=c水mΔt=4.2×103J/(kg ℃)×2.2kg×(100℃-23℃)=7.1148×105J;
用时700s消耗的电能为:
W'=P加热t'=1210W×700s=8.47×105J,
该电饭锅的热效率为:,
故该电饭锅的热效率值达到三级能效。
26.【答案】(1)高温挡
(2)电暖器在低温挡正常工作时的功率为1100W,电路中的电流大小为
(3)由题意知,用电高峰期电暖器在低温挡工作时,实际电压为210V,实际功率为900W,根据P=U2/R可得,此时R1的阻值为49Ω。由此可知,原电阻发生了变化。所以造成实际功率小于额定功率的原因,不只是因为实际电压小于额定电压造成的,用电器电阻变大也是其中一个原因。
27.【答案】(1)小肠;氨基酸
(2)肾小管
(3)氧气;左心房
(4)近心端
(5)滤过;C
28.【答案】(1)A;瓣膜
(2)肺;肺静脉
(3)胰岛
(4)重吸收
(5)神经
29.【答案】(1)对光
(2)保证小鱼正常呼吸
(3)低
(4)右下方
(5)3→1→2
30.【答案】(1)测量并记录加热后水的温度
(2)在相对密闭的环境中做实验
(3)A
31.【答案】(1)房室瓣
(2)B
(3)动脉
(4)肺
32.【答案】(1)化学;
(2)A
(3)无氧呼吸;异化作用
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
同课章节目录
