5.1硫及其化合物 第一课时 课件(共59张PPT) 2024-2025学年高一下学期化学人教版(2019)必修第二册
文档属性
| 名称 | 5.1硫及其化合物 第一课时 课件(共59张PPT) 2024-2025学年高一下学期化学人教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 9.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-13 00:00:00 | ||
图片预览










文档简介
(共59张PPT)
第一节 硫及其化合物
学习目标 素养目标
1.通过分析硫的原子结构,推断硫 元素可能的化学性质并进行证实,理解 物质的微观结构与宏观性质之间的关 系。 2.结合实验探究,了解二氧化硫的 物理性质和化学性质,能说出二氧化硫 的主要用途。 【变化观念与平衡思想】基于硫
元素为核心建立物质转化视角,能
够从物质类别和元素价态两个角
度,依据复分解反应和氧化还原反
应原理,分析硫及其化合物的化学
性质及含硫物质间的转化关系。
学习目标 素养目标
3.通过二氧化硫与水、氧气反应 的学习,初步建立可逆反应的概念。 4.通过实验探究,了解硫酸的酸性 和浓硫酸的特性,能设计实验检验硫酸 根离子。 【科学探究与创新意识】能根据
实验目的和假设设计实验方案,选
择适当的实验试剂,探究二氧化
硫、硫酸的物理和化学性质、硫
酸根离子的检验方法、不同价态
含硫物质的转化。
续表
学习目标 素养目标
5.知道含不同价态硫元素的物质 可以相互转化,并能设计实验进行探究 或验证,增强对氧化还原反应的认识。 6.能说出含硫物质进入大气的主 要途径,知道二氧化硫进入大气形成的 酸雨会危害环境,增强环保意识,培养 社会责任感 【科学态度与社会责任】 能说明
硫及其化合物的应用对社会发展
的价值和对环境的影响,能有意识
地运用所学知识和方法解决生
产、生活中的简单化学问题
续表
第1课时 硫和二氧化硫
学习任务一 硫的性质
学习任务二 二氧化硫的性质和用途
学习任务一 硫的性质
【新知自主预习】
1.硫元素的“位—构—性”
三
6
2
较弱
较强
2.单质硫的性质
(1)硫的物理性质
色、态 硬度 溶解性 熔点、沸点 密度
______晶 体,俗称 ______ 质脆, 易研成 粉末 难溶于水,____溶 于酒精,____溶于 二硫化碳 (熔)、 (沸)
黄色
硫黄
微
易
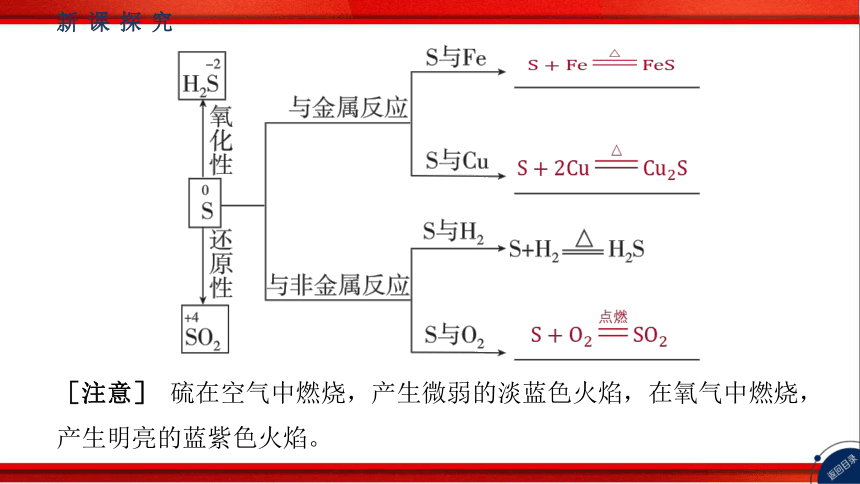
(2)硫的化学性质
硫单质中 元素显0价,处于中间价态,故硫单质既具有________又
具有________,写出下列反应的化学方程式。
氧化性
还原性
[注意] 硫在空气中燃烧,产生微弱的淡蓝色火焰,在氧气中燃烧,
产生明亮的蓝紫色火焰。
【实验活动探究】
某校化学兴趣小组通过实验探究硫的化学性质。
【实验1】将研细的硫粉和铁粉按照一定比例混合均匀,放在陶土网
上堆成条状或如图甲所示的形状。用灼热的玻璃棒触及一端,当混
合物呈红热状态时移开玻璃棒,观察发生的现象。
【实验2】取少量硫粉放入燃烧匙中,将燃烧匙放在酒精灯上加热至
硫粉熔化并燃烧后,迅速伸入盛满氧气的集气瓶(底部有少量水)
中,观察发生的现象。
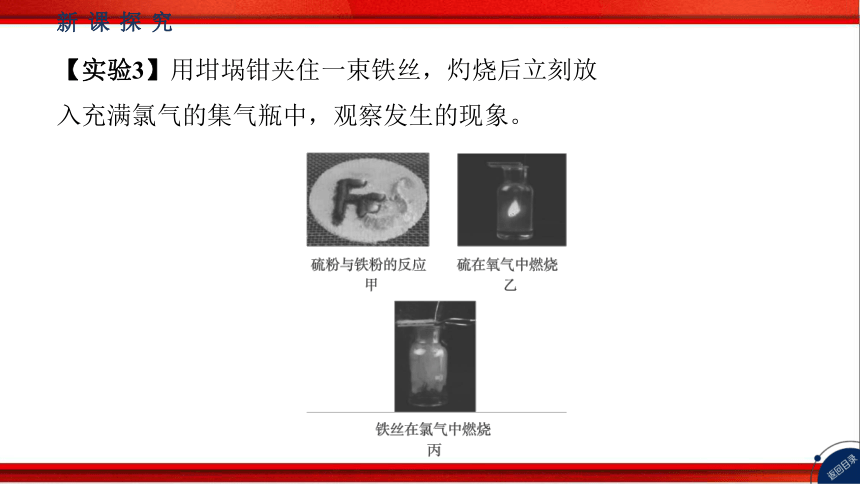
【实验3】用坩埚钳夹住一束铁丝,灼烧后立刻放
入充满氯气的集气瓶中,观察发生的现象。
问题一: 实验1中混合物持续红热,生成黑色固体 。据此得出什
么结论?试写出该反应的化学方程式。
提示:与反应生成时放出热量, 具有氧
化性; 。
问题二: 实验2中发出蓝紫色火焰,产生刺激性气
味的气体 。试写出该反应的化学方程式,体现
单质硫的什么性质?
提示: ;体现单质硫的还原性。
问题三: 实验3中铁丝剧烈燃烧,产生棕黄色的烟,生成 固体。
从微观角度分析与、反应产物中 元素价态不同的原因。
提示:原子半径比原子的大,非金属性:
,则单质的氧化性:;与变价
金属铁反应时,强氧化性的将 氧化生成
,弱氧化性的将氧化生成 。
【核心知识讲解】
1.从元素化合价角度认识单质硫的化学性质
2.硫、氯气与变价金属反应的比较
[注意] 变价金属(、等)与、 反应的产物取决于氧化剂
的氧化性,与氧化剂的用量无关。
【知识迁移应用】
例1 下列物质间的反应中,硫表现出还原性的是( )
A.硫与氢气 B.硫与氧气 C.硫与铁 D.硫与钠
[解析] 硫与氢气在加热条件下生成, 作氧化剂,表现出氧化性,
A不符合题意;
在加热条件下,硫与铁、钠反应分别生成 、, 作氧化剂,
表现出氧化性,C、D均不符合题意;
硫与氧气反应生成, 作还原剂,表现出还原性,B符合题意。
√
例2 下列物质中,不能由单质直接化合生成的是( )
A.①③ B.①②③ C.①②④ D.全部
[解析] 具有弱氧化性,与、反应分别生成 、
,;与点燃生成 ,不能直
接生成;与加热生成 ;
综上所述A项符合题意。
√
[易错警示]
单质与反应时,无论氧气是否足量,均生成 ,不能直接生成
,转化为 需要在催化剂、加热条件下才能进行。
学习任务二 二氧化硫的性质和用途
【新知自主预习】
一、 的物理性质
1.物理性质
颜色 气味 毒性 密度 溶解性
无色 有 ________ 气味 ____ 毒 比空气的 ____ ____溶于水,通常情况下,1体积的
水可以溶解约40体积的
刺激性
有
大
易
2.实验探究
实验操作 _______________________________________________________________________________________________
实验现象 试管内液面______, 试纸变成红色
结论 能溶于水,所得溶液呈____性
上升
酸
二、从“价—类”二维视角认识 的化学性质
中间
还原性
1.具有酸性氧化物的性质(物质类别)
(1)与水反应
①与水反应生成,不稳定,容易分解成与 ,
化学方程式为___________________。
②可逆反应:在____________,既能向____________进行,同时又
能向____________进行的反应。
同一条件下
正反应方向
逆反应方向
可逆反应特点:
[注意] 可逆反应这一概念的关键词是“同一条件”。例如,
和 不属于可逆反应。
(2)与碱溶液反应
与少量溶液反应: ;
与足量 溶液反应:_____________________________。
[注意]与碱溶液反应时,反应物的量影响反应及产物,若
不足,反应生成亚硫酸盐;若 足量,反应则生成亚硫酸氢盐。
2. 具有氧化性和还原性(元素价态)
(1)具有强还原性
(2)具有弱氧化性
与 溶液反应的化学方程式为_________________________,反应现
象为产生淡黄色浑浊。(注意:该反应常用于无机物的反应及推断)
3.具有漂白性[教材实验
实验操作 实验现象 实验分析
用试管取 的水溶 液,滴入 滴品红溶液,振 荡,观察溶液的颜色变化 ___________ ___ 与品红溶液反
应生成了无色物质
加热试管,注意通风,再观 察溶液的变化 ___________ ___________ 加热时无色物质
分解,恢复为原来的
颜色
品红溶液褪色
加热后溶液恢复红色
4. 的重要用途
(1)工业上常用 来漂白纸浆、毛、丝等。
(2) 可用于__________,还是一种食品添加剂。
杀菌消毒
【实验活动探究】
问题一: 若将等物质的量的和 同时通入品红溶液中,溶液的漂
白性是“强强联合”吗
提示:不是。将等物质的量的和 混合后,在溶液中发生反应:
,失去漂白能力。
问题二: 品红溶液中分别通入和 会出现什么现象 一段时间
后对其进行加热,现象又如何 紫色石蕊溶液中分别通入和 会
出现什么现象
提示:
【核心知识讲解】
1.和 的化学性质比较
共 性 与水 反应
共 性 与碱 反应 气体通入澄清石灰水 中,先生成沉淀,当气体过量 时沉淀又溶解: 气体通入澄清石灰水中,
先生成沉淀,当气体过量时
沉淀又溶解:
续表
共 性 与碱 性氧 化物 反应
弱氧 化性
差 异 性 还原 性 能被酸性高锰酸钾溶液、 、、 等氧化剂氧化 —
续表
差 异 性 漂白 性 能使品红溶液褪色 (暂时性、可逆性) —
鉴别方法 ①利用二氧化硫的还原性,用酸性高锰酸钾溶液或溴水 鉴别 ②利用二氧化硫的漂白性,用品红溶液鉴别 续表
除 杂 中 混有 少量 将气体通过饱和 溶液洗气或将气体通过酸性高锰 酸钾溶液洗气 续表
2.三种类型漂白原理的比较
【知识迁移应用】
例3 [2024·广东清远期中] SO2是一种食品添加剂,在食品的加工中起
着重要的作用,但如果使用不当就有可能造成食品中SO2残留量超标。
葡萄酒中添加适量的SO2能防止葡萄酒中的某些成分氧化变质,这是利
用了SO2的 ( )
A.氧化性 B.漂白性 C.还原性 D.有毒性
√
[解析] 葡萄酒中添加适量的SO2能防止葡萄酒中的某些成分氧化变质,
说明二氧化硫具有还原性,这是利用了SO2的还原性。
例4 实验室中为验证的性质,将 分别通入溴水、品红溶液、
硫化氢溶液、滴有酚酞的氢氧化钠溶液。下列说法错误的是( )
A.溴水褪色,体现 的还原性
B.品红溶液褪色,体现 的漂白性
C.硫化氢溶液浑浊,体现 的氧化性
D.滴有酚酞的氢氧化钠溶液褪色,体现 的漂白性
√
[解析] 通入溴水中发生反应:
, 作还原剂,体现其还原性,
A正确;
使品红溶液褪色,体现的漂白性,B正确;
通入硫化氢溶液中,发生反应:,
作氧化剂,体现其氧化性,C正确;
使滴有酚酞的 溶液褪色,其原因是和发生反应生成
盐和 ,溶液的碱性减弱,体现 是酸性氧化物的性质,与其漂
白性无关,D错误。
[易错警示]
(1) 的漂白性一般是指与有色有机物质的作用,与有色无机物质
的作用不是漂白性。
(2) 不能漂白酸碱指示剂,只能使紫色石蕊溶液变红,但不褪色。
(3)使卤水(氯水、溴水、碘水)、酸性 溶液等氧化性
试剂褪色,体现 的还原性。
1.[2024·四川南充高级中学期中]下列关于硫单质的说法不正确的是
( )
A.自然界中存在单质硫
B.硫在过量纯氧中燃烧的产物是三氧化硫
C.单质硫既有氧化性,又有还原性
D.试管内壁附着的硫可用二硫化碳溶解除去
√
[解析] 自然界中的硫既有游离态,又有化合态,游离态的硫主要存在
于火山喷口附近或地壳的岩层里,A正确;
硫在过量纯氧中燃烧的产物仍然是二氧化硫,B错误;
单质硫既可被还原到 价,也可被氧化到 价,因此单质硫既有氧
化性,又有还原性,C正确;
硫易溶于二硫化碳,因此可用二硫化碳溶解除去试管内壁附着的硫,
D正确。
2.下列关于 的叙述错误的是( )
A.是有毒的气体 B.能与 溶液反应
C.能使酸性溶液褪色 D. 能使紫色石蕊溶液褪色
[解析] 是有毒气体,A正确;
是酸性氧化物,能与 溶液反应,B正确;
具有还原性,能将还原为 而使溶液褪色,C正确;
具有漂白性,但不能漂白酸碱指示剂, 通入
紫色石蕊溶液中,溶液只变红色不褪色,D错误。
√
3.[2024·陕西渭南统考]中医药文化博大精深,其用药讲究十八反和
十九畏,其中有“硫黄原是火中精,朴硝一见便相争”,硫黄即硫单
质。下列说法中正确的是( )
A.根据化合价可知, 在化学反应中只能作还原剂
B.硫单质可以溶于热碱,体现氧化性和还原性
C.过量的硫与铜反应生成 ,表现硫单质的氧化性
D., 被氧化,作氧化剂
√
[解析] 硫单质中硫元素的化合价为0价,是的中间价态,故 既可作
氧化剂,又可作还原剂,A错误;
硫单质和热碱液反应生成金属硫化物、亚硫酸盐和水,金属硫化物中
硫元素的化合价为 价,亚硫酸盐中硫元素的化合价为 价,在反
应中,硫单质既体现氧化性,又体现还原性,B正确;
硫单质的氧化性较弱,与变价金属化合时,只能生成低价态金属硫化
物,如与、反应,生成、 ,C错误;
反应中 被氧化,化合价升高,作还原剂,D错误。
4.[2024·河北保定期末] 某同学为验证
的性质,在培养皿中放置几团浸有
不同物质的棉球,然后向 固体
上滴加 的浓硫酸,并迅速盖上培养
皿盖,实验装置如图所示。下列有关实验现象及解释均正确的是
[已知: ( )
选项 棉球所浸物质 实验现象 解释
A 品红溶液 褪色 具有氧化性
B 滴有酚酞的 溶液 不褪色 不能漂白酚酞
溶液
C 酸性 溶液 褪色 具有还原性
D 紫色石蕊溶液 变红 溶于水,溶液
呈碱性
√
[解析] 品红溶液褪色,说明具有漂白性,A错误;
与 溶液发生反应,生成盐和 ,溶液的碱性减弱,溶液会
褪色,B错误;
酸性溶液具有强氧化性,溶液褪色,说明 具有还原性,C
正确;
紫色石蕊溶液遇到会变红,其原因是 溶于水,溶液呈
酸性,D错误。
5.二氧化硫 主要用于生产硫酸,也可用作
防腐剂和抗氧化剂,还可用作漂白剂。实验室常
用固体和硫酸溶液反应制备 。某
同学利用如图所示装置(夹持装置已省略)制备
,并验证其部分性质。回答下列问题:
(1)按图组装好仪器后,应先检查装置的________。
气密性
[解析] 实验中有气体参与反应,因此按题图组装好仪器后,应先检
查装置的气密性。
(2)仪器的名称是__________;仪器 中盛放的试剂是__________
____。
(3)实验过程中,试管中的品红溶液褪色,这说明 具有______性。
圆底烧瓶
硫酸溶液
漂白
(4)从氯水、溶液、饱和溶液、酸性 溶液四种试剂中,
选择_____________加入试管进行实验,可验证 的氧化性,与此
实验有关的化学方程式为_________________________。
饱和溶液
[解析] 为验证二氧化硫的氧化性,应在试管 中加入还原性的物质,
尽管溶液具有还原性,但氧化性:,所以试管 中盛放
饱和溶液,二氧化硫和 发生氧化还原反应生成硫单质和水,
反应的化学方程式为 。
(5)从环境保护的角度考虑,进行上述实验还需对该装置加以改进,
其措施为___________________________________________________
_______。
在试管后添加一个装有氢氧化钠溶液的烧杯并加装防倒吸装置
[解析] 二氧化硫对环境有污染,不能直接排放到空气中,应在试管
后添加一个装有氢氧化钠溶液的装置并注意防倒吸,用于处理尾气。
(6)上述实验完成后,加热试管 ,可观察到的现象是___________
_________。
溶液由无色变为红色
[解析] 二氧化硫能与品红溶液中的有色物质结合而生成无色化合物,
这种无色化合物不稳定,遇热分解,恢复到原来的颜色。实验完成
后,加热试管 ,可观察到的现象是溶液由无色变为红色。
1.下列有关硫的说法中,不正确的是( )
A.硫有多种同素异形体
B.硫的化学性质与氧气相同
C.硫在空气中燃烧时,火焰呈淡蓝色;在氧气中燃烧时,火焰呈蓝
紫色
D.硫在一定条件下能与某些金属反应,生成金属硫化物
√
[解析] 硫有多种同素异形体,如单斜硫和斜方硫,故A正确;
和 是同主族的非金属单质,化学性质具有相似性,但不相同,
故B错误;
硫在空气中燃烧时,发出淡蓝色火焰,在氧气中燃烧时,发出蓝紫
色火焰,故C正确;
硫在一定条件下能与某些金属反应,生成金属硫
化物,如铁与硫混合加热生成硫化亚铁,故D正确。
2.[2024·北京顺义区杨镇一中月考]下列关于二氧化硫气体性质的描
述中,不正确的是( )
A.有刺激性气味
B.在相同条件下,密度比空气的小
C.能使品红溶液褪色
D.能与 溶液反应
[解析] 二氧化硫是无色有刺激性气味的有毒气体,A正确;
在相同条件下,二氧化硫密度比空气的大,B错误;
二氧化硫具有漂白性,能使品红溶液褪色,C正确;
二氧化硫是酸性氧化物,能与 溶液反应,D正确。
√
3. 既有氧化性又有还原性,还有漂白性。下列对它在变化中表现的
性质标注正确的是( )
使氯水褪色(漂白性)
使品红溶液褪色(漂白性)
通入氢硫酸( 溶液)中产生淡黄色浑浊(还原性)
使湿润的蓝色石蕊试纸变红(水溶液的酸性)
A.只有②④ B.只有③④ C.只有①③ D.①②③④
√
[解析] 使氯水褪色发生反应:
, 作还原剂,表现还原性,①错
误;使品红溶液褪色,表现漂白性,②正确; 通入氢硫酸
( 溶液)中产生淡黄色浑浊,发生反应:
,作氧化剂,表现氧化性,③错误; 使
湿润的蓝色石蕊试纸变红,其原因是与反应生成 而使其
水溶液呈酸性,④正确。
4.[2024·江苏扬州期末] 已知:
。实验室制取 时,下
列装置不能达到相应实验目的的是( )
________________ _____________________________
A.制备 B.检验
____________________ __________________________________
C.干燥 D.收集
√
[解析] 铜和浓硫酸加热可以获得,A正确;
能使品红溶液褪色,故能用品红溶液来检验,B正确;
可以用浓硫酸来干燥,但干燥气体需长进短出进行通气,装置C
不能实现实验目的,C错误;
密度比空气大,采用向上排空气法收集,并用 溶液进
行尾气处理,D正确。
第一节 硫及其化合物
学习目标 素养目标
1.通过分析硫的原子结构,推断硫 元素可能的化学性质并进行证实,理解 物质的微观结构与宏观性质之间的关 系。 2.结合实验探究,了解二氧化硫的 物理性质和化学性质,能说出二氧化硫 的主要用途。 【变化观念与平衡思想】基于硫
元素为核心建立物质转化视角,能
够从物质类别和元素价态两个角
度,依据复分解反应和氧化还原反
应原理,分析硫及其化合物的化学
性质及含硫物质间的转化关系。
学习目标 素养目标
3.通过二氧化硫与水、氧气反应 的学习,初步建立可逆反应的概念。 4.通过实验探究,了解硫酸的酸性 和浓硫酸的特性,能设计实验检验硫酸 根离子。 【科学探究与创新意识】能根据
实验目的和假设设计实验方案,选
择适当的实验试剂,探究二氧化
硫、硫酸的物理和化学性质、硫
酸根离子的检验方法、不同价态
含硫物质的转化。
续表
学习目标 素养目标
5.知道含不同价态硫元素的物质 可以相互转化,并能设计实验进行探究 或验证,增强对氧化还原反应的认识。 6.能说出含硫物质进入大气的主 要途径,知道二氧化硫进入大气形成的 酸雨会危害环境,增强环保意识,培养 社会责任感 【科学态度与社会责任】 能说明
硫及其化合物的应用对社会发展
的价值和对环境的影响,能有意识
地运用所学知识和方法解决生
产、生活中的简单化学问题
续表
第1课时 硫和二氧化硫
学习任务一 硫的性质
学习任务二 二氧化硫的性质和用途
学习任务一 硫的性质
【新知自主预习】
1.硫元素的“位—构—性”
三
6
2
较弱
较强
2.单质硫的性质
(1)硫的物理性质
色、态 硬度 溶解性 熔点、沸点 密度
______晶 体,俗称 ______ 质脆, 易研成 粉末 难溶于水,____溶 于酒精,____溶于 二硫化碳 (熔)、 (沸)
黄色
硫黄
微
易
(2)硫的化学性质
硫单质中 元素显0价,处于中间价态,故硫单质既具有________又
具有________,写出下列反应的化学方程式。
氧化性
还原性
[注意] 硫在空气中燃烧,产生微弱的淡蓝色火焰,在氧气中燃烧,
产生明亮的蓝紫色火焰。
【实验活动探究】
某校化学兴趣小组通过实验探究硫的化学性质。
【实验1】将研细的硫粉和铁粉按照一定比例混合均匀,放在陶土网
上堆成条状或如图甲所示的形状。用灼热的玻璃棒触及一端,当混
合物呈红热状态时移开玻璃棒,观察发生的现象。
【实验2】取少量硫粉放入燃烧匙中,将燃烧匙放在酒精灯上加热至
硫粉熔化并燃烧后,迅速伸入盛满氧气的集气瓶(底部有少量水)
中,观察发生的现象。
【实验3】用坩埚钳夹住一束铁丝,灼烧后立刻放
入充满氯气的集气瓶中,观察发生的现象。
问题一: 实验1中混合物持续红热,生成黑色固体 。据此得出什
么结论?试写出该反应的化学方程式。
提示:与反应生成时放出热量, 具有氧
化性; 。
问题二: 实验2中发出蓝紫色火焰,产生刺激性气
味的气体 。试写出该反应的化学方程式,体现
单质硫的什么性质?
提示: ;体现单质硫的还原性。
问题三: 实验3中铁丝剧烈燃烧,产生棕黄色的烟,生成 固体。
从微观角度分析与、反应产物中 元素价态不同的原因。
提示:原子半径比原子的大,非金属性:
,则单质的氧化性:;与变价
金属铁反应时,强氧化性的将 氧化生成
,弱氧化性的将氧化生成 。
【核心知识讲解】
1.从元素化合价角度认识单质硫的化学性质
2.硫、氯气与变价金属反应的比较
[注意] 变价金属(、等)与、 反应的产物取决于氧化剂
的氧化性,与氧化剂的用量无关。
【知识迁移应用】
例1 下列物质间的反应中,硫表现出还原性的是( )
A.硫与氢气 B.硫与氧气 C.硫与铁 D.硫与钠
[解析] 硫与氢气在加热条件下生成, 作氧化剂,表现出氧化性,
A不符合题意;
在加热条件下,硫与铁、钠反应分别生成 、, 作氧化剂,
表现出氧化性,C、D均不符合题意;
硫与氧气反应生成, 作还原剂,表现出还原性,B符合题意。
√
例2 下列物质中,不能由单质直接化合生成的是( )
A.①③ B.①②③ C.①②④ D.全部
[解析] 具有弱氧化性,与、反应分别生成 、
,;与点燃生成 ,不能直
接生成;与加热生成 ;
综上所述A项符合题意。
√
[易错警示]
单质与反应时,无论氧气是否足量,均生成 ,不能直接生成
,转化为 需要在催化剂、加热条件下才能进行。
学习任务二 二氧化硫的性质和用途
【新知自主预习】
一、 的物理性质
1.物理性质
颜色 气味 毒性 密度 溶解性
无色 有 ________ 气味 ____ 毒 比空气的 ____ ____溶于水,通常情况下,1体积的
水可以溶解约40体积的
刺激性
有
大
易
2.实验探究
实验操作 _______________________________________________________________________________________________
实验现象 试管内液面______, 试纸变成红色
结论 能溶于水,所得溶液呈____性
上升
酸
二、从“价—类”二维视角认识 的化学性质
中间
还原性
1.具有酸性氧化物的性质(物质类别)
(1)与水反应
①与水反应生成,不稳定,容易分解成与 ,
化学方程式为___________________。
②可逆反应:在____________,既能向____________进行,同时又
能向____________进行的反应。
同一条件下
正反应方向
逆反应方向
可逆反应特点:
[注意] 可逆反应这一概念的关键词是“同一条件”。例如,
和 不属于可逆反应。
(2)与碱溶液反应
与少量溶液反应: ;
与足量 溶液反应:_____________________________。
[注意]与碱溶液反应时,反应物的量影响反应及产物,若
不足,反应生成亚硫酸盐;若 足量,反应则生成亚硫酸氢盐。
2. 具有氧化性和还原性(元素价态)
(1)具有强还原性
(2)具有弱氧化性
与 溶液反应的化学方程式为_________________________,反应现
象为产生淡黄色浑浊。(注意:该反应常用于无机物的反应及推断)
3.具有漂白性[教材实验
实验操作 实验现象 实验分析
用试管取 的水溶 液,滴入 滴品红溶液,振 荡,观察溶液的颜色变化 ___________ ___ 与品红溶液反
应生成了无色物质
加热试管,注意通风,再观 察溶液的变化 ___________ ___________ 加热时无色物质
分解,恢复为原来的
颜色
品红溶液褪色
加热后溶液恢复红色
4. 的重要用途
(1)工业上常用 来漂白纸浆、毛、丝等。
(2) 可用于__________,还是一种食品添加剂。
杀菌消毒
【实验活动探究】
问题一: 若将等物质的量的和 同时通入品红溶液中,溶液的漂
白性是“强强联合”吗
提示:不是。将等物质的量的和 混合后,在溶液中发生反应:
,失去漂白能力。
问题二: 品红溶液中分别通入和 会出现什么现象 一段时间
后对其进行加热,现象又如何 紫色石蕊溶液中分别通入和 会
出现什么现象
提示:
【核心知识讲解】
1.和 的化学性质比较
共 性 与水 反应
共 性 与碱 反应 气体通入澄清石灰水 中,先生成沉淀,当气体过量 时沉淀又溶解: 气体通入澄清石灰水中,
先生成沉淀,当气体过量时
沉淀又溶解:
续表
共 性 与碱 性氧 化物 反应
弱氧 化性
差 异 性 还原 性 能被酸性高锰酸钾溶液、 、、 等氧化剂氧化 —
续表
差 异 性 漂白 性 能使品红溶液褪色 (暂时性、可逆性) —
鉴别方法 ①利用二氧化硫的还原性,用酸性高锰酸钾溶液或溴水 鉴别 ②利用二氧化硫的漂白性,用品红溶液鉴别 续表
除 杂 中 混有 少量 将气体通过饱和 溶液洗气或将气体通过酸性高锰 酸钾溶液洗气 续表
2.三种类型漂白原理的比较
【知识迁移应用】
例3 [2024·广东清远期中] SO2是一种食品添加剂,在食品的加工中起
着重要的作用,但如果使用不当就有可能造成食品中SO2残留量超标。
葡萄酒中添加适量的SO2能防止葡萄酒中的某些成分氧化变质,这是利
用了SO2的 ( )
A.氧化性 B.漂白性 C.还原性 D.有毒性
√
[解析] 葡萄酒中添加适量的SO2能防止葡萄酒中的某些成分氧化变质,
说明二氧化硫具有还原性,这是利用了SO2的还原性。
例4 实验室中为验证的性质,将 分别通入溴水、品红溶液、
硫化氢溶液、滴有酚酞的氢氧化钠溶液。下列说法错误的是( )
A.溴水褪色,体现 的还原性
B.品红溶液褪色,体现 的漂白性
C.硫化氢溶液浑浊,体现 的氧化性
D.滴有酚酞的氢氧化钠溶液褪色,体现 的漂白性
√
[解析] 通入溴水中发生反应:
, 作还原剂,体现其还原性,
A正确;
使品红溶液褪色,体现的漂白性,B正确;
通入硫化氢溶液中,发生反应:,
作氧化剂,体现其氧化性,C正确;
使滴有酚酞的 溶液褪色,其原因是和发生反应生成
盐和 ,溶液的碱性减弱,体现 是酸性氧化物的性质,与其漂
白性无关,D错误。
[易错警示]
(1) 的漂白性一般是指与有色有机物质的作用,与有色无机物质
的作用不是漂白性。
(2) 不能漂白酸碱指示剂,只能使紫色石蕊溶液变红,但不褪色。
(3)使卤水(氯水、溴水、碘水)、酸性 溶液等氧化性
试剂褪色,体现 的还原性。
1.[2024·四川南充高级中学期中]下列关于硫单质的说法不正确的是
( )
A.自然界中存在单质硫
B.硫在过量纯氧中燃烧的产物是三氧化硫
C.单质硫既有氧化性,又有还原性
D.试管内壁附着的硫可用二硫化碳溶解除去
√
[解析] 自然界中的硫既有游离态,又有化合态,游离态的硫主要存在
于火山喷口附近或地壳的岩层里,A正确;
硫在过量纯氧中燃烧的产物仍然是二氧化硫,B错误;
单质硫既可被还原到 价,也可被氧化到 价,因此单质硫既有氧
化性,又有还原性,C正确;
硫易溶于二硫化碳,因此可用二硫化碳溶解除去试管内壁附着的硫,
D正确。
2.下列关于 的叙述错误的是( )
A.是有毒的气体 B.能与 溶液反应
C.能使酸性溶液褪色 D. 能使紫色石蕊溶液褪色
[解析] 是有毒气体,A正确;
是酸性氧化物,能与 溶液反应,B正确;
具有还原性,能将还原为 而使溶液褪色,C正确;
具有漂白性,但不能漂白酸碱指示剂, 通入
紫色石蕊溶液中,溶液只变红色不褪色,D错误。
√
3.[2024·陕西渭南统考]中医药文化博大精深,其用药讲究十八反和
十九畏,其中有“硫黄原是火中精,朴硝一见便相争”,硫黄即硫单
质。下列说法中正确的是( )
A.根据化合价可知, 在化学反应中只能作还原剂
B.硫单质可以溶于热碱,体现氧化性和还原性
C.过量的硫与铜反应生成 ,表现硫单质的氧化性
D., 被氧化,作氧化剂
√
[解析] 硫单质中硫元素的化合价为0价,是的中间价态,故 既可作
氧化剂,又可作还原剂,A错误;
硫单质和热碱液反应生成金属硫化物、亚硫酸盐和水,金属硫化物中
硫元素的化合价为 价,亚硫酸盐中硫元素的化合价为 价,在反
应中,硫单质既体现氧化性,又体现还原性,B正确;
硫单质的氧化性较弱,与变价金属化合时,只能生成低价态金属硫化
物,如与、反应,生成、 ,C错误;
反应中 被氧化,化合价升高,作还原剂,D错误。
4.[2024·河北保定期末] 某同学为验证
的性质,在培养皿中放置几团浸有
不同物质的棉球,然后向 固体
上滴加 的浓硫酸,并迅速盖上培养
皿盖,实验装置如图所示。下列有关实验现象及解释均正确的是
[已知: ( )
选项 棉球所浸物质 实验现象 解释
A 品红溶液 褪色 具有氧化性
B 滴有酚酞的 溶液 不褪色 不能漂白酚酞
溶液
C 酸性 溶液 褪色 具有还原性
D 紫色石蕊溶液 变红 溶于水,溶液
呈碱性
√
[解析] 品红溶液褪色,说明具有漂白性,A错误;
与 溶液发生反应,生成盐和 ,溶液的碱性减弱,溶液会
褪色,B错误;
酸性溶液具有强氧化性,溶液褪色,说明 具有还原性,C
正确;
紫色石蕊溶液遇到会变红,其原因是 溶于水,溶液呈
酸性,D错误。
5.二氧化硫 主要用于生产硫酸,也可用作
防腐剂和抗氧化剂,还可用作漂白剂。实验室常
用固体和硫酸溶液反应制备 。某
同学利用如图所示装置(夹持装置已省略)制备
,并验证其部分性质。回答下列问题:
(1)按图组装好仪器后,应先检查装置的________。
气密性
[解析] 实验中有气体参与反应,因此按题图组装好仪器后,应先检
查装置的气密性。
(2)仪器的名称是__________;仪器 中盛放的试剂是__________
____。
(3)实验过程中,试管中的品红溶液褪色,这说明 具有______性。
圆底烧瓶
硫酸溶液
漂白
(4)从氯水、溶液、饱和溶液、酸性 溶液四种试剂中,
选择_____________加入试管进行实验,可验证 的氧化性,与此
实验有关的化学方程式为_________________________。
饱和溶液
[解析] 为验证二氧化硫的氧化性,应在试管 中加入还原性的物质,
尽管溶液具有还原性,但氧化性:,所以试管 中盛放
饱和溶液,二氧化硫和 发生氧化还原反应生成硫单质和水,
反应的化学方程式为 。
(5)从环境保护的角度考虑,进行上述实验还需对该装置加以改进,
其措施为___________________________________________________
_______。
在试管后添加一个装有氢氧化钠溶液的烧杯并加装防倒吸装置
[解析] 二氧化硫对环境有污染,不能直接排放到空气中,应在试管
后添加一个装有氢氧化钠溶液的装置并注意防倒吸,用于处理尾气。
(6)上述实验完成后,加热试管 ,可观察到的现象是___________
_________。
溶液由无色变为红色
[解析] 二氧化硫能与品红溶液中的有色物质结合而生成无色化合物,
这种无色化合物不稳定,遇热分解,恢复到原来的颜色。实验完成
后,加热试管 ,可观察到的现象是溶液由无色变为红色。
1.下列有关硫的说法中,不正确的是( )
A.硫有多种同素异形体
B.硫的化学性质与氧气相同
C.硫在空气中燃烧时,火焰呈淡蓝色;在氧气中燃烧时,火焰呈蓝
紫色
D.硫在一定条件下能与某些金属反应,生成金属硫化物
√
[解析] 硫有多种同素异形体,如单斜硫和斜方硫,故A正确;
和 是同主族的非金属单质,化学性质具有相似性,但不相同,
故B错误;
硫在空气中燃烧时,发出淡蓝色火焰,在氧气中燃烧时,发出蓝紫
色火焰,故C正确;
硫在一定条件下能与某些金属反应,生成金属硫
化物,如铁与硫混合加热生成硫化亚铁,故D正确。
2.[2024·北京顺义区杨镇一中月考]下列关于二氧化硫气体性质的描
述中,不正确的是( )
A.有刺激性气味
B.在相同条件下,密度比空气的小
C.能使品红溶液褪色
D.能与 溶液反应
[解析] 二氧化硫是无色有刺激性气味的有毒气体,A正确;
在相同条件下,二氧化硫密度比空气的大,B错误;
二氧化硫具有漂白性,能使品红溶液褪色,C正确;
二氧化硫是酸性氧化物,能与 溶液反应,D正确。
√
3. 既有氧化性又有还原性,还有漂白性。下列对它在变化中表现的
性质标注正确的是( )
使氯水褪色(漂白性)
使品红溶液褪色(漂白性)
通入氢硫酸( 溶液)中产生淡黄色浑浊(还原性)
使湿润的蓝色石蕊试纸变红(水溶液的酸性)
A.只有②④ B.只有③④ C.只有①③ D.①②③④
√
[解析] 使氯水褪色发生反应:
, 作还原剂,表现还原性,①错
误;使品红溶液褪色,表现漂白性,②正确; 通入氢硫酸
( 溶液)中产生淡黄色浑浊,发生反应:
,作氧化剂,表现氧化性,③错误; 使
湿润的蓝色石蕊试纸变红,其原因是与反应生成 而使其
水溶液呈酸性,④正确。
4.[2024·江苏扬州期末] 已知:
。实验室制取 时,下
列装置不能达到相应实验目的的是( )
________________ _____________________________
A.制备 B.检验
____________________ __________________________________
C.干燥 D.收集
√
[解析] 铜和浓硫酸加热可以获得,A正确;
能使品红溶液褪色,故能用品红溶液来检验,B正确;
可以用浓硫酸来干燥,但干燥气体需长进短出进行通气,装置C
不能实现实验目的,C错误;
密度比空气大,采用向上排空气法收集,并用 溶液进
行尾气处理,D正确。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
