2024-2025学年高一化学人教版(2019)上学期期末教学质量模拟检测(二)(含解析)
文档属性
| 名称 | 2024-2025学年高一化学人教版(2019)上学期期末教学质量模拟检测(二)(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-15 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
2024-2025学年高一化学人教版(2019)上学期期末教学质量模拟检测(二)(含解析)
注意事项:
1.答题前,考生先将自己的姓名准考证号码填写清楚,将条形码准确粘贴在考生信息条形码粘贴区。
2.选择题必须使用2B铅笔填涂;非选择题必须使用0.5毫米黑色字迹的签字笔书写,字体工整、笔迹清楚。
3.请按照题号顺序在答题卡各题目的答题区域内作答,超出答题区域书写的答案无效;在草稿纸、试卷上答题无效。
4.作图可先使用铅笔画出,确定后必须用黑色字迹的签字笔描黑。
5.保持卡面清洁,不要折叠,不要弄破、异皱,不准使用涂改液、修正带、刮纸刀。
可能用到的相对原子质量:
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目要求。
1.下列关于氧化钠和过氧化钠的叙述正确的是( )
A.在与水的反应中,氧化剂是,还原剂是水
B.和都是白色固体,都能与冷水作用得到和NaOH
C.相同物质的量的氧化钠和过氧化钠中阴离子物质的量之比为1:1
D.与都能与水反应生成碱,它们都是碱性氧化物
2.下列陈述I与陈述II均正确,且具有因果关系的是( )
选项 陈述I 陈述II
A 用重结晶法除去苯甲酸混有的 苯甲酸具有酸性
B 草木灰不能与混合使用 与反应生成氨气会降低肥效
C 用溶液检验 具有氧化性
D 用铝制容器盛装浓硝酸 铝与浓硝酸不反应
A.A B.B C.C D.D
3.为阿伏伽德罗常数的值。下列叙述正确的是( )
A.异丁烷分子中共价键的数目为
B.标准状况下,中电子的数目为
C.的溶液中的数目为
D.的溶液中的数目为
4.下列以物质的量为中心的计算正确的是( )
A.溶液中含有的物质的量为0.2mol
B.常温常压下,含有分子的物质的量为0.2mol
C.5.6gFe与足量氯气反应失去电子的物质的量为0.2mol
D.3.2g由、组成的混合气体中含有原子的物质的量为0.2mol
5.二氧化氯是国际上公认的安全、无毒的绿色消毒剂。“R7法”制备二氧化氯的优点是副产品氯气经处理后可循环利用,具体制备流程如图所示。消毒效率。
下列说法正确的是( )
A.和的消毒效率之比为71:18
B.反应①生成的离子方程式:
C.反应①消耗的硫酸与反应②生成的硫酸物质的量相等
D.反应②中作还原剂,物质X为
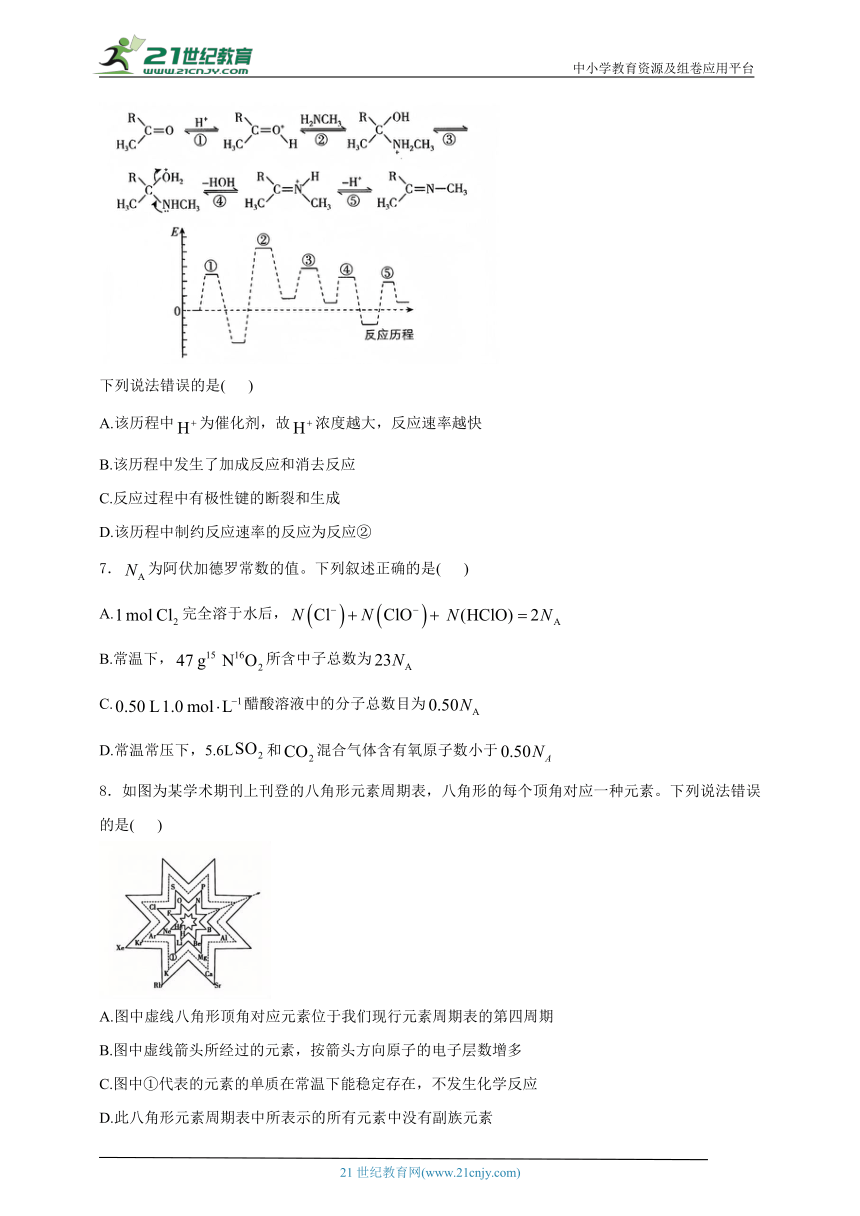
6.丙酮和甲胺的反应机理及能量图像如图所示。
下列说法错误的是( )
A.该历程中为催化剂,故浓度越大,反应速率越快
B.该历程中发生了加成反应和消去反应
C.反应过程中有极性键的断裂和生成
D.该历程中制约反应速率的反应为反应②
7.为阿伏加德罗常数的值。下列叙述正确的是( )
A.完全溶于水后,
B.常温下,所含中子总数为
C.醋酸溶液中的分子总数目为
D.常温常压下,5.6L和混合气体含有氧原子数小于
8.如图为某学术期刊上刊登的八角形元素周期表,八角形的每个顶角对应一种元素。下列说法错误的是( )
A.图中虚线八角形顶角对应元素位于我们现行元素周期表的第四周期
B.图中虚线箭头所经过的元素,按箭头方向原子的电子层数增多
C.图中①代表的元素的单质在常温下能稳定存在,不发生化学反应
D.此八角形元素周期表中所表示的所有元素中没有副族元素
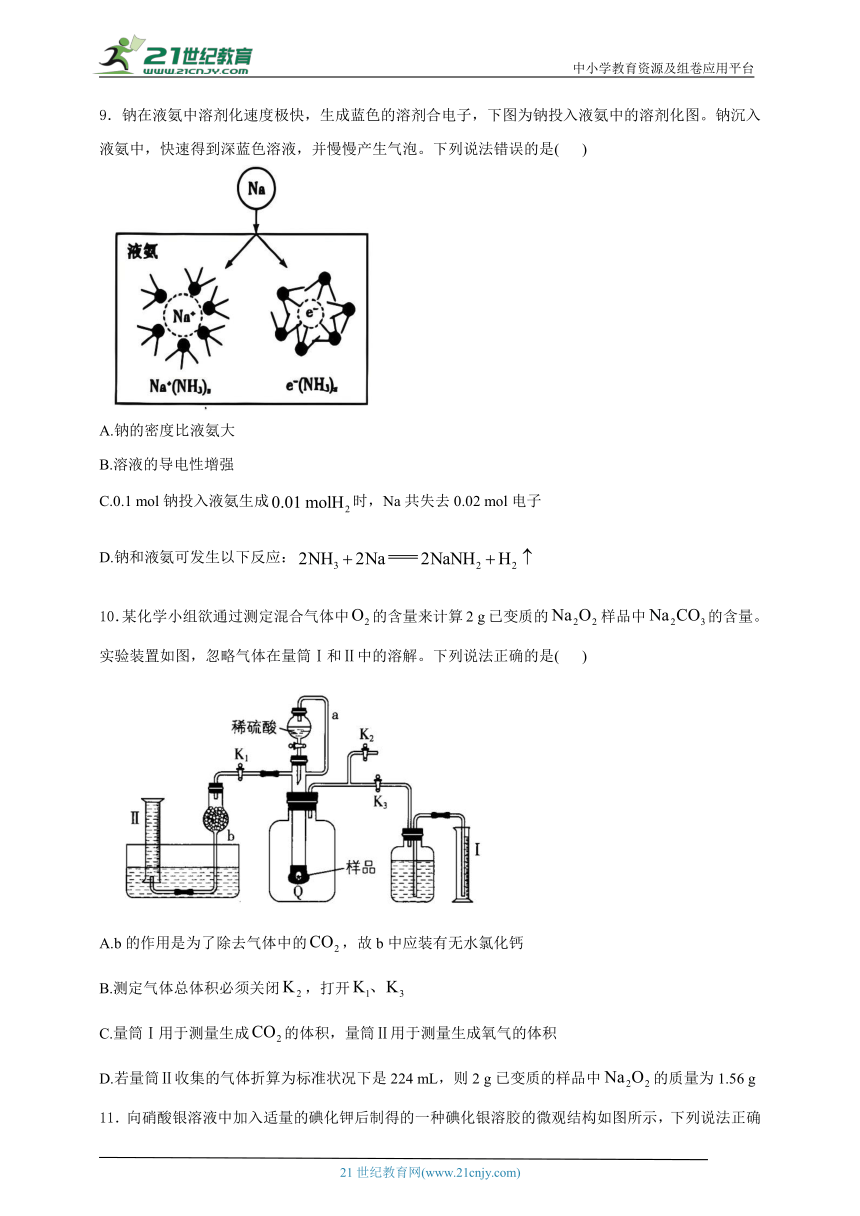
9.钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,下图为钠投入液氨中的溶剂化图。钠沉入液氨中,快速得到深蓝色溶液,并慢慢产生气泡。下列说法错误的是( )
A.钠的密度比液氨大
B.溶液的导电性增强
C.0.1 mol钠投入液氨生成时,Na共失去0.02 mol电子
D.钠和液氨可发生以下反应:
10.某化学小组欲通过测定混合气体中的含量来计算2 g已变质的样品中的含量。实验装置如图,忽略气体在量筒Ⅰ和Ⅱ中的溶解。下列说法正确的是( )
A.b的作用是为了除去气体中的,故b中应装有无水氯化钙
B.测定气体总体积必须关闭,打开
C.量筒Ⅰ用于测量生成的体积,量筒Ⅱ用于测量生成氧气的体积
D.若量筒Ⅱ收集的气体折算为标准状况下是224 mL,则2 g已变质的样品中的质量为1.56 g
11.向硝酸银溶液中加入适量的碘化钾后制得的一种碘化银溶胶的微观结构如图所示,下列说法正确的是( )
A.碘化银胶体粒子能吸附阳离子,从而使碘化银胶体带正电荷
B.用过滤的方法除去碘化银胶体中的硝酸钾溶液
C.碘化银溶胶中,胶体粒子的直径为1~100 nm
D.碘化银溶胶与硝酸银溶液的本质区别是前者会产生丁达尔效应
12.将400 mL NaCl和混合溶液分成两等份,第一份加入含a mol硝酸银的溶液,恰好使氯离子完全沉淀,第二份加入含b mol碳酸钠的溶液,恰好使钡离子完全沉淀,则测原混合液中钠离子的浓度为( )
A. B.
C. D.
13.短周期主族元素W、X、Y、Z、Q原子序数依次增大,形成的化合物是一种重要的食品添加剂,结构如下图。Z核外最外层电子数与X核外电子总数相等。W的原子半径在周期表中最小。下列有关叙述正确的是( )
A.原子半径大小:Y>Z>Q
B.该化合物中Y原子不满足8电子稳定结构
C.该化合物中,W、X、Y、Z、Q之间均为共价键
D.Q元素对应的单质能与水反应,也能与甲醇反应
14.120℃将10g下列物质在足量氧气中完全燃烧,将燃烧产物通过足量后,固体质量增加大于10g,该物质可能是( )
A. B. C. D.
二、非选择题:本题共4小题,共58分。
15.亚氯酸钠()是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊法制备亚氯酸钠的流程如图:
(1)反应①的化学方程式为:,该反应的还原产物是___________(写化学式)。
(2)在□补充反应②另一种产物,并配平此离子方程式,然后用单线桥法解题思路此化学反应。___________
________ +_________+_________=________+________+________□
(3)中Cl的化合价为___________,在反应②中___________(填字母)。
A.只能作氧化剂
B.只能作还原剂
C.既能作氧化剂也能作还原剂
(4)实验室采用马蒂逊法制备的实验装置如图甲所示:
已知:①的熔点为-59℃,沸点为11℃,的沸点为150℃。
②当温度低于38℃时,饱和溶液中析出的晶体是;当温度在38~60℃时,析出;温度高于60℃时,分解。
C中将装置浸入冰水浴中的目的是___________。
16.高锰酸钾是一种典型的强氧化剂。回答下列问题:
Ⅰ.在用酸性溶液处理和CuS的混合物时,发生的反应如下:
①(未配平)
②(未配平)
(1)下列关于反应①的说法中错误的是_______(填序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.生成2.24 L(标准状况下),转移电子的物质的量是0.8 mol
d.还原性的强弱关系是
Ⅱ.在稀硫酸中,与也能发生氧化还原反应。
(2)配平与反应的离子方程式。
(3)欲配制480 mL 溶液,需称()的质量为________g,需要的玻璃仪器有_____________________。
Ⅲ.实验室可由软锰矿(主要成分为)制备方法:先在高温下使软锰矿与过量KOH(s)和(s)反应生成(锰酸钾)和KCl;再用水溶解,滤去残渣;然后酸化滤液,使转化为和;最后滤去沉淀,浓缩结晶得到晶体。请回答:
(4)用软锰矿制备的化学方程式是_____________________。
(5)转化为的反应中氧化剂和还原剂的物质的量之比为_____________________。
17.过氧化钙()微溶于水,溶解度随温度降低而降低,化学性质与相似,可作医用防腐剂、消毒剂。如图是制备的一种方法。
回答下列问题:
(1)步骤Ⅰ中反应的离子方程式是_______________。
(2)步骤Ⅱ在冰水浴中进行,是为了防止挥发、___________(任写一条即可)。
(3)待结晶析出后通过____________(填操作)分离。
(4)与水缓慢反应,常用作鱼塘的供氧剂,其反应的化学方程式是___________。还可用于长途运输鱼苗,是因为________(填序号)。
a.可缓慢供氧 b.能吸收鱼苗呼出的 c.能潮解 d.可抑菌
(5)久置于空气中会生成。为测定某样品的纯度,取10 g样品加入足量稀盐酸,测得生成的质量为2.2 g,则样品中的质量分数为______。
18.我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。如图为联合制碱法的主要过程(部分物质已略去)。
已知:沉淀池中的反应为
请完成下列空白:
(1)煅烧炉中反应的化学方程式是________。
(2)已知物质X是一种酸性氧化物,则物质X是________(填化学式)。
(3)写出纯碱的主要用途________。(写出两种即可)
(4)若在小试管中加入一定量的饱和碳酸钠溶液,然后通入足量物质X,可观察到的实验现象为________,发生反应的离子方程式为________。
(5)某纯碱样品中含杂质,取样品,充分加热后,固体质量减少,此样品的质量分数为________。
参考答案
1.答案:C
解析:A.过氧化钠与水发生歧化反应,过氧化钠既是氧化剂又是还原剂,故A错误;
B.过氧化钠为淡黄色固体,氧化钠为白色固体,氧化钠与水反应只生成氢氧化钠,故B错误;
C.氧化钠中阴离子为氧离子,过氧化钠中阴离子为过氧根离子,则相同物质的量的氧化钠和过氧化钠中阴离子物质的量之比为1:1,故C正确;
D.过氧化钠与水反应生成氢氧化钠和氧气,不是碱性氧化物,故D错误;
故选:C。
2.答案:B
解析:A.用重结晶法除去苯甲酸混有的氯化钠是因为苯甲酸的溶解度随温度变化大,而氯化钠的溶解度随温度变化小,与苯甲酸是否具有酸性无关,故A错误;
B.草木灰的有效成分碳酸钾在溶液中水解使溶液呈碱性,氯化铵在溶液中水解使溶液呈酸性,草木灰与氯化铵混合使用时,碳酸钾溶液会与氯化铵溶液反应生成氨气会降低肥效,所以不能混施,故B正确;
C.铁离子能与硫氰酸根离子发生络合反应生成血红色的硫氰化铁,所以用硫氰化钾溶液检验铁离子,与铁离子能形成配位键有关,与铁离子的氧化性无关,故C错误;
D.铝在浓硝酸中会发生钝化,致密的钝化膜阻碍反应的继续进行,所以能用铝制容器盛装浓硝酸,故D错误;
故选B。
3.答案:A
解析:异丁烷的结构简式是,含13个共价键,故0.50 mol异丁烷分子中共价键的数目为,A正确;标准状况下为固体,不能用标准状况下的气体摩尔体积计算其物质的量,B错误;1.0 L pH=2的溶液中的数目为,C错误;溶液中部分水解,故的溶液中的数目少于,D错误。
4.答案:D
解析:
5.答案:B
解析:消毒效率,因为和作消毒剂时还原产物均为,所以共得5mol电子,共得2mol电子,两者的消毒效率之比为,A错误;根据反应①离子方程式可知,每生成,消耗,即消耗,而反应中每消耗1mol,生成和,即生成和2 mol HCl,故反应①消耗的硫酸是反应②生成的硫酸的物质的量的2倍,C错误;根据反应②的离子方程式可知,S的化合价升高,作还原剂,物质X是HCl与的混合物,D错误。
6.答案:A
解析:由题图可知,在反应①中被消耗,在反应⑤中又生成,因此是反应的催化剂,当浓度过大时,反应⑤的平衡会逆移,不利于获得最终产物,因此浓度不能过大,A错误;反应②使双键变为单键,是加成反应,反应④脱去小分子并生成双键,是消去反应,B正确;在反应过程中,有O-H等极性键的生成,也有C-O等极性键的断裂,C正确;根据“反应历程-能量”图像可知能垒最大的步骤是反应②,则制约反应速率的步骤为反应②,D正确。
7.答案:D
解析:与水的反应为可逆反应,不能进行到底,则1 mol 完全溶于水后,,A错误;常温下,的物质的量为,N原子的质子数为7,则中子数为,O原子的质子数为8,则中子数为,该物质含中子数总数为,B错误;醋酸溶液中含纯醋酸分子、水分子,则醋酸溶液中的分子总数目远大于,C错误;1个分子和1个分子都含有2个氧原子,常温常压条件下,大于,则常温常压下,和混合气体中含有氧原子数小于,D正确。
8.答案:C
解析:由图可知,每个八角形顶角对应元素均位于现行元素周期表的同一周期,则虚线八角形顶角对应元素为含K、Ca、Kr的第四周期元素,A正确;虚线箭头所经过的元素是第ⅣA族元素,按箭头方向原子的电子层数增多,B正确;图中①代表的元素是Na,Na和在常温下反应生成,C错误;此八角形元素周期表中只有主族元素和0族元素,没有副族元素,D正确。
9.答案:答案:C
解析:钠沉入液氨说明钠的密度比液氨大,A正确;液氨中没有能导电的离子,而钠投入液氨中生成和,能导电,说明溶液的导电性增强,B正确;0.1 mol钠投入液氨中,由于溶剂化速度极快,生成0.1 mol(氨合电子)时钠已经失去0.1 mol电子,故生成0.01 mol时,Na失去0.1 mol电子,C错误;反应中钠失去电子,只能是氢元素得到电子,所以钠和液氨可发生以下反应:,D正确。
10.答案:D
解析:b的作用是为了除去气体中的,无水氯化钙不能吸收二氧化碳,故b中不应装无水氯化钙,b中可以装碱石灰,A错误;测定气体总体积时必须关闭,打开, B错误;量筒Ⅰ用于测量生成的气体的总体积,量筒Ⅱ用于测量生成的氧气的体积,C错误;若量筒Ⅱ收集的气体折算为标准状况下是224 mL,则反应生成0.01 mol氧气,故2 g已变质的样品中的物质的量为0.02 mol,质量为1.56 g,D正确。
11.答案:答案:C
解析:碘化银胶体粒子能吸附阳离子,从而使碘化银胶粒带正电荷,碘化银胶体不带电荷,A错误;胶体粒子能透过滤纸,不能用过滤的方法除去碘化银胶体中的硝酸钾溶液,应该用渗析的方法除去碘化银胶体中的硝酸钾溶液,B错误;根据胶体的定义,碘化银溶胶中,胶体粒子的直径为1~100nm,C正确;碘化银溶胶与硝酸银溶液本质区别是分散质粒子直径不同,D错误。
12.答案:A
解析:第一份溶液中加入含硝酸银的溶液,发生反应:,氯离子恰好完全沉淀,则;同理,第二份溶液中加人含碳酸钠的溶液,恰好使钡离子完全沉淀,。根据电荷守恒可知每份溶液中,每份溶液中,溶液具有均一性,则原溶液中,选A。
13.答案:D
A.Y W为H、X为C、Y为N、Z为O、Q为Na,A.Y为N,Z为O,Q为Na,原子核外电子层数越多,原子半径越大,同周期元素从左到右原子半径减小,则原子半径:Q>Y>Z,故A错误;
B.该化合物中Y原子得到3个电子形成8电子稳定结构,故B错误;
C.该化合物中存在离子键和共价键,故C错误;
D.Q为Na,能与水、甲醇反应生成氢气,故D正确;
故选:D。
14.答案:B
解析:
15.答案:(1)
(2)
(3) +3;C
(4)增大的溶解度使其充分反应,防止温度过高使分解
解析:(1)反应①的化学方程式为:,是氧化剂,是还原剂,则该反应的还原产物是。
(2)由解题思路可知,反应在生成的同时,还有生成,则□对应的产物为,依据得失电子守恒的原则,的化学计量数分别为2、1,、的化学计量数分别为2、1,再利用质量守恒,便可配平的化学计量数。在反应中,中的O元素失电子,转移给中的Cl元素,转化电子数为。从而得出配平的离子方程式,然后用单线桥法解题思路此化学反应为:。
(3)中,Na显+1价,O显-2价,则Cl的化合价为+3,中O显-1价,反应②中既能作氧化剂也能作还原剂,故选C。
(4)实验室采用马蒂逊法制备,装置A用于制取,装置B用于收集,装置C中发生反应制取。
由于的热稳定性差,则C中将装置浸入冰水浴中的目的是:增大的溶解度使其充分反应,防止温度过高使分解。
16.答案:(1)d
(2)
(3)19.6;烧杯、玻璃棒、500 mL容量瓶、胶头滴管和量筒
(4)
(5)1:2
解析:(1)由题给信息可知,反应①中铜元素和硫元素的化合价升高被氧化,硫化亚铜是反应的还原剂,锰元素的化合价降低被还原,高锰酸钾是氧化剂、锰离子是还原产物,反应的离子方程式为。反应中铜元素和硫元素的化合价升高被氧化,a正确;由离子方程式可知,氧化剂高锰酸钾与还原剂硫化亚铜的物质的量之比为8:5,b正确;由离子方程式可知,反应生成5 mol二氧化硫时,转移电子的物质的量为40 mol,则标准状况下生成2.24 L二氧化硫时,转移电子的物质的量,c正确:由解题思路可知,硫化亚铜是反应的还原剂,锰离子是还原产物,由还原剂的还原性强于还原产物可知,硫化亚铜的还原性强于锰离子,d错误。
(2)由未配平的离子方程式可知,在稀硫酸中,高锰酸钾溶液与硫酸亚铁铵溶液反应生成硫酸铁、硫酸铵、硫酸锰和水,反应的离子方程式为。
(3)实验室没有480 mL容量瓶,所以配制溶液时,应选用500 mL容量瓶,由配制一定物质的量浓度溶液配制的步骤可知,实验过程中需要用到的玻璃仪器为胶头滴管、烧杯、玻璃棒、500 mL容量瓶和量筒,则需称取硫酸亚铁铵的质量为。
(4)由题意可知,用软锰矿制备锰酸钾发生的反应为二氧化锰与氢氧化钾和氯酸钾在高温下反应生成锰酸钾和氯化钾,反应的化学方程式为。
(5)由题意可知,锰酸钾转化为高锰酸钾的反应为酸性条件下锰酸根离子发生歧化反应生成高锰酸根离子、二氧化锰沉淀和水,反应的离子方程式为,由离子方程式可知,反应中氧化产物高锰酸根离子和还原产物二氧化锰的物质的量比为2:1,所以反应中氧化剂和还原剂的物质的量之比为1:2。
17.答案:(1)
(2)防止过氧化氢分解、降低产物的溶解度而析出
(3)过滤
(4);abd
(5)50%
解析:(1)步骤Ⅰ中碳酸钙与盐酸反应得到氯化钙、水和氧化碳气体,反应的离子方程式是。
(2)冰水浴可以防止挥发、过氧化氢分解,还可以降低产物的溶解度从而析出。
(3)过滤用于分离固液混合物,通过过滤把晶体从混合体系中分离。
(4)过氧化钙与水缓慢反应生成氢氧化钙、氧气,化学方程式为;过氧化钙与水缓慢反应生成氢氧化钙、氧气,故能缓慢供氧,正确;过氧化钙转变生成的氢氧化钙能吸收鱼苗呼出的气体,b正确;过氧化钙微溶于水,不能潮解,c错误;过氧化钙具有强氧化性,加入水中可以起到杀菌消毒的作用,d正确。
(5)10 g样品为和的混合物,加入足量稀盐酸发生反应生成二氧化碳,已知的质量为2.2 g,则10 g样品中碳酸钙的质量为5 g,10 g样品中的质量为10 g-5 g=5 g,则样品中的质量分数为。
18.答案:(1)
(2)
(3)纺织、制皂、造纸、制玻璃、工业碱、食用碱(写出其中两种,合理即可)
(4)有白色晶体析出;
(5)或
解析:
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
2024-2025学年高一化学人教版(2019)上学期期末教学质量模拟检测(二)(含解析)
注意事项:
1.答题前,考生先将自己的姓名准考证号码填写清楚,将条形码准确粘贴在考生信息条形码粘贴区。
2.选择题必须使用2B铅笔填涂;非选择题必须使用0.5毫米黑色字迹的签字笔书写,字体工整、笔迹清楚。
3.请按照题号顺序在答题卡各题目的答题区域内作答,超出答题区域书写的答案无效;在草稿纸、试卷上答题无效。
4.作图可先使用铅笔画出,确定后必须用黑色字迹的签字笔描黑。
5.保持卡面清洁,不要折叠,不要弄破、异皱,不准使用涂改液、修正带、刮纸刀。
可能用到的相对原子质量:
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目要求。
1.下列关于氧化钠和过氧化钠的叙述正确的是( )
A.在与水的反应中,氧化剂是,还原剂是水
B.和都是白色固体,都能与冷水作用得到和NaOH
C.相同物质的量的氧化钠和过氧化钠中阴离子物质的量之比为1:1
D.与都能与水反应生成碱,它们都是碱性氧化物
2.下列陈述I与陈述II均正确,且具有因果关系的是( )
选项 陈述I 陈述II
A 用重结晶法除去苯甲酸混有的 苯甲酸具有酸性
B 草木灰不能与混合使用 与反应生成氨气会降低肥效
C 用溶液检验 具有氧化性
D 用铝制容器盛装浓硝酸 铝与浓硝酸不反应
A.A B.B C.C D.D
3.为阿伏伽德罗常数的值。下列叙述正确的是( )
A.异丁烷分子中共价键的数目为
B.标准状况下,中电子的数目为
C.的溶液中的数目为
D.的溶液中的数目为
4.下列以物质的量为中心的计算正确的是( )
A.溶液中含有的物质的量为0.2mol
B.常温常压下,含有分子的物质的量为0.2mol
C.5.6gFe与足量氯气反应失去电子的物质的量为0.2mol
D.3.2g由、组成的混合气体中含有原子的物质的量为0.2mol
5.二氧化氯是国际上公认的安全、无毒的绿色消毒剂。“R7法”制备二氧化氯的优点是副产品氯气经处理后可循环利用,具体制备流程如图所示。消毒效率。
下列说法正确的是( )
A.和的消毒效率之比为71:18
B.反应①生成的离子方程式:
C.反应①消耗的硫酸与反应②生成的硫酸物质的量相等
D.反应②中作还原剂,物质X为
6.丙酮和甲胺的反应机理及能量图像如图所示。
下列说法错误的是( )
A.该历程中为催化剂,故浓度越大,反应速率越快
B.该历程中发生了加成反应和消去反应
C.反应过程中有极性键的断裂和生成
D.该历程中制约反应速率的反应为反应②
7.为阿伏加德罗常数的值。下列叙述正确的是( )
A.完全溶于水后,
B.常温下,所含中子总数为
C.醋酸溶液中的分子总数目为
D.常温常压下,5.6L和混合气体含有氧原子数小于
8.如图为某学术期刊上刊登的八角形元素周期表,八角形的每个顶角对应一种元素。下列说法错误的是( )
A.图中虚线八角形顶角对应元素位于我们现行元素周期表的第四周期
B.图中虚线箭头所经过的元素,按箭头方向原子的电子层数增多
C.图中①代表的元素的单质在常温下能稳定存在,不发生化学反应
D.此八角形元素周期表中所表示的所有元素中没有副族元素
9.钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,下图为钠投入液氨中的溶剂化图。钠沉入液氨中,快速得到深蓝色溶液,并慢慢产生气泡。下列说法错误的是( )
A.钠的密度比液氨大
B.溶液的导电性增强
C.0.1 mol钠投入液氨生成时,Na共失去0.02 mol电子
D.钠和液氨可发生以下反应:
10.某化学小组欲通过测定混合气体中的含量来计算2 g已变质的样品中的含量。实验装置如图,忽略气体在量筒Ⅰ和Ⅱ中的溶解。下列说法正确的是( )
A.b的作用是为了除去气体中的,故b中应装有无水氯化钙
B.测定气体总体积必须关闭,打开
C.量筒Ⅰ用于测量生成的体积,量筒Ⅱ用于测量生成氧气的体积
D.若量筒Ⅱ收集的气体折算为标准状况下是224 mL,则2 g已变质的样品中的质量为1.56 g
11.向硝酸银溶液中加入适量的碘化钾后制得的一种碘化银溶胶的微观结构如图所示,下列说法正确的是( )
A.碘化银胶体粒子能吸附阳离子,从而使碘化银胶体带正电荷
B.用过滤的方法除去碘化银胶体中的硝酸钾溶液
C.碘化银溶胶中,胶体粒子的直径为1~100 nm
D.碘化银溶胶与硝酸银溶液的本质区别是前者会产生丁达尔效应
12.将400 mL NaCl和混合溶液分成两等份,第一份加入含a mol硝酸银的溶液,恰好使氯离子完全沉淀,第二份加入含b mol碳酸钠的溶液,恰好使钡离子完全沉淀,则测原混合液中钠离子的浓度为( )
A. B.
C. D.
13.短周期主族元素W、X、Y、Z、Q原子序数依次增大,形成的化合物是一种重要的食品添加剂,结构如下图。Z核外最外层电子数与X核外电子总数相等。W的原子半径在周期表中最小。下列有关叙述正确的是( )
A.原子半径大小:Y>Z>Q
B.该化合物中Y原子不满足8电子稳定结构
C.该化合物中,W、X、Y、Z、Q之间均为共价键
D.Q元素对应的单质能与水反应,也能与甲醇反应
14.120℃将10g下列物质在足量氧气中完全燃烧,将燃烧产物通过足量后,固体质量增加大于10g,该物质可能是( )
A. B. C. D.
二、非选择题:本题共4小题,共58分。
15.亚氯酸钠()是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊法制备亚氯酸钠的流程如图:
(1)反应①的化学方程式为:,该反应的还原产物是___________(写化学式)。
(2)在□补充反应②另一种产物,并配平此离子方程式,然后用单线桥法解题思路此化学反应。___________
________ +_________+_________=________+________+________□
(3)中Cl的化合价为___________,在反应②中___________(填字母)。
A.只能作氧化剂
B.只能作还原剂
C.既能作氧化剂也能作还原剂
(4)实验室采用马蒂逊法制备的实验装置如图甲所示:
已知:①的熔点为-59℃,沸点为11℃,的沸点为150℃。
②当温度低于38℃时,饱和溶液中析出的晶体是;当温度在38~60℃时,析出;温度高于60℃时,分解。
C中将装置浸入冰水浴中的目的是___________。
16.高锰酸钾是一种典型的强氧化剂。回答下列问题:
Ⅰ.在用酸性溶液处理和CuS的混合物时,发生的反应如下:
①(未配平)
②(未配平)
(1)下列关于反应①的说法中错误的是_______(填序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.生成2.24 L(标准状况下),转移电子的物质的量是0.8 mol
d.还原性的强弱关系是
Ⅱ.在稀硫酸中,与也能发生氧化还原反应。
(2)配平与反应的离子方程式。
(3)欲配制480 mL 溶液,需称()的质量为________g,需要的玻璃仪器有_____________________。
Ⅲ.实验室可由软锰矿(主要成分为)制备方法:先在高温下使软锰矿与过量KOH(s)和(s)反应生成(锰酸钾)和KCl;再用水溶解,滤去残渣;然后酸化滤液,使转化为和;最后滤去沉淀,浓缩结晶得到晶体。请回答:
(4)用软锰矿制备的化学方程式是_____________________。
(5)转化为的反应中氧化剂和还原剂的物质的量之比为_____________________。
17.过氧化钙()微溶于水,溶解度随温度降低而降低,化学性质与相似,可作医用防腐剂、消毒剂。如图是制备的一种方法。
回答下列问题:
(1)步骤Ⅰ中反应的离子方程式是_______________。
(2)步骤Ⅱ在冰水浴中进行,是为了防止挥发、___________(任写一条即可)。
(3)待结晶析出后通过____________(填操作)分离。
(4)与水缓慢反应,常用作鱼塘的供氧剂,其反应的化学方程式是___________。还可用于长途运输鱼苗,是因为________(填序号)。
a.可缓慢供氧 b.能吸收鱼苗呼出的 c.能潮解 d.可抑菌
(5)久置于空气中会生成。为测定某样品的纯度,取10 g样品加入足量稀盐酸,测得生成的质量为2.2 g,则样品中的质量分数为______。
18.我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。如图为联合制碱法的主要过程(部分物质已略去)。
已知:沉淀池中的反应为
请完成下列空白:
(1)煅烧炉中反应的化学方程式是________。
(2)已知物质X是一种酸性氧化物,则物质X是________(填化学式)。
(3)写出纯碱的主要用途________。(写出两种即可)
(4)若在小试管中加入一定量的饱和碳酸钠溶液,然后通入足量物质X,可观察到的实验现象为________,发生反应的离子方程式为________。
(5)某纯碱样品中含杂质,取样品,充分加热后,固体质量减少,此样品的质量分数为________。
参考答案
1.答案:C
解析:A.过氧化钠与水发生歧化反应,过氧化钠既是氧化剂又是还原剂,故A错误;
B.过氧化钠为淡黄色固体,氧化钠为白色固体,氧化钠与水反应只生成氢氧化钠,故B错误;
C.氧化钠中阴离子为氧离子,过氧化钠中阴离子为过氧根离子,则相同物质的量的氧化钠和过氧化钠中阴离子物质的量之比为1:1,故C正确;
D.过氧化钠与水反应生成氢氧化钠和氧气,不是碱性氧化物,故D错误;
故选:C。
2.答案:B
解析:A.用重结晶法除去苯甲酸混有的氯化钠是因为苯甲酸的溶解度随温度变化大,而氯化钠的溶解度随温度变化小,与苯甲酸是否具有酸性无关,故A错误;
B.草木灰的有效成分碳酸钾在溶液中水解使溶液呈碱性,氯化铵在溶液中水解使溶液呈酸性,草木灰与氯化铵混合使用时,碳酸钾溶液会与氯化铵溶液反应生成氨气会降低肥效,所以不能混施,故B正确;
C.铁离子能与硫氰酸根离子发生络合反应生成血红色的硫氰化铁,所以用硫氰化钾溶液检验铁离子,与铁离子能形成配位键有关,与铁离子的氧化性无关,故C错误;
D.铝在浓硝酸中会发生钝化,致密的钝化膜阻碍反应的继续进行,所以能用铝制容器盛装浓硝酸,故D错误;
故选B。
3.答案:A
解析:异丁烷的结构简式是,含13个共价键,故0.50 mol异丁烷分子中共价键的数目为,A正确;标准状况下为固体,不能用标准状况下的气体摩尔体积计算其物质的量,B错误;1.0 L pH=2的溶液中的数目为,C错误;溶液中部分水解,故的溶液中的数目少于,D错误。
4.答案:D
解析:
5.答案:B
解析:消毒效率,因为和作消毒剂时还原产物均为,所以共得5mol电子,共得2mol电子,两者的消毒效率之比为,A错误;根据反应①离子方程式可知,每生成,消耗,即消耗,而反应中每消耗1mol,生成和,即生成和2 mol HCl,故反应①消耗的硫酸是反应②生成的硫酸的物质的量的2倍,C错误;根据反应②的离子方程式可知,S的化合价升高,作还原剂,物质X是HCl与的混合物,D错误。
6.答案:A
解析:由题图可知,在反应①中被消耗,在反应⑤中又生成,因此是反应的催化剂,当浓度过大时,反应⑤的平衡会逆移,不利于获得最终产物,因此浓度不能过大,A错误;反应②使双键变为单键,是加成反应,反应④脱去小分子并生成双键,是消去反应,B正确;在反应过程中,有O-H等极性键的生成,也有C-O等极性键的断裂,C正确;根据“反应历程-能量”图像可知能垒最大的步骤是反应②,则制约反应速率的步骤为反应②,D正确。
7.答案:D
解析:与水的反应为可逆反应,不能进行到底,则1 mol 完全溶于水后,,A错误;常温下,的物质的量为,N原子的质子数为7,则中子数为,O原子的质子数为8,则中子数为,该物质含中子数总数为,B错误;醋酸溶液中含纯醋酸分子、水分子,则醋酸溶液中的分子总数目远大于,C错误;1个分子和1个分子都含有2个氧原子,常温常压条件下,大于,则常温常压下,和混合气体中含有氧原子数小于,D正确。
8.答案:C
解析:由图可知,每个八角形顶角对应元素均位于现行元素周期表的同一周期,则虚线八角形顶角对应元素为含K、Ca、Kr的第四周期元素,A正确;虚线箭头所经过的元素是第ⅣA族元素,按箭头方向原子的电子层数增多,B正确;图中①代表的元素是Na,Na和在常温下反应生成,C错误;此八角形元素周期表中只有主族元素和0族元素,没有副族元素,D正确。
9.答案:答案:C
解析:钠沉入液氨说明钠的密度比液氨大,A正确;液氨中没有能导电的离子,而钠投入液氨中生成和,能导电,说明溶液的导电性增强,B正确;0.1 mol钠投入液氨中,由于溶剂化速度极快,生成0.1 mol(氨合电子)时钠已经失去0.1 mol电子,故生成0.01 mol时,Na失去0.1 mol电子,C错误;反应中钠失去电子,只能是氢元素得到电子,所以钠和液氨可发生以下反应:,D正确。
10.答案:D
解析:b的作用是为了除去气体中的,无水氯化钙不能吸收二氧化碳,故b中不应装无水氯化钙,b中可以装碱石灰,A错误;测定气体总体积时必须关闭,打开, B错误;量筒Ⅰ用于测量生成的气体的总体积,量筒Ⅱ用于测量生成的氧气的体积,C错误;若量筒Ⅱ收集的气体折算为标准状况下是224 mL,则反应生成0.01 mol氧气,故2 g已变质的样品中的物质的量为0.02 mol,质量为1.56 g,D正确。
11.答案:答案:C
解析:碘化银胶体粒子能吸附阳离子,从而使碘化银胶粒带正电荷,碘化银胶体不带电荷,A错误;胶体粒子能透过滤纸,不能用过滤的方法除去碘化银胶体中的硝酸钾溶液,应该用渗析的方法除去碘化银胶体中的硝酸钾溶液,B错误;根据胶体的定义,碘化银溶胶中,胶体粒子的直径为1~100nm,C正确;碘化银溶胶与硝酸银溶液本质区别是分散质粒子直径不同,D错误。
12.答案:A
解析:第一份溶液中加入含硝酸银的溶液,发生反应:,氯离子恰好完全沉淀,则;同理,第二份溶液中加人含碳酸钠的溶液,恰好使钡离子完全沉淀,。根据电荷守恒可知每份溶液中,每份溶液中,溶液具有均一性,则原溶液中,选A。
13.答案:D
A.Y W为H、X为C、Y为N、Z为O、Q为Na,A.Y为N,Z为O,Q为Na,原子核外电子层数越多,原子半径越大,同周期元素从左到右原子半径减小,则原子半径:Q>Y>Z,故A错误;
B.该化合物中Y原子得到3个电子形成8电子稳定结构,故B错误;
C.该化合物中存在离子键和共价键,故C错误;
D.Q为Na,能与水、甲醇反应生成氢气,故D正确;
故选:D。
14.答案:B
解析:
15.答案:(1)
(2)
(3) +3;C
(4)增大的溶解度使其充分反应,防止温度过高使分解
解析:(1)反应①的化学方程式为:,是氧化剂,是还原剂,则该反应的还原产物是。
(2)由解题思路可知,反应在生成的同时,还有生成,则□对应的产物为,依据得失电子守恒的原则,的化学计量数分别为2、1,、的化学计量数分别为2、1,再利用质量守恒,便可配平的化学计量数。在反应中,中的O元素失电子,转移给中的Cl元素,转化电子数为。从而得出配平的离子方程式,然后用单线桥法解题思路此化学反应为:。
(3)中,Na显+1价,O显-2价,则Cl的化合价为+3,中O显-1价,反应②中既能作氧化剂也能作还原剂,故选C。
(4)实验室采用马蒂逊法制备,装置A用于制取,装置B用于收集,装置C中发生反应制取。
由于的热稳定性差,则C中将装置浸入冰水浴中的目的是:增大的溶解度使其充分反应,防止温度过高使分解。
16.答案:(1)d
(2)
(3)19.6;烧杯、玻璃棒、500 mL容量瓶、胶头滴管和量筒
(4)
(5)1:2
解析:(1)由题给信息可知,反应①中铜元素和硫元素的化合价升高被氧化,硫化亚铜是反应的还原剂,锰元素的化合价降低被还原,高锰酸钾是氧化剂、锰离子是还原产物,反应的离子方程式为。反应中铜元素和硫元素的化合价升高被氧化,a正确;由离子方程式可知,氧化剂高锰酸钾与还原剂硫化亚铜的物质的量之比为8:5,b正确;由离子方程式可知,反应生成5 mol二氧化硫时,转移电子的物质的量为40 mol,则标准状况下生成2.24 L二氧化硫时,转移电子的物质的量,c正确:由解题思路可知,硫化亚铜是反应的还原剂,锰离子是还原产物,由还原剂的还原性强于还原产物可知,硫化亚铜的还原性强于锰离子,d错误。
(2)由未配平的离子方程式可知,在稀硫酸中,高锰酸钾溶液与硫酸亚铁铵溶液反应生成硫酸铁、硫酸铵、硫酸锰和水,反应的离子方程式为。
(3)实验室没有480 mL容量瓶,所以配制溶液时,应选用500 mL容量瓶,由配制一定物质的量浓度溶液配制的步骤可知,实验过程中需要用到的玻璃仪器为胶头滴管、烧杯、玻璃棒、500 mL容量瓶和量筒,则需称取硫酸亚铁铵的质量为。
(4)由题意可知,用软锰矿制备锰酸钾发生的反应为二氧化锰与氢氧化钾和氯酸钾在高温下反应生成锰酸钾和氯化钾,反应的化学方程式为。
(5)由题意可知,锰酸钾转化为高锰酸钾的反应为酸性条件下锰酸根离子发生歧化反应生成高锰酸根离子、二氧化锰沉淀和水,反应的离子方程式为,由离子方程式可知,反应中氧化产物高锰酸根离子和还原产物二氧化锰的物质的量比为2:1,所以反应中氧化剂和还原剂的物质的量之比为1:2。
17.答案:(1)
(2)防止过氧化氢分解、降低产物的溶解度而析出
(3)过滤
(4);abd
(5)50%
解析:(1)步骤Ⅰ中碳酸钙与盐酸反应得到氯化钙、水和氧化碳气体,反应的离子方程式是。
(2)冰水浴可以防止挥发、过氧化氢分解,还可以降低产物的溶解度从而析出。
(3)过滤用于分离固液混合物,通过过滤把晶体从混合体系中分离。
(4)过氧化钙与水缓慢反应生成氢氧化钙、氧气,化学方程式为;过氧化钙与水缓慢反应生成氢氧化钙、氧气,故能缓慢供氧,正确;过氧化钙转变生成的氢氧化钙能吸收鱼苗呼出的气体,b正确;过氧化钙微溶于水,不能潮解,c错误;过氧化钙具有强氧化性,加入水中可以起到杀菌消毒的作用,d正确。
(5)10 g样品为和的混合物,加入足量稀盐酸发生反应生成二氧化碳,已知的质量为2.2 g,则10 g样品中碳酸钙的质量为5 g,10 g样品中的质量为10 g-5 g=5 g,则样品中的质量分数为。
18.答案:(1)
(2)
(3)纺织、制皂、造纸、制玻璃、工业碱、食用碱(写出其中两种,合理即可)
(4)有白色晶体析出;
(5)或
解析:
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
