山东省即墨市移风中学鲁教版九年级化学全册 8.2 海水晒盐(共34张PPT)
文档属性
| 名称 | 山东省即墨市移风中学鲁教版九年级化学全册 8.2 海水晒盐(共34张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-04-05 00:00:00 | ||
图片预览









文档简介
课件34张PPT。第二节 海水“晒盐”阅读教材P35的内容,回答下列问题:1.目前,从海水中提取食盐的方法是什么?
2.“盐田法”通常由几部分组成?
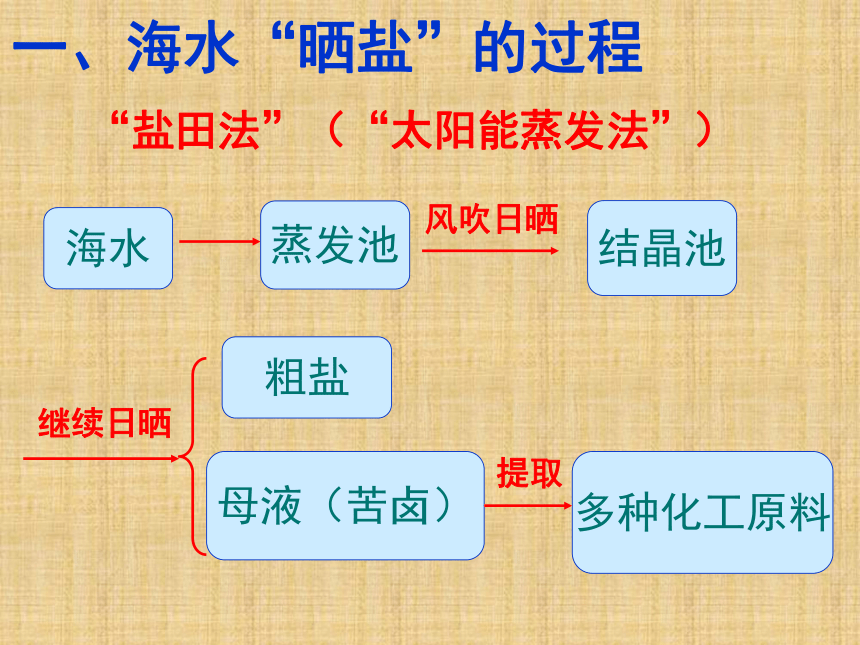
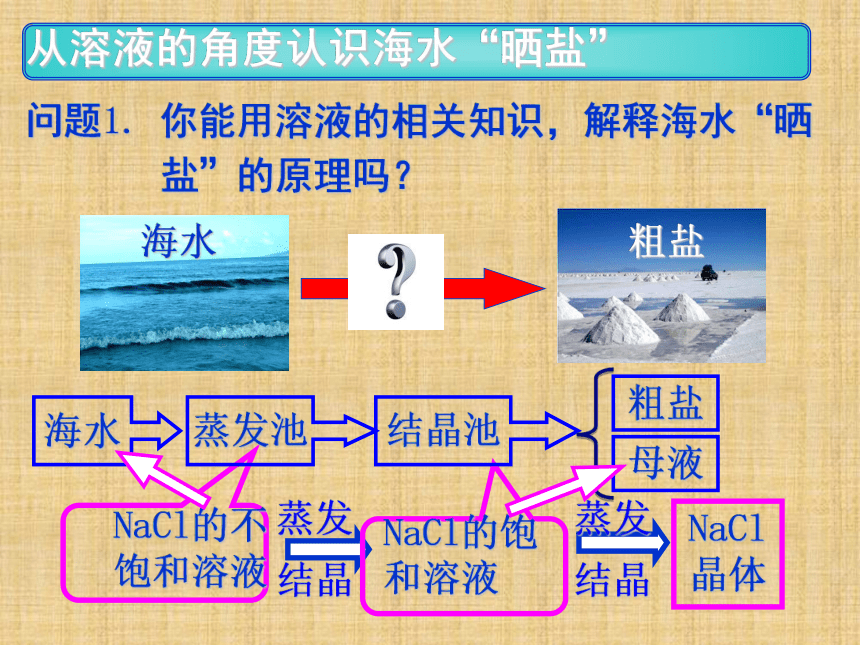
3.海水“晒盐”的过程是什么?一、海水“晒盐”的过程海水蒸发池结晶池粗盐母液(苦卤)多种化工原料“盐田法”(“太阳能蒸发法”)风吹日晒继续日晒提取问题1. 你能用溶液的相关知识,解释海水“晒 盐”的原理吗?NaCl 晶体NaCl的不饱和溶液NaCl的饱和溶液海水粗盐蒸发结晶蒸发结晶 根据以上认识,你能说说什么是饱和溶液吗?饱和溶液:
在一定温度下,在一定量的溶剂里,不能再继续溶解某种溶质的溶液就是该溶质的饱和溶液。回顾提升怎样判断一种溶液是否饱和?
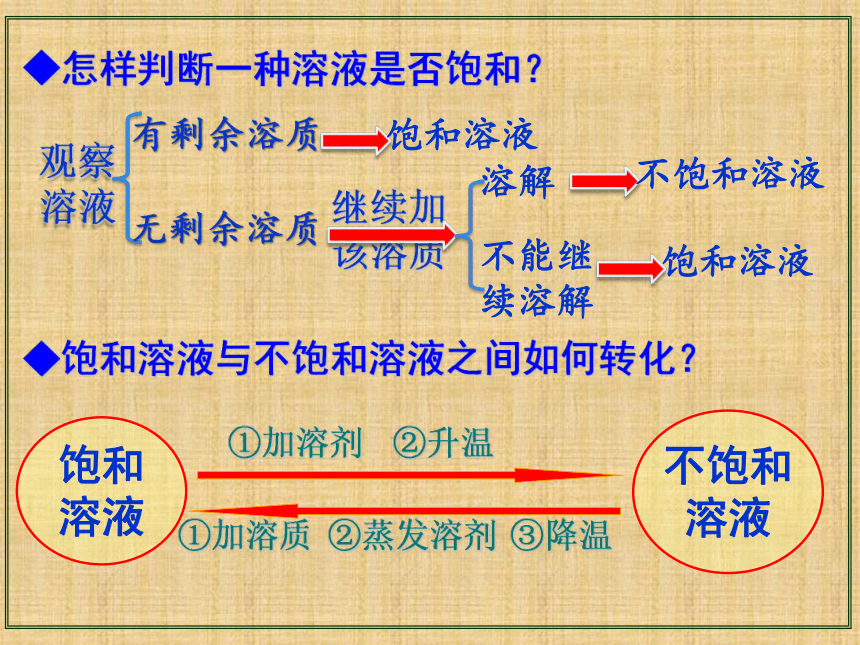
饱和溶液与不饱和溶液之间如何转化?①加溶质 ②蒸发溶剂 ③降温②升温①加溶剂饱和
溶液不饱和
溶液观察溶液有剩余溶质饱和溶液无剩余溶质继续加该溶质溶解不能继续溶解不饱和溶液饱和溶液◆饱和溶液与不饱和溶液之间如何转化?◆怎样判断一种溶液是否饱和?思考:
1.上述过程中,氯化钠溶液从不饱和变为饱和的途径是什么?你能够从现象上判断溶液何时饱和的吗你?
2.你认为哪些自然条件有利于海水“晒盐”?为什么? 取少许不饱和氯化钠溶液,滴在洁净的玻璃片上,用电热吹风机向玻璃片上的溶液吹热风,观察现象。活动天地结晶:一定条件下,固体物质从它的饱和溶液中以晶体的形式析出的过程叫结晶结晶方法:蒸发溶剂法、降温法C关于海水“晒盐”的叙述正确的是 ( )
A.利用海水降温析出晶体
B.海水晒盐后的母液因食盐减少而变成不
饱和溶液
C.利用阳光和风力使水分蒸发得到食盐
D.利用海水在阳光下分解得到食盐晶体跟踪训练实验探究1.提出问题:哪些因素影响固体物质在 水中的溶解限量?2.猜想假设:小贴士控制变量法:如果有许多因素会同时影响某一实验结果,当我们要研究其中的一种因素时,要控制其它因素保持不变,只研究这一个变量对实验结果的影响。活动一:探究固体物质在水中溶解限量的影响因素(2)温度(1)溶质(溶剂)的 种类(3)水的量溶解不溶不溶溶解实验探究影响物质溶解性的因素二、溶解度二、固体物质在水中的溶解度(一)影响固体物质在水中的溶解限量(溶解性)的因素1.溶质、溶剂种类3.温度2.溶剂质量(一) 溶解度的定义 在一定温度下,某固体物质在100g溶剂里达到饱和状态时所溶解的溶质质量,叫做这种物质的在这种溶剂里的溶解度。注意:条件:一定温度。
标准:100克溶剂
状态:饱和状态
单位:克请你来找茬,看看缺什么
1.20℃时,10g食盐溶解在100g水中,所以20℃时,食盐的溶解度是10g。2.100g水中溶解了36g食盐刚好达到饱和,所以食盐的溶解度是36g。3.在20℃时,100g水里最多溶解了33.3g氯化铵,所 20℃时氯化铵的溶解度是33.3。4.在20℃时,100g硝酸钾的饱和溶液里含硝酸钾24g
则20℃时硝酸钾的溶解度是24g。抢答20℃时,100g水中最多溶解36g氯化钠理解:20℃时氯化钠的溶解度为36g1.含义:20℃时,100g水中溶解氯化钠达到饱和状态时,质量为36g .深入探究2:20℃饱和溶液中:m溶质:m溶剂:m溶液:——:———:——3:求20℃饱和溶液中溶质质量分数——4:20℃将20g氯化钠固体加入50g水中,所得溶液质量是——,溶质质量分数是————9253426.7%6826.7%蒸发结晶、降温结晶三种典型物质溶解度曲线氢氧化钙溶解度/g问题3.固体物质溶解度随温度的变化有哪些规律?溶解度/g1.大多数物质的溶解度随温度的升高而增大,如KNO3。
2.少数物质的溶解度随温度的升 高变化不大 ,如NaCl。
3.极少数物质的溶解度随温度的升高而减小,如Ca(OH)2。
定义:表示物质溶解度随温度变化的曲线叫溶解度曲线
(1)查找0—100℃时物质的溶解度,并判断溶解性。.溶解度曲线有哪些应用?(2)比较相同温度时,不同物质溶解度的大小。(3)确定物质的溶解度受温度影响的程度,并据此确定物质结晶的方法。
(4)判断溶液是否饱和。降温结晶:提纯溶解度受温度变化影响比较大的物质如:硝酸钾
蒸发结晶:提纯溶解度受温度变化影响不大的物质如:氯化钠
(5)溶解度曲线交点意义:40℃A、 B溶解度相等。1.如图,A点表示_____________________,
所在溶液是______溶液;
2.B点表示______________________________;
3.80℃时,a的溶解度___ b的溶解度(填“>”“<”或“=”)请你试一试80℃时,a的溶解度为85g饱和a,b两物质在60 ℃时,溶解度相等为52g>不饱和 饱和 A.CB4.C点对于a物质是 _________溶液,
对于b物质是_________溶液。
溶解度与溶解性的关系几种固体物质溶解度曲线 1. 生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”。你能解释其中的道理吗?跟踪训练蒸发结晶降温结晶(冷却热饱和溶液)适用范围:溶解度随温度升高而显著增大的物质适用范围:溶解度随温度升高变化不大的物质多识一点结晶方法课外探究 对下列现象你熟悉吗?请查阅有关气体溶解度的相关资料,来解释一下吧!
(1)天气闷热时,鱼儿为什么总爱在水面上进行呼吸?
(2)喝了汽水后,你常会打嗝,这是什么原因?
(3)打开汽水瓶盖,你能看到什么现象?为什么?多识一点影响气体溶解度的因素温度越高气体的溶解度越小
压强越大气体的溶解度越大多识一点 1.A、B、C三种物质的溶解度曲线如图所示:
(1)40℃时B物质的溶解度是多少?
(2)m点表示什么意义?
(3)40℃时,三种物质的溶解度由小到大的顺序是( )(A) C、B、A
(B) A、B、C
(C) B、A、C
(D) B、C、AB 巩固练习2.下图是甲、乙、丙三种物质的溶解度曲线.下列说法正确的是( )
A.在t1℃时,三种物质的溶解度由大到小的顺序是甲>乙>丙
B.在t2℃时,甲、乙两物质的溶解度相等
C.甲、乙、丙三种物质的饱和溶液升温都会转化为不饱和溶液
D.当乙的饱和溶液中混有少量丙时,可采用降温结晶的方法析出丙 B3.甲、乙两种固体的溶解度曲线如下图。现将两试管分别装入甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体),再放进盛有冰水的烧杯里, 则下列说法正确的是( )
A.甲溶液中溶质的质量分数增大
B.乙溶液中剩余的固体减少
C.试管里甲、乙物质的溶解度都增大
D.试管里甲、乙两溶液中的溶质都减少
再放进盛有冰水的烧杯里, 则下列说
再放进盛有冰水的烧杯里, 则下列说
B4.根据下列几种物质溶解度曲线图,得到的结论正确的是( ) A.硝酸钾中混有少量氯化钠,采用蒸发结晶进行提纯
B.氢氧化钙饱和溶液降低温度后有晶体析出
C.80℃时,氯化钾与硫酸镁的溶解度相等
D.所有物质的溶解度均随温度的升高而增大或随温度 的降低而减小C 2. A、B、C三种物质的溶解度曲线如图所示:
40℃时B物质的溶解度是多少?
m点表示什么意义?
40℃时,三种物质的溶解度由小到大的顺序是( ) C、B、A
A、B、C
B、A、C
B、C、A7030B室温(20℃)时:S <0.01g易溶物可溶物微溶物 难溶物
(不溶物)S>10g1g<S<10g0.01g< S <1g多识一点1.降温结晶(冷却热饱和溶液):使溶解度随温度升高显著增大的物质从溶液中结晶析出,例如:KNO3结晶:一定条件下,固体物质从它的饱和溶液中以晶体的形式析出的过程叫结晶2.蒸发结晶法(蒸发溶剂法):使溶解度随温度升高而变化不明显的物质从溶液中结晶析出,例如:NaCl补充:影响气体溶解度的因素温度越高气体的溶解度越小
压强越大气体的溶解度越大问题4.观察下列三种物质的溶解度曲线,你能提出哪些问题? 将60℃时A、B、C的饱和溶液分别降温到40℃,三种物质溶液的溶质质量分数如何变化?
2.“盐田法”通常由几部分组成?
3.海水“晒盐”的过程是什么?一、海水“晒盐”的过程海水蒸发池结晶池粗盐母液(苦卤)多种化工原料“盐田法”(“太阳能蒸发法”)风吹日晒继续日晒提取问题1. 你能用溶液的相关知识,解释海水“晒 盐”的原理吗?NaCl 晶体NaCl的不饱和溶液NaCl的饱和溶液海水粗盐蒸发结晶蒸发结晶 根据以上认识,你能说说什么是饱和溶液吗?饱和溶液:
在一定温度下,在一定量的溶剂里,不能再继续溶解某种溶质的溶液就是该溶质的饱和溶液。回顾提升怎样判断一种溶液是否饱和?
饱和溶液与不饱和溶液之间如何转化?①加溶质 ②蒸发溶剂 ③降温②升温①加溶剂饱和
溶液不饱和
溶液观察溶液有剩余溶质饱和溶液无剩余溶质继续加该溶质溶解不能继续溶解不饱和溶液饱和溶液◆饱和溶液与不饱和溶液之间如何转化?◆怎样判断一种溶液是否饱和?思考:
1.上述过程中,氯化钠溶液从不饱和变为饱和的途径是什么?你能够从现象上判断溶液何时饱和的吗你?
2.你认为哪些自然条件有利于海水“晒盐”?为什么? 取少许不饱和氯化钠溶液,滴在洁净的玻璃片上,用电热吹风机向玻璃片上的溶液吹热风,观察现象。活动天地结晶:一定条件下,固体物质从它的饱和溶液中以晶体的形式析出的过程叫结晶结晶方法:蒸发溶剂法、降温法C关于海水“晒盐”的叙述正确的是 ( )
A.利用海水降温析出晶体
B.海水晒盐后的母液因食盐减少而变成不
饱和溶液
C.利用阳光和风力使水分蒸发得到食盐
D.利用海水在阳光下分解得到食盐晶体跟踪训练实验探究1.提出问题:哪些因素影响固体物质在 水中的溶解限量?2.猜想假设:小贴士控制变量法:如果有许多因素会同时影响某一实验结果,当我们要研究其中的一种因素时,要控制其它因素保持不变,只研究这一个变量对实验结果的影响。活动一:探究固体物质在水中溶解限量的影响因素(2)温度(1)溶质(溶剂)的 种类(3)水的量溶解不溶不溶溶解实验探究影响物质溶解性的因素二、溶解度二、固体物质在水中的溶解度(一)影响固体物质在水中的溶解限量(溶解性)的因素1.溶质、溶剂种类3.温度2.溶剂质量(一) 溶解度的定义 在一定温度下,某固体物质在100g溶剂里达到饱和状态时所溶解的溶质质量,叫做这种物质的在这种溶剂里的溶解度。注意:条件:一定温度。
标准:100克溶剂
状态:饱和状态
单位:克请你来找茬,看看缺什么
1.20℃时,10g食盐溶解在100g水中,所以20℃时,食盐的溶解度是10g。2.100g水中溶解了36g食盐刚好达到饱和,所以食盐的溶解度是36g。3.在20℃时,100g水里最多溶解了33.3g氯化铵,所 20℃时氯化铵的溶解度是33.3。4.在20℃时,100g硝酸钾的饱和溶液里含硝酸钾24g
则20℃时硝酸钾的溶解度是24g。抢答20℃时,100g水中最多溶解36g氯化钠理解:20℃时氯化钠的溶解度为36g1.含义:20℃时,100g水中溶解氯化钠达到饱和状态时,质量为36g .深入探究2:20℃饱和溶液中:m溶质:m溶剂:m溶液:——:———:——3:求20℃饱和溶液中溶质质量分数——4:20℃将20g氯化钠固体加入50g水中,所得溶液质量是——,溶质质量分数是————9253426.7%6826.7%蒸发结晶、降温结晶三种典型物质溶解度曲线氢氧化钙溶解度/g问题3.固体物质溶解度随温度的变化有哪些规律?溶解度/g1.大多数物质的溶解度随温度的升高而增大,如KNO3。
2.少数物质的溶解度随温度的升 高变化不大 ,如NaCl。
3.极少数物质的溶解度随温度的升高而减小,如Ca(OH)2。
定义:表示物质溶解度随温度变化的曲线叫溶解度曲线
(1)查找0—100℃时物质的溶解度,并判断溶解性。.溶解度曲线有哪些应用?(2)比较相同温度时,不同物质溶解度的大小。(3)确定物质的溶解度受温度影响的程度,并据此确定物质结晶的方法。
(4)判断溶液是否饱和。降温结晶:提纯溶解度受温度变化影响比较大的物质如:硝酸钾
蒸发结晶:提纯溶解度受温度变化影响不大的物质如:氯化钠
(5)溶解度曲线交点意义:40℃A、 B溶解度相等。1.如图,A点表示_____________________,
所在溶液是______溶液;
2.B点表示______________________________;
3.80℃时,a的溶解度___ b的溶解度(填“>”“<”或“=”)请你试一试80℃时,a的溶解度为85g饱和a,b两物质在60 ℃时,溶解度相等为52g>不饱和 饱和 A.CB4.C点对于a物质是 _________溶液,
对于b物质是_________溶液。
溶解度与溶解性的关系几种固体物质溶解度曲线 1. 生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”。你能解释其中的道理吗?跟踪训练蒸发结晶降温结晶(冷却热饱和溶液)适用范围:溶解度随温度升高而显著增大的物质适用范围:溶解度随温度升高变化不大的物质多识一点结晶方法课外探究 对下列现象你熟悉吗?请查阅有关气体溶解度的相关资料,来解释一下吧!
(1)天气闷热时,鱼儿为什么总爱在水面上进行呼吸?
(2)喝了汽水后,你常会打嗝,这是什么原因?
(3)打开汽水瓶盖,你能看到什么现象?为什么?多识一点影响气体溶解度的因素温度越高气体的溶解度越小
压强越大气体的溶解度越大多识一点 1.A、B、C三种物质的溶解度曲线如图所示:
(1)40℃时B物质的溶解度是多少?
(2)m点表示什么意义?
(3)40℃时,三种物质的溶解度由小到大的顺序是( )(A) C、B、A
(B) A、B、C
(C) B、A、C
(D) B、C、AB 巩固练习2.下图是甲、乙、丙三种物质的溶解度曲线.下列说法正确的是( )
A.在t1℃时,三种物质的溶解度由大到小的顺序是甲>乙>丙
B.在t2℃时,甲、乙两物质的溶解度相等
C.甲、乙、丙三种物质的饱和溶液升温都会转化为不饱和溶液
D.当乙的饱和溶液中混有少量丙时,可采用降温结晶的方法析出丙 B3.甲、乙两种固体的溶解度曲线如下图。现将两试管分别装入甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体),再放进盛有冰水的烧杯里, 则下列说法正确的是( )
A.甲溶液中溶质的质量分数增大
B.乙溶液中剩余的固体减少
C.试管里甲、乙物质的溶解度都增大
D.试管里甲、乙两溶液中的溶质都减少
再放进盛有冰水的烧杯里, 则下列说
再放进盛有冰水的烧杯里, 则下列说
B4.根据下列几种物质溶解度曲线图,得到的结论正确的是( ) A.硝酸钾中混有少量氯化钠,采用蒸发结晶进行提纯
B.氢氧化钙饱和溶液降低温度后有晶体析出
C.80℃时,氯化钾与硫酸镁的溶解度相等
D.所有物质的溶解度均随温度的升高而增大或随温度 的降低而减小C 2. A、B、C三种物质的溶解度曲线如图所示:
40℃时B物质的溶解度是多少?
m点表示什么意义?
40℃时,三种物质的溶解度由小到大的顺序是( ) C、B、A
A、B、C
B、A、C
B、C、A7030B室温(20℃)时:S <0.01g易溶物可溶物微溶物 难溶物
(不溶物)S>10g1g<S<10g0.01g< S <1g多识一点1.降温结晶(冷却热饱和溶液):使溶解度随温度升高显著增大的物质从溶液中结晶析出,例如:KNO3结晶:一定条件下,固体物质从它的饱和溶液中以晶体的形式析出的过程叫结晶2.蒸发结晶法(蒸发溶剂法):使溶解度随温度升高而变化不明显的物质从溶液中结晶析出,例如:NaCl补充:影响气体溶解度的因素温度越高气体的溶解度越小
压强越大气体的溶解度越大问题4.观察下列三种物质的溶解度曲线,你能提出哪些问题? 将60℃时A、B、C的饱和溶液分别降温到40℃,三种物质溶液的溶质质量分数如何变化?
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
